

问题 :乐伐替尼(靶向药物)和帕姆丽珠单抗(免疫*制剂抑**)单药均能作为治疗转移性透明肾细胞癌(RCC)的药物,但是关于乐伐替尼与帕姆单抗联合治疗RCC的疗效未有报道。
结果 :143例被评估患者的中位随访时间为19.8个月。既往未经过任何治疗组患者客观缓解率(ORR)为72.7%,既往接受过非免疫治疗组患者ORR为41.2%,既往接受过免疫治疗组患者ORR为55.8%。出现3级和4级治疗相关不良反应分别占57%和7%。
意义 : 乐伐替尼联合帕姆单抗治疗RCC表现出优越的疗效,且具备患者可接受的安全性。
01
研 究 背 景
透明肾细胞癌发生率约占肾细胞癌患者的70%-75%,舒尼替尼或帕佐帕尼单药等靶向药物目前能够作为转移性透明肾细胞癌的一线治疗方案。
早期研究发现,晚期肾细胞癌患者接受免疫检查点*制剂抑**(ICIs)联合TKI靶向*制剂抑**,或者接受双免疫药物联合疗法,具有更加优越的治疗效果。然而,对于既往接受免疫单药治疗后的患者,免疫联合靶向的疗效评估目前未有报道。
联合治疗有效的主要原因是免疫药物和靶向单药对透明肾细胞癌均具有一定疗效,其中帕姆单抗治疗ORR为36.4%,乐伐替尼治疗ORR为27%。
本研究共招募了145例患者(其中2例为非透明肾细胞癌被后期分析排除) ,其中既往未接受任何治疗患者22例,既往接受过非ICIs治疗患者17例,既往接受过ICIs治疗患者104例。
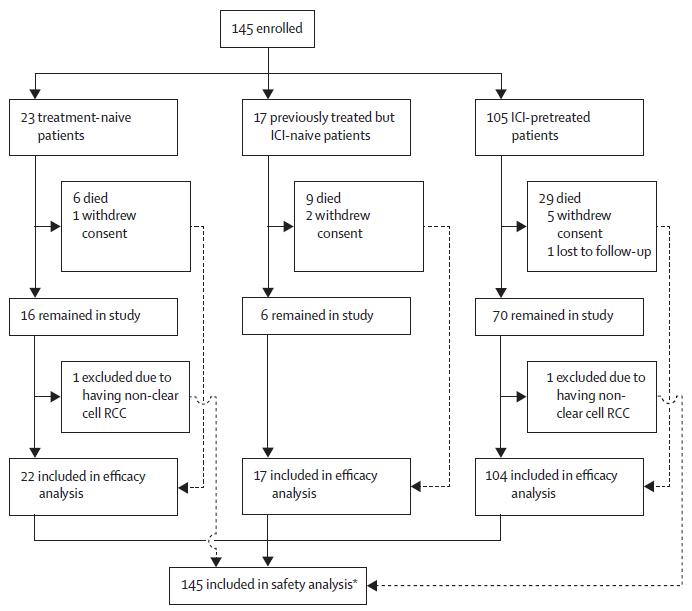
▲ 患者入组分析
02
研 究 结 果
2.1 联合治疗患者反应率
本研究的首要研究终点为接受治疗24周后患者的客观反应率(ORR)。
既往未接受任何治疗患者的ORR为72.7%(16/22),其中PR占77.3%,SD占22.7%;
既往接受过非ICIs治疗患者ORR为41.2%(7/17),其中PR占52.9%,SD占41.2%,PD占5.9%;
既往接受过ICIs治疗患者ORR为55.8%(58/104),其中PR占62.5%,SD占29.8%,PD占3.8%。
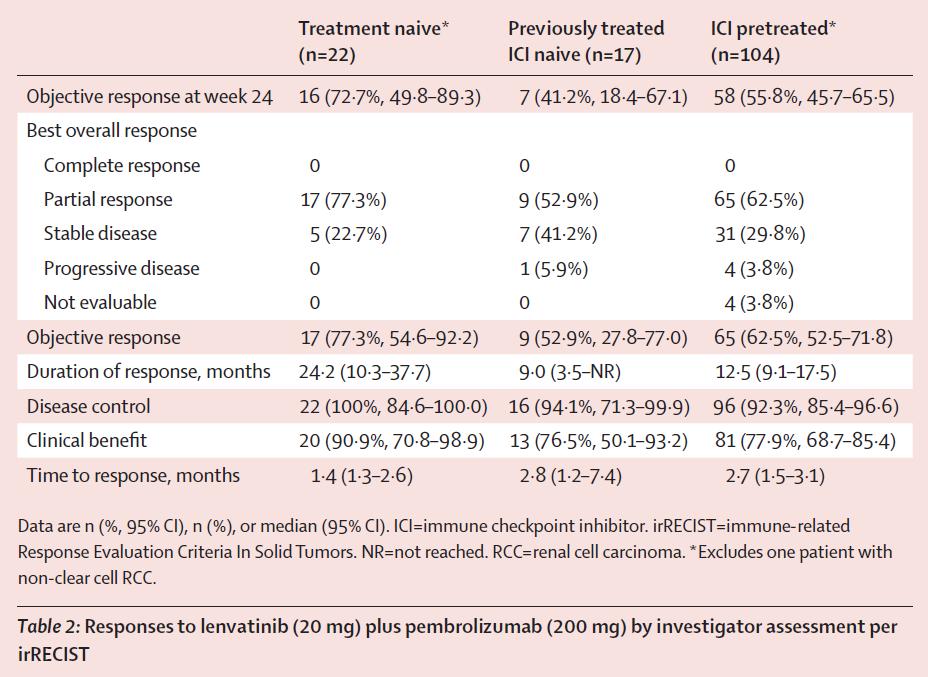
▲ 三组患者ORR分析
2.2 患者肿瘤变化评估
本研究评估了三组患者治疗前后的肿瘤变化(RECIST评估),包括:22例既往未接受任何治疗患者、17例既往接受过非ICIs治疗患者、101例既往接受过ICIs治疗患者。
分析结果显示,大多数患者接受联合治疗后肿瘤变小,每组至少有四分之一患者的肿瘤缩小率为50%。其中,1例未经任何治疗组患者、1例未经ICIs治疗组患者和3例既往接受ICIs治疗患者的肿瘤缩小率达100%。
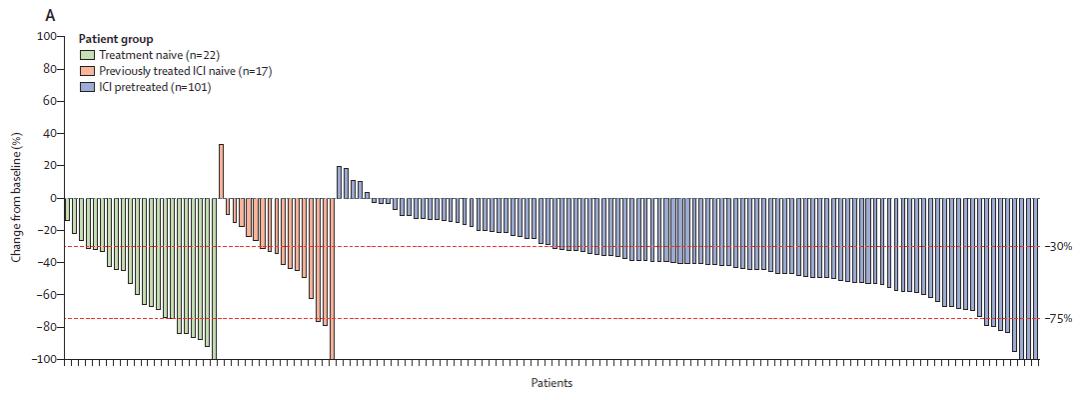
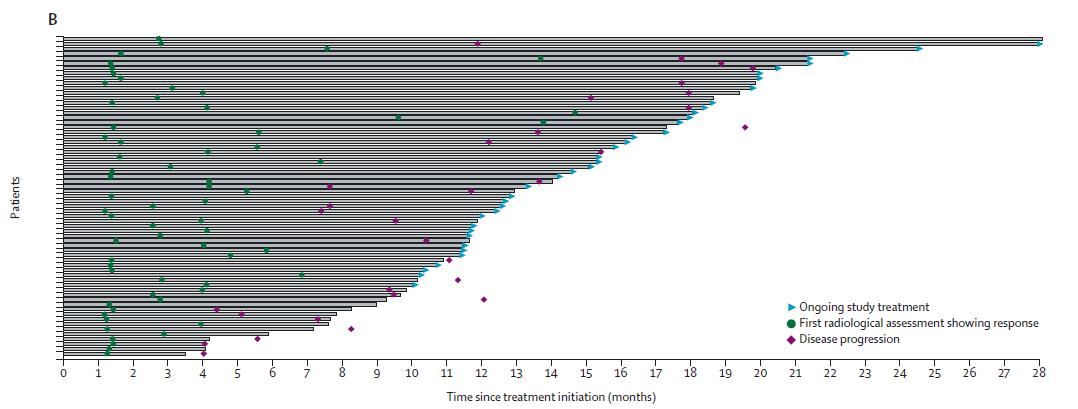
▲ 治疗前后肿瘤变化
2.3 每组患者无疾病生存期PFS和总生存期OS分析
截止研究终点,未接受任何治疗的15例患者、既往未接受过ICIs治疗的12例患者、以及既往接受ICIs治疗的59例患者出现疾病进展或死亡。
随后,研究人员分别对每组患者无进展生存期PFS和总生存期OS进行分析。PFS分析结果显示,所有患者中位PFS为18.9个月。其中未接受任何治疗患者中位PFS为24.1个月(95% CI 11.7-31·7);既往未接受过ICIs治疗患者中位PFS为11.8个月(95% CI 5.5-12.2);既往接受ICIs治疗患者中位PFS为12.2个月(95% CI 9.5-17.7)。
OS分析结果显示,3组患者的总OS未达到,其中未接受任何治疗患者中位随访时间为29.5个月;既往未接受过ICIs治疗患者中随访时间为30.3个月;既往接受ICIs治疗患者中位随访时间为16.6个月。
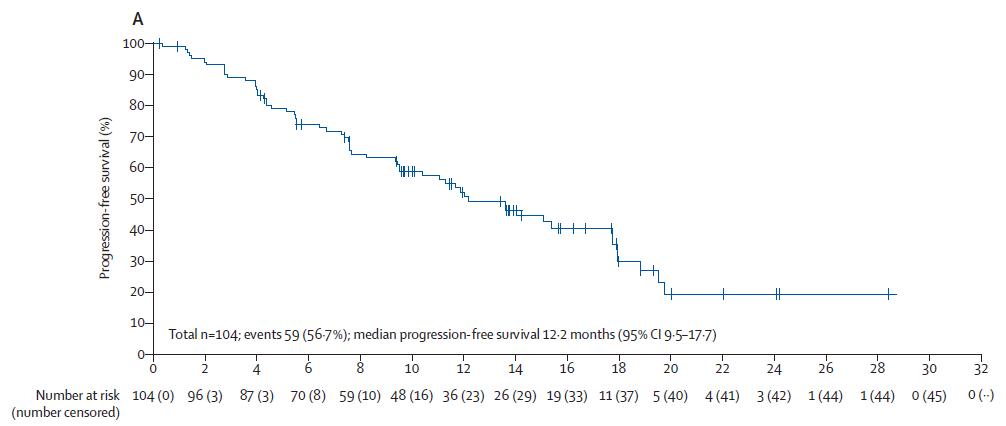
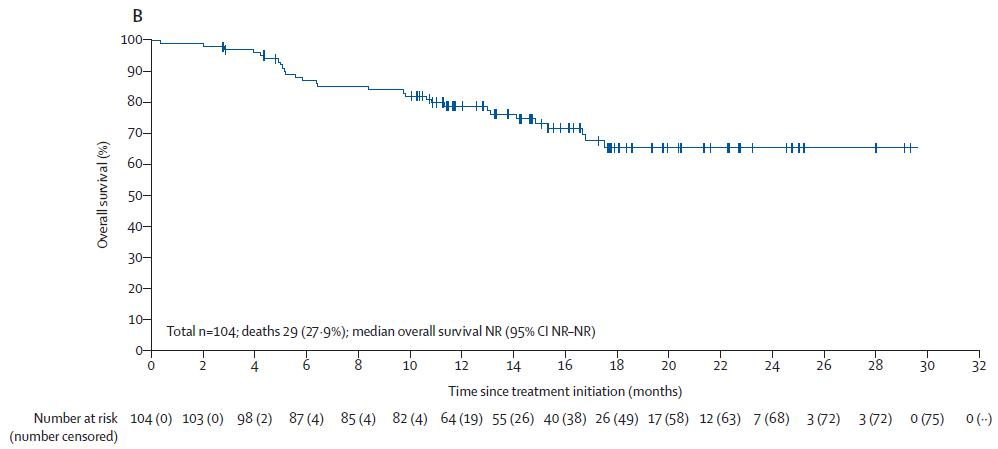
▲ 不同患者PFS及OS分析
2.4 接受治疗患者副反应分析
治疗相关不良反应统计结果显示,144例患者(99%)至少发生一次及以上治疗相关不良事件。145例患者中,82例(57%)发生3级治疗相关不良事件,10例(7%)发生4级治疗相关不良事件。
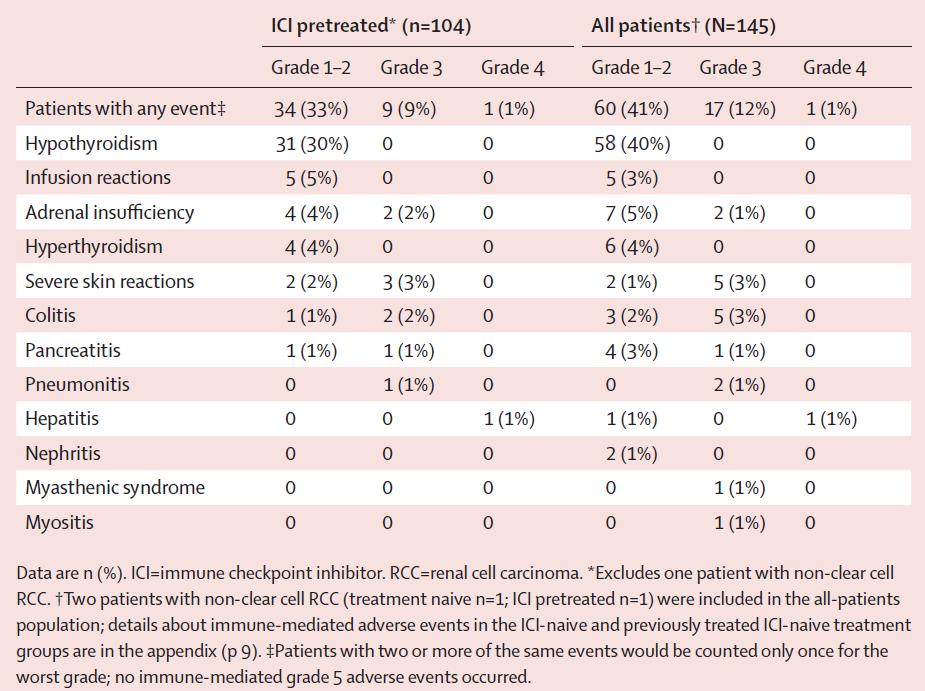
▲ 治疗相关不良反应统计
03
研 究 结 论
本研究结果证实,对于既往未接受过任何治疗,以及既往已接受过治疗(包括ICIs治疗)的转移性肾细胞癌患者,免疫检查点*制剂抑**联合靶向治疗方案具有一定的抗肿瘤效果。
参考文献
1. Choueiri TK, Motzer RJ. Systemic therapy for metastatic renal-cell carcinoma. N Engl J Med. 2017; 376: 354–66.
2. Rini BI, Plimack ER, Stus V, et al. Pembrolizumab plus axitinib versus sunitinib for advanced renal-cell carcinoma. N Engl J Med. 2019; 380: 1116–27.
3. Rassy E, Flippot R, Albiges L. Tyrosine kinase inhibitors and immunotherapy combinations in renal cell carcinoma. Ther Adv Med Oncol. 2020; 12: 1758835920907504.
4. Choueiri TK, Powles T, Burotto M, et al. Nivolumab plus cabozantinib versus sunitinib for advanced renal-cell carcinoma. N Engl J Med. 2021; 384: 829–41.
5. Cai C, Tang J, Shen B, et al. Preclinical trial of the multi-targeted lenvatinib in combination with cellular immunotherapy for treatment of renal cell carcinoma. Exp Ther Med. 2017; 14: 3221–28.
6. Matsuki M, Hoshi T, Yamamoto Y, et al. Lenvatinib inhibits angiogenesis and tumor fibroblast growth factor signaling pathways in human hepatocellular carcinoma models. Cancer Med. 2018;7: 2641–53.
7. Motzer RJ, Bacik J, Schwartz LH, et al. Prognostic factors for survival in previously treated patients with metastatic renal cell carcinoma. J Clin Oncol. 2004; 22: 454–63.
8. Ravi P, Mantia C, Su C, et al. Evaluation of the safety and efficacy of immunotherapy rechallenge in patients with renal cell carcinoma. JAMA Oncol. 2020; 6: 1606–10.
