2017年,TCGA团队在Nature上发布了最新的食管癌基因整合图谱1,分别阐述了食管鳞癌和食管腺癌两种不同类型食管癌的基因特征,并据此将食管鳞癌分为三个亚型:ESCC1、ESCC2、ESCC3。
ESCC1以亚洲越南患者居多,具有抗氧化通路(NRF2)激活的特征。这一通路的激活与肿瘤细胞化疗耐药相关。同时,ESCC1 还具有SOX2/TP63的扩增、YAP1扩增和VGLL4/ATG7缺失(Hippo通路的激活)等特征。
ESCC2以东欧和南美人群为主,有着更高的Notch1或ZNF750突变频率、CDK6扩增频率、以及KDM6A、KDM2D、PTEN或PIK3R1的失活改变。在ESCC2亚型中富有白细胞浸润,但是尚不清楚其浸润白细胞亚型及其对免疫治疗的指导意义。
ESCC3以北美人群为主,是一个较为特殊的类型。其细胞周期通路的改变和TP53突变较少,但是仍然保持较高水平的PI3K通路的激活和染色体相关修饰基因的改变(KMT2D/MLL2,SMARCA4)。
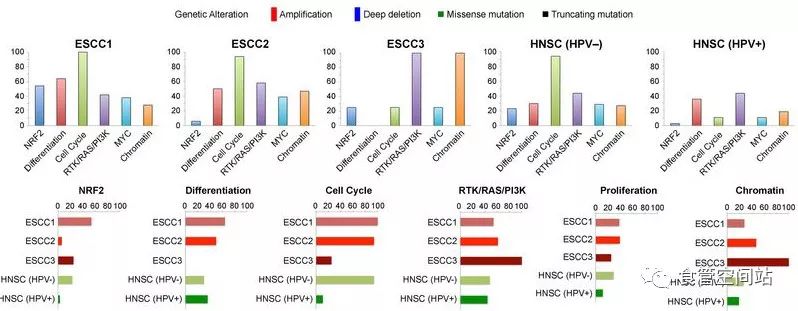
仔细分析这篇文章的结果,发现其对我国食管癌的临床指导意义有限,主要原因包括:(1) 我国患食管癌人数占了全球一半以上,却未被纳入分析,食管癌流行病学的地域差异显示越南患者并不能代表我国患者的特征;(2)用于分型的样本量太小,总人数仅有90人,其中ESCC1为50人,ESCC2为36人,ESCC3为4人;(3)我国大多数食管癌患者就诊时已处于晚期,然而这篇文章分析的是早期或进展期食管鳞癌的手术切除样本。根据肿瘤演化学说,早期和进展期的分子分型并不能代表晚期食管癌的分子特征。
因此,食管空间站团队针对近年来中国食管癌患者的基因组学信息进行系统地梳理并归纳总结,以飨读者:
【单核苷酸变异】
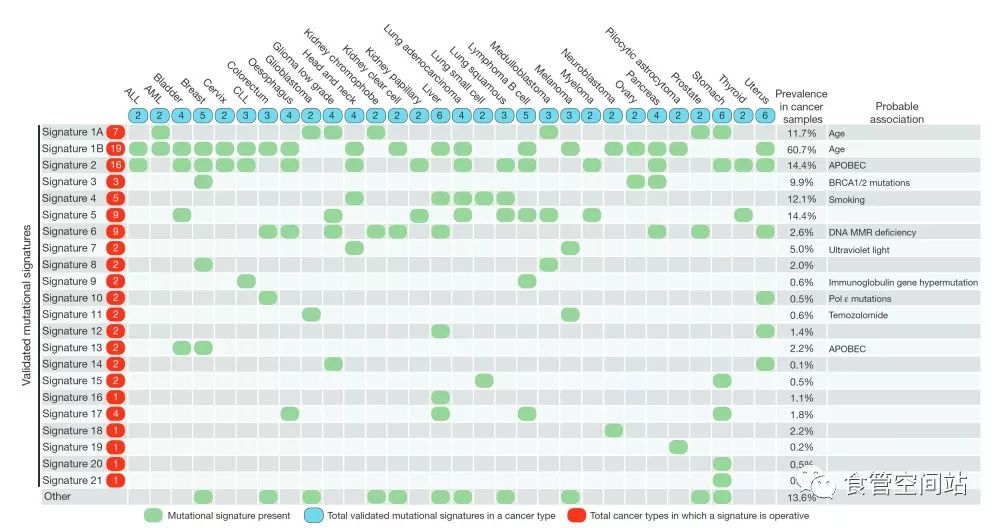
肿瘤多由体细胞突变引发。体细胞突变常由多种不同生物学过程所诱导,如吸烟、饮酒、紫外线照射、DNA错配修复缺陷等,这些不同的突变过程形成了特定的突变模式,即突变特征。2013年,Nature杂志公布了21种人类肿瘤的突变特征2,其中食管癌中存在的有Signature 1B (与年龄相关)、Signature2(与APOBEC酶活性相关)、Signature6(与DNA错配修复缺陷)和Signature17(病因未明)。
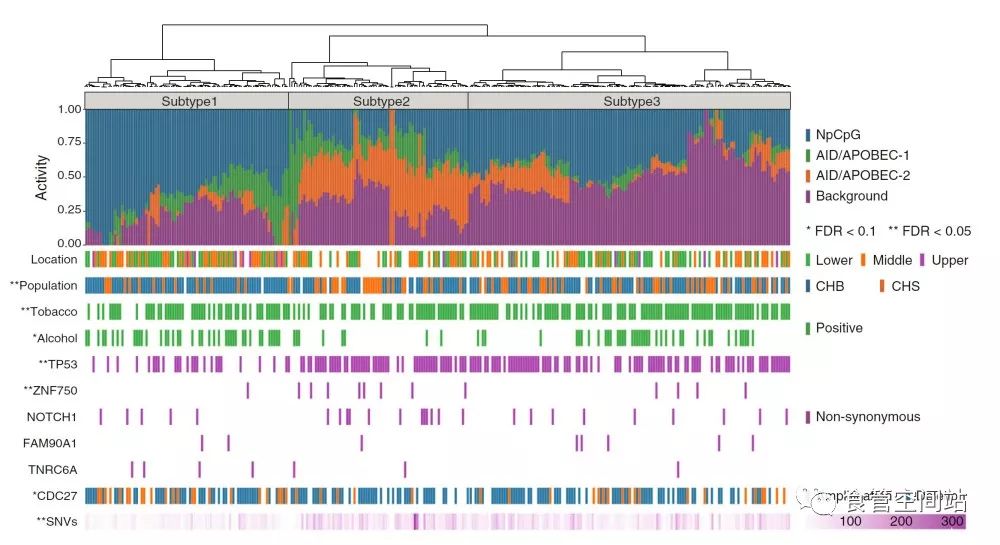
在食管癌中,最常见的单核苷酸变异是C:G>T:A,其次是C:G>G:C,根据食管癌SNV变异谱,可以分为三类3,4:1)具有APOBEC酶活性的突变特征:在TpCpX碱基位点发生C>G/T;2)“NpCpG”:在NpCpG碱基位点发生C > T;3)多因素混杂型:Signature 3、4、9等一些未知特征的复合体。这三类分型也在日本食管鳞癌得到证实5。通常认为吸烟与食管癌相关,但是多个测序分析并没有在这些核苷酸变异里找到与吸烟相关的突变特征4,6,同时最新的荟萃分析也表明,在食管鳞癌高发的中国,吸烟与食管癌的关系非常微弱7。
【突变基因】
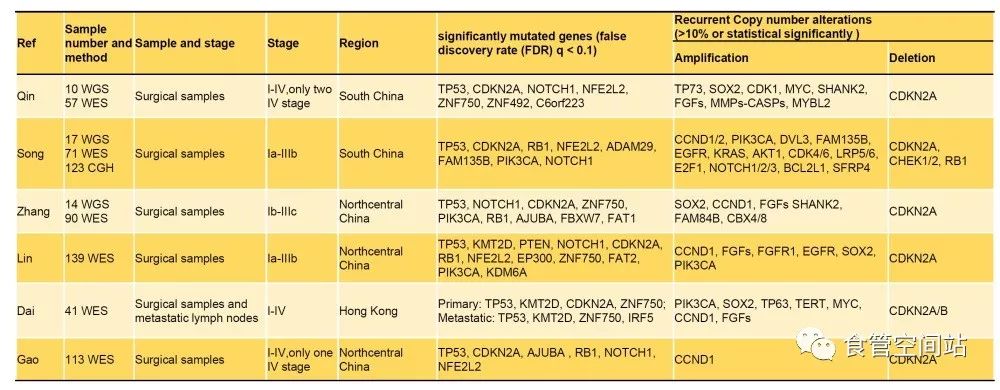
由于食管癌的突变广泛而复杂,异质程度高。因此,大部分研究团队使用MutSigCV算法来确定起着驱动作用的突变基因(significantly mutated genes,SMG)。虽然各个研究6,8-11所得到的SMG有一定差异,但大部分趋于一致,主要有TP53, CDKN2A, NFE2L2, ZNF750, NOTCH1和RB1等。以TP53最为多见,而其他SMG的出现频率较小。其中Notch1和ZNF750是调控鳞状上皮分化的基因,其突变常见于各种鳞癌。Notch1突变为食管鳞癌突变的早期事件,I期突变率35%,III期突变率8%12;而ZNF750则更多见于转移性食管鳞癌中,存在该突变者更易发生淋巴转移9。这些SMG在生物学上的促癌功能多已经经过验证,而携带这些SMG的患者预后往往较差,如TP539,EP3006,FAM135B8,TET25等。食管癌早期病变——鳞状上皮化生和食管癌的基因组差异并不是很大13,但在早期病变*特中**有CDKN2A/2B超甲基化的现象14,可能作为未来食管癌早期诊断的标志物。
【拷贝数变异】
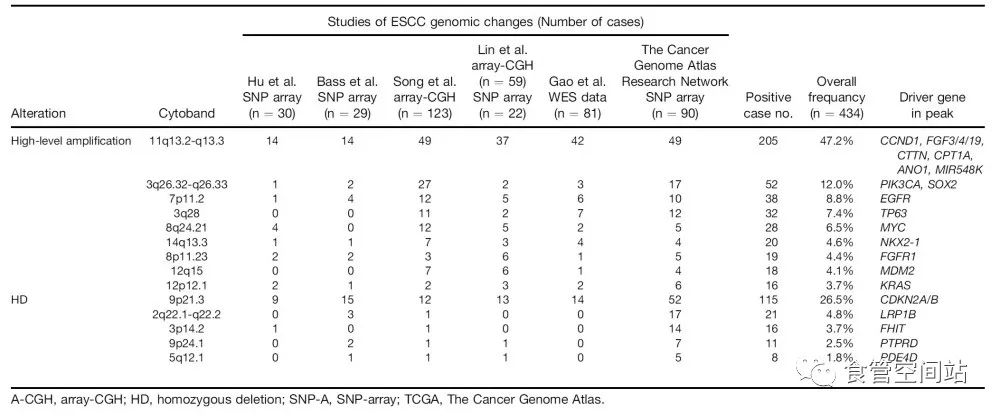
最常见基因扩增区域是11q13.2-q13.3,包含了CCND1,FGF3/4/19,最常见的缺失区域是9p21.3,是CDKN2A/2B的坐落位点。 其他的常见的局部扩增还包括8p11.23 (FGFR1), 8q24.21 (MYC), 7p11.2 (EGFR),12p12.1 (KRAS), 12q15 (MDM2), 3q26 (TP63和PRKCI),3q26.32–q26.33 (SOX2和PIK3CA)14q13.3 (NKX2-1);其他同源性缺失还有2q22.1–q22.2(LRP1B), 9p24.1 (PTPRD),和3p14.2 (FHIT)等。
【基因融合】
基因融合在食管鳞癌中较为散在,多为个案报道,主要有以下几类:FGFR1-TACC315、EIF3E-RAD51B16、TRAPPC9-CLVS116、HLA-E-HLA-B17、GOLM1-MAK1018。其中FGFR1-TACC3为明显的驱动因素,而且也是可治疗性的靶点,并在其他瘤种的临床试验中已证实有效,但其在食管癌的发生频率只有1%。
【食管鳞癌相关通路】
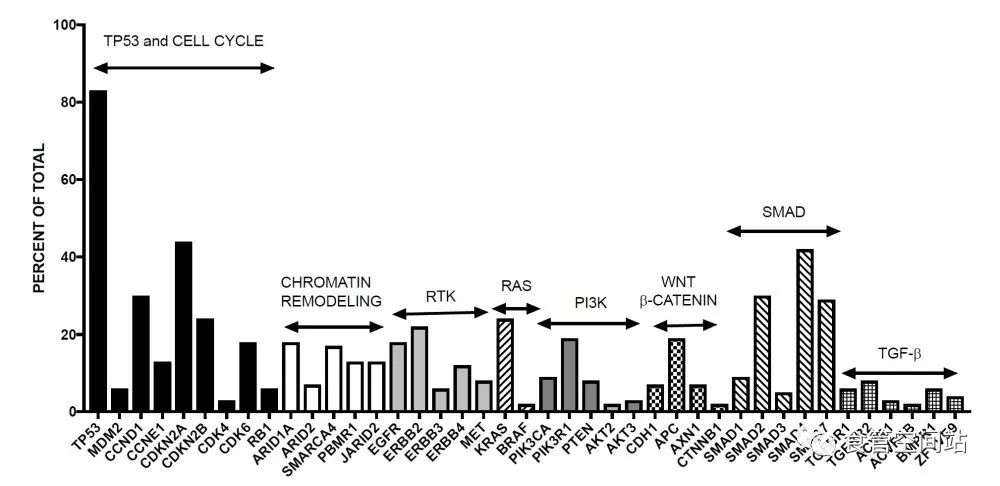
结合突变、拷贝数变异和基因融合,可以看出,食管鳞癌主要涉及的通路为细胞周期和凋亡相关通路,其他高频改变通路有PI3K/mTOR通路、Notch通路(通常在早期肿瘤中改变12)、NFR2通路、表观或组蛋白修饰通路(在转移性食管癌多见9)、FGF通路、Wnt/β-catenin通路和Hedgehog通路,这些通路形成合力促进了食管癌的发生发展。
综上所述,我国食管鳞癌的分子特征与西方患者有明显的差异,而且异质性高,驱动因素复杂,这也恰恰是目前食管鳞癌治疗近20余年停滞不前的症结所在。近年来,基因组学、表观组学、蛋白组学和生物信息分析技术等的发展,为我们全面、立体、动态解码食管鳞癌的分子生物学信息提供了先进的*器武**,同时也为精准靶向和免疫治疗提供了理论基础。但是如何研读,并转化这些信息,走出一条符合我国国情的食管癌治疗之路,是当前我国科学家和肿瘤科医生的努力方向之一。
参考文献
1、Cancer Genome Atlas Research, N. et al.Integrated genomic characterization of oesophageal carcinoma.Nature 541, 169-175, doi:10.1038/nature20805 (2017).
2、Alexandrov, L. B. et al.Signatures of mutational processes in human cancer.Nature 500, 415-421, doi:10.1038/nature12477 (2013).
3、Guo, J. et al.Germline and somatic variations influence the somatic mutational signatures of esophageal squamous cell carcinomas in a Chinese population.BMC genomics 19, 538, doi:10.1186/s12864-018-4906-4 (2018).
4、Zhang, L. et al. Genomic analyses reveal mutational signatures and frequently altered genes in esophageal squamous cell carcinoma. Am J Hum Genet 96, 597-611, doi:10.1016/j.ajhg.2015.02.017 (2015).
5、Sawada, G. et al. Genomic Landscape of Esophageal Squamous Cell Carcinoma in a Japanese Population. Gastroenterology 150, 1171-1182, doi:10.1053/j.gastro.2016.01.035 (2016).
6、Gao, Y. B. et al. Genetic landscape of esophageal squamous cell carcinoma. Nat Genet 46, 1097-1102, doi:10.1038/ng.3076 (2014).
7、Yang, X. et al. Smoking and alcohol drinking in relation to the risk of esophageal squamous cell carcinoma: A population-based case-control study in China. Scientific reports 7, 17249, doi:10.1038/s41598-017-17617-2 (2017).
8、Song, Y. et al. Identification of genomic alterations in oesophageal squamous cell cancer. Nature 509, 91-95, doi:10.1038/nature13176 (2014).
9、Dai, W. et al. Whole-exome sequencing reveals critical genes underlying metastasis in esophageal squamous cell carcinoma. The Journal of pathology, doi:10.1002/path.4925 (2017).
10 、Qin, H. D. et al. Genomic Characterization of Esophageal Squamous Cell Carcinoma Reveals Critical Genes Underlying Tumorigenesis and Poor Prognosis. Am J Hum Genet 98, 709-727, doi:10.1016/j.ajhg.2016.02.021 (2016).
11、Lin, D. C. et al. Genomic and molecular characterization of esophageal squamous cell carcinoma. Nat Genet 46, 467-473, doi:10.1038/ng.2935 (2014).
12、Cheng, C. et al. Genomic analyses reveal FAM84B and the NOTCH pathway are associated with the progression of esophageal squamous cell carcinoma. GigaScience 5, 1, doi:10.1186/s13742-015-0107-0 (2016).
13、Chen, X. X. et al. Genomic comparison of esophageal squamous cell carcinoma and its precursor lesions by multi-region whole-exome sequencing. Nature communications 8, 524, doi:10.1038/s41467-017-00650-0 (2017).
14、Ishii, T. et al. Oesophageal squamous cell carcinoma may develop within a background of accumulating DNA methylation in normal and dysplastic mucosa. Gut 56, 13-19 (2007).
15、Mizukami, T. et al. Identification of a FGFR3-TACC3 fusion in esophageal cancer. Annals of oncology : official journal of the European Society for Medical Oncology 28, 437-438, doi:10.1093/annonc/mdw550 (2017).
16、Cheng, C. et al. Whole-Genome Sequencing Reveals Diverse Models of Structural Variations in Esophageal Squamous Cell Carcinoma. Am J Hum Genet 98, 256-274, doi:10.1016/j.ajhg.2015.12.013 (2016).
17、Jiang, Y. Z., Li, Q. H., Zhao, J. Q. & Lv, J. J. Identification of a novel fusion gene (HLA-E and HLA-B) by RNA-seq analysis in esophageal squamous cell carcinoma. Asian Pacific journal of cancer prevention : APJCP 15, 2309-2312 (2014).
18、Zhang, H. et al. Aberrant chimeric RNA GOLM1-MAK10 encoding a secreted fusion protein as a molecular signature for human esophageal squamous cell carcinoma. Oncotarget 4, 2135-2143, doi:10.18632/oncotarget.1465 (2013).
(本文转自食管空间站)