
JCBFM(IF=6.960)
据统计,即便在发达国家,每1000个新生儿中就可能有4个出现缺氧缺血性脑病,严重威胁着新生儿的健康。而发表于 Journal of Cerebral Blood Flow and Metabolism 的《Neuronal GPR81 regulates developmental brain angiogenesis and promotes brain recovery after a hypoxic ischemic insult》(神经元GPR81调节发育性脑血管生成,促进缺氧缺血性损伤后的脑恢复)针对这一问题提出了对策。
研究背景
围产期缺氧/缺血( HI )脑损伤会对新生儿的神经发育造成非常严重的后果,至今仍是一个重大的临床问题。有人认为,在缺血期间积累的糖酵解衍生乳酸可以防止缺血损伤,但其作用机制尚不清楚。因此,作者试图阐明G蛋白偶联受体(GPR81)在小鼠出生后缺氧缺血性脑损伤模型中参与缺氧诱导的脑损伤及其机制,以制定有效的干预措施。
研究思路
作者首先假设乳酸通过其GPR81控制出生后的脑血管生成,并在HI损伤后发挥保护作用,发现GPR81主要在大脑皮层和海马的神经元中表达。通过野生小鼠和GPR81缺失的小鼠对比,在脑室内注射乳酸盐,证明乳酸通过GPR81参与发育性脑血管生成,并通过恢复受损的微血管减轻HI损伤。
研究结果
1. GPR81受体明显位于发育中脑的神经元
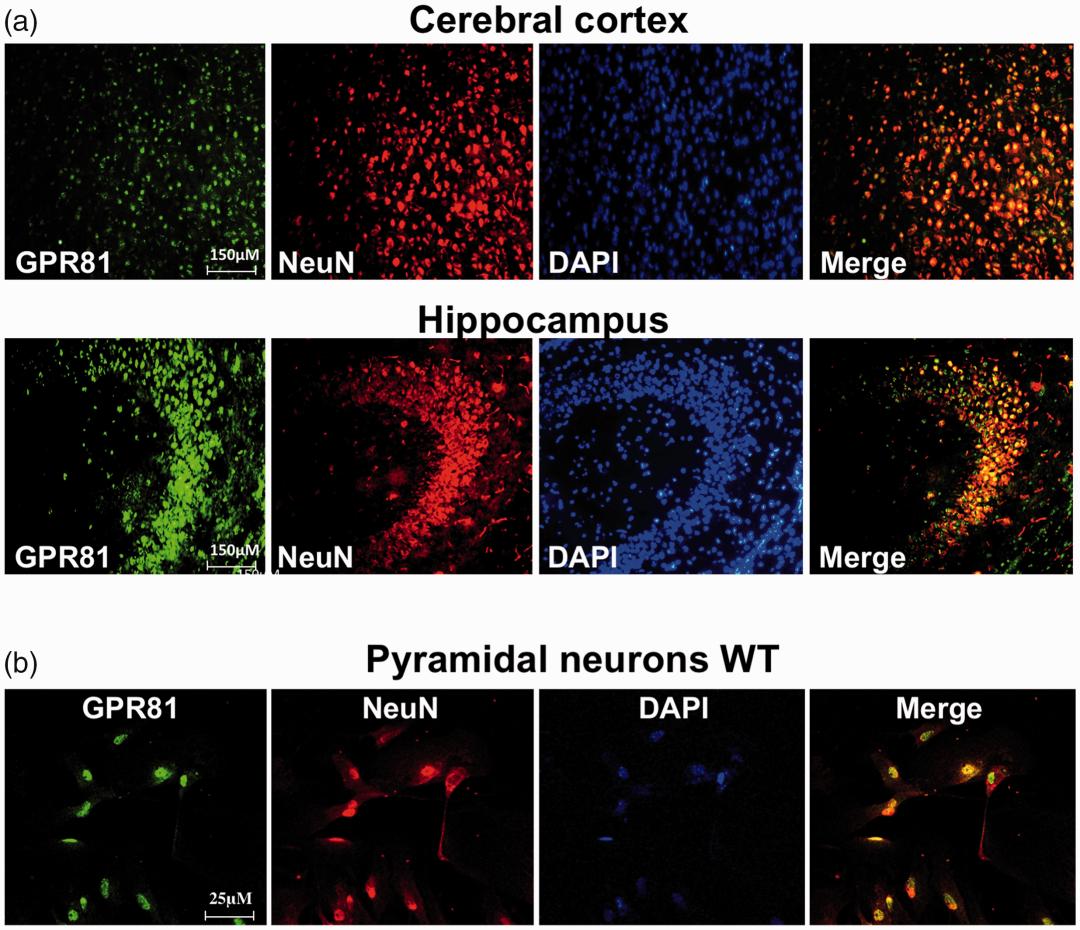
作者通过双重免疫组化标记来评估GPR81受体的定位,发现GPR81KO动物中不存在GPR81免疫反应,而GPR81主要表达于大脑皮层和海马的神经元(NeuN+细胞)。从WT GPR81的海马区分离培养的原代新生儿锥体神经元细胞证明神经元中是存在GPR81的;也正如预期那样,作者发现GPR81基因缺失小鼠的脑匀浆中均不含GPR81。
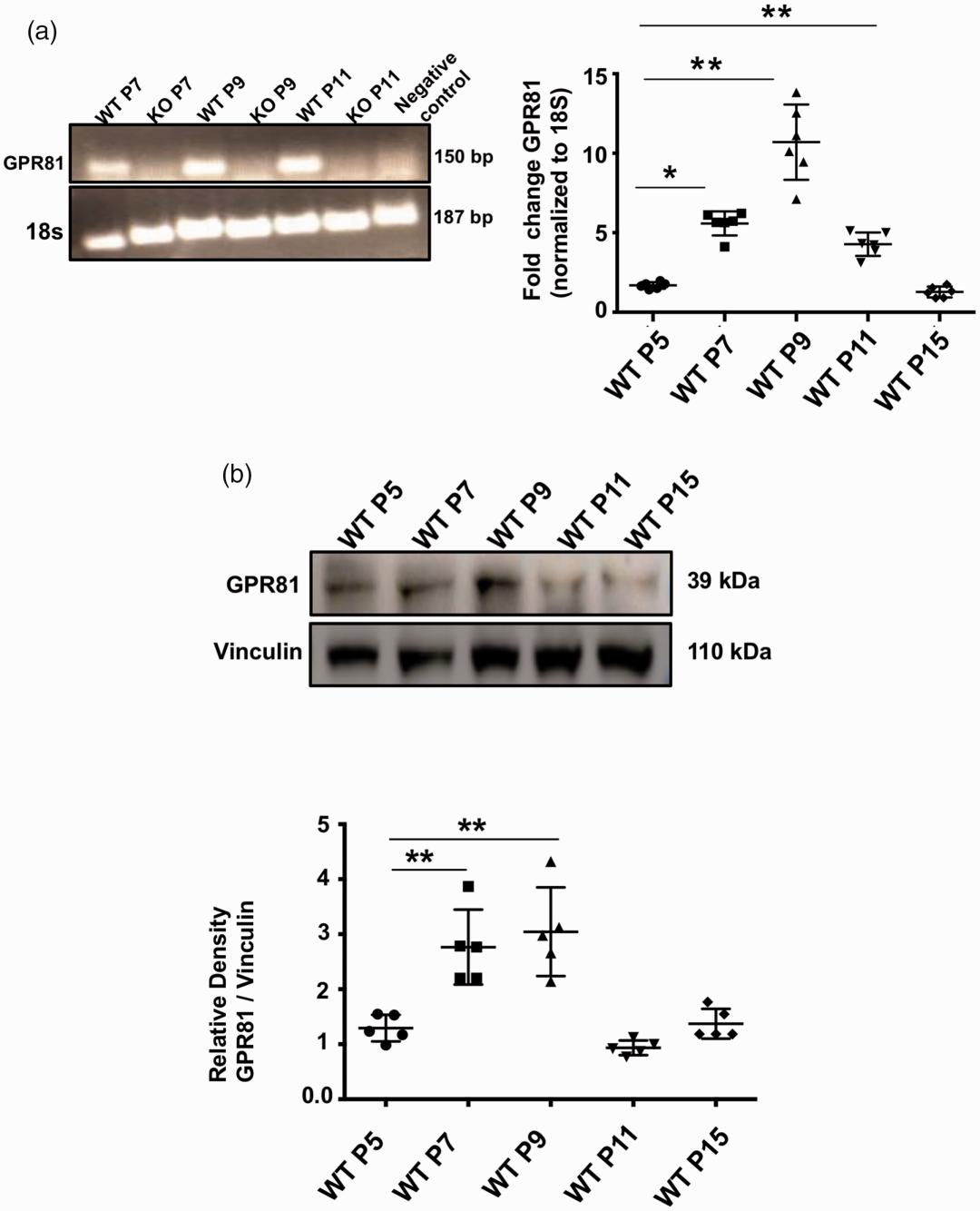
2. GPR81通过控制血管生成因子参与发育性脑血管生成
作者评估了野生小鼠发育中的大脑中血管生成和炎症因子(已知影响血管生成)的表达,尤其是VEGF-A, Ang-1, Ang-2, PDGFBB, CCL2, COX-2和抗血管生成TSP-1。所有测量的血管生成因子在出生后早期增加,并在P9达到峰值,与GPR81相似;而TSP-1的表达在同期呈下降趋势。GPR81基因敲除逆转了在同一时期测量的所有因素的变化。
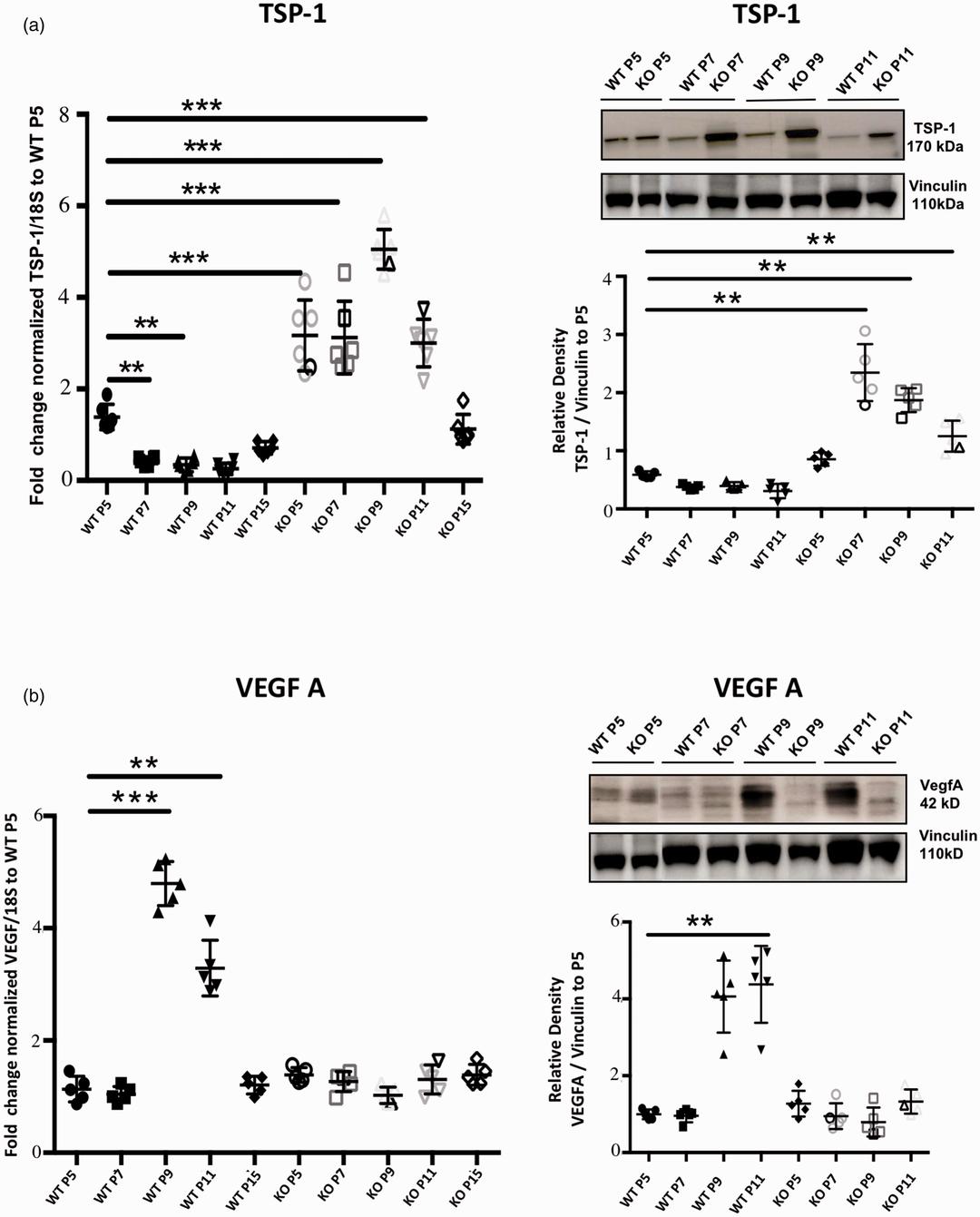
这些实验表明,在野生型小鼠中,乳酸增加了促血管生成VEGF-A、Ang-1、Ang-2、PDGF的水平,抑制了血管静态因子TSP-1的水平;乳酸对gpr81基因缺失小鼠无效。
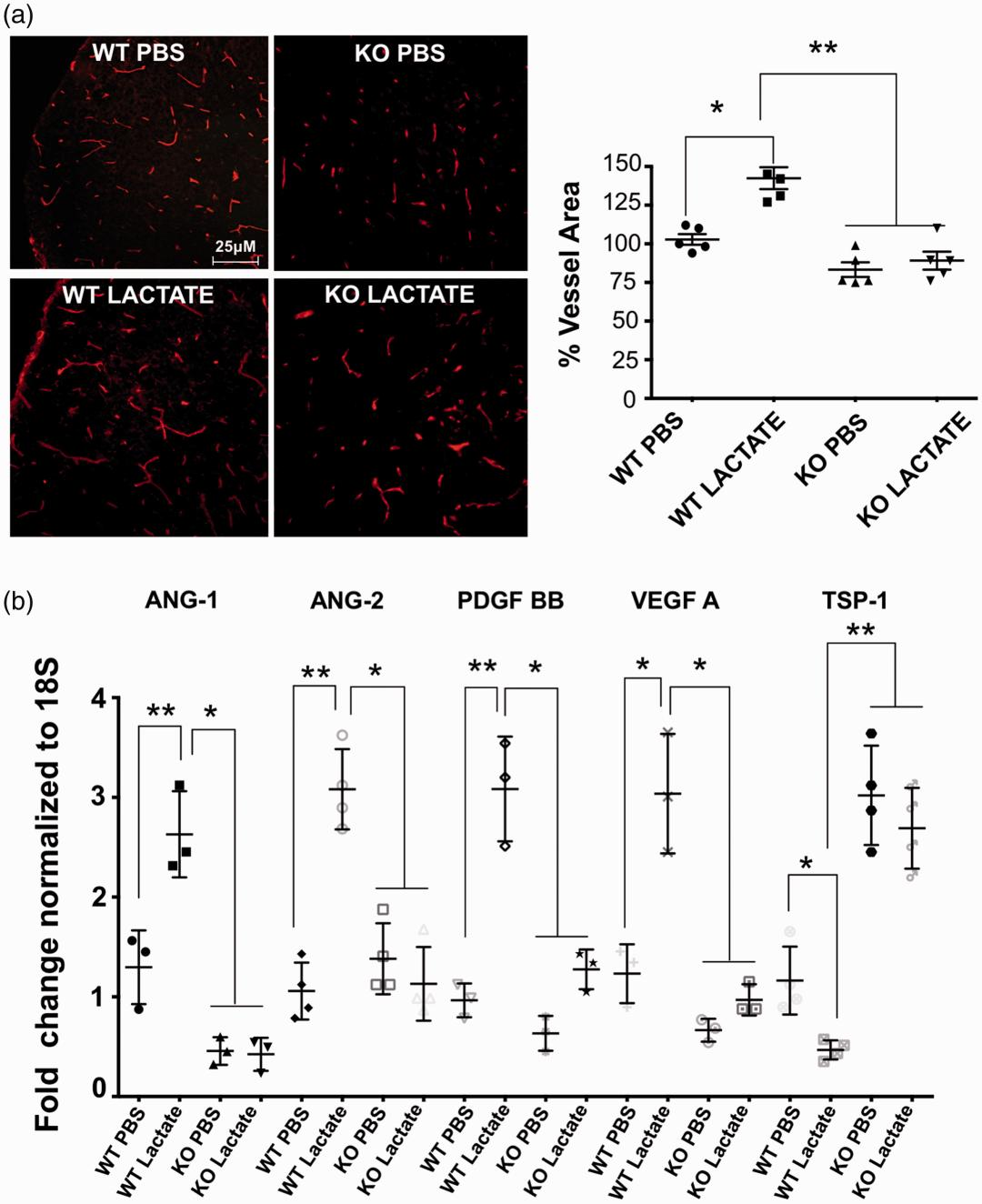
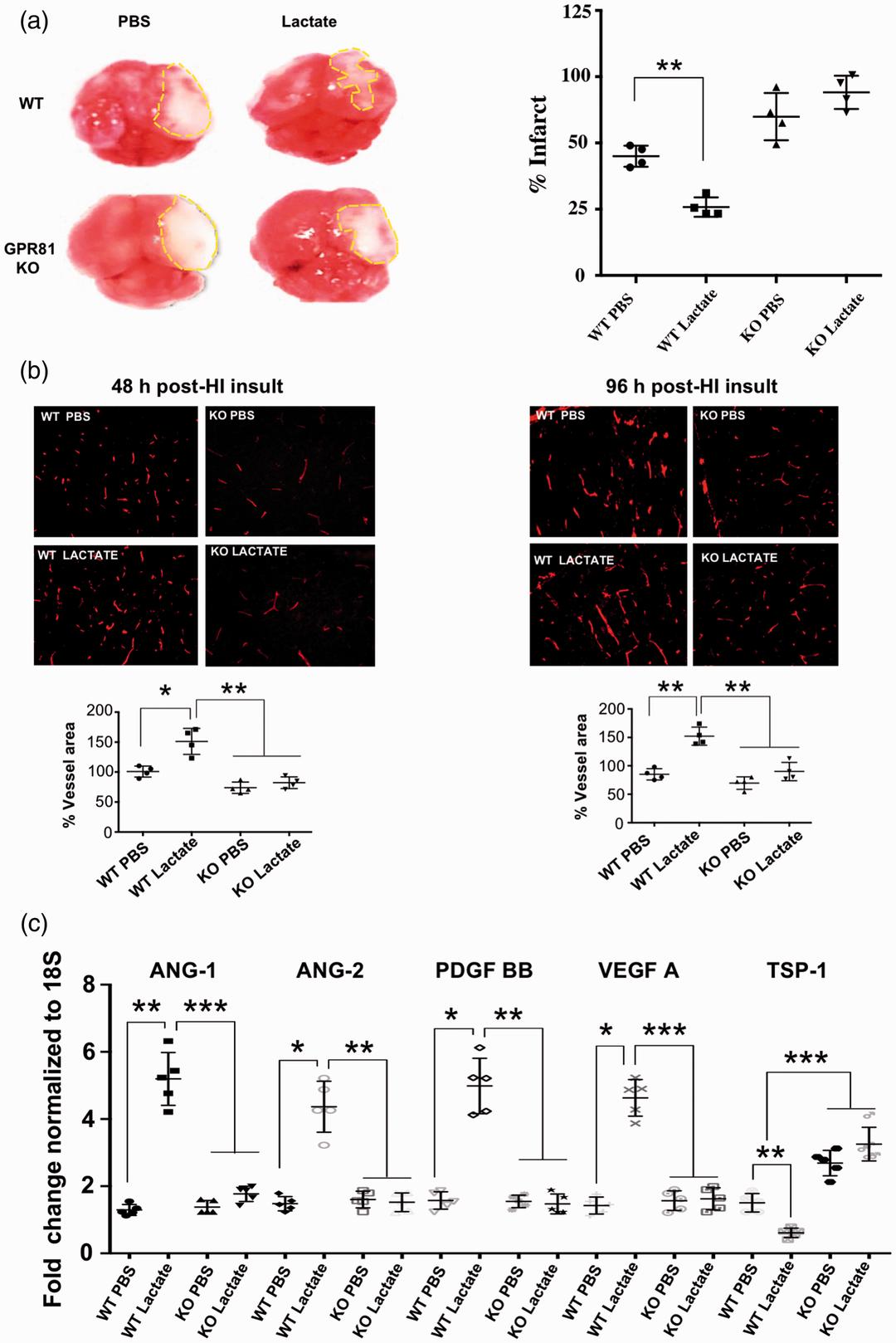
3. 乳酸可减少围产期HI损伤继发的梗死面积
作者对新生小鼠(P7)进行永久性左颈动脉结扎,然后进行1.5小时缺氧(8% O2);在P4注射乳酸(估计心室内/室周浓度:10mM)。乳酸可使野生型小鼠的梗死面积在HI后96小时后减少50%;相反,GPR81缺失小鼠的梗死面积增加,此时乳酸无效。在HI后的48小时和96小时,乳酸使野生型小鼠中的梗死周围区域(半暗带)的血管密度增大,使GPR81缺失小鼠中的降低。乳酸诱导的血管生成与野生型动物中促血管生成因子(VEGF-A, PDGF-BB, Ang1和Ang-2)的连续增加和抗血管生成TSP-1的抑制相关;乳酸对gpr81基因缺失小鼠无效。
研究结论
通过研究GPR81作用的代谢产物乳酸受体在发育和HI后脑血管中的作用,发现它通过上调VEGF-A等血管生成因子和下调TSP-1来加强血运重建,从而减轻HI卒中后的脑损伤。据此推测,选择性长效GPR81激动剂可能在HI损伤中发挥良好的效果。