
来源:“Research科学研究”微信公众号
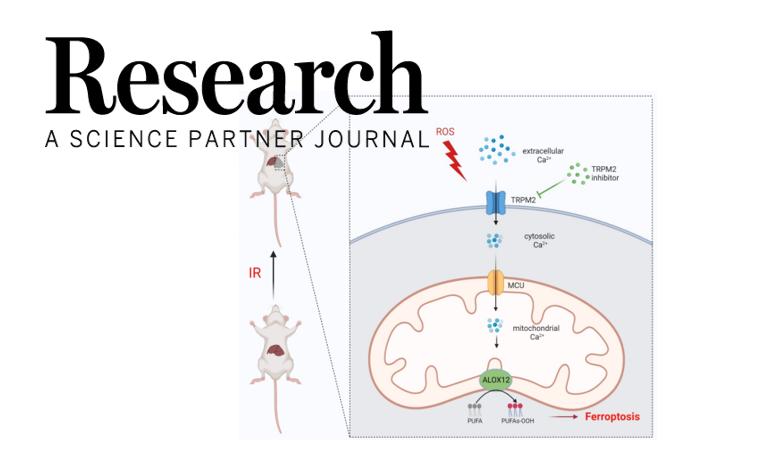

近日,浙江大学林辉团队和余沛霖团队合作报道了靶向瞬时受体电位离子通道Transient Receptor Potential Melastatin type 2(TRPM2)通过抑制细胞铁死亡进而有效缓解肝缺血再灌注损伤的新发现。相关成果以题为“TRPM2 Mediates Hepatic Ischemia–Reperfusion Injury via -Induced Mitochondrial Lipid Peroxidation through Increasing ALOX12 Expression”发表在Research上。
Citation:
Zhong C, Yang J, Zhang Y, Fan X, Fan Y, Hua N, Li D, Jin S, Li Y, Chen P et al., TRPM2 Mediates Hepatic Ischemia–Reperfusion Injury via -Induced Mitochondrial Lipid Peroxidation through Increasing ALOX12 Expression. Research 2023;6:Article 0159.
https://doi.org/10.34133/research.0159
研究背景
肝切除是治疗肝脏疾病尤其是肝脏恶性肿瘤和肝胆管结石的重要手段。由于肝脏血供丰富且脉管结构复杂,减少和控制出血是降低肝切除手术死亡率和并发症的关键。肝血流阻断技术是肝切除术中应用最广泛的出血控制技术,但是,阻断入肝血流可引发肝组织缺血再灌注损伤,尤其对合并肝硬化病人,会增加引发肝功能衰竭甚至死亡可能。减少甚至阻断缺血再灌注对肝功能的损害一直是肝脏外科中的重大难题。此外,肝缺血再灌注损伤也是诱发肝移植术后患者排异反应和肝功能衰竭的高危因素。尽管目前有一些术前预处理的方法来缓解该损伤,然而效果有限且存在不确定性,因此,深入研究肝缺血再灌注损伤的病理生理机制并开发新的干预技术和方法具有重要的学术意义和临床价值。
肝缺血再灌注过程分为缺血期和再灌注期,再灌注期产生的活性氧(Reactive Oxygen Species,ROS)被认为是导致该损伤的重要因素,ROS可诱导炎症反应,还可通过诱导细胞发生凋亡、自噬等直接造成损伤。新的研究发现肝缺血再灌注损伤过程肝细胞也出现明显的铁死亡。
该团队前期研究证实靶向TRPM2通道——一种细胞膜上的ROS感受器,可有效缓解脑缺血再灌注损伤,另有研究发现抑制或敲除TRPM2可缓解小鼠心脏和肾脏的缺血再灌注损伤。TRPM2在肝缺血再灌注损伤中是否也发挥重要作用,其分子机制是什么?围绕这一“科学问题”,研究团队开展了联合攻关。
研究进展
研究人员构建肝缺血再灌注动物模型,发现肝缺血再灌注损伤伴随TRPM2表达增加。接着作者利用TRPM2敲除型和野生型小鼠再次制备肝缺血再灌注损伤动物模型,发现敲除TRPM2后,肝组织损伤面积降低、肝功能血清学指标趋于正常、炎症指标降低,肝损伤显著缓解(图1)。
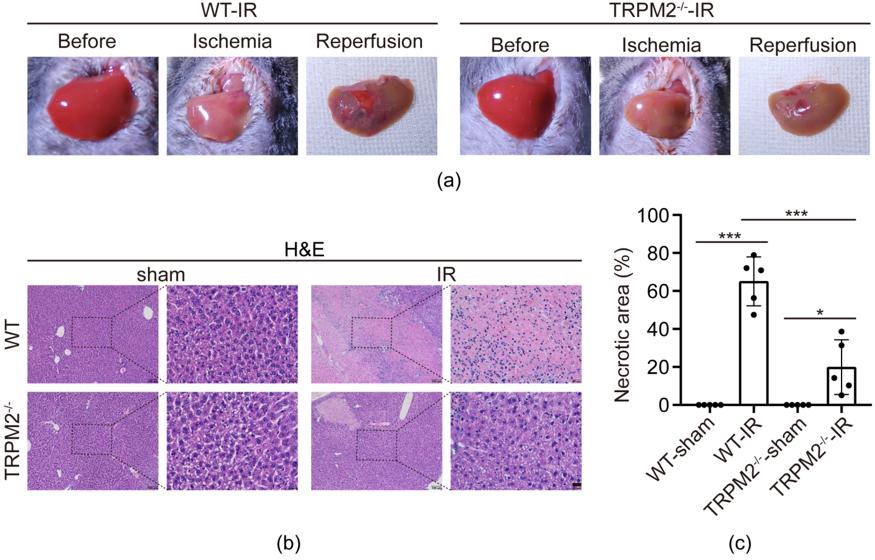
图1 动物模型发现敲除TRPM2显著缓解肝缺血再灌注损伤
为了研究TRPM2介导的肝缺血再灌注损伤的分子机制,研究人员对健康和肝缺血再灌注损伤的肝组织进行转录组分析,经过差异蛋白聚类分析及细胞和动物水平的验证发现TRPM2介导的损伤与铁死亡相关通路密切关联。进一步使用铁死亡诱导剂(1S,3R)-RSL3(RSL3)构建铁死亡细胞模型,发现使用实验室自主设计合成的TRPM2小分子*制剂抑**A10减少脂质过氧化物的累积、铁死亡关键蛋白的异常表达等,表明TRPM2介导肝缺血再灌注过程中铁死亡的发生(图2)。
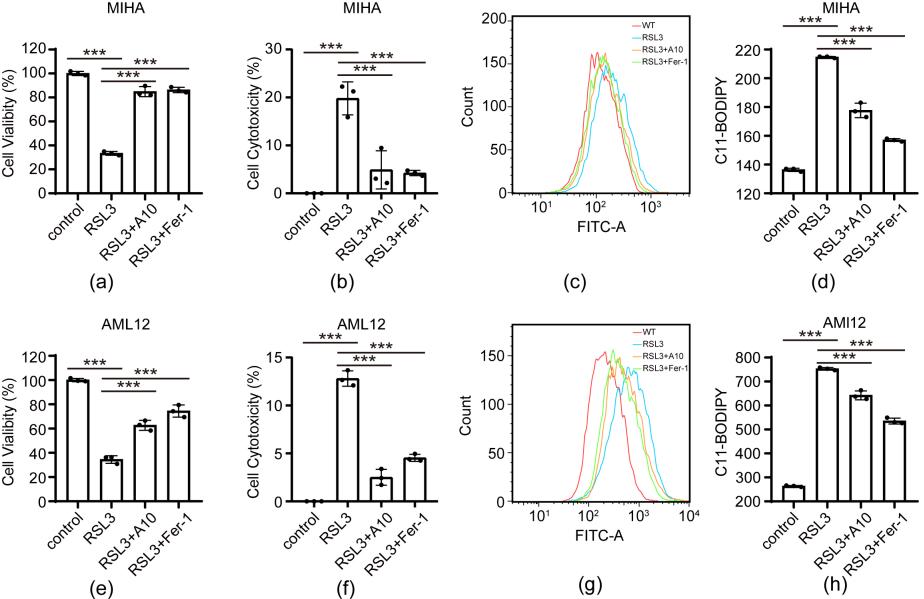
图2 细胞模型发现TRPM2介导肝细胞铁死亡
已有研究认为TRPM2主要通过促进钙离子内流调控下游信号通路,作者细胞模型发现肝缺血再灌注过程中钙离子内流增加,并且主要聚集在线粒体,线粒体累积钙离子后出现明显的脂质过氧化物的累积,促进细胞铁死亡(图3)。并进一步发现钙离子聚集在线粒体后使脂氧合酶ALOX12表达增加,ALOX12是直接催化脂质过氧化的关键蛋白酶,已有研究证实其表达量增加可诱发铁死亡。
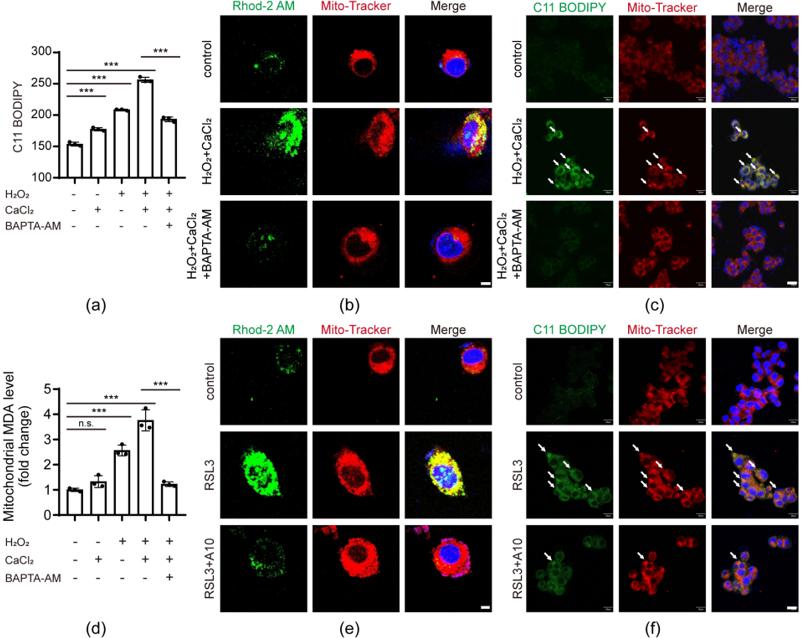
图3 TRPM2诱导钙离子内流并聚集在线粒体进而促进细胞铁死亡
综上所述,肝缺血再灌注过程中,TRPM2被激活,促进钙离子内流,钙离子累积在线粒体,使脂氧合酶ALOX12表达增加,该酶通过促进脂质过氧化直接诱发肝细胞铁死亡,加重损伤。最后,作者在动物水平验证使用TRPM2小分子*制剂抑**A10干预对肝缺血再灌注损伤的影响。结果表明,术前尾静脉注射A10显著缓解肝缺血再灌注损伤,铁死亡*制剂抑**也具有显著缓解该损伤的效果(图4)。
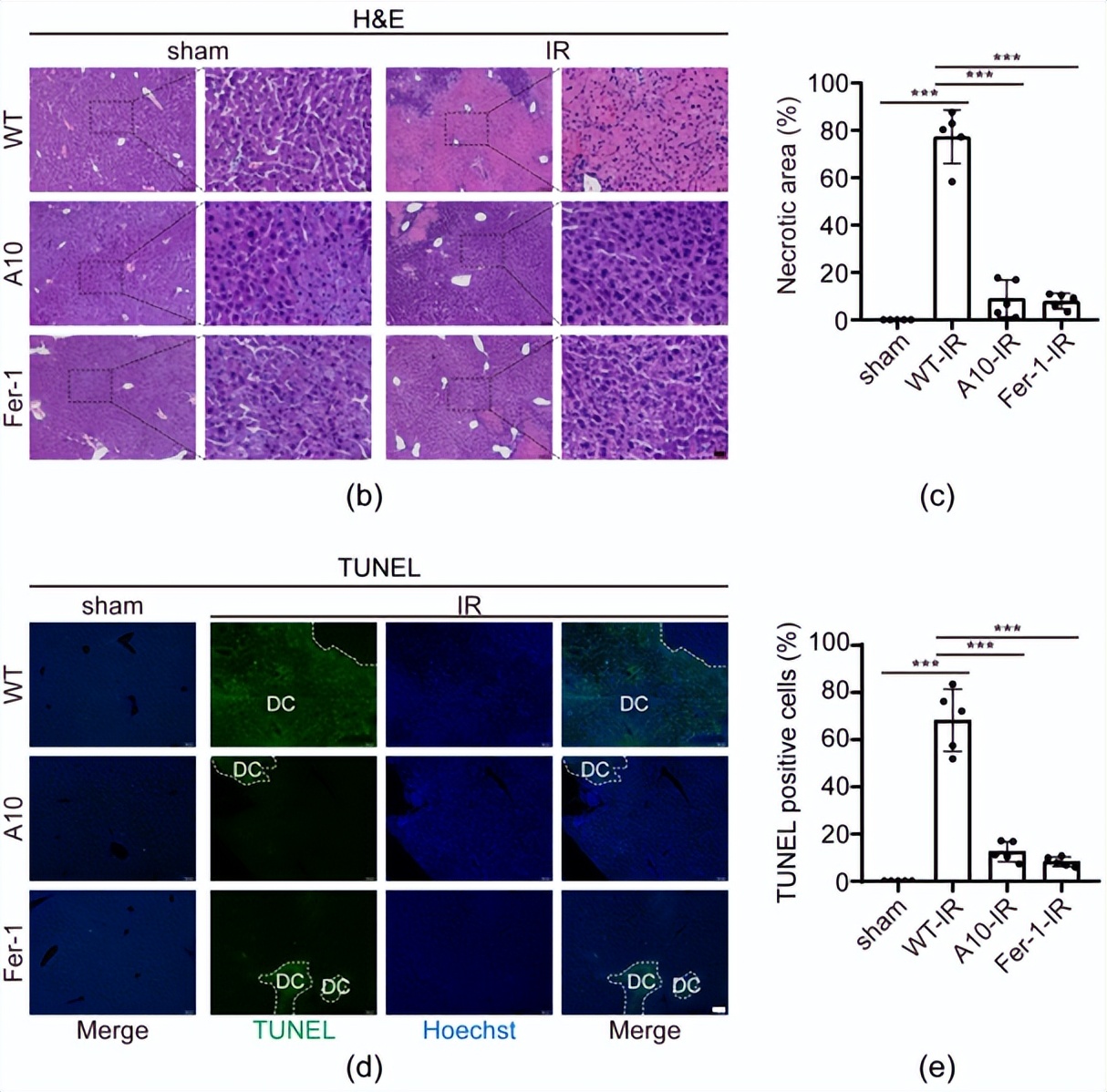
图4 动物模型验证TRPM2小分子*制剂抑**与铁死亡*制剂抑**在肝缺血再灌注损伤*功中**能
未来展望
本研究中,作者在体内外水平证实了TRPM2在肝缺血再灌注损伤中的关键作用,详细阐明了TRPM2介导铁死亡促进肝缺血再灌注损伤的分子机制,进而验证了靶向TRPM2的小分子*制剂抑**A10在缓解肝缺血再灌注损伤中的重要价值,不仅加深对肝缺血再灌注损伤病理生理机制的理解,还为肝缺血再灌注的临床防治提供了新的方向及潜在的靶向药物。
作者简介

余沛霖副教授,现任浙江大学浙江大学公共卫生学院卫生毒理学系副教授,博士生导师。主要研究方向为综合利用毒理学、药理学、生物化学、分子生物学及药物化学等多种手段,揭示氧化应激相关离子通道蛋白的基本特性及其在神经、生殖、呼吸等多个系统中介导多种毒理及病理作用的功能及分子机制,并通过药物筛选和化学修饰的方法找寻特异性配体以进行有效的毒理及病理作用预防及干预(https://person.zju.edu.cn/0012113)。

林辉教授现任浙江大学生物医学工程与仪器科学学院副院长,浙江大学医学院附属邵逸夫医院互联网与人工智能办公室主任,浙江大学医学院附属邵逸夫医院普外科主任医师,浙江大学医学院博士生导师。主要从事肝胆胰肿瘤致病机制研究与精准诊疗技术研发,借助医工信多学科交叉,在外科手术导航、肿瘤靶向治疗以及智慧医疗等领域开展了积极探索(https://person.zju.edu.cn/3307017)。