
阅读文章前辛苦您点下“关注”,方便讨论和分享,为了回馈您的支持,我将每日更新优质内容。

依据水凝胶可以弹性体上产生强韧黏附的特性,可以使用光掩膜法在弹性体Ecoflex上面原位形成水凝胶电路。就是使用光掩膜在Ecoflex表面上形成水凝胶电路的模型示意图。水凝胶的成胶方法与之前类似,并加入溴酚蓝(BPB)做染色剂。
经紫外光引发2h后,可以用流水轻松冲去未反应的水凝胶,进而得到光引发聚合形成的导电水凝胶电路。(b-g)所示,水凝胶电路在接通电源后可以点亮小灯泡。

此外,分别对水凝胶电路进行横向拉伸、斜向拉伸,弹性体Ecoflex和水凝胶电路同时发生形变,但电路依然为通路,灯泡依旧点亮;除去外部施加的应力后,弹性体Ecoflex和水凝胶电路都恢复原始状态,灯泡依旧点亮。利用这种性质,我们可以在弹性体上形成所需的水凝胶电路,得到可拉伸变形的柔性电路。
这一性质大大扩展了柔性电路的应用前景。水凝胶与各种材料之间的黏合对于许多现有的和新兴的应用是必不可少的。其中湿材料(即合成水凝胶和生物组织)之间的强韧黏附正在迅速发展,但仍面临许多问题。

长期以来,水凝胶中水的含量丰富的特点使水凝胶难以黏附到包括其自身在内的大多数材料上。而水凝胶与水凝胶的黏附可以用于水凝胶离子电子学、药物递送和水凝胶修补等诸多方面;水凝胶与生物组织的黏附是生物电子学、组织黏合剂、伤口闭合、生物医学的关键。
锁志刚[58]以藻酸盐(Alg)、1-(3-二甲基氨丙基)-3-乙基碳二亚胺酸盐(NHS)、N-羟基琥珀酰亚胺(EDC)和己二酸二酰肼(AAD)作为胶水以黏合水凝胶,其黏附能通常只有300J/m2左右。
本章以BSA和EDC/NHS为原料制备得到BSA胶水,通过BSA分子和EDC/NHS的扩散和化学交联,以共价键、拓扑连接和能量耗散等方式,实现水凝胶与水凝胶以及水凝胶与生物组织的黏附。本章测试了BSA胶水用于水凝胶与水凝胶、水凝胶与生物组织上的黏附性能,并探究了相关机理。

此外还探索了BSA胶水在水凝胶修补、水凝胶传感器修复以及超级传感器组装上的应用。采用“一锅煮”的方法制备BSA/PAAm双网络水凝胶。具体而言,先加入蛋白质BSA、单体AAm以及交联剂MBA,匀速搅拌至完全溶解。
然后加入光引发剂,继续搅拌至其溶解。随后抽氧充氮三次,注入预先准备的模具中。80℃下水浴十分钟,然后在紫外光(8W,365nm)下引发一小时。即可得到BSA/PAAm双网络水凝胶。其他水凝胶也以上述方法制备。称取一定质量的BSA,置于磁力搅拌器上匀速搅拌至形成淡黄色均匀溶液。分别将EDC和NHS配成500mg/mL的溶液待用。
使用前,分别量取计算好的EDC和NHS溶液,加入到BSA溶液中。轻轻摇匀后,迅速滴加在水凝胶界面上,立即盖上另一个水凝胶或生物组织,然后放入模具中。在25℃的水浴锅中保温反应30分钟。
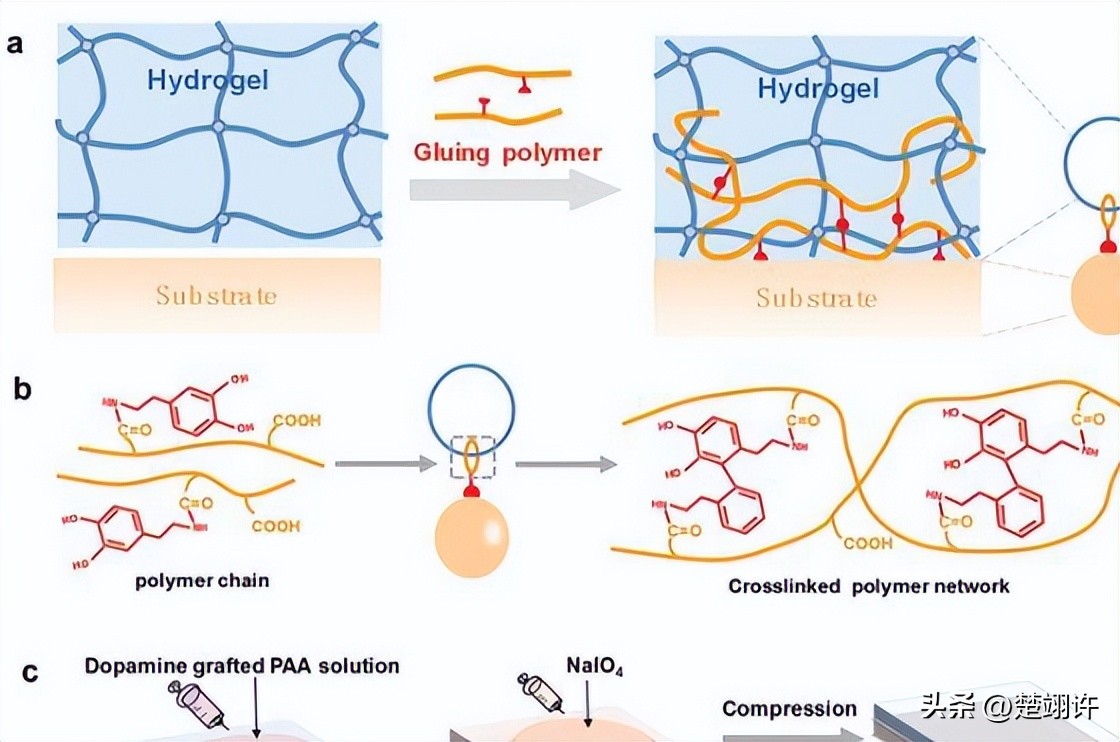
(a)所示,将预先溶解好的EDC和NHS溶液加入BSA水溶液中混合得到BSA胶水,随后迅速滴加在BSA/PAAm双网络水凝胶上,最后立即盖上水凝胶((b))或者生物组织((c)),温室条件下反应一定时间后,就可以通过BSA胶水中BSA分子和EDC/NHS分子的扩散与化学反应可以将水凝胶和生物组织黏合在一起。
(d)是EDC/NHS分子化学交联BSA分子的机理图。具体而言,BSA分子上的羧基与EDC的碳二亚胺基(N=C=N)可以发生化学反应,进而生成一种不稳定的σ-酰基异脲酯,随后该产物又能与NHS发生化学反应生成一种亚稳态的NHS羧酸酯,最后,NHS羧酸酯与另一个BSA分子上的氨基(-NH2)发生化学反应,生成酰胺键(-O-NH-)以交联两个BSA分子。

BSA分子上带有大量的氨基与羧基,因此胶水中的BSA分子不仅可以与胶水中的BSA分子形成化学交联,也可以经过扩散作用与水凝胶中的BSA分子发生反应,此外还可以与其他带有氨基与羧基的材料表面(例如生物组织)产生化学反应并形成化学键,可以得到水凝胶的黏附性能。本章观察了BSA胶水与水凝胶黏附界面的形貌与结构,在BSA胶水中加入溴酚蓝(BPB)以染色和标识BSA分子。
通过BSA胶水的黏合,BSA/PAAm双网络水凝胶之间并没有观察到间隙的存在;从Br元素的能谱中也可以观察到,Br元素在BSA胶水凝胶层中的富集和通过扩散作用在水凝胶两侧的均匀分布。
(c)、(d)所示,BSA胶水在BSA/PAAm双网络水凝胶与PAAm单网络水凝胶的黏合界面中也没有观察到间隙的存在;从Br元素的能谱中可以看到,Br元素在BSA胶水凝胶层和BSA/PAAm双网络水凝胶中有明显的分布,而在PAAm单网络水凝胶中Br元素的含量较少。这可能是胶水中BSA和EDC/NHS因为BSA分子的弱交联而过分扩散,这也是其黏附能较弱的原因。

(f)是BSA胶水在BSA/PAAm双网络水凝胶中室温反应半小时时的偏光显微照片。从中同样可以看到,水凝胶之间没有间隙的存在,并且也观察到了BSA胶水的扩散效果。此外,还通过偏光显微镜观察了不同反应时间下BSA/PAAm双网络水凝胶黏合界面的情况。(g)分别是1min、5min、10min、20min、60min和180min时的偏光显微照片,可以看到。随着反应时间的增加,BSA胶水会逐渐扩散到两侧的水凝胶中。结果证明,在BSA胶水与水凝胶形成黏附的过程中存在着扩散作用。
水凝胶的力学性能
本章系统地考察了经EDC/NHS化学交联的BSA单网络水凝胶和BSA/PAAm双网络水凝胶的力学性能。使用单轴拉伸对两种水凝胶进行拉伸性能的测定。(a)和所示,经EDC/NHS化学交联的BSA单网络水凝胶的拉伸性能较差,其弹性模量(Et)、断裂应力(σt,f)和断裂能(W)分别为85kPa、0.061MPa和0.089MJ/m3,而且其拉伸断裂比(εt,f)仅为1.92。

与之相反,作为水凝胶本体的BSA/PAAm双网络水凝胶的拉伸性能较好,其弹性模量(Et)、断裂应力(σt,f)和断裂能(W)分别为453kPa、0.41MPa和5.02MJ/m3,同时还具有很好的拉伸性能,其拉伸断裂比(εt,f)为22.22。
此外,我们还考察了两种水凝胶的能量耗散行为。从(b)中可以发现,经EDC/NHS化学交联的BSA单网络水凝胶在λ=2时的耗散能(Uhys)为0.018MJ/m3;BSA/PAAm双网络水凝胶在λ=10时的耗散能(Uhys)为0.92MJ/m3,这证明了BSA/PAAm双网络水凝胶具有良好的能量耗散行为。

我们还考察了两种水凝胶的撕裂能。如(c)、(d)所示,经EDC/NHS化学交联的BSA单网络水凝胶的撕裂能(Tt)为246J/m2,而BSA/PAAm双网络水凝胶的撕裂能(Tt)为1323J/m2,这证明了BSA/PAAm双网络水凝胶具有较好的韧性。综合以上结果可以发现,BSA/PAAm双网络水凝胶具有良好的拉伸性能和能量耗散,而作为胶水层的BSA单网络水凝胶也有一定的拉伸性能和能量耗散。
BSA胶水的黏附性能
BSA胶水对BSA/PAAm双网络水凝胶有很强的黏附。本章对BSA/PAAm双网络水凝胶进行剪切黏附测试,(a)可以看到,两个BSA/PAAm双网络水凝胶之间的剪切黏附强度高达250kPa,(b)为剪切黏附测试过程中的照片,可以看到在测试中也出现了明显地应力发白的现象。通过对比BSA胶水对PAAm单网络水凝胶和BSA/PAAm双网络水凝胶的180°剥离测试结果可以发现,BSA/PAAm双网络水凝胶的黏附能是PAAm单网络水凝胶的65倍,其黏附能分别为3997J/m2和61J/m2,这体现了水凝胶中BSA分子的作用。

(e)、(f)分别为两种水凝胶的测试过程,可以看到,BSA/PAAm双网络水凝胶的界面之间明显地应力发白现象,这一结果表明在水凝胶黏附界面和水凝胶本体中存在着较强的能量耗散;而PAAm单网络水凝胶的界面之间则没有应力发白现象。
结果证明,BSA胶水对BSA/PAAm双网络水凝胶之间的黏附属于强韧黏附。本章考察了BSA胶水中的化学交联剂EDC/NHS含量和BSA浓度对水凝胶黏附性能的影响。
中可以看到,当EDC/NHS的含量为6%时,水凝胶的黏附性能最好,其黏附能为2567J/m2,这一结果与本课题组之前的数据相吻合;而当EDC/NHS的含量为0%时,水凝胶的黏附能仅有27J/m2,这体现了BSA胶水中化学交联剂EDC/NHS的作用。
由于当EDC/NHS的含量过低时,BSA分子与胶水中BSA和水凝胶中BSA分子的交联程度过低,导致水凝胶的黏合层的机械性能过低;而当EDC/NHS的含量过高时,BSA分子与胶水中和水凝胶中的BSA分子交联速度过快,影响了BSA分子的扩散及BSA与水凝胶的交联,导致水凝胶的黏合层的机械性能过低,机械性能过低会影响水凝胶的黏附性能。

当胶水中BSA浓度为300mg/mL时水凝胶的黏附性能最好,其黏附能为3997J/m2。当BSA浓度过低时,胶水形成的凝胶层强度较低;而当BSA浓度过高时,胶水形成凝胶层的速度过快,这抑制了BSA和EDC/NHS进一步扩散的效果。
可以看到,BSA胶水的最优配比为:BSA为300mg/mL,EDC/NHS为6%。可以通过(f)中的模具来控制BSA胶水涂层的厚度以探究胶水涂层厚度对水凝胶黏附性能的影响。
和中可以发现,当BSA胶水涂层厚度为200μm时,水凝胶的黏附性能最高,其黏附能为3997J/m2。这是因为当胶水涂层厚度过低时,涂层中的BSA的量不足,难以形成有效的黏附。
而当BSA胶水涂层的厚度过大时,水凝胶之间会存在着比较厚的化学交联BSA凝胶层,而由于经化学交联的BSA单网络水凝胶的力学性能较差,在剥离过程中BSA单网络水凝胶易发生破坏,进而导致水凝胶的黏附性能变差。

此外,我们还考察了测试过程中剥离速率对水凝胶黏附性能的影响可以发现,当剥离速率过低时水凝胶中能量耗散较慢,故其黏附能不高;当剥离速率过高时水凝胶中能量耗散速率跟不上剥离速率,故其黏附能也有所下降。
当剥离速率为50mm/min时,水凝胶的能量耗散速率与剥离速率较为匹配,故而水凝胶的黏附能最高,最优黏附能为3997J/m2。
除此之外,本章还考察了BSA/PAAm双网络水凝胶中BSA含量对水凝胶黏附性能的影响。可以看到,当BSA含量较低时,水凝胶的黏附性能较。
这是因为BSA含量过低,BSA/PAAm双网络水凝胶中的能量耗散较差且可反应基团较少;但BSA含量过高时,胶水中的EDC/NHS更容易与BSA化学交联,这抑制了其扩散效果,故黏附能降低。综上可知,BSA/PAAm双网络水凝胶的最优配比:AAm为30wt%,BSA为400mg/mL。

本章比较了不同凝胶时间对水凝胶黏附性能的影响。随着凝胶时间的增加,BSA胶水与水凝胶之间的黏附能出现先增加后减小的趋势,然后达到稳态。(c)是BSA胶水的流变曲线,可以发现,当12分钟的时候,BSA胶水通过EDC/NHS的化学交联,出现了凝胶溶胶转变点。这一结果与上述结果相呼应,即在10分钟和20分钟之间,黏附能出现了剧增。可以看出,当凝胶时间为30分钟时,BSA胶水与水凝胶的黏附性能最强,这一结果与BSA胶水本身的凝胶时间存在一定的差异性,这体现了BSA胶水在形成黏附过程中的扩散作用。

综上所述,最优的凝胶时间是水凝胶中化学键形成和胶水中BSA以及EDC/NHS扩散共同作用的结果。随后随着凝胶时间的增加,BSA胶水与水凝胶的黏附性能逐渐降低至2000J/m2,到达了稳态平衡。
参考文献:
- Zhou J, Ellis A V, Voelcker N H. Recent developments in PDMS surface modification for microfluidic devices [J]. Electrophoresis, 2010, 31(1): 2-16.
- Chen Q, Liu Z. Albumin Carriers for Cancer Theranostics: A Conventional Platform with New Promise [J]. Advanced Materials, 2016, 28(47): 10557-10566.