编者按
人体疾病纷繁多样,不痛不痒的小毛病有时并不代表没事儿,可能是身体发出的早期警报。在第三届白求恩精神研究会内分泌和糖尿病学分会肾上腺学组年会(暨第二届天津滨海内分泌及代谢论坛)上,华中科技大学同济医学院附属协和医院夏文芳教授分享了一例隐藏20年的疾病真相,一起来看看。

夏文芳教授
患者基本信息
患者男性,43岁,主因“发现左侧*丸睾**增大20年,再发右侧肾上腺占位2个月”就诊。
现病史
患者20年前自觉左侧*丸睾**较右侧增大,无明显不适,未重视。13年前因“胆囊结石”在外院术前检查时发现左侧肾上腺占位,予以左侧肾上腺切除,术后病理提示肾上腺皮质腺瘤。近1年来,患者觉左侧*丸睾**渐增大,可触及包块。2个月前在外院行左侧*丸睾**切除术时,发现右侧肾上腺占位。
既往史
既往有胆囊结石、慢性胃炎、十二指肠溃疡、肝血管瘤。
个人史及婚育史
足月顺产,出生体重及身长均正常,外阴为正常男性表型。母亲孕期无特殊用药史及放射性物质接触史。13岁时身高较同龄男性高,之后身高增长缓慢。吸烟20年,每日20支,否认嗜酒。20年前结婚,婚后1年和8年分别育2女。
体格检查
体温36.6℃,脉搏78次/分,血压125/80 mmHg,身高168 cm,体重64 kg,体重指数(BMI)22.68 kg/m2。浅表淋巴结未及肿大,全身可见皮肤色素沉着,以颊膜、牙龈、腋窝、乳晕色素明显,无满月脸、水牛背、皮肤紫纹等。余查体未见明显异常。左侧*丸睾**缺如。患者自幼觉皮肤黝黑,无特殊不适,未予重视。
辅助检查
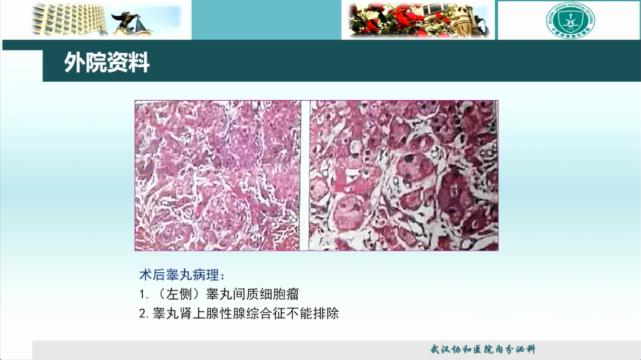
外院*丸睾**、附睾超声示双侧*丸睾**切面形态失常,左、右侧*丸睾**大小分别为4.6 cm×2.3 cm、3.5 cm×1.6 cm,实质回声不均;左侧*丸睾**可见范围4.1 cm×2.1 cm稍高回声区,边界尚清,内部回声不均;右侧*丸睾**可见一大小2.3 cm×1.6 cm稍高回声区,边界尚清,内部回声不均。外院术后*丸睾**病理考虑*丸睾**间质细胞瘤,*丸睾**肾上腺性腺综合征不能排除。
本院肾上腺平扫+增强CT示左侧肾上腺显示欠清,右侧肾上腺轮廓饱满,双侧肾上腺区见多发结节影,密度尚均匀,以右侧为明显,最大者直径约3.0 cm,边缘清晰,CT值约37 Hu,增强呈明显均匀强化。垂体磁共振检查未见明显异常。


诊疗思路及经过
问题1
对于肾上腺占位,如何制定诊疗计划?
肾上腺意外瘤可能是肾上腺皮质和髓质的良、恶性肿瘤以及转移瘤,也可能是感染性疾病、血肿。内分泌科医生需从以下三方面思考:有无内分泌症状和体征?占位是否有内分泌功能?良性还是恶性?基于指南的诊疗路径进行相关检查。
从检查结果来看,血常规、尿常规、大小便常规、肝/肾功能、血糖、血电解质、肿瘤标志物、β-人绒毛膜促性腺激素(β-hCG)均正常,胸片、心电图正常,甲状腺功能及形态(B超)、甲状旁腺激素均正常。性激素检查示黄体生成素(LH)和卵泡刺激素(FSH)水平下降,催乳素(PRL)、孕酮(PROG)、雌酮(E1)水平升高,提示患者病变与性激素水平异常有一定关联。
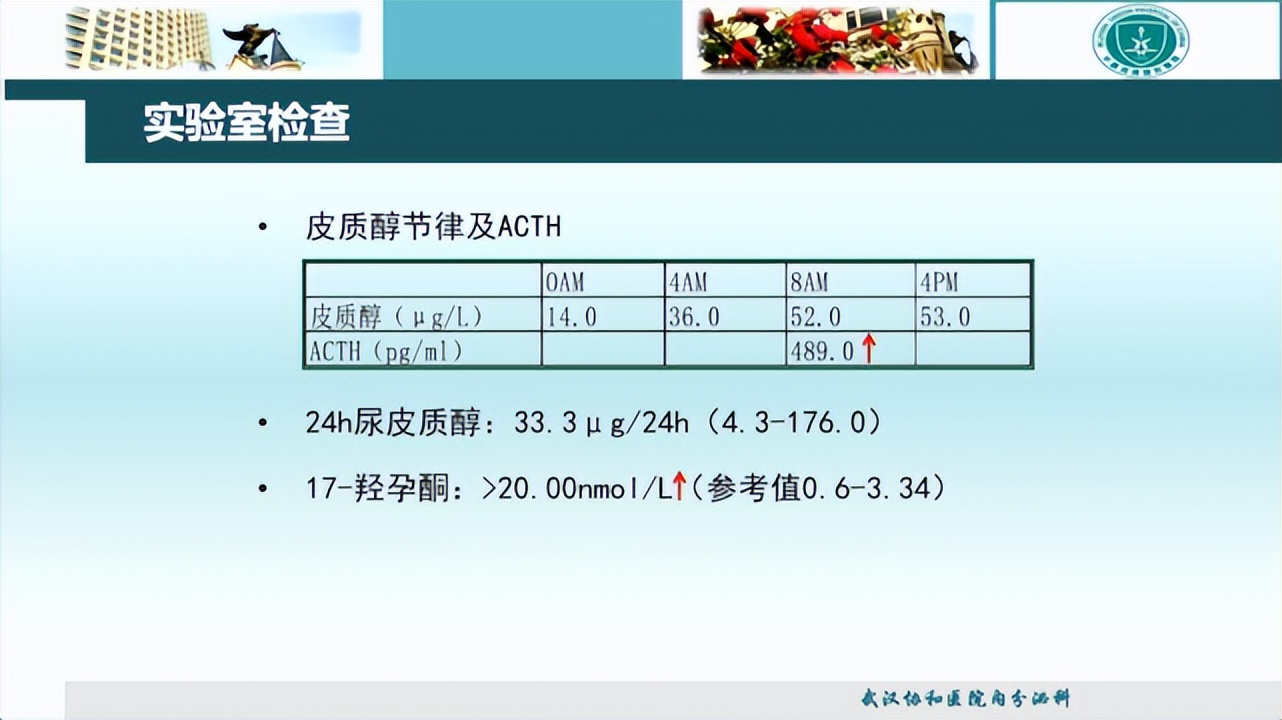
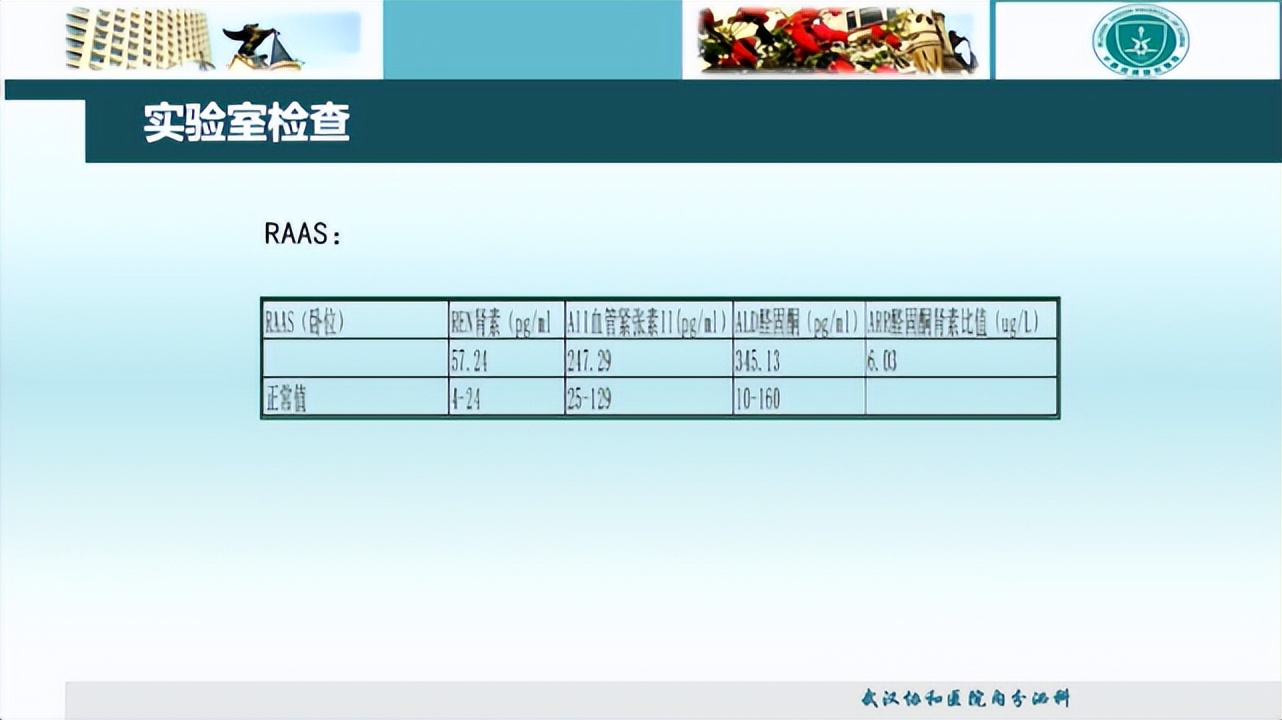
皮质醇节律及促肾上腺皮质激素(ACTH)检查发现,ACTH水平明显升高,血皮质醇水平基本正常。24h尿皮质醇正常。因患者存在肾上腺占位,对其常规行17-羟孕酮(17-OHP)检查,结果>20 nmol/L。肾素-血管紧张素-醛固酮系统(RAAS)检查示醛固酮/肾素比值(ARR)6.03,判断患者醛固酮肾素水平基本正常。

问题2
基于激素水平检测,考虑什么疾病?
由于患者17-OHP明显升高,而17-OHP是21-羟化酶缺乏症(21-OHD)的特异性诊断指标和主要治疗监测指标。基础17-OHP检测值可被划分为3个区段来指导21-OHD的诊断和分型:
>300 nmol/L(10000 ng/dl):典型的21-OHD
6~300 nmol/L(200~10000 ng/dl):非典型的21-OHD(NCAH)
<6 nmol/L(200 ng/dl):不支持先天性肾上腺增生症(CAH)或为NCAH
根据该患者无典型症状以及17-OHP>20 nmol/L,考虑诊断为NCAH。
指南推荐采用标准17-OHP检测进行筛查,需要时应行ACTH兴奋试验以确诊。如结果仍不确定或用于遗传咨询时,可进行基因分型。对该患者行ACTH兴奋试验,结果显示其各个时间点的17-OHP水平均高于正常值,皮质醇和脱氢表雄酮(DHEA)水平无明显升高。又对患者家系进行基因检测,发现患者本人及其母亲、姐姐、两个女儿均属于杂合突变,患者CYP21A2基因呈复合型杂合突变,突变位点为CYP21A2 c.196_197insT的杂合核苷酸变异。

根据以上检查结果,患者被诊断为先天性肾上腺增生症(21-羟化酶缺乏)伴*丸睾**肾上腺残余肿瘤,即CAH(21-OHD)-TART,这是一种常染色体隐性遗传性疾病。
CAH是由于肾上腺皮质类固醇合成通路各阶段各类催化酶的缺陷,引起皮质类固醇合成障碍,以21-OHD最常见。世界范围内,典型的21-OHD发病率约为1:15000,非典型的21-OHD发病率约为1:1000。
21-OHD由编码21-羟化酶(P450c21)的CYP21A2基因突变引起,导致皮质醇低下,经负反馈使ACTH分泌增加,刺激肾上腺皮质细胞增生。雄激素合成通路无缺陷,在高ACTH刺激下,堆积的17-OHP和孕酮向雄激素转化增多(旁路代谢亢进),进而引起高雄激素血症。盐皮质激素合成通路阻滞,使孕酮不能向醛固酮转化,导致醛固酮水平低下。
该患者皮质醇水平低下并不显著,反而ACTH水平明显升高;高雄激素血症不显著,反而雌激素水平明显升高。查阅资料发现,高雄激素血症患者体内可发生自我代偿,可表现为过度芳香化,进而导致雌激素水平升高。而雌激素水平升高会抑制LH和FSH的分泌,这时雄激素水平升高反而不显著。这可以部分解释该患者性激素检查所示低LH、低FSH及高雌激素水平。醛固酮水平低下更常见于典型的21-OHD患者,该患者并未出现。21-OHD临床表现多样,其酶缺陷程度因基因型而异;大部分患者为NCAH,该病例即如此。


问题3
CAH为什么会有*丸睾**的改变?
肾脏、肾上腺和性腺共同起源自中胚层的泌尿生殖嵴,在胚胎发育过程中,肾上腺细胞迁徙途经部位或在原始性腺内可有肾上腺皮质细胞残留,成为异位的肾上腺皮质残余组织。在正常人体内,这些残余组织不再生长;但在CAH患者中,在高ACTH刺激下,可发生*丸睾**内肾上腺残余瘤(TART)。若CAH合并性早熟,应警惕TART。CAH男性患者3岁后每年行*丸睾**B超检查,尤其在围青春期,避免影响生育能力。
该患者既幸运,又不幸。幸运的是,其病情并不太严重,故婚后仍保持生育能力;不幸的是,早在20年前其*丸睾**即增大,但未予以重视,导致之后经历多次手术,*丸睾**问题仍未解决,且右侧肾上腺再发肿瘤。
问题4
如何治疗?切或不切?
根据2018年美国内分泌学会CAH指南,CAH的经典治疗为皮质醇替代治疗。替代治疗的剂量和方案应结合年龄和发育期个体化设定,并尽可能控制在最低有效剂量,避免对生长抑制和发生医源性库欣综合征。

该患者面临的紧迫问题是需要抑制ACTH分泌,避免肾上腺及*丸睾**肿瘤进一步增大。遂予以其地塞米松0.75 mg qd治疗,3个月后复诊ACTH正常,降至6.7 pg/ml,调整地塞米松剂量为0.375 mg qd,并维持至今。
随访时主要监测17-OHP和雄烯二酮,17-OHP可反映ACTH被抑制状态,但需综合判断。抑制过高的ACTH一直是CAH替代治疗的难点之一,但国际诊治共识中未将ACTH列入治疗监测项目。*丸睾**、肾上腺的影像学检查已被列为CAH必要的随访项目。2年后对患者进行随访,虽然其仅用地塞米松0.375 mg qd治疗,但影像学检查对比治疗前后的肾上腺肿瘤发现右侧明显缩小、左侧也有缩小。
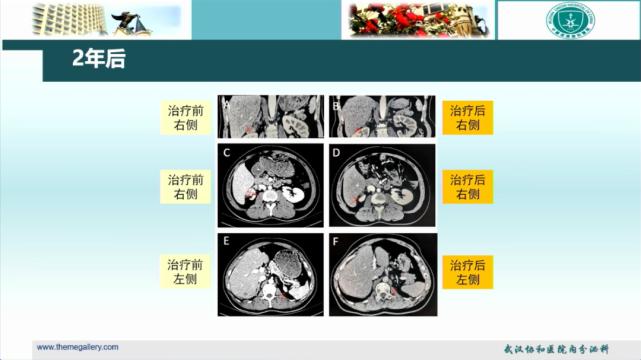
该患者还需考虑手术吗?TART受ACTH影响,一般临床可通过药物调节激素水平使TART缩小并消失,一般不建议行双侧肾上腺切除。当肾上腺肿块直径>7 cm或激素治疗后肿瘤仍在进展,或有可疑恶变征象时,建议进行肾上腺切除术。*丸睾**肿块如激素治疗无效或病灶虽缩小却不消失,或病变对*丸睾**功能产生明显影响时,可行剔除术。
小结
本例患者历时20年,经过两次外科手术后方得确诊,因此,需要对该类疾病及时反思与分析。男性若过早出现阴毛、胡须、*疮痤**、早期出现生长加速等症状,应高度警惕CAH的可能。2016年欧洲肾上腺意外瘤指南建议,所有患者都应详细询问病史和进行体格检查,尤其是生长参数和性腺功能检查。对于*丸睾**占位性病变,需警惕肾上腺来源可能。

专家简介
夏文芳 教授
主任医师,华中科技大学同济医学院附属协和医院内分泌科副主任、诊断教研室副主任。美国乔治亚医学院分子医学和遗传学研究所博士后。中华医学会内分泌学分会骨质疏松学组委员,中华医学会糖尿病学分会流行病学组、教育学组委员,中国女医师协会糖尿病专业委员会委员,中国老年医学学会骨与关节分会委员,湖北省医学会糖尿病分会常务委员,武汉市医学会内分泌学分会副主任委员。人民卫生出版社国家医学教育题库命题专家。从事内分泌及代谢性疾病临床、研究、教学20余年。主持多项国家、省部级自然科学基金项目及教改项目,研究结果已在国际期刊JCB、PNAS、JBMR等杂志发表。获得全国“优秀住培指导老师”、湖北省一流课程负责人。
声明:本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该等信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。