
医脉通编译整理,未经授权请勿转载。
研究一
程序性细胞死亡蛋白-1(PD-1)及其配体(PD-L1)抗体是极具代表性的免疫检查点*制剂抑**,在癌症免疫治疗史中更是具有里程碑的意义。然而,PD-1*制剂抑**在未经选择的实体瘤患者中,有效率只有10%至30%,而起初具有良好治疗效果的患者,随着药物的长期使用也可能产生耐药。因此如何提高有效率及攻克其耐药性是国内外癌症专家共同关注和亟待解决的问题。
日前,西奈癌症中心的研究人员进行的一项新研究已经确定了一种药物--FDA批准的药物达沙替尼(dasatinib),极大地增强了抗PD-1治疗其他癌症的免疫疗法的治疗效果。他们的研究结果以“Targeting DDR2 enhances tumor response to anti–PD-1 immunotherapy”为题发表在《Science Advances》上。
研究背景
抗程序性死亡-1(PD-1)受体及其程序性死亡配体(PD-L1)的抗体药物,主要是通过克服患者体内的免疫抑制,重新激活患者自身的免疫细胞来*伤杀**肿瘤。
不可控的免疫反应或过度表达的自身抗原可引起炎性组织损伤和自身免疫性疾病,为了防止这种情况的发生,机体的免疫反应受到刺激和抑制信号之间的平衡调节,这些信号被统称为免疫检查点。
免疫检查点是免疫激活的重要调节因子,它们在维持免疫平衡和预防自身免疫性疾病中起着关键作用。活化的T细胞是免疫效应功能的主要介质。T细胞表达多个共抑制受体,如淋巴细胞活化基因3(lymphocyte-activation gene 3,LAG 3),PD-1和CTLA-4。机体利用这些免疫检查点分子来调节T细胞对自身蛋白、慢性感染以及肿瘤抗原的反应。不同免疫检查点分子的作用通路并不同。
早在去年,王洁教授团队利用TCGA和ICGC数据库,分析了不同DDR通路基因变异与TMB和新生抗原的关系,以及在免疫治疗疗效预测中的意义。DDR通路中任意一个基因突变被定义为该DDR通路突变,8条通路中任意一条通路突变与TMB和新抗原水平升高显着正相关。
单一DDR通路基因变异的中位TMB值为52(基于TCGA的WES数据),低于既往研究定义的TMB-H的水平。该研究将TMB前25%定义为TMB-H,通过ROC曲线发现,2条通路共突变时对TMB-H和新生抗原的预测灵敏度和约登指数最大,提示2条通路(DDR2基因)共突变可以更好的预测TMB-H和高的新抗原水平更高,免疫治疗获益可能性更高。
DDR2 是一种由纤维胶原蛋白激活的受体酪氨酸激酶, 因此在胶原细胞相互作用的调节中起着关键作用。DDR2通过诱导癌细胞扩散和生长来帮助肿瘤侵入健康组织。虽然其受到几种FDA批准的受体酪氨酸激酶*制剂抑**的抑制, 但由于达沙替尼在体外和体内都是DDR2最有效的*制剂抑**, 而且其在肿瘤临床试验中的使用情况也很普遍, 因此我们的研究中选择了达沙替尼。
研究介绍
研究人员发现,用达沙替尼来耗尽DDR2,他们能够通过结合两种药物来提高癌细胞对抗PD-1治疗的敏感性,这比单独使用两种药物要有效得多。候选基因DDR2通过shRNA介导的敲除和用dasatinib(达沙替尼)进行药理抑制试验。
通过五种不同的肿瘤组织——膀胱、乳房、结肠、肉瘤和黑色素瘤——在小鼠体内的同种基因模型—研究表明,与单药治疗相比,DDR2的消耗增加了抗-PD-1治疗的敏感性。用抗-PD-1和DDR2酪氨酸激酶抑制因子dasatinib联合治疗肿瘤小鼠,导致了肿瘤负荷的降低。
进一步探索发现,RNA-seq和CyTOF分析显示,在DDR2缺失的肿瘤中和联合抗-PD-1治疗的患者中,有较高的CD8+T细胞群。在这两种情况下,靶向DDR2和抗-PD-1治疗被证明是非常有效的跨多种不同类型的癌症在临床前的体内模型。
癌症的新一代免疫治疗方法突出了实验室发现的重要性,它们可以在临床上快速检测,跨越多种疾病类型,为患者提供免疫治疗本身可能无法达到的最佳效果。这项研究也为肿瘤免疫治疗提供了新的思路和方法,为提升治疗效果、改善疾病预后提供了非常有意义的参考和借鉴。
研究二
近日,著名期刊《自然·医学》刊登了耶鲁大学医学院陈列平团队的研究。
在这个研究中,王俊和孙静玮博士等报告了一个全新的、广泛存在于多种肿瘤中的免疫抑制分子Siglec-15。
Siglec-15不是个简单的免疫抑制分子,它的表达水平竟与PD-L1的表达是互斥的。简单来说,对绝大多数肿瘤而言,有PD-L1高表达就没有Siglec-15;有Siglec-15高表达就没有PD-L1。

陈列平教授
这就意味着,那些对PD-1/PD-L1抗体不响应的肿瘤,Siglec-15抗体可能就是它们的克星。
Siglec-15抗体的抗癌作用可能是PD-1/PD-L1抗体互补的,而不是PD-1/PD-L1抗体的另一个翻版。
第一个人源化Siglec-15抗体NC318的临床1/2期研究(NCT03665285)已在2018年底招募患者。
临床试验招募页面
近年来,靶向肿瘤微环境免疫抑制的免疫疗法已经在癌症治疗上取得不小的成功,其中最有代表性的就是靶向PD-1/PD-L1通路的免疫检查点*制剂抑**。
尽管如此,科学家也注意到,PD-1/PD-L1抗体只对少于40%的实体瘤有作用,寻找能弥补PD-1/PD-L1抗体不足的新靶点迫在眉睫。
很多的研究都证明,这样的靶点应该是广泛存在的。肿瘤微环境中除了PD-L1高表达之外,缺少*伤杀**性T细胞、调节性T细胞积累、肿瘤相关巨噬细胞和髓源性抑制细胞的聚集,以及抑制性分子、细胞因子、代谢产物的上调,免疫刺激分子的下调等,都能成为解决免疫抑制的新靶点。
不过,有个问题是,上述的许多机制缺乏肿瘤微环境特异性,靶向这些途径可能会导致免疫系统的广泛激活,最终导致自身免疫疾病。
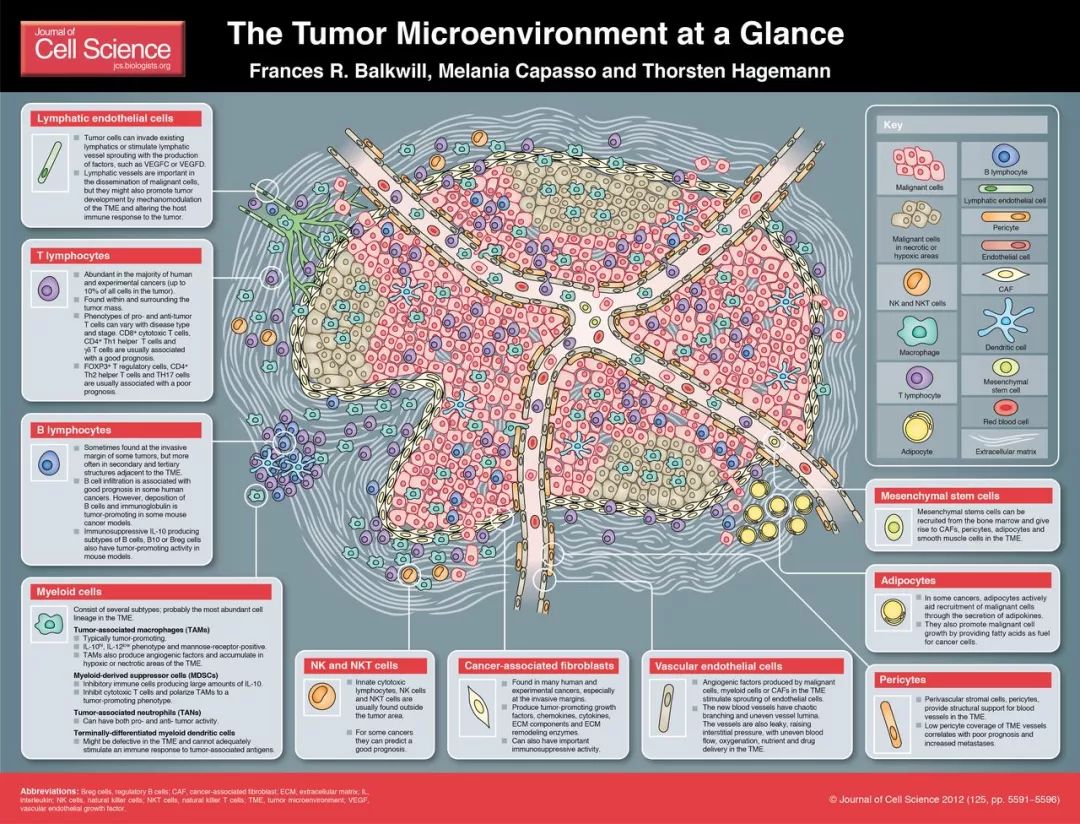
复杂的肿瘤微环境
为了在体外筛选到调节T细胞活性的细胞表面分子,研究人员首先构建了一个高通量筛选平台(genome-scale T cell activity array, TCAA)。这个TCAA包含了超过6500个人类基因,涵盖了90%的跨膜蛋白。
平台搭建完成之后,研究人员首先用之前已经发现的T细胞激活或抑制蛋白,证实了这个系统的可靠性没问题。然后开始大规模的筛选工作,发现Siglec-15这个跨膜蛋白可以持续抑制T细胞的活性,并且表现出了满足正常化癌症免疫治疗的主要特征。因此,研究人员决定从这个蛋白入手试试看。
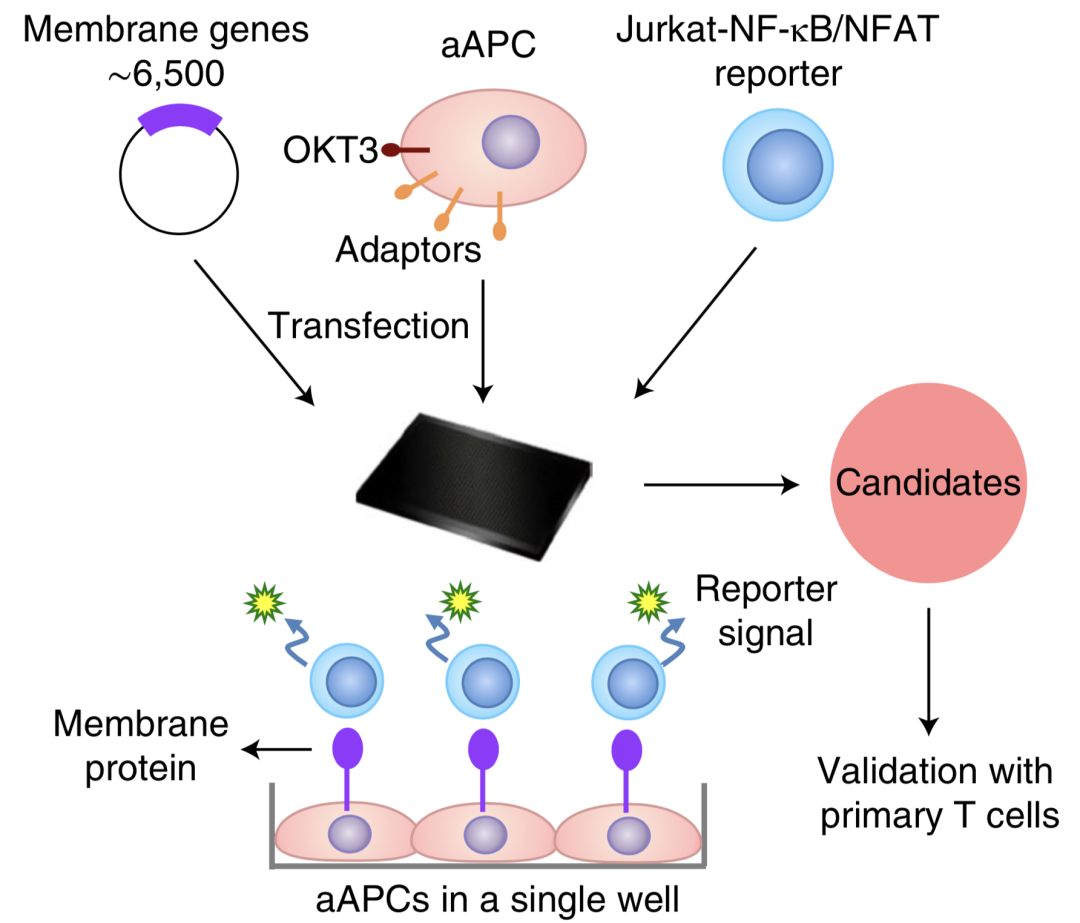
筛选平台示意图
这第一步,就是分析它的分布。分析各种细胞的RNA表达情况,研究人员发现,Siglec-15在绝大多数人体正常组织和各种免疫细胞亚群中的表达很少,但巨噬细胞是个例外。
同时,研究人员还利用TCGA数据库的数据,做了个Meta分析。他们发现,在人体多种肿瘤中,Siglec-15的mRNA表达量都是升高的。例如:肠癌、子宫内膜样癌、甲状腺癌、膀胱癌、肾癌、肺癌和肝癌等等。
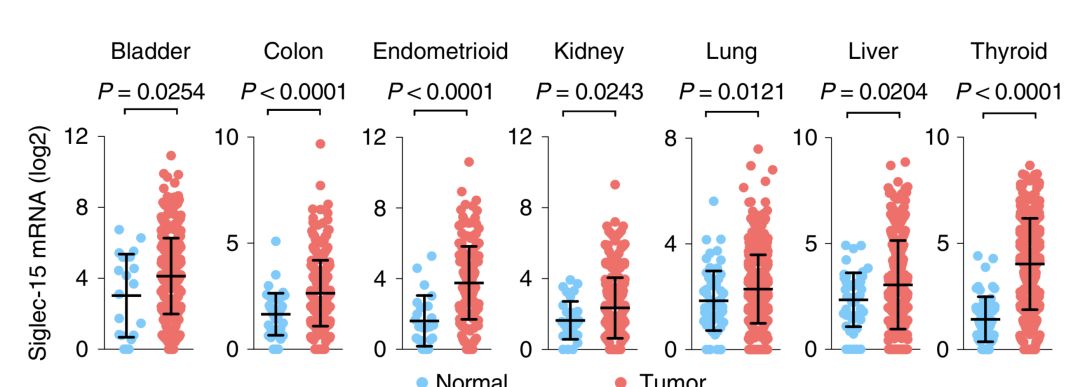
为了进一步确认,研究人员还找到了241个人体非小细胞肺癌肿瘤组织样本,做了免疫组化分析。结果,他们在肿瘤细胞、肿瘤相关的基质细胞,以及肿瘤相关的髓系细胞上发现了Siglec-15的身影。
更有意义的是,研究人员发现PD-L1的表达与Siglec-15的表达之间没有相关性,只有3.2%的组织中两者均存在。这暗示,二者之间可能是互斥的关系,靶向Siglec-15的药物,有可能恰好是PD-1/PD-L1抗体的有力补充。
Siglec-15的这种分布特点让它具备了PD-1/PD-L1一样的优点,是个属于肿瘤微环境的选择性靶点。小鼠体内敲除Siglec-15基因没有引发自身免疫疾病,也证实了这一点。
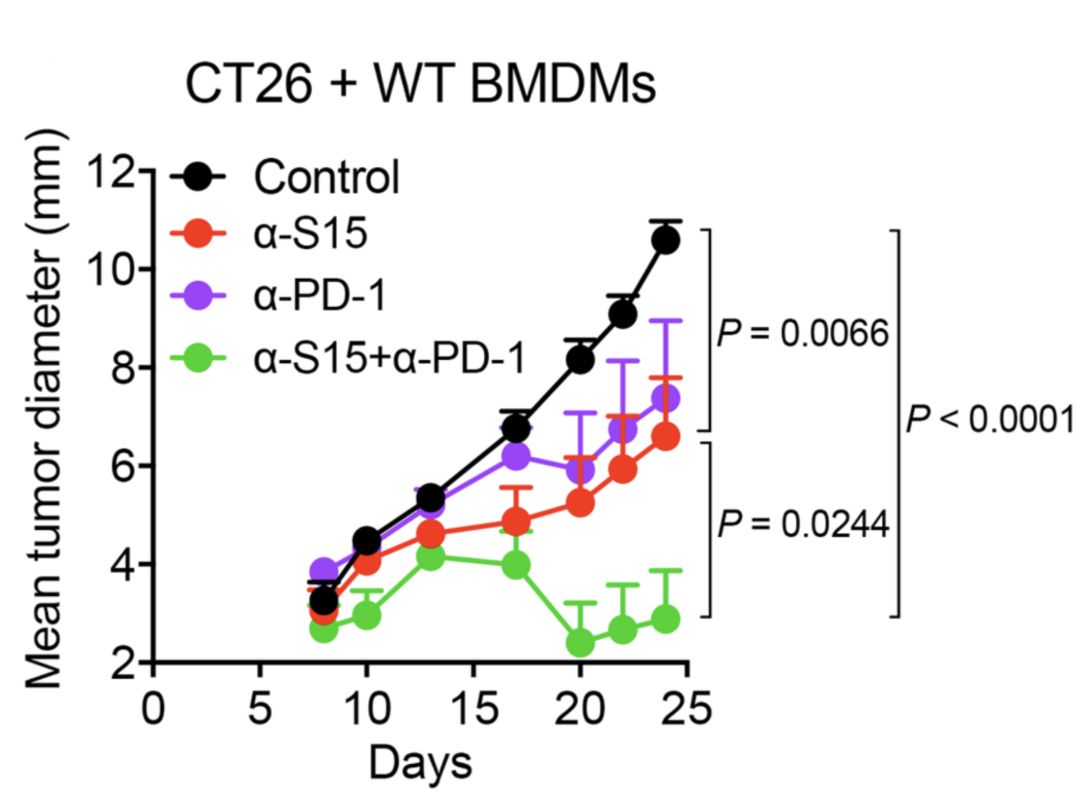
Siglec-15抗体α-S15在小鼠模型上抑制肿瘤生长效果与PD-1抗体持平
二者联合效果更赞
随后研究人员分别在Siglec-15敲除的小鼠身上,以及使用Siglec-15抗体α-S15阻断的方法,证明抑制Siglec-15的表达或者活性,可以提高小鼠抵抗多种肿瘤的能力。
通过分析,研究人员发现阻断Siglec-15之后,肿瘤中的CD8阳性T细胞和自然*伤杀**细胞显著增加,而Treg、CD4阳性的T细胞,以及自然*伤杀**T细胞和B细胞没有增加。还有一些免疫抑制细胞有所减少。而且,CD8阳性T细胞的IFN-γ等细胞因子的产生能力也显著提升。
如果用特异性抗体去除CD8阳性T细胞的话,那么阻断Siglec-15对肿瘤的生长就不会有任何影响了。
以上数据证明,阻断Siglec-15可以让肿瘤微环境的免疫正常化,且不会引起严重的自身免疫反应。
参考来源:
[1].Jun Wang, Jingwei Sun, et al. Siglec-15 as an immune suppressor and potential target for normalization cancer immunotherapy.[J]. Nature Medicine, 2019.
[2].https://www.clinicaltrials.gov/ct2/show/NCT03665285?term=03665285&rank=1
[3].Dong H, Strome S E, Salomao D R, et al. Tumor-associated B7-H1 promotes T-cell apoptosis: a potential mechanism of immune evasion.[J]. Nature Medicine, 2002, 8(8): 793-800.
[4].Chen L, Han X. Anti–PD-1/PD-L1 therapy of human cancer: past, present, and future[J]. Journal of Clinical Investigation, 2015, 125(9): 3384-3391.
[5].Megan M. Tu, Francis Y. F. Lee, Robert T. Jones, et al. Targeting DDR2 enhances tumor response to anti–PD-1 immunotherapy. Science Advances 20 Feb 2019
推荐阅读
1. 一表读懂:小儿骨髓增生异常综合征
2. 血液药物最新国际进展
3. 一表读懂:低血浆血管性血友病因子(VWF)两大情况

点击下方“阅读全文”了解更多