
作者:蓝鲸晓虎
本文为作者授权医脉通发布,未经授权请勿转载。
 与全身使用相比,激素吸入给药通常不引起严重不良反应,但与细胞色素P4503A4*制剂抑**联用时,可能引起激素体内积聚诱发下丘脑-垂体-肾上腺轴抑制。本文介绍一例使用利托那韦加强抗逆转录病毒疗法的患者使用氟替卡松吸入剂后发生医源性库欣综合征的病例。
与全身使用相比,激素吸入给药通常不引起严重不良反应,但与细胞色素P4503A4*制剂抑**联用时,可能引起激素体内积聚诱发下丘脑-垂体-肾上腺轴抑制。本文介绍一例使用利托那韦加强抗逆转录病毒疗法的患者使用氟替卡松吸入剂后发生医源性库欣综合征的病例。
案例呈现
40岁男性,因半年来体重增加、腹部及四肢出现纹路到内分泌科就诊(2013.1)。
➤简要病史
慢性阻塞性肺病和物质滥用(酒精、*草烟**和静脉注射*洛因海**)。患者于25岁时诊断为HIV-1感染。33岁开始用洛比那韦/利托那韦400mg/100mg bid,沙奎那韦1000mg bid,替诺福韦300mg/天1次。就诊前最近一次CD4+T细胞计数为518/mm3,HIV1 RNA无法检出。
35岁时患者被诊断为慢性阻塞性肺病(COPD),使用氟替卡松/沙美特罗250µg/50µg bid,噻托溴铵18µg qd进行治疗。一年后出现右股骨头缺血性坏死,并进行了全髋关节置换术。
患者于2013年1月首次就诊(已使用吸入激素5年)。主诉腹部和颈部体积逐渐增大,6个月内体重增加15kg,腹部和四肢出现条纹、乳房发育、脚踝水肿、勃起功能障碍。体检发现多毛、“满月”脸、向心性肥胖(BMI 35kg/m2)、颈背部脂肪增多、近端肌肉萎缩、腹部、手臂和大腿出现宽大、形态各异的紫癜纹、高血压。

(向心性肥胖、腹部宽大及形态各异的紫色纹理)
➤辅助检查
血清和尿皮质醇及低血清促肾上腺皮质激素(ACTH)浓度偏低,表明HPA轴受抑制。此外,还检测到血脂异常和高促性腺激素性性腺功能减退(见下表)。骨密度扫描(BDS)显示骨密度降低(腰椎Z评分为-3.6),符合骨质疏松。
主要实验室检查结果变化趋势
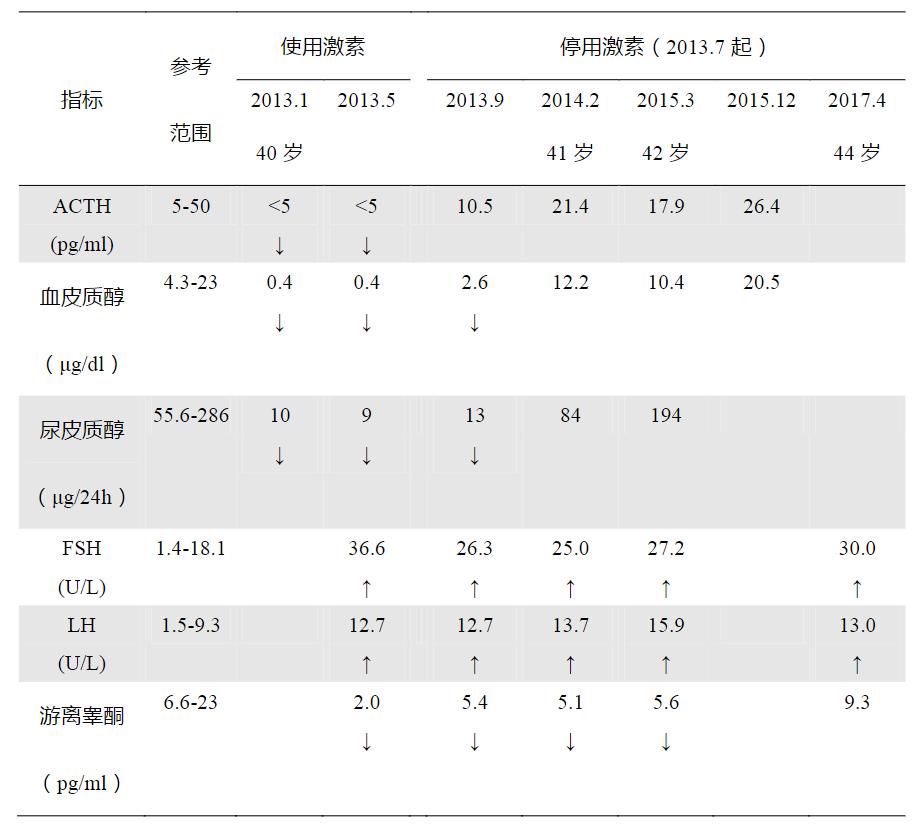
➤如何进行鉴别诊断
根据上述发现,诊断为吸入氟替卡松继发的医源性库欣综合征。
对于接受抗病毒治疗患者库欣综合征的鉴别诊断,需要考虑ART相关的脂肪代谢障碍,HIV相关性脂肪代谢障碍表现为外周肌萎缩。而激素引起的脂肪代谢障碍表现为体重增加,向心性脂肪分布和背部脂肪增厚。本例患者的临床表现均指向库欣综合征。血尿、皮质醇和促肾上腺皮质激素浓度异常明确了这一诊断。
还必须区分医源性和内源性库欣综合征。医源性库欣综合征时,过量的外源性糖皮质激素对下丘脑和垂体产生负反馈,内源性皮质醇合成受到抑制,ACTH和皮质醇浓度降低。然而,如果患者正在服用氢化可的松,血皮质醇浓度并不能区分皮质醇的来源,其他类固醇激素也可能干扰测定结果。
➤治疗与随访
逐渐减少氟替卡松的剂量,同时启动降压和他汀类药物治疗。
使用减半剂量的氟替卡松4个月后,患者仍表现为HPA轴抑制,于是继续减量,最终停用氟替卡松/沙美特罗。
2013年7月改用吲达卡特罗(长效β受体激动剂)150µg qd。9月时,库欣综合征症状好转,血清和尿皮质醇接近参考值,ACTH恢复正常。2017年4月最近一次随访,实验室检查除了FSH、LH持续偏高外,睾酮已恢复正常。
CYP3A4*制剂抑**与激素的相互作用
本病例描述了由利托那韦和氟替卡松之间的相互作用引起医源性库欣综合征并发多灶性骨坏死。
利托那韦是肝CYP3A4的强效*制剂抑**,可增加联合抗逆转录病毒药物中其他蛋白酶*制剂抑**的浓度,并提高HIV治疗的成功率。但利托那韦也能增加糖皮质激素的浓度,因为后者也是CYP3A4的底物。因此,这种相互作用可导致代谢受损和全身激素蓄积、肾上腺功能抑制和库欣综合征。
与其他吸入性皮质类固醇相比,氟替卡松对HPA轴的抑制作用最强,与药代动力学特性——糖皮质激素受体结合力高,半衰期长、亲脂性强,因而与分布容积更大有关。这些特点有助于氟替卡松的全身蓄积,使其易受药物相互作用的影响。
CYP3A4*制剂抑**
CYP3A4是CYP3A亚家族的主要成员,也是成人肝微粒体CYP450中最重要的成分,约占其总量的30%-40%,居第1位,甚至有的个体CYP3A4含量可达到P450总量的60%。该酶主要表达在小肠、肝脏和肾脏。可按作用强度对CYP3A4*制剂抑**进行分类:
强效*制剂抑**(引起药物血浆AUC值至少增加5倍或清除率降低80%以上)
-
蛋白酶*制剂抑**:利托那韦、茚地那韦、奈非那韦、沙奎那韦
-
抗生素:克拉霉素、泰利霉素、氯霉素
-
唑类抗真菌药:酮康唑、伊曲康唑、泊沙康唑、伏立康唑
-
其他:奈法唑酮(抗抑郁药)
中效*制剂抑**(引起血浆AUC值至少增加2倍或清除率降低50%-80%)
-
抗心律失常药(胺碘酮、决奈达隆、维拉帕米、地尔硫䓬)
-
大环内酯类抗生素(红霉素)
-
唑类抗真菌药(氟康唑、咪康唑)
-
其他:西咪替丁、环丙沙星、环孢菌素、氟伏沙明、伊马替尼
弱*制剂抑**(引起血浆AUC值增加1.25~2倍,或清除率降低20%-50%)
丁丙诺啡、西洛他唑、加巴喷丁、雷尼替丁、雷诺嗪、他克莫司、替格瑞洛、丙戊酸、氨氯地平
未指明效力
*麻大**二酚、米非司酮、诺氟沙星
发生不良反应后的处理
发生医源性库欣综合征后,干预方法包括使用另一种不抑制CYP3A4的抗逆转录病毒替代利托那韦,或在维持利托那韦的基础上更换氟替卡松,如改用对CYP450代谢依赖性较低的吸入性皮质类固醇激素(如倍氯米松)、白三烯拮抗剂(如孟鲁司特)或抗胆碱能药物(如噻托溴铵)舒张支气管。
需暂停激素治疗时,应逐步减量。外源性皮质类固醇抑制HPA轴,随着外源性皮质类固醇激素的突然停止,HPA轴不能迅速产生内源性皮质醇,从而导致急性肾上腺功能不全。
综上,在接受利托那韦(或其他CYP3A4*制剂抑**)的患者中,避免使用激素治疗,包括鼻内或吸入剂等“非全身性”给药途径。因气道病变必须使用吸入激素时,氟替卡松不宜作为首选。


参考文献
1. Figueiredo J, Serrado M, Khmelinskii N, do Vale S. Iatrogenic Cushing syndrome and multifocal osteonecrosis caused by the interaction between inhaled fluticasone and ritonavir. BMJ Case Rep. 2020; 13(5): e233712.
2. Mahlab-Guri K, Asher I, Gradstein S, et al. Inhaled fluticasone causes iatrogenic Cushing’s syndrome in patients treated with ritonavir. J Asthma 2011; 48: 860–32
3. Epperla N, McKiernan F. Iatrogenic Cushing syndrome and adrenal insufficiency during concomitant therapy with ritonavir and fluticasone. Springerplus 2015; 4: 455.
4. Saberi P, Phengrasamy T, Nguyen DP. Inhaled corticosteroid use in HIV-positive individuals taking protease inhibitors: a review of pharmacokinetics, case reports and clinical management. HIV Med 2013; 14: 519–29.
5. Pollett S, Graves B, Richards B, et al. Avascular necrosis in a HIV patient receiving ritonavir and inhaled fluticasone. Int J STD AIDS 2014; 25: 458–60.
6. Kaviani N, Bukberg P, Manessis A, et al. Iatrogenic osteoporosis, bilateral hip osteonecrosis, and secondary adrenal suppression in an HIV-infected man receiving inhaled corticosteroids and ritonavir-boosted highly active antiretroviral therapy. Endocr Pract 2011; 17: 74–8.
7. Wood BR, Lacy JM, Johnston C, et al. Adrenal insufficiency as a result of ritonavir and exogenous steroid exposure: report of 6 cases and recommendation for management. J Int Assoc Provid AIDS Care2015; 14: 300–5.
8. Azevedo L, Pêgo H, Souto Moura T, et al. Iatrogenic Cushing’s syndrome and osteoporosis due to an interaction between fluticasone and ritonavir. BMJ Case Rep2015; 2015: bcr2015211080.
9.Ashby J, Goldmeier D, Sadeghi-Nejad H. Hypogonadism in human immunodeficiency virus-positive men. Korean J Urol 2014; 55: 9–16.