摘要:非洲猪瘟(African Swine fever,ASF)是由非洲猪瘟病毒(African Swine fever virus,ASFV)感染家猪和各种野猪(非洲野猪、欧洲野猪等)引起一种急性、出血性、烈性传染病,2018年8月3日我国确诊首例非洲猪瘟疫情。目前,国内外均没有有效的非洲猪瘟疫苗和药物有针对性防控此病。
细胞因子在体内通过旁分泌、自分泌或内分泌等方式发挥作用,具有多效性、重叠性、拮抗性、协同性等多种生理特性,形成了十分复杂的细胞因子调节网络,对疫病防控起着重要作用。
关键词:非洲猪瘟 细胞因子
非洲猪瘟对我国养猪业形成了致命打击,首先希望全球非瘟研究专家早日研究清楚非瘟病毒,制备行之有效的疫苗或药物针对此病,同时养殖场面临着巨大损失又不可以坐以待毙,要积极努力寻找各种方法(切断传播途径,提高易感动物免疫力、清除传染源)降低非瘟发生,减少损失。
由于该病原生物学特性决定,非洲猪瘟病毒基因类型多,数量庞大,免疫逃逸机制复杂多样,可逃避宿主免疫细胞的清除。现阶段已研制的一些非洲猪瘟疫苗,虽然能诱导产生一定水平的抗体,但并不具备中和非洲猪瘟病毒的能力,无法达到有效防控非洲猪瘟的目的。
ASFV 感染猪只后能够造成严重的病理损伤包括高热、 多脏器的出血、充血性肿大、肺脏水肿、肺脏出血、白细胞减少、 血小板减少等,其致病机制是病毒和宿主细胞相互作用,进而产生一系列的病理反应。
ASFV 能够通过呼吸道、消化道以及肌肉等多种途径感染猪只,并首先在扁桃体、下额淋巴结或其他局部淋巴结中复制 ,之后病毒随血液或淋巴液扩散,形成病毒血症,并前往其他二级器官复制(2-3 dpi),在肝脏、肺脏、骨髓、肾脏、肠道中都能检出病毒的存在[1](Plowright et al., 1969)。
ASFV造成的病变以多脏器的出血为典型特征,曾经认为ASFV对血管内皮细胞的感染和破坏是造成病变的主要因素[2](Colgrove et al., 1969),但是随后的研究表明,典型的出血症状出现在内皮细胞感染前,因此ASFV造成的急性病理损伤主要是由单核-巨噬细胞导致的[3-5](Carrasco et al. 1997: Carrasco et al. 1996b: Gomez-Villamandos et al., 1995a)。
ASFV感染初期的主要靶细胞是存在于组织中的单核-巨噬细胞,病毒在其中复制并随之扩散到其他组织器官;随后病毒开始大量感染其他类型的细胞 ,己确定的细胞种类包括:肝细胞、肝肾毛细血管内皮细胞、扁桃体上皮细胞、纤维母细胞、网状细胞、平滑肌细胞、血管外周细胞、肾小球系膜细胞、巨核细胞、淋巴细胞、嗜中性粒细胞等 ,虽然ASFV能够感染多种类型细胞,但是其感染复制的关键场所是单核-巨噬细胞系统(免疫系统)。
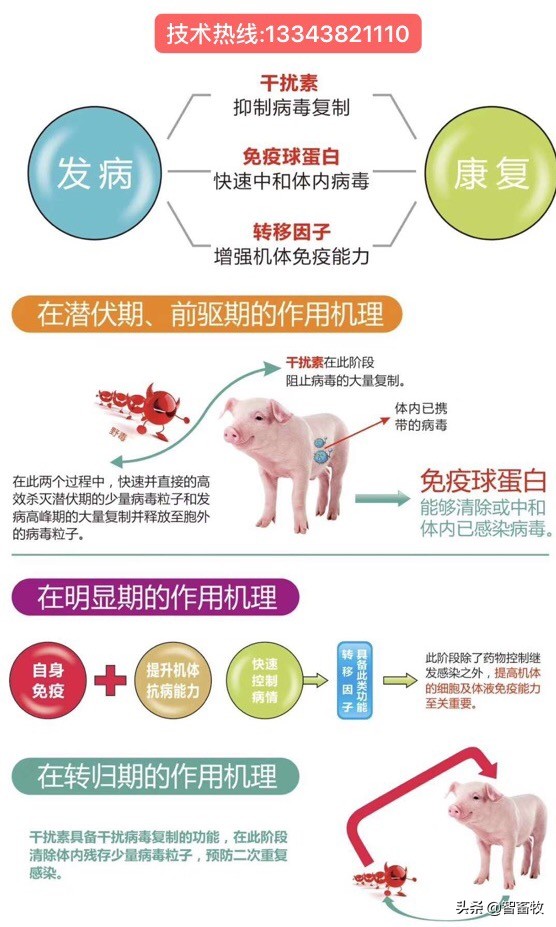
猪感染非洲猪瘟病毒以后,首先将抑制猪自身分泌Ⅰ型干扰素(干扰素α和β),非洲猪瘟病毒是一种典型囊膜病毒,对Ⅰ型干扰素非常敏感,通过抑制干扰素的抗病毒效应实现在猪体内的巨噬细胞大量增殖,猪感染非洲猪瘟病毒到发病的时间长短取决于非洲猪瘟病毒从感染细胞(巨噬细胞)中排出的数量和体外排出的途径,国外有人做过攻毒试验(格鲁吉亚2007/1型非洲猪瘟高毒力毒株),与国内目前爆发的非洲猪瘟毒株类型高度类似,一般通过接触途径在9-13天之后可以在血液中检测到非洲猪瘟病毒,其传播速度与饲养方式和猪群免疫力紧密相关。目前已经证明ASFV感染动物体后,能够激发良好的细胞免疫应答。
ASFV 感染宿主后能够在血清和组织中检测到大量 TNFα,IFNα/β,IL-1β、IL-6和IL-8[6,7](Karalyan et al.,2012;Salguero et al.,2002),使用ASFV抗原对病毒感染猪外周血淋巴细胞进行剌激, 也能够呈现特异性T淋巴细胞增殖,且能分泌大量IL-2,干扰素-γ等 CMI 相关细胞因子,证明了ASFV感染宿主后能够激发针对病毒的特异性细胞免疫应答[8] (Sanchez Vizcaino et al.,1981);实验表明病毒感染 4 周后, PBMC 中T淋巴细胞增殖反应达到顶峰 ,并被归类为记忆性辅助 T 细胞[9-11] (Alonso et al.,1997;Casal et al.,1987; Revilla et al.,1992)。
细胞因子的分泌对 CMI 有十分重要的调节作用。IFN-γ的产生对于免疫细胞抗病毒功能的上调有非常重要的作用。鉴于ASFV主要靶细胞是巨噬细胞, IFN-γ分泌就显得尤为重要。
研究表明同源毒株的再次感染能够激发良好的 IFN-γ的产生[11] (Revilla et al.,1992),而异源毒株之间则存在较大差异,与基因型和分离株特性均有关系[12] (King et al,2011)。值得注意的是,异源毒株之间低激发 IFN-γ 产生的能力,与彼此交叉保护力呈现正相关性[12,13](Fishbourne et al.,2013; Kinget al.,2011),表明对于ASFV 诱导的免疫应答特征目前尚不完全清晰。
目前科学家对非洲猪瘟的致病机理研究有了很大进展,但依然存在大量的疑惑未能解开,我们目前已知的非洲猪瘟知识依然相当匮乏,仍有许多问题仍未得到解答。非洲猪瘟(ASF)的发病机制非常复杂,涉及活化的单核吞噬系统释放炎症因子,趋化因子和免疫调节因子,导致内皮功能障碍;先天和后天免疫系统的改变,导致感染病毒的复制不受限制,并能直接引起器官和内皮细胞的损伤;诱导凝血障碍导致弥散性血管内凝血和动物死亡,经大量文献报道非洲猪瘟破坏免疫系统,以及免疫逃避。
细胞因子在体内通过旁分泌、自分泌或内分泌等方式发挥作用,具有多效性、重叠性、拮抗性、协同性等多种生理特性,形成了十分复杂的细胞因子调节网络,对疫病防控起着重要作用。之非瘟发生以来,虽然没有见到文献具体报道干扰素与白介素对非瘟病毒的免疫调节机制,但经大量客户反馈,猪只使用干扰素与白介素可降低感染几率,减少感染后的伤亡。
干扰素-α能干扰病毒在细胞内复制,使机体及时的监视病毒和抵抗病毒的感染。干扰素进入机体后与正常细胞表面干扰素受体结合,诱导细胞表达抗病毒蛋白,抗病毒蛋白从而阻断病毒DNA与宿主细胞核糖体结合,进而起到阻断或干扰病毒复制。同时,干扰素也可增强NK细胞对病毒感染细胞和肿瘤细胞*伤杀**,活化巨噬细胞。
白细胞介素-4(IL-4)其主要作用是使活化的B细胞分裂增殖,能促使静止的B细胞表达MHC-2类分子和分泌IgE,增强B细胞的抗原递呈能力,因此也称为B细胞刺激因子。其次IL-4也是辅助性T细胞(CD4+T细胞)的自分泌性生长因子;此外,IL-4还能促进细胞毒性T细胞的活性,可增强巨噬细胞的功能;同时巨噬细胞递呈抗原的能力及对肿瘤细胞的细胞毒素作用也显著增强。可维持和促进肥大细胞的增殖,促进骨髓造血前体细胞的增殖,诱导髓样细胞定向分化;诱导内皮细胞表达血管细胞粘附分子-1(vcam-1),对淋巴细胞的迁移具有一定意义。
依据机体免疫反应机理,猪感染非洲猪瘟病毒以后,首先将抑制猪自身分泌Ⅰ型干扰素(干扰素α和β),非洲猪瘟病毒是一种典型囊膜病毒,对Ⅰ型干扰素非常敏感,通过抑制干扰素的抗病毒效应实现在猪体内的巨噬细胞大量增殖,减少非瘟病毒数量,降低猪场感染非瘟病毒导致死亡,而白细胞介素-4是机体免疫反应重要的免疫调节因子,因此干扰素-α与白细胞介素-4对降低非瘟的发生发挥重要作用。
降低非瘟发生几率,三仪在行动,结合传染病控制三要素(传染源、传播途径、易感动物)和三仪相关生物兽药给出建议:
1、因为非洲猪瘟属于接触性烈性传染病,因此做好猪场环境生物安全重中之重,把控好非瘟病毒的各载体生物安全控制(活猪、车辆、物品、人员、其他动物、昆虫、空气、水、饲料、药品等)。
严控猪场人员随意进出猪场,不同猪舍的养猪人员不能串舍,每栋猪舍门口放置专用鞋子和消毒设置,舍内配置专用饲养用具。严禁与猪场无关人员进入猪场,给猪场运送饲料等物品的车辆停留在猪场隔离区,经消毒后才能进入猪场合适区。
严格消毒措施:建议猪舍内每3天用醛灭净与另外一种敏感消毒剂交替使用消毒一次,消毒前必须把猪舍地面、养殖床上的粪便污物清扫干净再喷洒醛灭净消毒剂。
商品猪的出售、保育猪的转群要一次性结束,出售、转群后的空舍要进行彻底消毒,冲洗、熏蒸、地面消毒要综合进行。彻底消毒后的猪舍最好闲置2到3周,使猪舍彻底干燥、安全后方可进猪,切记不能不分批次的循环进出猪只。
猪场内务必做好“四害”的清除,四害——苍蝇、蚊子、老鼠、蟑螂。
猪场内的消毒固然重要,根据该病的传染情况,猪舍外环境的消毒同等重要,它是切断病原传入猪场的极其重要的手段。猪场内每栋猪舍之间的路道、猪场出入口、猪场周边环境、通往猪场道路的适当距离每3天用醛灭净和3-5%的烧碱交替消毒一次。
2、保护易感动物
任何病原都是对抵抗力低的动物产生更大的危害,任何传染病都是抵抗力低的先发生并且死亡更快、更多,再严重的传染病最后都会把抵抗力强留下。所以提高猪群的免疫力尤为重要,可采取免疫疗法,结合三仪技术建议使用下列方案提高猪群免疫力,降低发病风险:
猪场做疫苗时使用“好伴侣”稀释混合肌注:好伴侣成分:白细胞介素-4、转移因子、生理盐水。
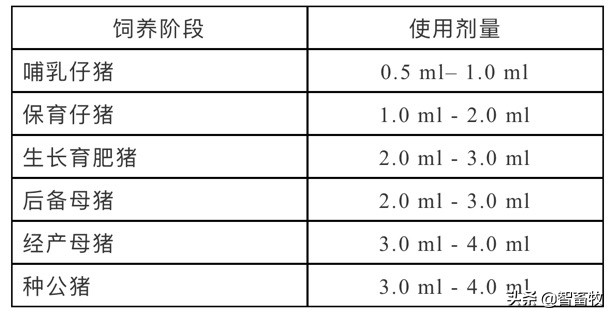
其中每1000Kg饲料添加三仪“三肽”500g-1Kg,连用7-10天。三肽主要成分为干扰素-α、白细胞介素4、免疫球蛋白、葡萄糖。本品添加的重要意义在于稳定猪场猪瘟、蓝耳、伪狂、腹泻等病毒病的发生,降低猪场对非瘟防控的压力。同时要解决好猪场霉菌毒素的危害,建议脱霉剂使用要持续不断, 定期使用梅长江(酶+益生菌),按照说明计量添加,每次使用15天,有效平衡肠道菌群,修复损伤肠道黏膜,避免黏膜损伤给病原提供侵入门户。
人的恐惧心理比非瘟更可怕,养殖从业人员要有信心,科学应对,把控生物安全细节,降低感染机会,让猪场活下来!俗话说“留得青山在,不怕没柴烧”,科学躲过目前的危害,以稳定健康的猪群,迎接2019年下半年的高行情到来。
特别说明:此病事关重大,故贡献一点思考,希望对有用之人有用!请同行和专家们拍砖!
参考文献:
1 Plowright, w., Paker, J., Peirce, M. A.,1969.Aferican swine fever virus in ticks (Ornithodoros moubata , murray) collected from animal burrows in Tanzania .Nature221(5185),1071-1073.
2 Colgrove, G.S., Haelterman, E.O., Coggins, L., 1969.
Pathogenesis of African swine fever in young pigs. American journal of veterinary research 30(8),1343-1359.
3 Carrasco, L., Chacon. M.d.l. F., Martin de Las Mulas, J.,
Gomez-villamandos, J.C., Sierra, M.A., Villeda, C.J., Wilkinson, P. J., 1997. Ultrastructural changes related to the lymph node haemorrhages in acute African swine fever.
Research in veterinary science 62(3), 199-204.
4 Carrasco, L., de Lara, F.C., Martin de las Mulas, J., Gomez-villamandos, J,C., Hervas, J., Wilkinson, P. J., Sierra, M.A. ,1996b. Virus association with lymphocytes in acute African swine fever.Veterinary research 27(3), 305-312.
5 Gomez-villamandos, J.C., Hervas, J., Mendez, A., Carrasco, L., Martin de las Mulas, J., Villeda, C.J. ,Wilkinson,P.J.,Sierra,M.A., 1995a.Experimental African swine fever: apoptosis of lymphocytes and virus replication in other cells.The Journal of general virology 76(Pt 9), 2399-2405.
6Karalyan, Z., Zakaryan, H., Sargsyan, K., Voskanyan, H., Arzumanyan, H., Avagyan, H., Karalov,E., 2012. Interferon status and white blood cells during infection with African swine fever
virus in vivo. Veterinary immunology and immunopathology
145(1-2) , 551-555
7 Salguero, F.J., Ruiz-villamor, E., Bautista, M.J., Sanchez Cordon, P. J.,Carrasco, L., Gomez-villamandos, J.C., 2002. Changes in macrophages in spleen and lymph nodes during acute African swine fever:expression of cytokines. Veterinary immunology and immunopathology 90(1-2), 11-22.
8 Sanchez-vizcaino, J, M., Slauson, D.O., Ruiz-gonzalvo,F., Valero, F., 1981. Lymphocyte function and cell-mediated immunity in pigs with experimentally induced African swine fever.American journal of veterinary research 42(8).1335-1341.
9 Alonso, F., Dominguez, J., Vinuela, E., Revilla, Y,, 1997.African swine fever virus-specific cytotoxic T lymphocytes recognize the 32 kDa immediate early protein(vp32). Virus research 49(2), 123-130.
10 Casal, I., Vinuela, E., Enjuanes, L., 1987. Synthesis of African swine fever(ASF)virus-specific antibodies in vitro in a porcine leucocyte system Immunology 62(2), 207-213.
11Revilla, Y., Pena,L.,Vinuela,E,1992. Interferon gamma production by African swine fever virus specific lymphocytes. Scandinavian journal of immunology 35(2), 225-230.
12King, K., Chapman, D., Argilaguet, J.M., Fishbourne,E., Hutet, E., Cariolet, R., Hutchings, G., Oura,C.A., Netherton, C. L., Moffat, K., Taylor, G., Le Potier,M.F. ,Dixon, L. K. ,Takamatsu,H.H., 2011.
Protection of European domestic pigs from virulent African isolates of African swine fever virus by experimental immunisation. Vaccine
29(28),4593-4600.
13Fishbourne, E., Abrams, C.C.,Takamatsu,H.H., Dixon,L, K. ,2013. Modulation of chemokine and chemokine receptor expression following infection of porcine macrophages with African
swine fever virus. Veterinary microbiology 162(24),937-943.