当我们说到神经退行性疾病,除了阿尔茨海默病,就是帕金森了。近年来帕金森发病人数暴涨,可是我们仍然对这种疾病近乎一无所知。
在所有的帕金森病例中,90%的疾病发病原因不明,被称为特发性帕金森(iPD);剩下的10%具有较为明确的遗传基础,表现出家族发病趋势,其中LRRK2错义突变是常染色体显性遗传帕金森病最常见的原因,患者LRRK2蛋白过量表达,这样的病例占了整体病例的3%。[1,2]
不过实际上我们远远低估了LRRK2在帕金森病中的重要性!近期的《科学转化医学》刊登了匹兹堡大学研究者的新发现——无论是否突变,LRRK2都在帕金森病发展中有关键作用,无突变的特发性帕金森患者也存在LRRK2蛋白过度激活,神经元细胞自噬功能受损,导致α-突触核蛋白的异常积累,参与帕金森疾病发展[3]!
换句话说,无论是否存在LRRK2突变,帕金森患者可能都存在LRRK2蛋白过度活跃的问题,那么LRRK2*制剂抑**可能是治疗帕金森病的好方法!

LRRK2是目前为止与帕金森关联最大的单个基因,2004年才被研究者发现[4]。研究者认为,最常见的LRRK2错义突变会导致LRRK2蛋白激酶过度活跃,这与帕金森的发病有关[5]。
LRRK2蛋白的作用底物是包含Rab10的一系列蛋白,这些蛋白在维持细胞内运输、自噬等功能上有关键作用[6],LRRK2则会抑制它们的功能。
不过LRRK2蛋白本身在细胞内表达量很低,如何在细胞精度上检测它的活性是一大难点。
针对这个问题,匹兹堡大学研究者开发了一种新的检测方法。LRRK2蛋白激活条件下,其蛋白序列Ser1292位点会发生磷酸化[7,8];另一方面,和 14-3-3蛋白结合会降低LRRK2的活性[9]。通过检测这两种信号,研究者就能够间接地测定LRRK2蛋白的活性了。
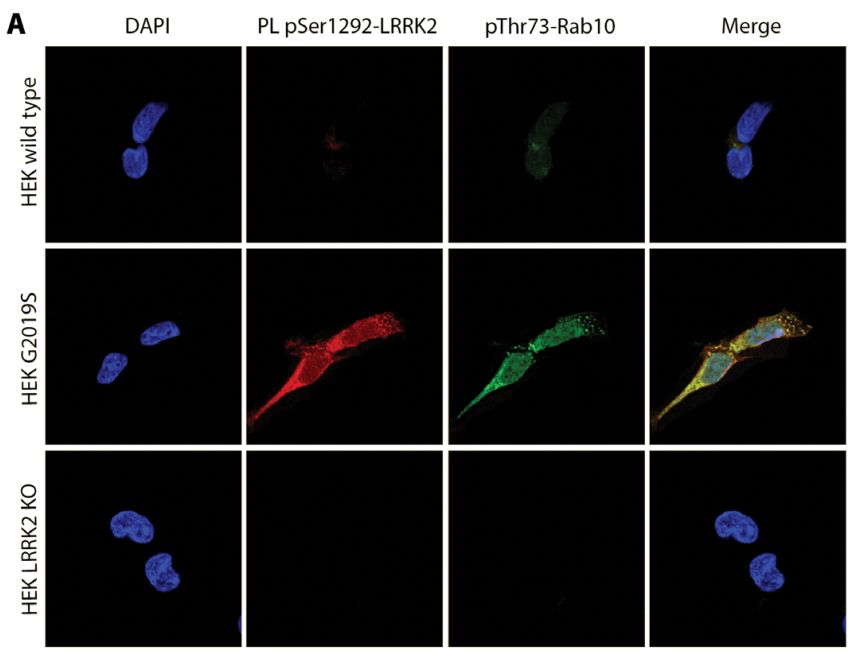
从上至下:正常细胞/LRRK2突变细胞/LRRK2缺失细胞
用这种方法,研究者检测了7名死于特发性帕金森的患者和8名相应年龄无帕金森死者的大脑。对照组大脑黑质的多巴胺神经元中,Ser1292磷酸化和Rab10水平很低,14-3-3蛋白水平较高,说明对照组脑内LRRK2蛋白活性很低;而帕金森患者脑内Ser1292和Rab10信号分别是6倍和4倍,14-3-3蛋白却只有对照组的五分之一,说明特发性帕金森患者脑内居然也存在LRRK2的过度激活!
LRRK2也在小胶质细胞中表达[10]。同样,来自帕金森患者的小胶质细胞Ser1292信号水平是对照组的2倍。
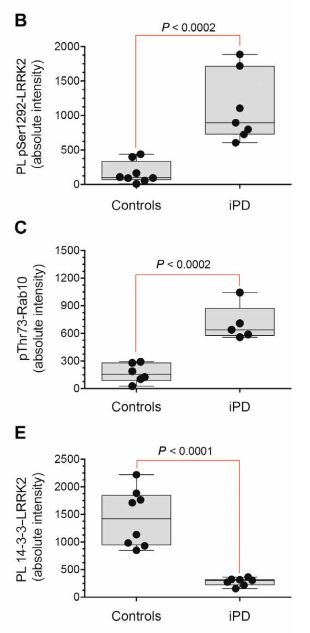
可见帕金森患者Ser1292、Rab10信号增加,14-3-3信号降低,表示LRRK2活性增加
随后研究者又检测了两种临床常用的帕金森大鼠模型,鱼藤酮导致的线粒体损伤模型[11]和hSNCA基因工程介导的α-突触核蛋白过表达模型[12]。果然,这两种模型鼠脑中均出现了LRRK2的过度激活!
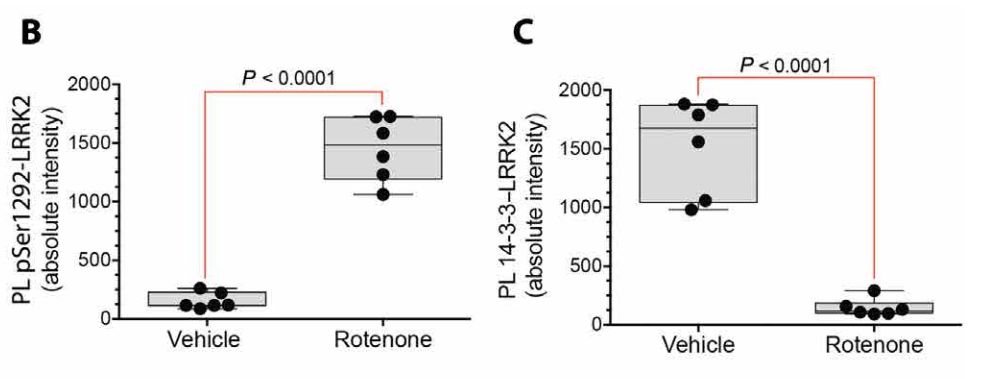
鱼藤酮模型
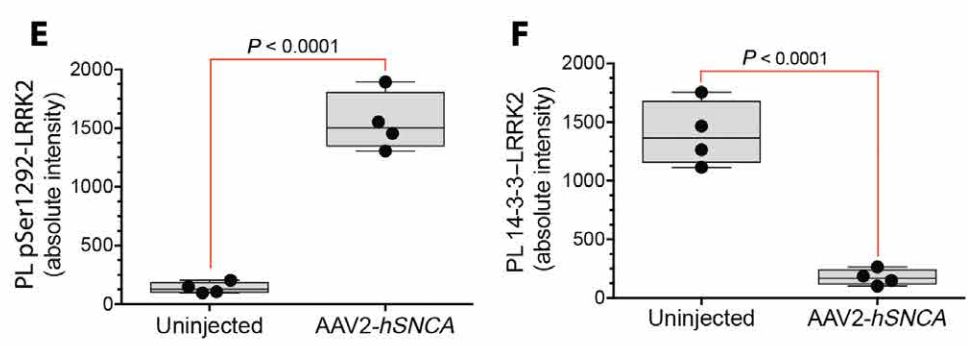
基因工程模型
那么具体是什么机制激活了LRRK2呢?
在这两种动物模型中,都存在α-突触核蛋白过表达,导致其形成寡聚体和磷酸化,而这两种形式都会损伤线粒体的功能[13],增加活性氧(ROS)的形成。研究者猜测,很有可能是活性氧激活了LRRK2!
为了验证这个猜测,研究者用过氧化氢处理了正常基因型的细胞,结果显示随着过氧化氢剂量的增加,LRRK2蛋白果然被逐渐激活,而且使用抗氧化剂α-生育酚还可以阻断这种激活作用!
看来就是活性氧的锅了!
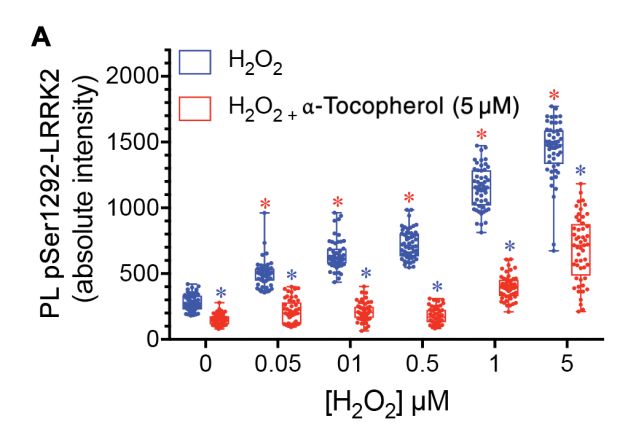
过氧化氢导致LRRK2信号增强,抗氧化剂α-生育酚阻断该作用
那么,既然知道了特发性帕金森也存在LRRK2激酶激活的情况,LRRK2激酶*制剂抑**是不是可以延缓疾病的发展呢?
研究者给鱼藤酮诱导期间的大鼠服用了LRRK2激酶*制剂抑**PF-360。鱼藤酮显著增加了大鼠脑内的LRRK2激酶活性,PF-360则有效地阻断了这种诱导,而且还阻止了磷酸化α-突触核蛋白的积累!
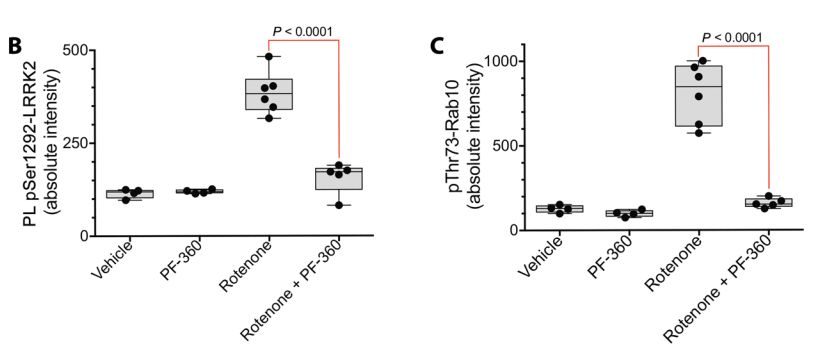
LRRK2*制剂抑**阻止了LRRK2激活
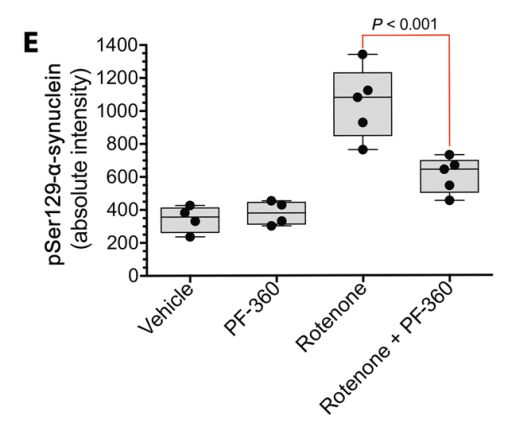
LRRK2*制剂抑**显著减少了α-突触核蛋白的积累
研究者进一步分析了α-突触核蛋白积累的原因,发现大鼠脑内自噬的标志物Lamp1显著降低,这与患者脑内检测的结果是一致的,表明存在自噬功能障碍,这导致神经元不能及时清除大脑“废物”,造成α-突触核蛋白的异常积累。
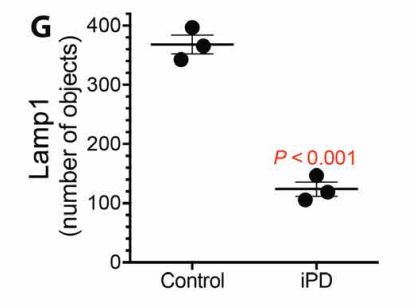
患者脑内自噬标志物Lamp1显著降低
本研究的通讯作者J.T. Greenamyre博士在采访中说道,“我们的研究结果表明,帕金森病的遗传和环境因素都可以与LRRK2蛋白活性联系起来。这是很重要的,因为正在 为少数LRRK2突变患者开发的药物,很可能会让更多患者受益。”[14]
研究者们计划下一步继续探究,是否可以预防由LRRK2过度活跃导致的神经变性,并确定将环境压力因素与LRRK2激活联系起来的机制。
去年年底,第一个LRRK2*制剂抑**1期临床结束,试验结果喜人[15]。期盼研究者快快搞清LRRK2的角色定位,或许多年不见进展的帕金森病,很快就要迎来新疗法了~
编辑神叨叨
说到帕金森,我们对这个疾病的了解真是太少了,甚至很可能是错误的。想知道具体怎么回事吗?快打开《Medical Trend》了解一下吧!


参考资料:
[1] C. Paisán-Ruiz, S. Jain, E. W. Evans, W. P. Gilks, J. Simón, M. van der Brug, A. López de Munain, S. Aparicio, A. M. Gil, N. Khan, J. Johnson, J. R. Martinez, D. Nicholl, I. M. Carrera, A. S. Peňa, R. de Silva, A. Lees, J. F. Marti-Massó, J. Pérez-Tur, N. W. Wood, A. B. Singleton, Cloning of the gene containing mutations that cause PARK8-linked Parkinson’s disease. Neuron 44, 595–600 (2004).[2]A. Zimprich, S. Biskup, P. Leitner, P. Lichtner, M. Farrer, S. Lincoln, J. Kachergus, M. Hulihan, R. J. Uitti, D. B. Calne, A. J. Stoessl, R. F. Pfeiffer, N. Patenge, I. C. Carbajal, P. Vieregge, F. Asmus, B. Müller-Myhsok, D. W. Dickson, T. Meitinger, T. M. Strom, Z. K. Wszolek, T. Gasser, Mutations in LRRK2 cause autosomal-dominant parkinsonism with pleomorphic pathology. Neuron 44, 601–607 (2004).
[3]http://stm.sciencemag.org/content/10/451/eaar5429
[4]Paisán-Ruíz C, Jain S, Evans EW, Gilks WP, Simón J, van der Brug M, López de Munain A, Aparicio S, Gil AM, Khan N, Johnson J, Martinez JR, Nicholl D, Carrera IM, Pena AS, de Silva R, Lees A, Martí-Massó JF, Pérez-Tur J, Wood NW, Singleton AB (November 2004). "Cloning of the gene containing mutations that cause PARK8-linked Parkinson's disease". Neuron. 44 (4): 595–600. doi:10.1016/j.neuron.2004.10.023. PMID 15541308[5]E. Greggio, S. Jain, A. Kingsbury, R. Bandopadhyay, P. Lewis, A. Kaganovich, M. P. van der Brug, A. Beilina, J. Blackinton, K. J. Thomas, R. Ahmad, D. W. Miller, S. Kesavapany, A. Singleton, A. Lees, R. J. Harvey, K. Harvey, M. R. Cookson, Kinase activity is required for the toxic effects of mutant LRRK2/dardarin. Neurobiol. Dis. 23, 329–341(2006).
[6]M. Steger, F. Tonelli, G. Ito, P. Davies, M. Trost, M. Vetter, S. Wachter, E. Lorentzen,G. Duddy, S. Wilson, M. A. S. Baptista, B. K. Fiske, M. J. Fell, J. A. Morrow, A. D. Reith, D. R. Alessi, M. Mann, Phosphoproteomics reveals that Parkinson’s disease kinase LRRK2 regulates a subset of Rab GTPases. eLife 5, e12813 (2016).
[7]K. B. Fraser, A. B. Rawlins, R. G. Clark, R. N. Alcalay, D. G. Standaert, N. Liu; Parkinson’s Disease Biomarker Program, A. B. West, Ser(P)-1292 LRRK2 in urinary exosomes is elevated in idiopathic Parkinson’s disease. Mov. Disord. 31, 1543–1550 (2016).[8] Z. Sheng, S. Zhang, D. Bustos, T. Kleinheinz, C. E. Le Pichon, S. L. Dominguez, H. O. Solanoy, J. Drummond, X. Zhang, X. Ding, F. Cai, Q. Song, X. Li, Z. Yue, M. P. van der Brug, D. J. Burdick, J. Gunzner-Toste, H. Chen, X. Liu, A. A. Estrada, Z. K. Sweeney, K. Scearce-Levie, J. G. Moffat, D. S. Kirkpatrick, H. Zhu, Ser1292 autophosphorylation is an indicator of LRRK2 kinase activity and contributes to the cellular effects of PD mutations. Sci. Transl. Med. 4, 164ra161 (2012).
[9]N. J. Lavalley, S. R. Slone, H. Ding, A. B. West, T. A. Yacoubian, 14-3-3 Proteins regulate mutant LRRK2 kinase activity and neurite shortening. Hum. Mol. Genet. 25, 109–122(2016).
[10]M. S. Moehle, P. J. Webber, T. Tse, N. Sukar, D. G. Standaert, T. M. DeSilva, R. M. Cowell, A. B. West, LRRK2 inhibition attenuates microglial inflammatory responses.J. Neurosci. 32, 1602–1611 (2012).
[11]J. T. Greenamyre, J. R. Cannon, R. Drolet, P.-G. Mastroberardino, Lessons from the rotenone model of Parkinson’s disease. Trends Pharmacol. Sci. 31, 141–142 (2010).[12]A. Ulusoy, M. Decressac, D. Kirik, A. Björklund, Viral vector-mediated overexpression of a-synuclein as a progressive model of Parkinson’s disease. Prog. Brain Res. 184,89–111 (2010).
[13]R. Di Maio, P. J. Barrett, E. K. Hoffman, C. W. Barrett, A. Zharikov, A. Borah, X. Hu, J. McCoy, C. T. Chu, E. A. Burton, T. G. Hastings, J. T. Greenamyre, a-Synuclein binds to TOM20 and inhibits mitochondrial protein import in Parkinson’s disease. Sci. Transl. Med. 8, 342ra378 (2016).
[14]https://www.sciencedaily.com/releases/2018/07/180726090040.htm
[15]http://parkinsonslife.eu/strong-results-announced-lrrk2-inhibitor-parkinsons-clinical-trial/

奇点:50万极客医生热爱的医疗科技媒体

本文作者 | 代丝雨
“希望疾病也能回头。”