在上一期,我们介绍了肿瘤免疫治疗的第二枚导弹Ipilimumab抗体。本期,我们介绍肿瘤免疫治疗的第三枚导弹PD-1*制剂抑**:Pembrolizumab抗体。


第三章
PD-1*制剂抑**:
Pembrolizumab抗体
一、什么是Pembrolizumab抗体?
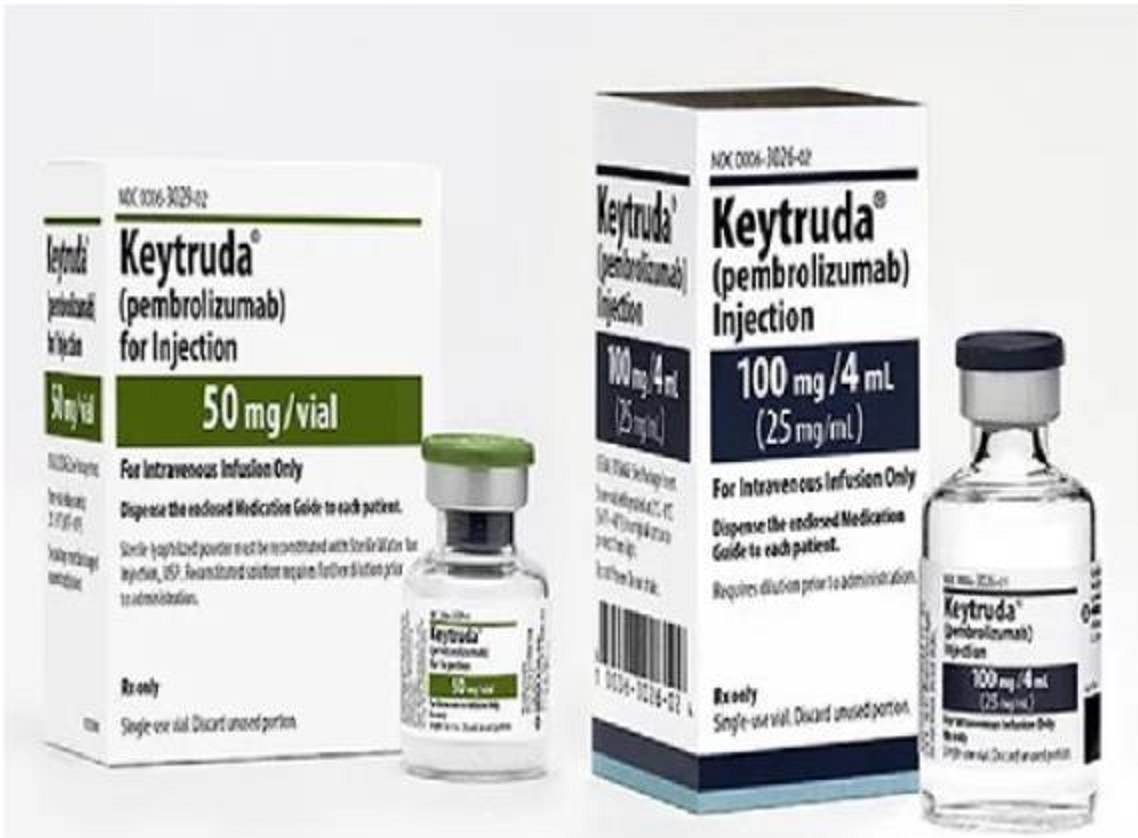
2014年9月5日,美国FDA首次批准由美国默沙东公司(Merck&Co)开发的Pembrolizumab抗体(英文通用名,中文通用名:帕博利珠单抗,英文商品名:Keytruda,中文商品名:可瑞达,俗称K药)用于治疗转移性黑色素瘤。由于Pembrolizumab抗体的英文商品名是Keytruda,因而被人们俗称“K药”。这是美国FDA批准的首个PD-1*制剂抑**。
说明一下,公司在美国与加拿大称为默克(Merck),在其他地区称为默沙东(Merck Sharp&Dohme或MSD Sharp&Dohme,简称MSD)。此后,2015年被FDA批准用于晚期黑色素瘤的一线治疗,2016年被批准用于一线治疗治疗PD-L1高表达的(≥50%)晚期非小细胞肺癌患者。

说起用Pembrolizumab抗体(以下简称“K药”)治疗黑色素瘤,最有名的例子应该是美国前总统卡特。他在90岁高龄被发现患上黑色素瘤,而且出现了肝转移、脑转移。如此高龄当然无法用化疗,于是他选择了使用“K药”配合放疗的联合疗法,结果肿瘤完全消失了!
“K药”是一种人源化单克隆抗体,可与PD-1受体结合,阻断它与PD-L1和PD-L2相互作用,通过PD-1通路介导的免疫反应对肿瘤起到抑制作用。
特别值得一提的是,2017年5月23日,美国FDA加速批准了美国默沙东公司研发的“K药”用于治疗具有微卫星高度不稳定性或错配修复基因缺陷(mismatch repair deficient,dMMR)分子特征,且不可切除或转移性实体瘤的成人和儿童癌症患者,成为第一个所谓的“广谱抗癌药”。
这是一件大事,具有里程碑式的意义。因为,这是全世界第一个批准的,依照生物标志物而不是肿瘤部位进行区分的抗肿瘤药,而且是成人和儿童通吃。也就是说,不管是什么癌症,只要是MSI-H或dMMR阳性,都可以使用“K药”治疗。“K药”再次创造历史。
微卫星高度不稳定性(MSI-H)或错配修复基因缺陷(dMMR),都是非常拗口,且不知所云的专业名词。对大家来说,这些名字完全不重要,知道下面几点就好:
第一,错配修复(mismatch repair,MMR)是维持细胞染色体稳定的重要机制,如果MMR相关基因发生突变,DNA在复制过程中发生的错误(MSI-H)就没有办法及时修复,这也是癌症发生的原因之一。这种亚型肿瘤的特点,就是修复DNA的一些重要蛋白失去功能。这导致DNA出错概率大大增加,因此这类癌细胞中出现大量的DNA突变。
第二,MSI-H与dMMR是两种常见的遗传异常,含有这两种变异的肿瘤,细胞内的DNA修复机制往往会受到影响,不能正常发挥作用。
第三,这是在很多实体瘤中都存在的一种亚型,带有这些异常的肿瘤分布非常广泛。MSI-H实体瘤囊括的适应症有:结肠直肠癌、小肠肿瘤、肉瘤、子宫内膜癌、乳腺癌、甲状腺癌、胆管癌、尿路上皮细胞癌、腹膜后腺癌、胃癌、食管癌、小细胞肺癌、胰腺癌、前列腺癌、肾细胞癌。因此,通过遗传变异特征而非病发部位来区分这些癌症,对于治疗有着更好的指导意义。
第四,这类肿瘤如果进展到晚期,通常对化疗不敏感,而且由于DNA突变多,容易进化而产生耐药,因此传统上讲患者的预后较差。但随着PD-1/PDL-1*制剂抑**的出现,柳暗花明又一村,这类肿瘤对免疫疗法的响应异常好,远超绝大多数肿瘤类型。
二、免疫疗法PD-1赛道的领先者
这次“K药”获FDA批准用于MSI-H/dMMR难治癌症患者的意义,不仅仅在于扩大了“K药”的治疗范围,更在于开启了癌症治疗的一个全新时代:首次体现了精准医疗“异病同治”的概念,谱写了划时代新篇章。
2018年5月,FDA批准了关于“K药”增加新适应症的补充申请,用于治疗携带一种特定基因特征的任何实体瘤。成为首款不依据肿瘤来源,而是依据生物标志物进行区分的抗肿瘤疗法。美国《科学》杂志也发表了一重要文章,进一步证实“K药”作为“广谱抗癌药”的实力。从全球范围获批适应证数量而言,“K药”是目前用于治疗晚期瘤种最广泛的免疫药物,它已在全球80多个国家与地区获批使用。
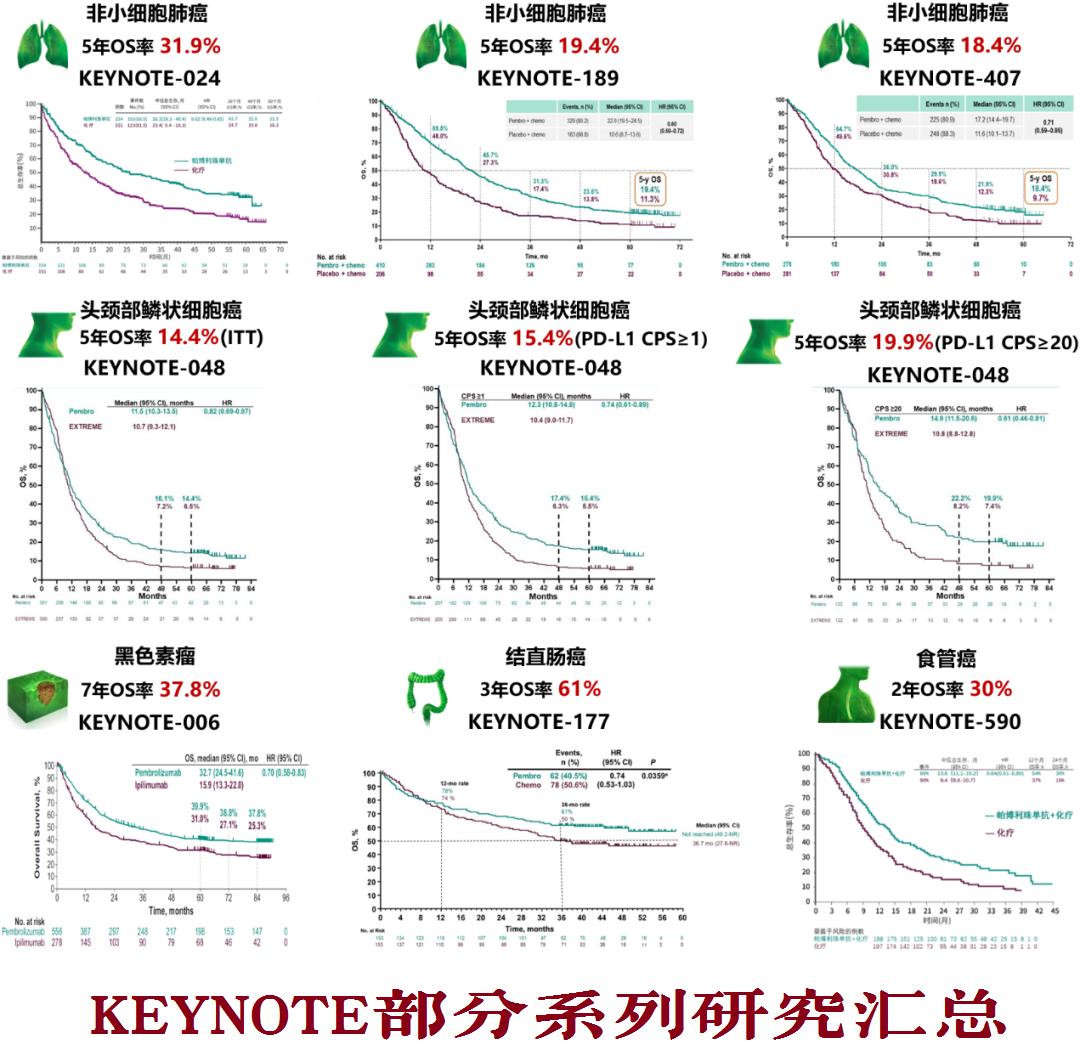
2022年9月13日闭幕的2022年欧洲肿瘤内科学会(ESMO)年会公布了多项PD-1免疫检查点*制剂抑**Pembrolizumab(“K药”)治疗不同癌种的长期生存(OS)随访数据,包括:
K药联合含铂化疗一线治疗转移性非鳞和鳞状非小细胞肺癌(NSCLC)的全球多中心III期临床研究KEYNOTE-189和KEYNOTE-407的五年OS随访数据。
K药单药一线治疗以及联合化疗一线治疗复发或转移性头颈部鳞癌(HNSCC)的III期临床研究KEYNOTE-048。

K药单药二线治疗不可切除肝细胞癌(HCC)的KEYNOTE-240随访4.5年的OS,和K药二线/后线治疗HNSCC的KEYNOTE-040 6年OS随访数据。
这五项KEYNOTE皆为多中心、随机对照III期临床研究,但它们带来的适应症获批命运截然不同,有些成功获批并成为治疗领域的里程碑,而有些则因差之毫厘而令人扼腕叹息。但KEYNOTE研究系列对于长生存的探索却让它们又殊途同归,合力彰显免疫治疗长生存的玄妙。
值得一提的是在2022年9月2日发布的最新版美国NCCN NSCLC治疗指南(2022 v4)中,K药联合含铂化疗仍是唯一获“优先推荐”(Preferred)指定的治疗PS评分0-1的晚期转移性鳞或非鳞NSCLC方案。而其他多项联合治疗方案,虽然也都有大型III期临床研究结果“背书”,但只获得“其它推荐”(Other Recommendation)的指定。

三、“K药”在中国
2018年7月25日,国家食品药品监督管理总局正式批准“K药”在中国上市,用于晚期黑色素瘤患者治疗。
“K药”进入中国时间较“O药”晚,是因为我国黑色素瘤患者与欧美患者的亚型不同,需要我国的临床试验数据以证明“K药”的疗效。“K药”的获批,对中国患者和医学界都是一个值得振奋的消息,值得三呼“OK”!
一是因为,“K药”能显著延长患者的生存期,部分患者实现了长期生存,甚至实现了临床治愈,这意味着部分晚期多发转移的肿瘤患者,可以活过5-10年。
二是因为,“K药”具有广泛的适应症,在多种肿瘤中都表现出良好的获益。
截至目前,“K药”在国内获批的适应症已经达到10个,用于单药或联合用药治疗黑色素瘤、非小细胞肺癌、食管癌、头颈部鳞状细胞癌、MSI-H/dMMR结直肠癌,为这些肿瘤患者带来了新的生存希望。

四、“K药”在美国
而“K药”在美国FDA获批的适应症更多。截至目前,“K药”在美国FDA共批准了18个癌种,其中2个血液肿瘤,16个实体瘤。合计约45个适应症,分别是:
1、黑色素瘤(晚期治疗、术后辅助);
2、非小细胞肺癌(鳞癌一线、非鳞癌一线、一线单药、后线单药);
3、头颈部鳞癌(一线联合、一线单药);
4、经典霍奇金淋巴瘤(一线单药、后线单药);
5、原发性纵隔大B细胞淋巴瘤(后线单药);
6、尿路上皮癌;晚期治疗、非肌层浸润性膀胱癌(NMIBC)
7、MSI-H/dMMR实体瘤(前线治疗后进展或无满意可选的治疗选择);
8、MSI-H/dMMR结直肠癌(1)(单药)
9、胃癌(一线联合);
10、食管癌(一线联合、后线单药);

11、宫颈癌(一线联合、后线单药);
12、肝癌(二线单药);
13、默克细胞癌(晚期单药);
14、肾癌(一线联合阿昔替尼、一线联合仑伐替尼、术后辅助);
15、子宫内膜癌(一线联合、二线单药);
16、TMB-H实体瘤(单药治疗经前线系统治疗且无后线满意方案的不可切除或转移期TMB≥10不可切除或转移期实体瘤);
17、皮肤鳞状细胞癌(晚期单药);
18、三阴性乳腺癌(新辅助/辅助、晚期治疗)
注:小细胞肺癌后线适应症已经撤回。
“K药”作为免疫疗法PD-1赛道的领先者,近年来在销售量上的增长速度令业界和投资人感到振奋。2022年第一季度该产品营收超过48亿美元,创下新高,第二季度继续增长到52.52亿美元,这意味着,该产品的半年营收已经超过了百亿美元。而对于“K药”来说,获批更多适应症也是稳住其地位并提高营收的关键。只是现在看来,他们似乎已经开始后劲不足了。

四、“K药”的封王之路却充满坎坷
根据默沙东公开信息,他们代号“KEYNOTE-921”的临床试验,是“K药”联合化疗治疗转移性去势抵抗性前列腺癌的研究。根据公开信息,受试者是1030名未经化疗但是疾病已进展或对下一代激素药物不耐受者。他们接受了历时约2年的治疗,主要终点有轻微的改善趋势但未达到预设目标。
这已经是“K药”第二次在前列腺癌领域受挫。年初,K药联合PARP*制剂抑**Lynparza(奥拉帕利)的疗法的三期研究,刚刚因为未达到主要终点且3到5级不良事件发生风险提高而被默沙东终止。
根据默沙东公告,这项试验与代号LEAP-002的“K药”联合仑伐替尼治疗不可切除肝细胞癌试验的具体数据将很快在医学会议上公布。
PD-1作为成功获批产品最多的免疫检查点*制剂抑**,已经成为免疫疗法的基石,有“抗癌神药”之称。其中K药更是被誉为“免疫之王”。

2014年9月4日,默沙东的K药仅用了164天,就在美国本土拿到了FDA认可,获批上市。此前百时美施贵宝的O药(Opdivo)已经在日本获批,此后罗氏的T药(Tecentriq)等也相继获批,在经过几年的角逐之后2018年,K药一骑绝尘,成为全球卖得最好的免疫检查点*制剂抑**。
2021年该药全球年销售额171.86亿美元,今年上半年的销售额已经超过了100亿美元。不仅把“老对手”O药远远甩在身后——2021年收入75.23亿美元,距离赶超百时美施贵宝的修美乐(化学名:阿达木单抗)似乎也只有一步之遥。
可以说,“K药”的封王之路却充满坎坷!
最新数据显示,2022年H1财报显示,辉瑞、莫德纳的新冠疫苗销售额分别220.75亿美元和104.56亿美元,其中辉瑞疫苗的销售额同比增长达到了95%。老“药王”修美乐虽然增速放缓,销售额也以100.99亿美元险胜“K药”。
同时,紧随其后的百时美施贵宝/辉瑞的抗凝血药阿哌沙班(Eliquis)和辉瑞新冠肺炎小分子药奈玛特韦(Paxlovid)销售额也都追得很紧,分别达到99.83亿美元和95.85亿美元。
而且“K药”的关键专利又将在2028年面临到期问题。
可以说,“K药”在这场“药王”争夺赛中腹背受敌,处于一种焦灼的状态。
而它所处的PD-1/PD-L1赛道,又偏偏是一个市场空间广阔,但竞争异常激烈的领域。
弗若斯特沙利文数据显示,到2023年全球PD-1/PD-L1市场空间预计可以达到639亿美元。早年行业预计,中国的相应市场可达2000亿元到3000亿元,近年来疯狂“内卷”之下,市场空间大幅萎缩萎缩,行业预计仍可达到500亿元以上的空间。
由此也激发了全球医药研发领域史无前例的“氪金”运动。
自从2014年K药获FDA批准以来,该公司的研发投入也在持续增加,到2020年研发投入巅峰135.58亿美元,相当于2014年2倍以上。累计研发投入接近760亿美元,在全球巨头中也能排到前几位。有业内人士向虎嗅分析,这与近年来该公司在K药上临床试验投入增加有关。

在中国,根据药智网的统计数据,研发投入最多的药也是PD-1——君实生物的特瑞普利单抗,已经已经消耗36.79亿元,一骑绝尘,远超第二位的康希诺新冠疫苗——8.55亿元。排在第四位的恒瑞医药的卡瑞利珠单抗也已经花掉了7.4亿元。
IQVIA统计数据显示,全球已有5761项涉及PD-1/PD-L1*制剂抑**的试验在推进中,2021年以来的新研究中九成左右都是联合疗法。其中也包括大批中国药企。
K药的研究更是远超同行。全球临床试验注册登记平台显示,近年来,围绕K药的临床试验总数接近2000条。
另据默沙东官网,该公司主导开展的K药研究多达1600多项,涉及“各种癌症和治疗环境”。
仅K药与仑伐替尼联合,就超过15个临床试验,涉及10多个癌种,除了肝细胞癌,还有子宫内膜癌、黑色素瘤、非小细胞肺癌、肾细胞癌、头颈癌、胆道癌、结直肠癌、胃癌、食管癌、胶质母细胞瘤和胰腺癌。
而同样的,在这个平台上可以查询到的关于修美乐的研究只有700多项,尽管在过去几十年里,这款药已经提起了200多项专利申请,树起了上百个专利围墙。
K药如此大量的临床试验背后也是巨大的资金投入。更糟糕的是,在这些研究中还往往有罗氏、辉瑞等劲敌如影随形。
这些都令K药的封王之路困难重重,不仅是市场推广上的比拼,更是在适应症开发领域的全面攻坚战,是对企业研发能力、财力和耐力的全面考验。

附录一:
Pembrolizumab抗体(帕博利珠单抗,K药,Keytruda)在美国获批适用症时间线具体如下(截至2023年4月21日):
1、2023年4月14日
获得美国FDA批准,联合含氟嘧啶和铂类化疗药物,用于一线治疗局部晚期不可切除或转移性胃癌或胃食管交界处(GEJ)腺癌患者的补充生物制剂许可申请(sBLA)。
2、2023年4月3日
获得FDA加速批准,联合恩诺单抗(Padcev,enfortumab vedotin-ejfv,简称EV)一线治疗不适合接受含顺铂化疗的局部晚期或转移性尿路上皮癌(La/mUC)。这是首款PD-1单抗与ADC(抗体偶联药物)联合获批实体肿瘤的新疗法。
3、2023年3月29日
获批用于经FDA批准的检测方法确定的不可切除或转移性高度微卫星不稳定型(MSI-H)或错配修复缺陷型(dMMR)实体瘤成人和儿童患者。这些患者在既往治疗后出现进展,并且没有令人满意的替代治疗方案。
4、2023年1月16日
获得FDA批准,作为单药辅助疗法治疗经手术切除与铂类化疗后的IB、II、IIIA期非小细胞肺癌(NSCLC)成人患者。
5、2022年3月21日
帕博利珠单抗获得FDA批准,用于治疗MSL-H/dMMR晚期子宫内膜癌患者。这些患者在任何情况下既往全身治疗后出现疾病进展,并且不适合接受根治性手术或放疗。
6、2021年11月18日
获得FDA批准,作为手术后某些肾细胞癌(RCC)患者的单药辅助治疗。
7、2021年10月13日
获得FDA批准,联合化疗、联合或不联合贝伐珠单抗,用于治疗肿瘤表达PD-LI(CPSZl)的耐药、复发性或转移性宫颈癌患者。
8、2021年8月11日
获得FDA批准,联合仑伐替尼(lenvatinib)用于晚期肾细胞癌(RCC)一线治疗。
9、2021年7月27日
获得FDA批准,联合化疗作为新辅助治疗用于高危早期三阴性乳腺癌患者,术后继续单药辅助治疗。
10、2021年7月22日
获得FDA批准,联合仑伐替尼(lenvatinib)用于特定类型的晚期子宫内膜癌患者。
11、2021年7月6日
新适应症获得FDA批准,用于局部晚期皮肤鳞状细胞癌(cSCc)。
12、2021年7月1日
默克提供美国三线胃癌药物适应症的最新进展。
13、2021年5月5日
获得FDA批准,联合曲妥珠单抗和化疗作为局部晚期不可切除或转移性HER2阳性胃或胃食管交界处腺癌的一线治疗。
14、2021年3月23日
获得FDA批准,用于局部晚期不能切除或转移性HER2阳性胃或胃食管交界处腺癌的一线治疗。
15、2021年3月1日
默克提供美国转移性小细胞肺癌药物治疗的最新情况。(已经撤回适应症)

16、2020年11月13日
获得FDA加速批准,与化疗联用,用于不可切除局部复发性或转移性三阴性乳腺癌(TNBC)患者。
17、2020年10月15日
获得FDA批准,治疗接受过一线疗法的复发/难治性经典型霍奇金淋巴瘤(cHL)成人患者以及难治性经典型霍奇金淋巴瘤(cHL)或经二线及二线以上治疗后复发的经典型霍奇金淋巴瘤(cHL)儿童患者。
18、2020年6月29日
获得FDA批准,单药用于不可切除或转移性微卫星高度不稳定性(MSL-H)或错配修复缺陷(dMMR)结直肠癌患者的一线治疗。
19、2020年6月24日
获得FDA批准,单药用于不能通过手术或放化疗治愈的复发或转移性皮肤鳞状细胞癌(csCC)患者。
20、2020年6月17日
获得FDA批准,治疗具有高肿瘤突变负荷(TMB-H)210个突变/兆碱基(使用FDA指定的检测)的无法切除或转移性实体瘤的成年和儿童患者。并且这些患者在先前的治疗后已有进展,尚没有令人满意的替代治疗选择。TMB-H(第二项不限制癌种适应症)。
21、2020年4月28日
帕博利珠单抗获得FDA批准,以每六周400 mg的额外推荐剂量用于Al批准的成人适应症。
22、2020年1月8日
获得FDA批准,用于卡介苗(BCG)无应答、高危、原位、有无乳头状肿瘤、无法或不愿手术的非肌肉侵入型膀胱癌(NMIBC)治疗。
23、2019年9月17日
获得FDA批准,联合仑伐替尼用于治疗特定晚期子宫内膜癌患者。这些患者为系统治疗后疾病进展不适合手术或放疗的且不伴有微卫星不稳定性高(MS-H)或错配修复缺陷(dMMR)的患者。
24、2019年7月31日
获得FDA批准,单药用于二线治疗复发性局部晚期或转移性食管鳞状细胞癌(ESCC)患者。
25、2019年6月18日
获得FDA批准,单药被批准用于既往接受过铂类为基础的化疗和至少一种其他疗法后出现进展的转移性小细胞肺癌患者的三线治疗(已撤回适应症)。
26、2019年6月11日
获得FDA批准,单药治疗肿瘤表达PD-1(综合阳性分数CPS2)的复发或转移头颈癌患者,或与铂和尿(FU)联合用,无论患者的PD-L表达多少(一线治疗)。
27、2019年4月22日
获得FDA批准,与阿昔替尼(axitinib)联合作为晚期肾细胞癌患者的一线治疗。
28、2019年4月11日
获得FDA批准,单药一线治疗PD-LI表达(TPS21%)且无EGFR和ALK基因突变的期或转移性非小细胞肺癌。
29、2019年2月19日
获得FDA批准,用于完全切除后淋巴结转移的黑色素瘤患者的辅助治疗。
30、2018年12月19日
获得FDA批准,治疗复发性局部晚期或转移性默克(Merkel)细胞癌患者。

31、2018年11月9日
获得FDA批准,治疗先前接受过索拉非尼(Sorafenib)治疗的肝细胞癌(HCC)患者。
32、2018年10月30日
获得FDA批准,联合卡铂和紫杉醇或白蛋白结合型紫杉醇(Abraxane)一线治疗转移性鳞状非小细胞肺癌(NSCLC)患者。
33、201年8月21日
获得FDA批准,联合培美曲塞和卡铂一线治疗转移性非鳞状非小细胞肺癌(NSGNSCLC)患者,EGFR和ALK突变均阴性。
34、2018年月13日
获得FDA批准,用于治疗难治性原发性纵隔大B细胞淋巴瘤(PMBCL)的成人和儿科患者,至少使用两线治疗后仍旧复发的。
35、2018年6月12日
获得FDA批准,用于治疗复发或转移性宫颈癌患者,病情在化疗中或化疗后出现进展,肿瘤表达PD-LI(CPSZI)。
36、2017年8月22日
获得FDA批准,用于复发性局部晚期或转移性胃癌/胃食管结合部腺癌,且肿瘤表达PD-Ll的患者(经FDA批准的检测试剂检测)。
37、2017年5月23日
获得FDA批准,治疗成人及儿童的不可切除或转移性、微卫星高度不稳定(MS-H)或配修复陷(dMMR)的实体瘤患者。
38、2017年5月18日
获得FDA批准,用于局部晚期或转移性尿路上皮癌的患者,包括一线治疗含铂(cispolatin)化疗方案的局部晚期或转移性尿路上皮癌患者,该适应症是基于肿瘤缓解持续时间加速批准;二线治疗︰接受含铂化疗期间或化疗后病情进展、或受含铂化疗新辅助治疗或辅助治疗12个月内病情进展的局部晚期或转移性尿路上皮癌患者。
39、2017年5月10日
获得FDA批准,联合培美曲塞+卡铂获批一线治疗转移性非鳞状非小细胞肺癌(NSCLC),不受PD-LI表达的限制。
40、2017年3月15日
获得FDA批准,用于难治性经典型霍奇金淋巴瘤(cHL),或者三次以上主要治疗后疾病复发的成人与儿童患者。
41、2016年10月24日
获得FDA批准,用于一线治疗PD-LI表达强阳性(肿瘤细胞表达PD-Ll250%),EGFR和ALK突变均为阴性的转移性非小细胞肺癌。
42、2016年8月5日
获得FDA批准,用于含铂化疗后疾病进展的复发性/转移性头颈部鳞状细胞癌(HNSCC)患者。
43、2015年12月18日
获得FDA批准,用于治疗晚期黑色素瘤的更广泛的适应症,一线治疗晚期不可切除或转移性黑色素瘤。
44、2015年10月2日
获得FDA批准,用于治疗肿瘤表达PD-LI(TPS21%)、含铂疗期间或之后疾病进展的转移性非小细胞肺癌(NSCLC)。
45、2014年9月4日
获得FDA批准,用于接受过伊匹木单抗(lpilimumab)治疗但仍有进展,或对伊匹木单抗和BRAF*制剂抑**双重耐药的BRAF V600基因变异的晚期黑色素瘤。

附录二:
Pembrolizumab抗体(帕博利珠单抗,K药)中国获批适应症时间线(截至2023年4月21日)
1、2022年11月7日
获批联合化疗用于经充分验证的检测评估肿瘤表达PD-L1(综合阳性评分(CPS≥20))的早期高危三阴乳腺癌(TNBC)患者的治疗。
2、2022年10月9日
获批单药用于既往接受过索拉非尼或含奥沙利铂化疗的肝细胞癌(HCC)患者的治疗。
3、2021年9月3日
获批单药用药KRAS、NRAS和BRAF基因均为野生型、不可切除或转移性高微卫星不稳定性(MSI-H)或错配修复基因缺陷型(dMMR)结直肠癌(CRC)患者的一线治疗。
4、2020年12月9日
获批一线治疗食管癌。
5、2020年6月19日
获批治疗PD-L1阳性(综合阳性评分CPS≥10)、既往一线全身治疗失败的局部晚期或转移性食管鳞状细胞癌(ESCC)。
6、2019年9月30日
获批单药一线治疗PD-L1表达阳性(TPS≥1%)的EGFR、ALK-局部晚期或转移性非小细胞肺癌。
7、2019年11月26日
获批联合卡铂、紫杉醇或白蛋白紫杉醇一线治疗鳞状非小细胞肺癌。
8、2019年4月2日
获批联合培美曲塞、顺铂一线治疗EGFR和ALK阴性的转移性非鳞状非小细胞肺癌。
9、2018年7月26日
获批治疗经一线治疗失败的不可切除或转移性黑色毒瘤。


1. 奇云. 机体的免疫反应是如何被激活的?——2011年诺贝尔生理学或医学奖解读[J]. 生物化学与生物物理进展, 2011, 38(10):900-907.
2. 奇云. 机体的免疫反应是如何被激活的?[J]. 生命世界, 2012(1):44-51.
3. 奇云. 抗独特型抗体研究的新进展[J]. 生物化学与生物物理进展, 1990(5):356-358.
4. 奇云. 干细胞研究与治疗性克隆[J]. 世界科技研究与发展, 2001, 23(5):33-43.
5. 奇云. 打开探究人体细胞分化和演变的大门[J]. 物理通报(2):1-4.
6. 奇云. 发现调控细胞循环周期的神秘物质[J]. 世界科学, 2001, (11):7-8.
7. 奇云. 发现调控细胞循环周期的神秘物质[J]. 世界科学, 2001, (11):7-8.
8. 奇云. 纳米医学的新分支——纳米肿瘤学[J]. 卷宗,2011(6):68-68.
9. 奇云. 抗癌新药紫杉醇的研究进展[J]. 生命的化学, 1994, 14(1):37-38.
10. 奇云. P53基因与癌症[J]. 生物学教学, 1995(5):4-6.
11. 奇云. 抗肿瘤新药紫杉醇研究进展[J]. 世界科学, 1994(3):14-15.
12. 奇云. 战胜癌症的成功之路:—阻断癌细胞转移[J]. 现代化, 1992, 14(2):22-23.
13. 奇云. 人体防御素研究的现状与展望[J]. 生命的化学, 1992(12):23-24.
14. 奇云. 让细胞改变命运[J]. 科技潮, 2012, (11):58-61.
15. 奇云. 2001年诺贝尔生理学或医学奖介评—— 三位科学家与三种神秘物质[J]. 科学对社会的影响, 2001(4):12-15.
16. 奇云. 光敏药物与激光治癌[J]. 现代物理知识, 1990(02):30-31+10.
17. 奇云. 抗肿瘤新药紫杉醇研究进展[J]. 河南肿瘤学杂志, 1995, 8(3):233-235.
18. 奇云. 2001年诺贝尔生理学或医学奖获得者及其研究成果简介[J]. 肿瘤防治杂志, 2002,9(2):219-220.
19. 奇云. "生物导弹"由来说[J]. 发明与革新, 1994(1):26-27
20. 奇云. 解放后的前中央研究院化学究研所[J]. 生物化学与生物物理进展, 1990(5):356-358.
21. 奇云. “谈癌色变”该易字[J]. 发明与创新(综合科技), 1992(2):23.
22. 奇云. 细胞粘附分子的功能和临床意义[J]. 卷宗, 2011(7):94-95.
23. 奇云. 2001年诺贝尔生理学或医学奖获得者及其研究成果[J]. 国外医学情报, 2002, 23(1):6-11,17.
24. 奇云. 抗肿瘤新药紫杉醇研究开发动态[J]. 今日科技, 1993(7):4-5.
25. 奇云. 2013值得关注的6大科学领域[J]. 科技潮, 2013(3):54-57.
26. 奇云. 抗肿瘤新药紫杉醇研究进展[J]. 中国生化药物杂志, 1996, 17(3):131-135.
27. 奇云. 不治而愈的奥秘[J]. 发明与创新:综合科技, 1992, (7):24.
28. 奇云. 揭开T细胞免疫的神秘面纱[J]. 生物学教学, 1997(10):1-3.
29. 奇云. 21世纪的纳米医学展望[J]. 现代诊断与治疗(3):154-155.
30. 奇云. 干细胞研究与治疗性克隆[J].世界科技研究与发展,2001,23(5):33-43.
31. 奇云. 人体防御素研究的现状与展望[J].生命的化学,1992,12(5):23-24.
32. 奇云. 打开探究人体细胞分化和演变的大门[J].物理通报(2):1-4.
33. 奇云. 发现调控细胞循环周期的神秘物质[J].世界科学,2001,(11):7-8.
34. 奇云. 发现调控细胞循环周期的神秘物质——2001年诺贝尔生理学或医学奖揭晓[J].世界科学,2001,(11):7-8.
35. 奇云. 现代免疫学在中医药领域的新发展——中药的细胞免疫研究[J]. 临床荟萃, 1986(10):37.
36. 奇云. 2019年新晋诺奖得主威廉·凯林[J]. 生命世界, 2020(2):46-51.
37. 奇云. 2019年新晋诺奖得主彼得·拉特克利夫[J]. 生命世界, 2020(3):34-41.
38. 奇云. 机体的免疫反应是如何被激活的?——2011年诺贝尔生理学或医学奖成果解读[J]. 生命世界, 2012(1):44-51.
39. 奇云. 美日免疫学家折桂诺奖[J]. 生命世界, 2019(4):4-7.
40. 奇云. 癌症治疗的免疫战争[J]. 生命世界, 2019(4):1.
41. 奇云. 松开免疫系统的"刹车"[J]. 生命世界, 2019(4):10-13.
42. 奇云. 本庶佑的科学贡献[J]. 生命世界, 2019(4):18-20.
43. 奇云. 陈列平的科学贡献和遗憾[J]. 生命世界, 2019(4):21-23.
44. 奇云. 詹姆斯·艾利森的科学贡献[J]. 生命世界, 2019(4):12-17.
45. 奇云. 免疫系统三“向导”——2011年诺贝尔生理学或医学奖获奖者介绍[J].生命世界,2011(12):58-63.
备注:
以上参考文献,是作者早年发表在科学期刊上的与本文相关的文章。有兴趣者可到国内外相关文献数据库浏览或*载下**全文。

肿瘤免疫治疗的故事(连载一)
肿瘤免疫治疗的故事(连载二十九)
肿瘤免疫治疗的故事(第16-20期导读)
癌症治疗的革命:CAR-T细胞疗法的前世今生(导读)
人类史上最为惨烈的传染病(第一集)——鼠疫篇(导读)
《2021年诺贝尔生理学或医学奖专题》导读(13篇重磅文章在此!)
2022年诺贝尔生理学或医学奖专题(《奇云空间》13期连载导读)
《生物恐怖主义专题》(1-6期)导读
恐惧症探秘(第1-4期导读)
《舌尖上的安全》(第16——20期导读)
深度解读科幻大片背后的科学元素(导读)
“人类基因组计划”探秘(第6-11期导读)
人类进化的今天和明天
基因 . 女人和莎士比亚
犹太人超凡的智慧哪里来?

扮演上帝?创造生命奇迹的合成生物学(上)
扮演上帝?创造生命奇迹的合成生物学(下)
“地球村”拉响外来物种入侵警报!中国打响反入侵*击狙**战
生活中的电磁辐射
航天育种:来自太空的神奇
人造生命:超越自然,还是带来毁灭?
蚂蚁应用抗生素比人类早五千万年
人的寿命极限是多少?科学界没有标准答案
科学家破译爱情密码! 科学家破译爱情密码!
科学家的故事汇编(第五辑)
“Y染色体危机“”引发科学争议
神经科学中,有关“祖母细胞”的有趣故事
发表还是不发表?两篇科研论文的传奇故事
双唇点燃的“化学反应”
南极病毒将开启潘多拉魔盒?

中国发现新病毒!这颗“狼牙”会吃人
埃博拉病毒卷土重来!地球开启免疫模式?
鸟在花丛化蜂行——迷人的“小妖精”,独特精致的蜂鸟
看《猿族崛起》,话人类“*亲近**”——人与猿的相同与不同(7)
看《猿类崛起》,话人类“*亲近**”——人与猿的相同与不同(1)
画说人科动物(2)——大猩猩
基因是人类的“酒司令”
舌尖上的安全(23)——面粉中,有多少非法添加让人心有余悸?
舌尖上的安全(23)——面粉中,有多少非法添加让人心有余悸?