自从1879年约瑟夫·约翰·汤姆逊发现电子以来,电子以何种方式围绕着原子核运动,一直是研究原子核结构的重点。电子实在是太小了,连最先进的科学仪器都无法观察到,更何况它以接近光速运动着。所以,以现在的科学技术水平来直接观察电子及其运动很难办到。

电子概率分布图
那有些人不仅要问,电子运行的轨道,包括原子的结构不都已经清楚了吗?那它们是怎么被发现的呢?回答这一问题,我们可以来追溯一下原子,电子,质子,中子等量子发现的过程,它们都不是被直接观察到的,包括后来发现的夸克,胶子,介子等粒子都是通过实验间接得到的。质子是通过α粒子撞击金箔反弹到反映板上得到的,而夸克胶子是用强子对撞机使两束质子流以接近光的速度相撞,破碎基本粒子形成的痕迹来发现的··· ···
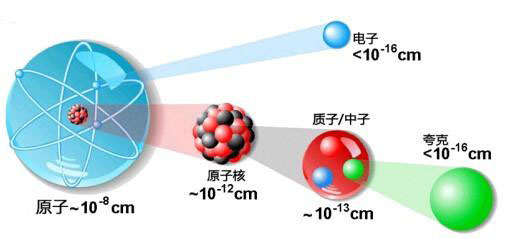
原子结构
因此,通过观察粒子在不同状态下与媒介发生了何种反应,从而间接推导出该粒子的基本性质,这也是一种相对有效的科学探索方法。电子围绕原子核的运动的秘密,也是通过间接观察和实验逐步揭开的。

解密的关键,就是原子的光谱。其实,对光的研究很早就开始了,天空中的彩虹就引发了无数人的猜想。1666年,牛顿把通过玻璃棱镜的太阳光分解成了从红光到紫光的各种颜色的光谱,他发现白光是由各种颜色的光组成的。
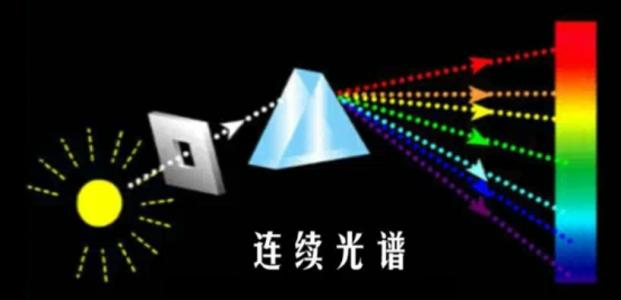
其后一直到1802年,渥拉斯顿观察到了光谱线,其后在1814年夫琅和费也独立地发现它。牛顿之所以没有能观察到光谱线,是因为他使太阳光通过了圆孔而不是通过狭缝。在1814~1815年之间,夫琅和费公布了太阳光谱中的许多条暗线,并以字母来命名,其中有些命名沿用至今。此后便把这些线称为夫琅和费暗线。

光谱实验装置
其后,科学家利用光谱作定性化学分析的新方法,并用这种方法发现了几种当时还未知的元素,并且证明了太阳里也存在着多种已知的元素。我们知道,原子中结构最简单的就是氢原子,科学家就从氢原子着手,利用光谱分析的方法逐步打开了通往微观物质的大门。

不同的原子拥有不同的光谱
氢原子光谱中最强的一条谱线是1853年由瑞典物理学家埃斯特朗探测出来的。此后的20年,在星体的光谱中观测到了更多的氢原子谱线。1885年,一名叫巴耳末(J. J. Balmer)的物理学家在观察星体的氢光谱中发现了一个规律,即这些谱线的波长关系可以唯象地表达为一个简单的经验公式,即巴耳末公式。
在三年后的1888年,瑞典物理学家里德伯(J. Rydberg)在研究碱金属谱线时,发现了碱金属谱线的规律,并将巴耳末推广成为了著名的里德伯公式。

氢原子光谱
尽管氢原子光谱线的波长的表示式十分简单,不过当时对其起因却茫然不知。对照有阳光照射的连续光谱,氢原子光谱上有明显的断痕,把光谱分成了很多段,是不连续的,其颜色也不尽相同。其实光也是一种电磁波,不同颜色的光代表不同频率的电磁波,即不同的能量。一直到1913年,丹麦物理学家尼尔斯.玻尔在普朗克的量子理论和爱因斯坦的光子学说的基础上,对它作出了明确的解释。

玻尔原子模型
简单的来说,玻尔认为:
1.电子不是随意占据在原子核的周围,而是在固定的层面上运动,在圆形轨道上绕核运动。
2.电子在不同轨道上运动时,其能量是不同的。轨道离核愈远,能量愈高。
3.当电子从一个层面跃迁到另一个层面时,原子便吸收或释放能量。为了解释氢原子线状光谱这一事实,玻尔在行星模型的基础上提出了核外电子分层排布的原子结构模型。但是 ,玻尔的原子模 型却无法说明多电子原子的光谱,甚至不能说明氢原子光谱的精细结构,以及电子在轨道上是如何运动的。
一直到1926年、量子力学发展后,薛定谔方程式才解释了原子中的电子波动,定下关于新概念“轨道”的函数。