编者按:最近连续收麦,众小编有点吃不消,趁着端午休整几天。就在这期间我们国家小麦抗病遗传研究上连续出现几个重要进展!令人振奋!今天,我们推送由中国科学院遗传与发育生物学研究所刘志勇课题组和中国农业科学院作物科学研究所李洪杰课题组等单位合作克隆的两个小麦抗*粉白**病基因Pm5e和Pm41。具体内容如下,敬请赏析。

1.研究背景
小麦*粉白**病是广泛流行的真菌性病害,严重影响小麦的产量和品质。目前已经发现60多个抗*粉白**病基因(Pm)位点,其中只有Pm3、Pm38/Yr18/Lr34/Sr57、Pm8、Pm46/Yr46/Lr67/Sr55、Pm2、Pm60、 Pm17、Pm21和Pm24先后被克隆。
我国小麦地方品种蕴含丰富的抗*粉白**病基因资源,目前只有Pm24被克隆(Nature Commun | 刘志勇组与李洪杰组合作克隆小麦抗*粉白**病基因Pm24)。Pm5e(复壮30)位于Pm5位点,有Pm5a、Pm5b、 Pm5c、Pm5d和Pm5e等多个复等位基因;泾惠30及其提纯复壮的复壮30(Pm5e载体)曾在1950-1970年间广泛种植于陕西关中平原和渭北塬,近80年来仍对我国80%的*粉白**菌菌株具有抗性(Xie et al., 2020),表明Pm5e基因具有持久和广谱的抗性。
2.Pm5e精细定位
首先利用高感*粉白**病品种农大015 与复壮30构建的重组自交系进行了两轮BSR-Seq分析(图1)。分别选取农大015×复壮30的RIL群体中60个纯合抗病和60个纯合感病的RIL家系构建了抗病混池和感病混池进行转录组测序,利用BSR-seq分析出的抗、感池间SNP/InDel开发分子标记,在3,705个F2:3家系作图群体上进行精细作图,将抗*粉白**病基因Pm5e定位在分子标记WGGC13073和WGGC201之间0.17 cM遗传区间;再利用Pm5e两侧分子标记WGGC6892和WGGC11541从精细定位群体中筛选重组体,用15个纯合抗病和20个纯合感病重组家系再次构建抗、感混合池,进行第二次转录组测序,并继续开发分子标记,将Pm5e定位在分子标记WGGB2和WGGB3之间0.04 cM遗传区间,对应中国春基因组13.5 kb的物理区间。两轮BSR-Seq分析提升了定位区间作图的精度,直接鉴定出与目标基因相关联的基因组区段和序列变异。
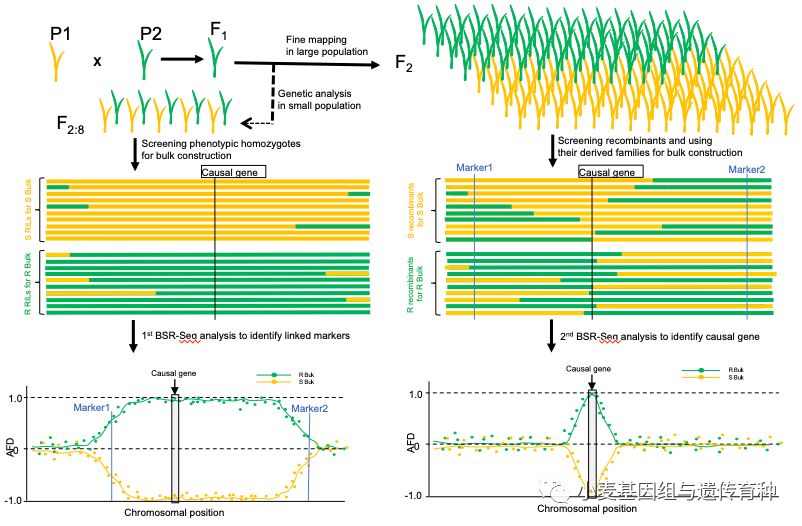
图1 两轮BSR-Seq进行基因定位示意图(Xie et al., 2020)
3.Pm5e的克隆
Pm5e定位区间在中国春参考基因组序列中注释出3个基因:Rx-cc-like基因RXL、具有NBS-LRR结构域基因NLR和具有C2结构域的基因C2。根据中国春序列分别在复壮30和农大015中扩增包括这3个候选基因的13.5 kb基因组序列,发现RXL和NLR基因呈“头对头”的位置关系,两个基因的ATG间隔1387 bp。与感病品种农大015相比,复壮30中的RXL基因外显子上存在一个A/G的同义SNP(分子标记WGGB2)、一个C/T的非同义SNP和一处7 bp的缺失,缺失导致该基因编码框发生改变;复壮30中的NLR基因第一个外显子上存在一个C/T同义SNP,第三个外显子上存在A/G和C/T两个非同义SNP,第四个外显子上存在C/G和G/A两个非同义SNP;C2基因上不存在序列差异,仅在5'-UTR区存在GA两个核苷酸的缺失(WGGB3),且在抗病混池和感病混池RNA-Seq数据中未发现剪切方式和表达量的差异。与感病材料中国春相比,抗病亲本复壮30仅在NLR基因的第四个外显子上存在C/G和G/A两个非同义SNP,分别是c.C3022G和c.G3033A,RXL和C2基因不存在序列差异(图2)。由于Rx-cc-like和NBS-LRR类型的基因均与抗病性相关,因此将RXL和NLR都作为候选基因进行功能验证。
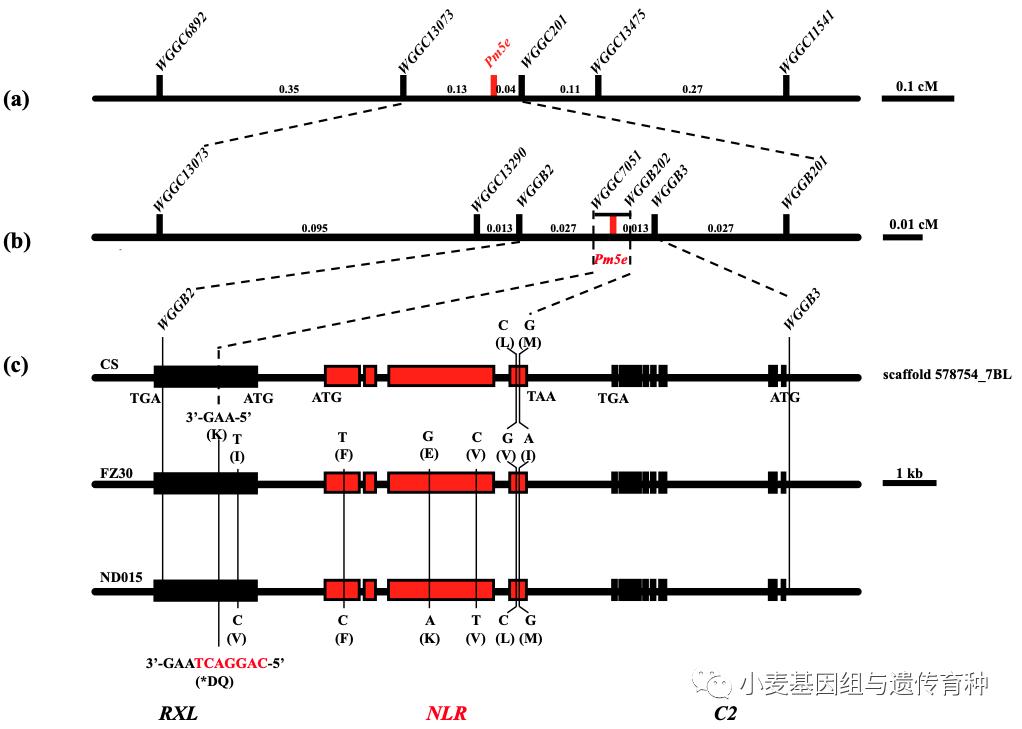
图2 小麦抗*粉白**病基因P m5e的图位克隆(Xie et al., 2020)
4.Pm5e候选基因的突变体验证
利用EMS处理复壮30种子创制突变体库,对2,500个M2代家系幼苗人工接种*粉白**菌E20菌株进行筛选,发现了29个感病家系。通过扩增这些纯合感病突变体的13.5 kb定位区间基因组序列,在C2基因上未检测到序列变异,有4个突变体在RXL基因上发生了非同义SNP突变,有5个突变体在NLR基因上发生了突变,其中Mu3097的突变导致氨基酸的改变;Mu2384的突变发生在第2个外显子和第2个内含子的交界处,导致剪切方式发生改变;Mu2586和Mu2717的突变导致翻译提前终止;Mu3208的突变为LRR结构域上15 bp的缺失(图3)。另有20个突变体未检测到序列变异。这表明RXL和NLR基因的突变都可能导致复壮30*粉白**抗性的丧失。由于RXL和NLR是“头对头”的位置关系,所以两个基因可能互为启动子,无法判断RXL上的4个点突变是影响了自身的功能还是影响了NLR的功能。NLR基因的翻译提前终止、剪切方式改变、LRR结构域缺失等突变体表明NLR基因功能的丧失可能导致了复壮30*粉白**病抗性丧失,NLR更有可能是抗*粉白**病基因Pm5e。
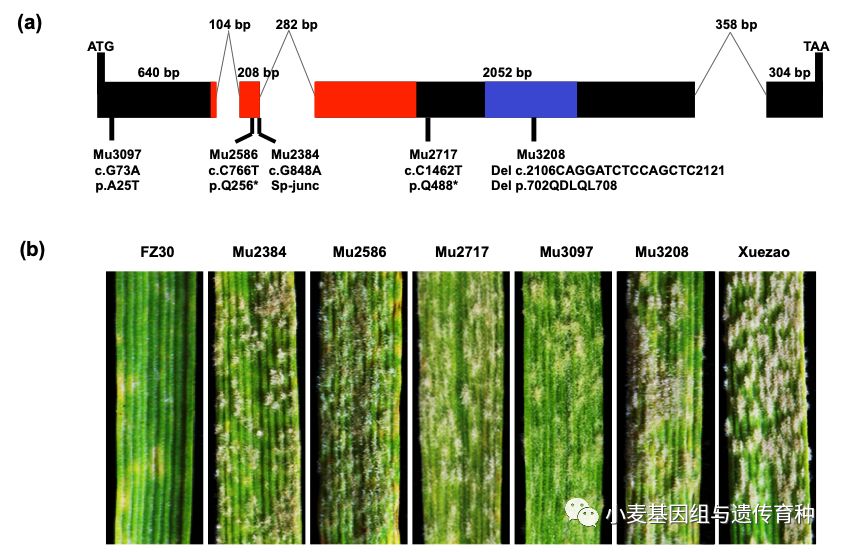
图3 Pm5e位点的突变体功能验证(Xie et al., 2020)
5.Pm5e候选基因的转基因验证
为了进一步验证RXL和NLR基因的抗*粉白**病功能,分别构建了NLR基因自身启动子驱动的基因组全长序列互补载体和玉米Ubiquitin启动子驱动全长CDS的过表达载体,以及RXL基因自身启动子驱动基因组全长序列的互补载体,利用农杆菌介导遗传转化高感*粉白**病的小麦品种Fielder,利用E20菌株接种T0代转基因植株和T1代家系,发现NLR基因的互补载体和过表达载体转基因阳性植株对*粉白**菌E20表现高抗,而RXL基因互补载体的阳性转基因家系都表现高感反应型(图4) ,表明NLR基因是小麦抗*粉白**病基因Pm5e。
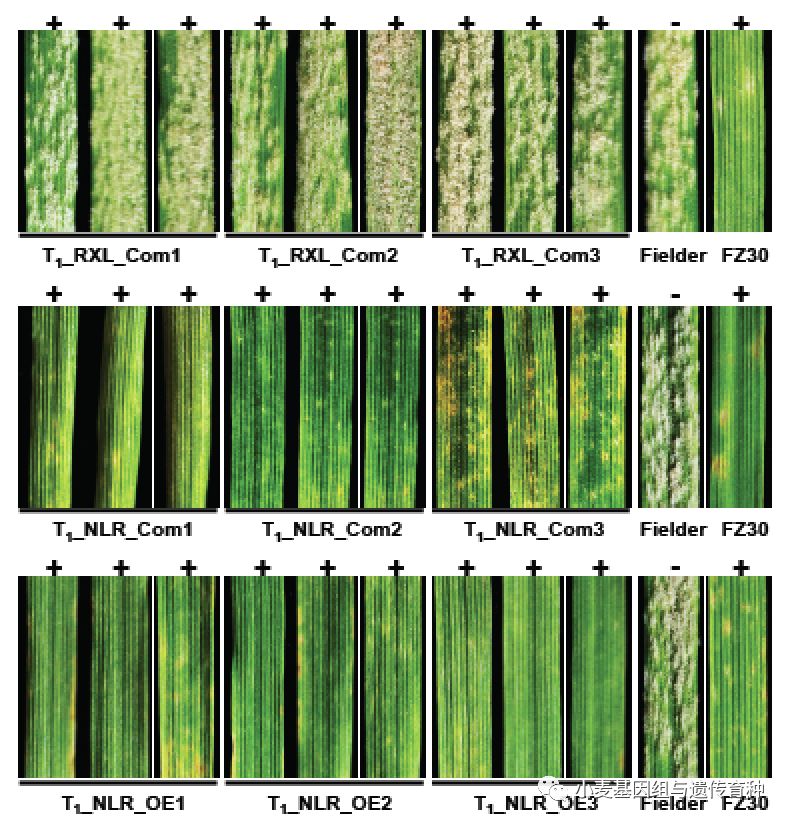
图4 P m5e位点的转基因功能验证(Xie et al., 2020)
6.Pm5e基因NLR的单倍型分析
感病品种中国春和抗病亲本复壮30相比,NLR基因仅在第4个外显子上存在2个非同义SNP(c.C3022G和c.G3033A)。为了进一步明确NLR基因这两个SNP与其抗*粉白**病功能的关系,利用覆盖这两个位点的标记WGGB202对来自35个国家和地区的989份小麦材料进行序列扩增。发现其中的261份材料由于序列变异较大,用引物WGGB202无法扩增(之后开发了一个可以成功扩增该类群的新标记WGGB199);在728份扩增成功的材料中,序列比较发现该区域可分为3种单倍型,分别是HapGA、HapGG和HapCG,其中HapGA仅包括24份高抗*粉白**病的材料(图5)。
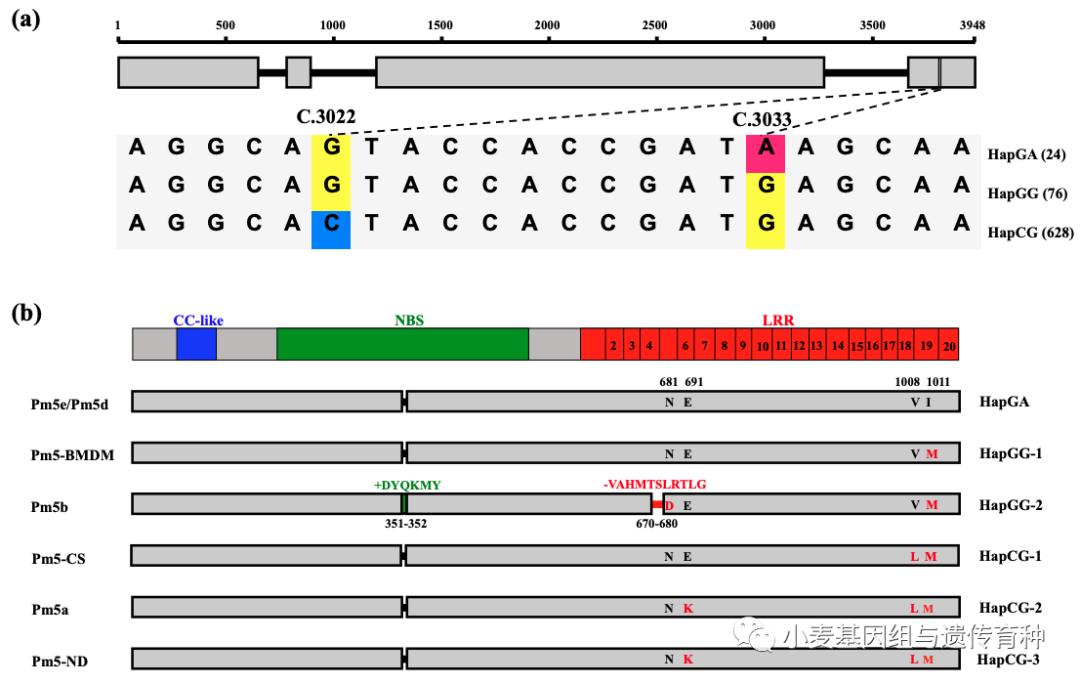
图5 Pm5基因位点的单倍型变异(Xie et al., 2020)
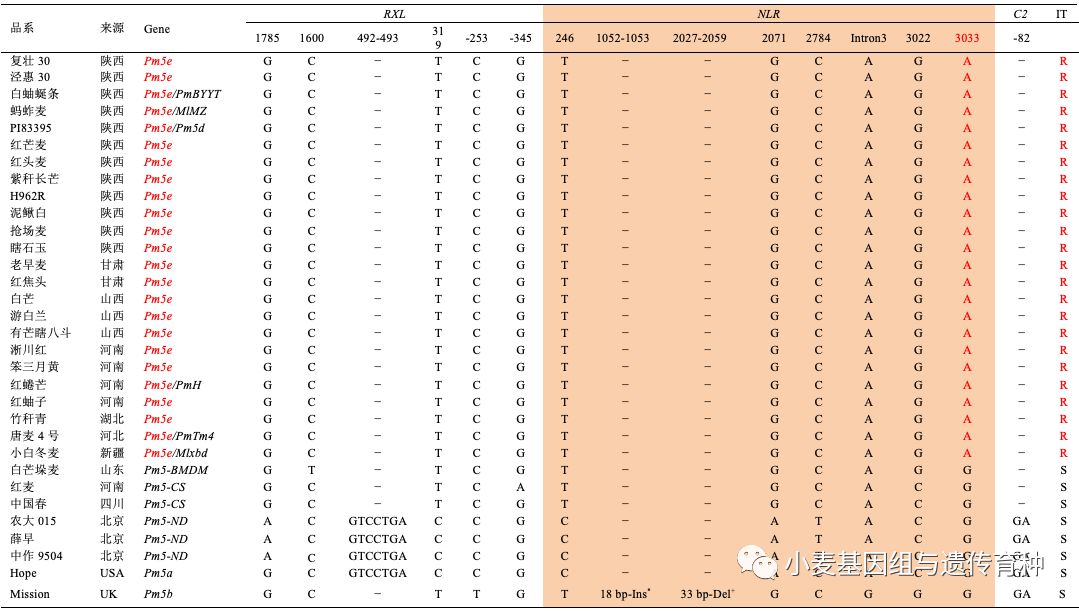
这些HapGA单倍型材料中的NLR基因所在13.5 kb基因组序列完全一致,说明HapGA单倍型所有材料均含有Pm5e等位基因,其中包括小白冬麦(Mlxbd)、红蜷芒(PmH)、蚂蚱麦(Mlmz)、唐麦4号(PmTm4)、游白兰(PmYBL)和白蚰蜒条(PmBYYT)等,这些材料的抗*粉白**病基因均位于Pm5位点或其相近位置。从来源上看,含有Pm5e的材料全部是我国西北关中平原及其周边地区的地方品种(表1)。
表1 小麦抗*粉白**病基因Pm5的单倍型序列变异(Xie et al., 2020)
7.Pm5e基因的选择驯化与来源追溯
Pm5e(HapGA)在小麦种质资源中的比例很低,而且只分布在我国部分小麦地方品种及其衍生品种中,3种单倍型在种质资源中所占的比例HapCG>HapGG>HapGA。秦汉时期关中平原地区土地肥沃、灌溉条件优越,农业生产比较发达。小麦被引入我国之后,得以在这一地区大规模种植,当时温暖潮湿的气候条件(竺可桢 1972)可能有利于*粉白**菌的繁殖,在*粉白**菌的选择压力下,Pm5位点主要的单倍型HapCG驯化出HapGG,之后HapGG单倍型在当地发生自然突变,产生了稀有变异HapGA,即Pm5e,而含有该单倍型的抗病小麦被当地农民收集和保存下来(图6)。
共线性和进化分析表明,Pm5基因组区域在普通小麦中国春的7A/7B/7D染色体、野生二粒小麦Zavitan的7A/7B染色体、粗山羊草AL8/78的7D染色体和大麦Morex的7H染色体存在良好的共线性关系,说明该基因组区段在小麦族里高度保守。NLR蛋白在粗山羊草和野生二粒小麦中的同源蛋白相似性较高,其次是大麦,在短柄草、水稻、乌拉尔图小麦、玉米、谷子、高粱中相似性很低,而且均位于非共线性的基因组区域,说明该基因可能产生于禾本科作物分化之后。
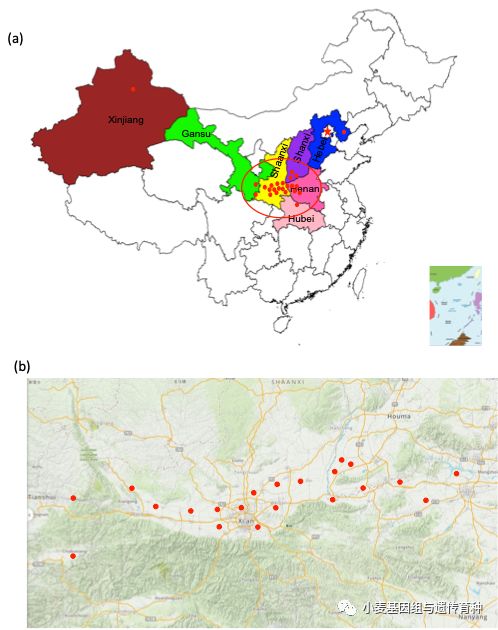
图6 Pm5e在中国(a)和关中平原周边地区(b)的分布(Xie et al., 2020)
8.影响Pm5e基因功能的关键自然变异位点解析
为进一步了解Pm5位点在小麦品种资源中的序列变异,我们比较了Pm5e与其它等位基因之间的序列差异。与Pm5e相比,感*粉白**病的Pm5-BMDM属于HapGG-1类型,仅在第4个外显子上存在一个SNP(c.A3033G),非常可能是Pm5e自然突变的供体类型;Pm5b (Misson) 属于HapGG-2类型,在第3个内含子有一个SNP,在第4个外显子上存在SNP (c.A3033G),在NB-ARC结构域有18 bp的插入,在LRR结构域有33 bp缺失,导致LRR motif的数量减少。利用基因枪瞬时转化法证实了Pm5b具有抗*粉白**病功能(图7a);我们发现Pm5d 与 Pm5e所在的13.5 kb基因组区域序列完全一致,表明P m5d与Pm5e是相同的等位基因,这与其均来源于陕西地方品种相一致;感病类型Pm5-CS 属于HapCG-1类型,仅存在2个SNP;Pm5a (Hope)属于HapCG-2类型,在其编码的NLR蛋白N端有一个同义SNP,在第5个LRR motif后面有一个非同义SNP,C端有2个非同义SNP;Pm5-ND 属于HapCG-3类型,比HapCG-2类型在C端多了一个同义SNP;Pm5-AK58 属于HapCG-4类型,一个13,176 bp的反转座子插入并替换了基因区722 bp的序列,这种类型可以用分子标记WGGB58检测(图5)。
等位变异和关联分析发现,位于Pm5e编码的NLR蛋白C端c.G3033A变异(对应氨基酸为p.M1011I)对Pm5e基因抗*粉白**病功能至关重要,该碱基的改变使高感*粉白**病的NLRG等位基因(Pm5-BMDM)突变为高抗NLRA等位基因(Pm5e),对应的氨基酸由Met突变为Ile,增加了NLR蛋白C末端的疏水性,从而引起二级和三级结构差异。利用Phyre2网站预测了Pm5e蛋白和仅差一个氨基酸的Pm5-BMDM蛋白结构,发现两个预测蛋白在二级和三级结构上均存在差异,说明有可能是该氨基酸的变异导致抗病小体蛋白构象发生改变,使其在与病原菌效应因子识别时功能发生改变。
目前克隆到的小麦抗*粉白**病基因均为显性遗传,而含有Pm5e基因的小麦品种和地方品种的*粉白**病抗性多呈隐性遗传,或不完全显性遗传(小麦抗*粉白**病基因Pm5(一))。在人工接种*粉白**菌后,复壮30叶片上的菌丝数量和菌丝长度都显著低于农大015,且可以观察到活性氧爆发,表明Pm5e可抑制*粉白**菌的侵染和生长;农大015与复壮30的*种杂**F1植株叶片上菌丝数量和长度呈中间型,同样也可以观察到活性氧爆发,表现一定的抗性反应,说明Pm5e为部分显性基因,或不完全显性基因(图7b,7c)。同时,*粉白**病菌接种后,Pm5e受*粉白**菌诱导表达,在接种后6h表达量最高(图7d),表达丰度一直高于感病品种农大015,表明Pm5e的高表达可能与维持*粉白**病抗性有关。
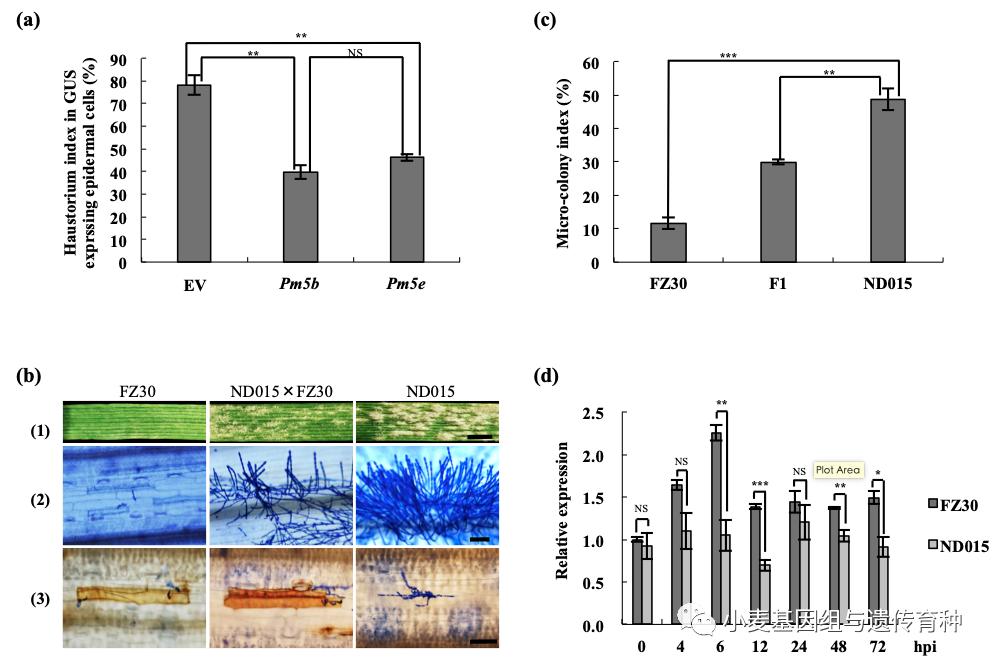
图7 Pm5b等位基因功能验证和Pm5e的表达模式(Xie et al., 2020)
9.Pm5e的利用价值
综上所述,Pm5e编码典型的NLR蛋白,该基因C端的稀有单核苷酸变异c.G3033A对*粉白**病抗性功能的获得至关重要,这种稀有等位变异仅存在于我国小麦种质中,尤其是以关中平原地区为核心的地方品种中。根据这一单核苷酸变异开发的KASP标记可以有效地区分小麦种质资源中的Pm5e单倍型(图8),应用于分子标记辅助选择育种。Pm5e的克隆和稀有单核苷酸变异c.G3033A的发现为小麦抗*粉白**病分子设计育种和基因组编辑育种提供了宝贵的基因资源。
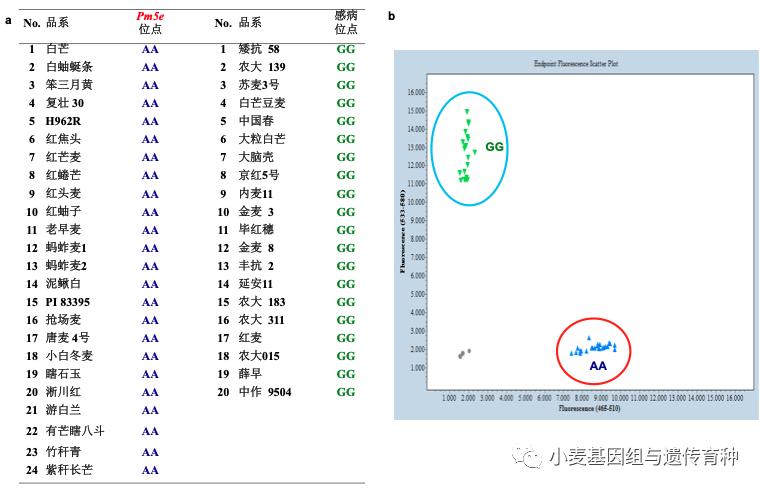
图8 P m5e位点的KASP标记检测(Xie et al., 2020)
小麦抗*粉白**病基因Pm5e(NLR)的克隆研究由中国科学院遗传与发育生物学研究所刘志勇课题组、中国农业科学院作物科学研究所李洪杰课题组、美国USDA-ARS西部研究中心Yong-Qiang Gu课题组、河南科技学院、河南平顶山学院、中国农业大学、美国UC Davis和Kansas State University等单位的研究人员合作完成。从胡铁柱2005年开始对唐麦4号中的抗*粉白**病基因进行分子标记定位,李静婷、谢菁忠、王丽丽、王勇和郭广昊等多位研究生同学先后参与了该项目的接力式研究,研究结果2020年6月22日在线发表于New Phytologist杂志(Xie et al., 2020i et al., 2020)。
参考文献
1. 竺可桢 (1972) 中国近五千年来气候变迁的初步研究。中国科学 16(2):168-189
2. Xie JZ, Guo GH, Wang Y, Hu TZ, Wang LL, Li JT, Qiu D, Li YH, Wu QH, Lu P, Chen YX, Dong LL, Li MM, Zhang HZ, Zhang PP, Zhu KY, Li BB, Deal KR, Huo NX, Zhang Y, Luo MC, Liu SZ, Gu YQ*, Li HJ*, Liu Z*. (2020) A rare single nucletide variant inPm5econfers powdery mildew resistance in common wheat. New Phytologist. DOI:10.1111/nph.16762

1.研究渊源
野生二粒小麦(Triticum dicoccoides, 2n = 4x = 28, AABB)是普通六倍体小麦的祖先种,起源于中东“新月沃土”地区,经历了长期的自然演变,积累了丰富的遗传多样性,进化出多样化的抗*粉白**病基因,是小麦抗病育种珍贵的遗传资源。从野生二粒小麦中已经发掘出Pm16、Pm26、Pm30、Pm36、Pm41 、 Pm42和Pm64等7个抗*粉白**病基因,还有MlZec1、MlIW72、PmG16、Ml3D232、MlIW170、PmAs846、PmG3M、MlIW172和MlIW30等多个临时命名的基因。其中野生二粒小麦品系IW2全生育期免疫或高抗*粉白**病(IT 0; -1, 图1)。IW2采自以色列Mount Hermon地区,是中国农业大学孙其信教授与以色列海法大学进化研究所Tzion Fahima教授和Eviatar Nevo教授执行中囯-以色列合作研究项目期间从以色列引进的野生二粒小麦。
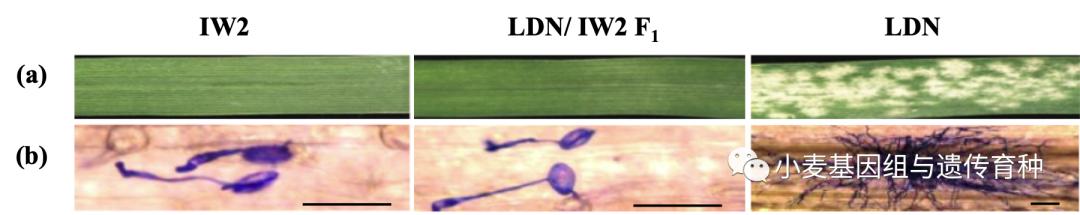
图1 野生二粒小麦IW2和硬粒小麦Langdon及其*种杂**F1代对*粉白**病菌的反应(Li et al., 2020)
2.Pm41的命名与定位三部曲
2.1 初次遥望
用高感*粉白**病的硬粒小麦品种Langdon(LDN,IT 4)与IW2配制遗传分离群体,利用*粉白**菌E09菌株接种F1、F2代和F2:3家系进行抗性遗传分析,发现IW2的*粉白**病抗性由显性单基因控制,后正式命名为Pm41。通过BSA分析发现,位于3BL染色体臂上的6个SSR标记Xwmc326、Xbarc77、Xbarc84、Xwmc687、Xgwm114和Xwmc236与Pm41基因连锁。利用中国春第三部分同源群的缺体-四体、双端体和缺失系将Pm41基因定位于3BL末端Bin 0.63-1.00染色体物理区间。进一步开发出与Pm41基因连锁的EST-STS标记BE489472 、 BE637789和BE517780,整合到遗传图谱,将Pm41基因定位于BE489472和XWMC687之间2.7cM的遗传区间(图2; Li et al., 2009)。

图2 抗*粉白**病基因Pm41分子标记定位(Li et al., 2009)
2.2 再次相近
此后,利用175个Langdon/IW2 F6代重组自交系群体对Pm41基因进一步定位。采用比较基因组学分析发现,Pm41位点基因组区域与短柄草2号染色体、水稻1号染色体和高粱3号染色体同源区间存在良好的共线性关系,据此开发了19个多态性分子标记,加密了Pm41遗传连锁图谱,将其定位于XWGGC1505和XWGGC1507两个分子标记之间0.6 cM的遗传区间,并找到与Pm41共分离的分子标记XWGGC1506。该区间对应短柄草11.7 kb、水稻19.2 kb和高粱24.9 kb的基因组区域(Wang et al., 2014)。
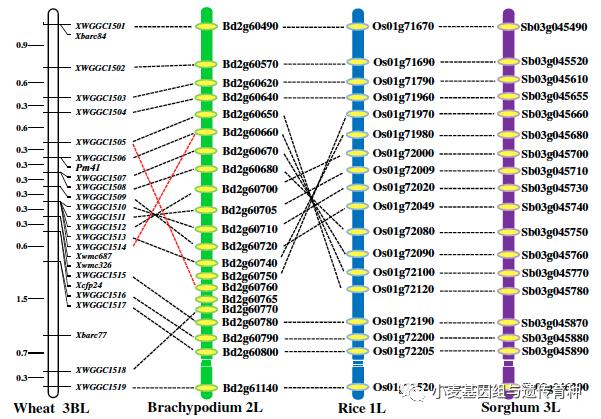
图3 抗*粉白**病基因Pm41比较基因组学定位(Wang et al., 2014)
2.3 “梅花三弄”
李淼淼等利用55个采自不同生态区的*粉白**菌菌株对IW2进行抗性鉴定,发现IW2对其中51个菌株(92.73%)表现抗性,说明Pm41的抗谱较广。BSR-Seq分析发现小麦3BL染色体上富集Pm41关联SNP最多,利用这些SNP序列和中国春3B染色体参考基因组序列,开发了8个与Pm41紧密连锁的多态性分子标记。利用2,448个Langdon/IW2 F2遗传作图群体,将Pm41基因定位于M171和M160两个分子标记之间0.08 cM的遗传区间,M78和M97分子标记与Pm41共分离(图4a)。对中国春3BL染色体参考基因组的Pm41基因定位区间进行基因注释分析发现,该区段包含4个蛋白质编码基因,但没有发现明显的抗病相关基因,推测野生二粒小麦IW2和普通小麦中国春在Pm41位点可能存在较大的序列变异。
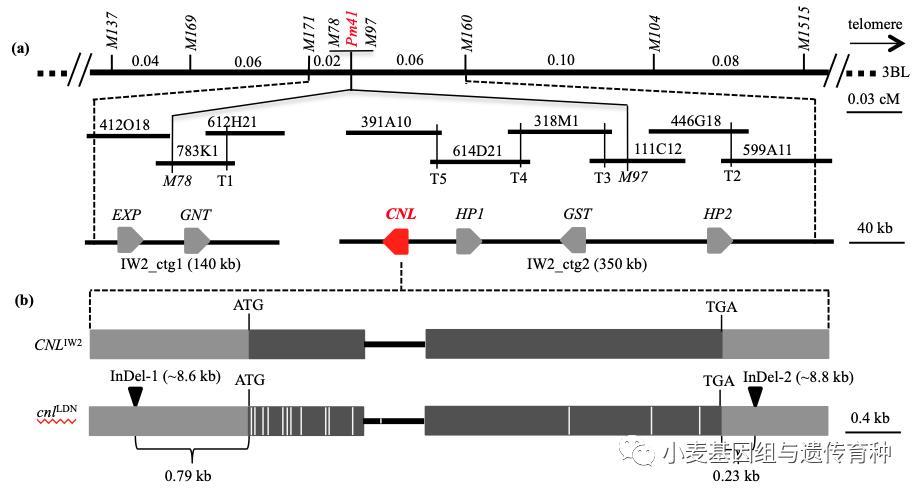
图4 抗*粉白**病基因Pm41的图位克隆(Li et al., 2020)
3.终于相遇- Pm41的克隆
为了克隆Pm41基因,构建了IW2品系BAC文库,采用染色体登录和步移的策略构建了Pm41基因的物理图谱。IW2的BAC文库含有326,784个HindIII酶切位点BAC克隆,平均插入片段120 kb。首先利用与Pm41距离最近的紧密连锁或共分离分子标记M78、M97、M160和M171筛选BAC文库获得4组阳性BAC克隆。通过BAC测序和序列组装,利用阳性BAC克隆末端序列设计5个特异标记T1-T5继续筛选BAC文库。最终获得9个阳性BAC克隆构建的BAC跨叠群(图4),BAC测序和序列拼接获得两个非重叠的contigs序列,IW2_ctg1 (140 kb) 和 IW2_ctg2 (350 kb)。两条contigs注释出6个蛋白质编码基因,其中包含一个抗病基因CNL,被视为Pm41的候选基因(图4)。此后,四倍体野生二粒小麦 “Zavitan”和硬粒小麦“Svevo”的参考基因组陆续释放,将Pm41位点基因组区域在IW2、Zavitan、Svevo和中国春中进行共线性分析,发现CNL/cnl基因仅存在于四倍体小麦3B染色体上,而在六倍体中国春中是缺失的(图5)。
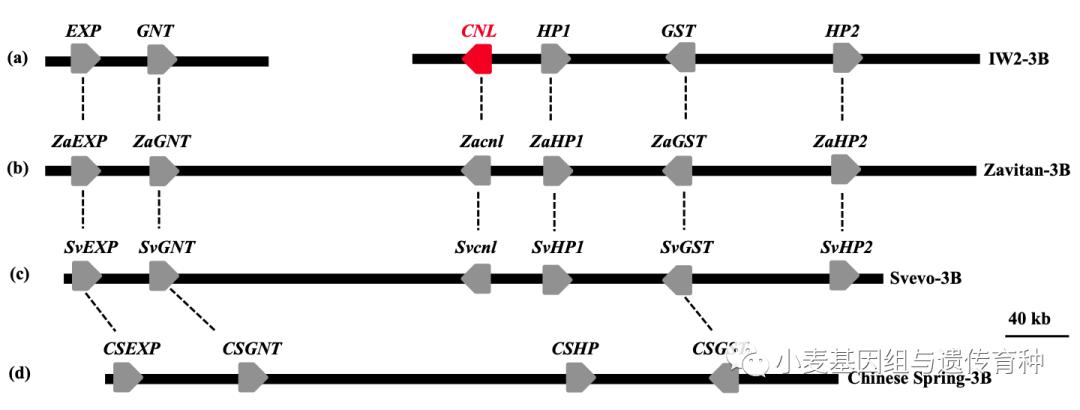
图5 Pm41基因组区段在小麦种间的比较(Li et al., 2020)
4.揭开面纱- Pm41的序列分析、验证及同源性分析
4.1序列变异分析
序列分析显示,与IW2中的CNL IW2相比,Zavitan、Svevo和LDN中的cnl等位基因在起始密码子ATG之前0.79 kb启动子区和3′ UTR区分别存在一个~8.6 kb mutator sub-class 插入缺失(InDel-1) 和~8.8 kb CACTA sub-class插入缺失(InDel-2),此外在基因编码区也存在多处SNP差异(图4b)。基因表达分析显示,在接种*粉白**菌前后,抗病野生二粒小麦亲本IW2中的CNL均有表达(图5a),并且明显受到病原菌的诱导(图5b),而感病硬粒小麦亲本Longdon的等位基因cnl不表达(图5a)。
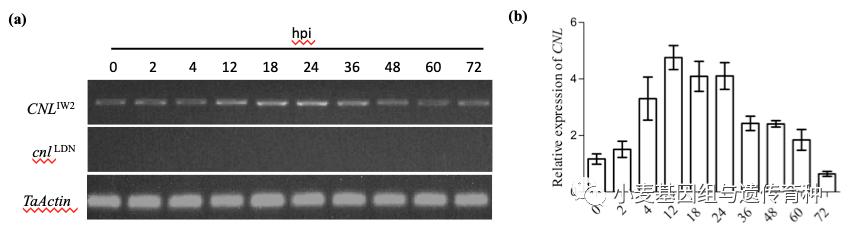
图6Pm41候选基因CNL的表达分析(Li et al., 2020)
4.2突变体验证
为了验证CNL基因是否具有抗*粉白**病的功能,我们利用EMS诱变创制IW2感*粉白**病突变体。根据M2代和M3代苗期接种鉴定,获得7个高感*粉白**病的突变体家系。进一步对这7个感病突变体的CNL基因全长DNA序列进行序列分析,发现这些突变体在CNL基因上都发生了错义突变或无义突变(图4)。其中M73 (G302E)、M215 (P354L)和M88 (S434N)错义突变位于NBS保守结构域上,M163 (R885W)、M198 (L816F)和 M113 (G872D)错义突变位于LRR保守结构域上。M107 (Q650*)中位于LRR结构域的无义突变导致蛋白翻译提前终止(图7)。这些突变体证明CNL基因对于Pm41的*粉白**病抗性是必需的。
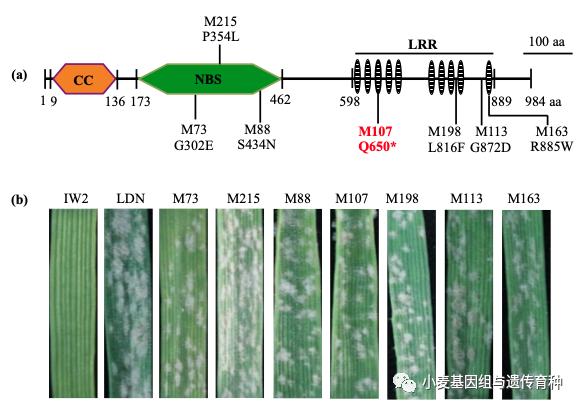
图7 Pm41候选基因的突变体功能验证(Li et al., 2020)
4.3转基因验证
我们分别构建了玉米Ubiquitin启动子驱动CNL基因全长CDS的过表达载体和CNL基因自身启动子驱动的CNL基因组全长序列的表达载体,采用农杆菌介导遗传转化高感*粉白**病小麦品种Fielder。利用E09菌株接种T0代转基因植株和T1代家系,发现CNL基因的过表达和自身启动子表达载体转基因阳性植株对E09菌株均表现高抗或免疫反应。基因表达分析显示T2过表达株系OECNL-5和互补转基因株系CNL-5 中的CNL转基因明显受到*粉白**菌诱导而上调表达,进一步证明了CNL为抗*粉白**基因Pm41(图8)。
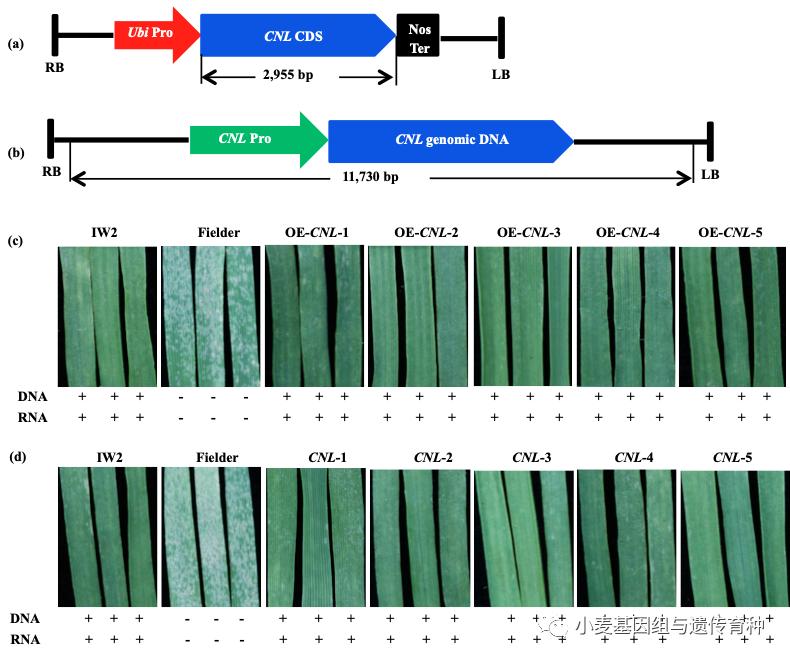
图8 Pm41候选基因的转基因功能验证(Li et al., 2020)
4.4同源性分析
分析PM41蛋白在麦类植物和其他植物中的同源蛋白发现,PM41同源蛋白只存在于野生二粒小麦Zavitan(TRIDC3BG077810)、硬粒小麦Svevo (TRITD3Bv1G261150.1)和Kronos(scaffold_036708)、普通小麦 Claire (scaffold_083040)的3B染色体,以及大麦Morex(Horvu3Hr1G112930.1)的3H染色体上。而在乌拉尔图小麦(AA)、粗山羊草(DD)、野生二粒小麦、硬粒小麦和中国春的A和D亚基因组上均没有直系同源蛋白。聚类分析显示PM41蛋白在其他植物中也未有同源蛋白存在。
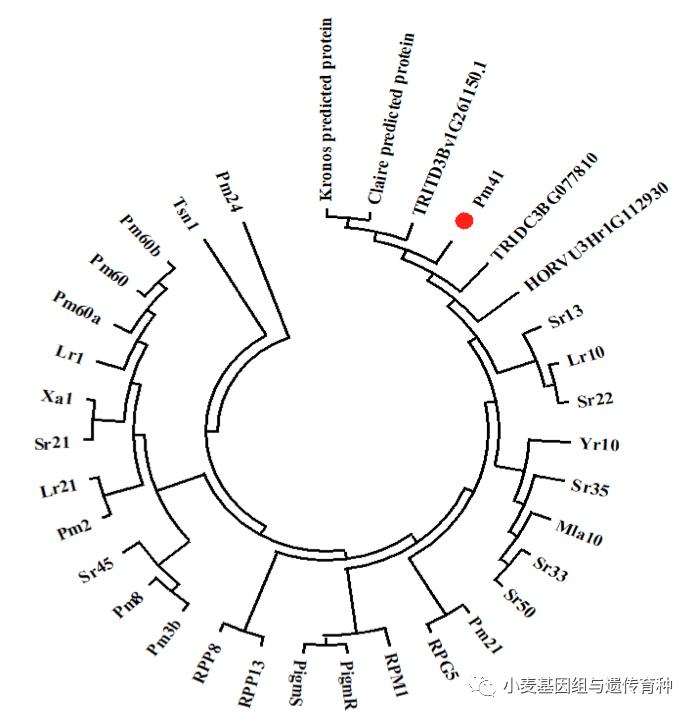
图9 Pm41抗病蛋白与小麦中部分抗病蛋白的聚类分析(Li et al., 2020)
5.探寻历史足迹-地理分布及单倍型分析
为了探明Pm41基因的地理分布和单倍型,开发了Pm41的功能标记WGGB427,分析了来自世界不同国家和地区的796份四倍体小麦和1122份普通小麦,只有8份(1.81%)野生二粒小麦品系(包括IW2)含有Pm41基因,进一步扩增基因全长序列发现其中5份材料的基因序列与Pm41完全一致,1份材料在第二个外显子上存在一处同义突变,1份材料在启动子区存在一处SNP。通过接种E09菌株发现,这些野生二粒小麦材料均表现免疫或高抗反应型。从地理分布上看,这8份野生二粒小麦均来自于以色列Mount Hermon及附近地区,与同样来源于野生二粒小麦的抗条锈病基因Yr15和Yr36的分布区域有部分重叠(图10; Huang et al., 2016;Klymiuk et al., 2019)。根据功能标记WGGB427的鉴定结果可将CNL基因划分为3种单倍型组(Hap-1、Hap-2和Hap-3),其中Hap-1包括携带CNL基因的8份野生二粒小麦材料,Hap-2包括像Longdon类型的728份四倍体小麦和726份普通小麦材料中的感病等位基因cnl,Hap-3包括如中国春类型的60份四倍体小麦和396份普通小麦材料,其中缺失了Pm41位点。

图10 Pm41基因的分布(Klymiuk et al., 2019; Li et al., 2020)
6.潜力无限-在抗病育种的应用价值
小麦抗*粉白**病基因Pm41编码的CNL蛋白是首次从野生二粒小麦中克隆的抗*粉白**病蛋白。野生二粒小麦是普通小麦的直接祖先,根据地理分布可划分为南部居群和北部居群,现代生物学和考古学证据显示小麦的驯化主要发生在北部居群(包括土耳其东南部地区)。从地理分布看,Pm41基因主要存在于野生二粒小麦的南部居群,而野生二粒小麦的北部居群、栽培二粒小麦、硬粒小麦和普通小麦中均不含有该基因,说明Pm41基因与同样来源于野生二粒小麦南部居群的抗条锈病基因Yr15和Yr36类似,在进化出来后就被限制在其发源地周边的野生二粒小麦居群中,没有参与到小麦的驯化和多倍化过程。转基因实验显示,Pm41基因在普通小麦Fielder中仍然表现高抗或免疫*粉白**病,说明该基因可以作为一个尚未利用的优异抗*粉白**病基因资源用于现代小麦抗病育种中。
小麦抗*粉白**病基因Pm41(CNL)的克隆由中国科学院遗传与发育生物学研究所刘志勇课题组、中国农业科学院作物科学研究所李洪杰课题组、中国农业大学、湖北省农业科学院植保土肥研究所、以色列海法大学和美国UC Davis等单位的研究人员合作完成。李根桥、王振忠、李淼淼、李贝贝等研究生同学先后参与了该项研究。研究结果2020年6月24日在线发表于New Phytologist杂志(Li et al., 2020)。
主要参考文献
-
Huang L, Sela H, Feng L, Chen Q, Krugman T, Yan J, Dubcovsky J, Fahima T. (2016) Distribution and haplotype diversity of WKSresistance genes in wild emmer wheat natural populations. Theoretical and Applied Genetics, 129: 921-934
-
Klymiuk V, Fatiukha A, Fahima T. (2019) Wheat tandem kinase provide insights on disease resistance gene flow and host-parasite co-evolution. Plant Journal, 98: 667-679
-
Li GQ, Fang TL, Zhang HT, Xie CJ, Li HJ, Yang TM, Nevo E,Fahima T, Sun QX, Liu ZY. (2009) Molecular identification of a new powdery mildew resistancegene Pm41 on chromosome 3BL derived from wild emmer (Triticum turgidum var. dicoccoides). Theoretical and Applied Genetics, 119: 531-539.
-
Li MM, Dong LL, Li BB, Wang ZZ, Xie JZ, Qiu D, Li YH, Shi WQ, Yang LJ, Wu QH, Chen YX, Lu P, Guo GH, Zhang HZ, Zhang PP, Zhu KY, Li YW, Zhang Y, Wang RG, Yuang CG, Liu W, Yu DZ, Luo MC, Fahima T, Nevo E, Li HJ, Liu ZY. (2020) A CNL protein in wild emmer wheat confers powdery mildew resistance. New Phytologist. DOI:10.1111/nph.16761
-
Wang ZZ, Cui Y, Chen YX, Zhang DY, Liang Y, Zhang D, Wu QH, Xie JZ, Ouyang SH, Li DL, Huang YL, Lu P, Wang GX, Yu MH, Zhou SH, Sun QX, Liu ZY. (2014) Comparative genetic mapping and genomic region collinearity analysis of the powdery mildew resistance gene Pm41. Theoretical and Applied Genetics, 127: 1741-1751
