Drugfocus药研视界 今天
评审要闻
我国第二家企业盐酸氨基葡萄糖胶囊通过仿制药一致性评价
近日,通过国家药品监督管理局网站获悉,浙江诚意药业股份有限公司的盐酸氨基葡萄糖胶囊(规格 240mg)已通过仿制药质量和疗效一致性评价,这是我国第二家通过企业,首家通过仿制药一致性评价的企业是浙江海正药业股份有限公司。另外,还有7家企业进行了本品参比制剂备案,准备开展仿制药一致性评价。
盐酸氨基酸葡萄糖胶囊是从天然原料甲壳素中提取盐酸氨基葡萄糖原料药制备得到的海洋类药品,临床用于治疗以及预防全身所有部位的骨关节炎。
批 准 情 况
本周,美国共批准品种1个(Type 5-新配方或新生产者)。我国CDE最新通过审评品种2个,均为补充申请。具体情况见下表。
本周美国FDA 批准的新药(NDA和BLA)
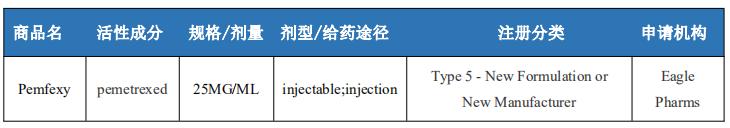
本周通过我国CDE审评的品种
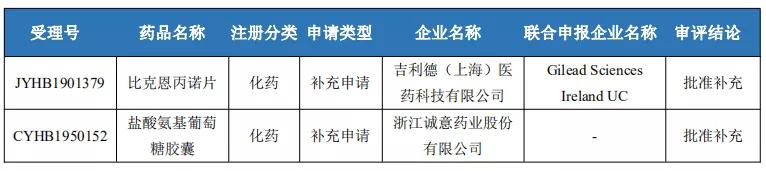
国内申报情况
本周,我国药审中心受理药品申报57项,其中化药49项,生物制品8项。1类新药申报2项,其中化学药1项(进口报临床),生物药1项(国产报临床)。化药2类改良型新药1项,化药3、4类仿制药申报生产分别为2项和4项;一致性评价申报8项,进口5类申报1项。
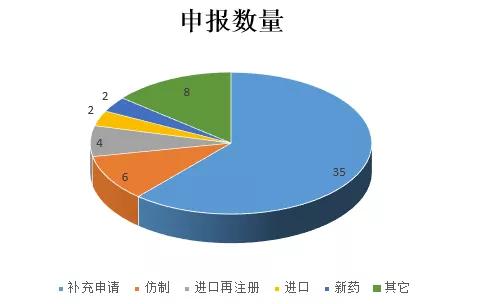
本周药品申报类型分析
本周国内1类新药申报情况
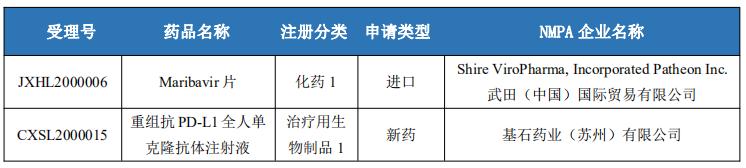
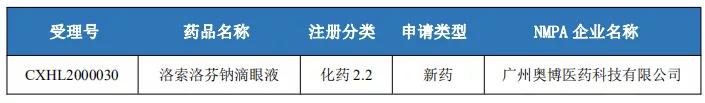
本周国内2类新药申报情况
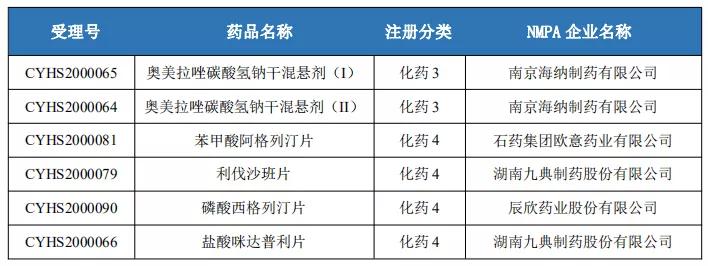
本周国内3、4类仿制药申报情况
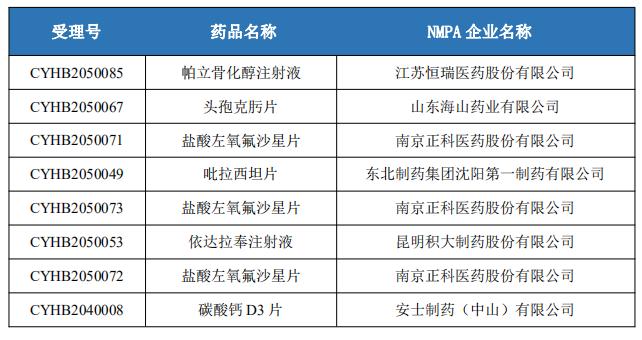
本周仿制药一致性评价申报情况
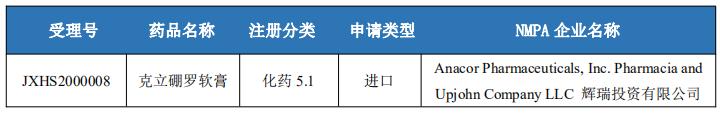
本周我国5类进口药申报情况
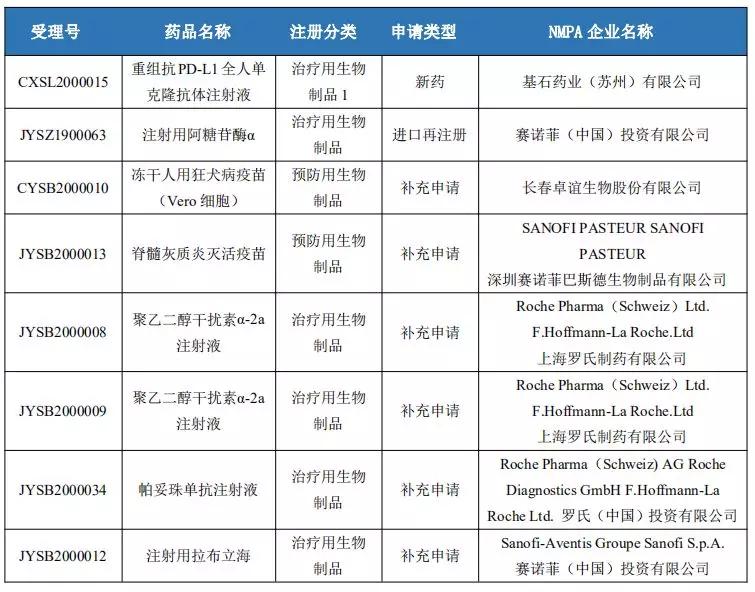
本周我国生物制品申报情况
整理:田田
编辑:唐辉
