痛风性关节炎(GA)是一种代谢性疾病,是由于尿酸钠晶体(MSU)沉积在关节腔引起的关节炎[1],急性发作时常表现为病变关节红肿、局部皮肤温度升高、疼痛剧烈,具有起病急、易反复、预后差的特点。在我国大约有1.1%的人口患有GA[2],发病率逐年升高[3],并且年轻化趋势越发明显。有研究表明,随着GA发病率的上升,并发肥胖、高血压、高脂血症、糖尿病等疾病的概率升高[4-5],严重影响患者的健康、生活质量,造成沉重的经济负担[6]。
中医认为GA急性发作时其病机主要为毒热、痰湿交结于关节,以实热证为主。刺血疗法是中医外治疗法中的一种,即在病变部位迅速点刺以泄出一定量的血液来达到泄热、活血化瘀作用。壮医药线点灸为极具岭南地区特色的一种民族医药疗法,选取相关穴位利用壮医药线来进行点灸,通过药线的温热及药效对穴位进行刺激,使通路传导通畅、三气复归同步来引热外出、散瘀活血、消炎止痛等。
Toll样受体(TLRs)/髓样分化因子88(MyD88)信号通路调控着GA的发生发展[7],GA急性发作时MSU直接激活TLR,激活的TLR可通过MyD88的C端Toll/白介素-1受体(TIR)结构域形成复合物,最终激活核因子κB(NF-κB)[8]。NF-κB被活化后,启动相关基因的转录,促进炎症细胞因子的释放,不断增强放大炎症反应。IκB激酶β(IKK-β)在NF-κB激活的过程中作为关键元件和双向调节分子,在整个信号通路的表达当中起到至关重要的调节作用。有研究表明蠲痹历节清方具有很好的降尿酸效果,同时还可减轻痛风关节的局部炎症,其干预靶点为TLR4、MyD88、IKK-β和NF-κB抑制物α同分异构体(IκB-α)[9]。壮医药线点灸及刺血疗法对GA具有确切的疗效可能是其通过上调局部抗炎因子来发挥其抗炎作用,减少炎症细胞浸润,改善GA局部组织坏死,促进受损关节功能恢复[10-12]。在本研究中通过将尿酸钠悬浮液注入关节腔构建急性痛风性关节炎(AGA)大鼠模型,探讨基于TLRs/MyD88信号通路上刺血疗法以及壮医药线点灸对AGA的治疗作用和抗炎机制。无论是刺血疗法亦或是壮医药线点灸,其操作均十分简便,具有显著的疗效,不良反应较小,经济负担较轻,尤为适合在基层医院推广。
1 材料与方法
1.1 实验材料
1.1.1 实验动物 2021年5月—2022年3月选取SPF级SD雄性大鼠60只,体质量(200±20)g,购于湖南斯莱克公司〔实验动物许可证号:SCXK(湘)2019-0004〕。本研究取得广西中医药大学伦理委员会批准(DW20210426-055)。实验大鼠均分笼饲养于广西中医药大学科学实验中心动物实验室,饲养条件:室温(22±1)℃,湿度(50±10)%,实行12 h∶12 h 光暗照明循环,保持动物房环境安静,饲养期间自由进食饮水,定期清洁、消毒。
1.1.2 实验试剂 秋水仙碱(合肥博美生物科技有限公司,货号:QC8624);尿酸钠(美国Sigma-Aldrich公司,货号:U2875);苏木素-伊红(HE)染色试剂盒(武汉百仟度生物科技有限公司,货号:B1002);环氧化酶2(COX-2)(货号:RA22955)、白介素(IL)-8(货号:RA20553)、IL-10(货号:RA20090)酶联免疫吸附试验(ELISA)试剂盒购自Biowamp公司;BCA蛋白定量试剂盒购自BIOSHARP公司(货号:BL521A);MyD88(货号:bs-1047R)、IKK-β(货号:bs-4880R)抗体购于北京博奥森生物技术有限公司;GAPDH(货号:60004-1-lg)购于武汉三鹰生物技术有限公司;辣根过氧化物酶标记山羊抗兔(货号:A0208)、辣根过氧化物酶标记山羊抗小鼠(货号:A0216)均购于上海碧云天生物技术有限公司。
1.2 实验方法
1.2.1 实验动物分组 适应性饲养7 d后,将60只大鼠随机分为6组:空白组、模型组、刺血组、药线组,秋水仙碱组、刺血结合药线组,每组10只。
1.2.2 AGA大鼠模型制备 将0.9%氯化钠溶液0.2 mL注射至空白组大鼠右侧踝关节腔内。将剩余4组大鼠放至小动物麻醉机中,吸入异氟烷麻醉后抽取0.2 mL的尿酸钠悬浮液,于大鼠右侧踝关节后侧30°~40°方向进针进入关节腔,针下有明显的落空感时将尿酸钠悬浮液注入到关节腔内,踝关节对侧关节囊鼓起即为AGA大鼠造模成功。
1.2.3 右踝关节内外踝横截面直径 观察造模6、12、24、48、72 h后右踝关节肿胀度,在干预治疗前采取游标卡尺测量各组大鼠右踝关节内外踝横截面直径,每只大鼠连续测量右踝关节3次,读取数值取平均值并记录。
1.2.4 干预治疗方式 于造模24、48、72 h后进行干预治疗,每次治疗前对大鼠进行称重,灌胃标准为每100 g给药1 mL。秋水仙碱组给予5%秋水仙碱混悬液进行灌胃;刺血组选取AGA大鼠右踝关节局部最肿胀点即阿是穴,用6号注射针头在该处进行点刺放血,放血量约为0.1 mL。药线组沿着大鼠阿是穴采用壮医梅花围灸法进行药线点灸,即以阿是穴为中心点,围着中心点环形均匀点灸6壮。刺血结合药线组则为两种治疗方法结合进行治疗,操作方法与刺血组和药线组一致,即在阿是穴处先进行刺血疗法后再进行壮医药线梅花围灸法治疗。除秋水仙碱组以外的各组大鼠均以等量纯水灌胃。
1.2.5 大鼠标本采集 末次干预治疗结束后,腹腔注射10%水合氯醛对大鼠麻醉后于腹主动脉采血,4 ℃,3 000 r/min(离心半径8 cm),离心15 min,取上清液放入-80 ℃冰箱冻存。取血结束后立即处死大鼠,充分打开右踝关节腔,可看到关节软骨下的淡黄透亮光滑有韧性的组织,即为关节滑膜,每组随机选取7只大鼠右踝关节滑膜组织放至冻存管保存于液氮中用于蛋白免疫印迹法(Western blot)检测,将剩下3只大鼠右踝关节取下后,放至离心管中,加入4%的多聚甲醛溶液使组织固定用于HE染色。
1.2.6 右踝关节滑膜组织病理改变 将固定好的大鼠右踝关节依次梯度乙醇进行脱水,将样品包埋在石蜡中并切片。按照HE染色试剂盒说明书步骤进行操作,中性树胶封片,显微镜下观察右踝关节滑膜组织病理改变。
1.2.7 血清IL-8、IL-10、COX-2水平 按照ELISA试剂盒说明书进行操作,检测各组大鼠血清IL-8、IL-10、COX-2水平。
1.2.8 右踝关节滑膜组织MyD88、IKK-β水平 取各组大鼠右踝关节滑膜组织,加入裂解液进行组织裂解提取总蛋白,使用BCA试剂盒进行蛋白浓度测定,上样、电泳、转膜,5%脱脂牛奶封闭1 h。加入MyD88、IKK-β、GAPDH一抗,4 ℃低温孵育过夜,将膜用TBS-T缓冲液冲洗5次,加入相应的二抗在37 ℃下孵育1 h,洗膜后,使用ECL发光液使蛋白质条带可视化并采用一体式化学发光仪拍摄照片,运用Image J软件进行分析。
1.3 统计学方法 采用SPSS 21.0统计学软件进行数据分析,符合正态分布的计量资料采用(x±s)表示,多组间比较采用单因素方差分析,组间两两比较使用LSD-t检验;重复测量资料采用两因素重复测量方差分析。以P<0.05 为差异有统计学意义。
2 结果
2.1 各组大鼠的一般情况 空白组大鼠正常进食饮水,精神状态方面良好,毛发颜色自然有光泽,活动自如,反应迅速,动作敏捷;造模大鼠精神状态不佳,进食减少,毛发粗糙、暗黄、杂乱无序,右踝局部肤温升高,发红肿胀,活动量明显减少;干预治疗后刺血组、药线组,秋水仙碱组、刺血结合药线组大鼠较模型组一般情况均改善明显;秋水仙碱组大鼠出现腹泻,刺血组、药线组及刺血结合药线组大鼠二便正常。
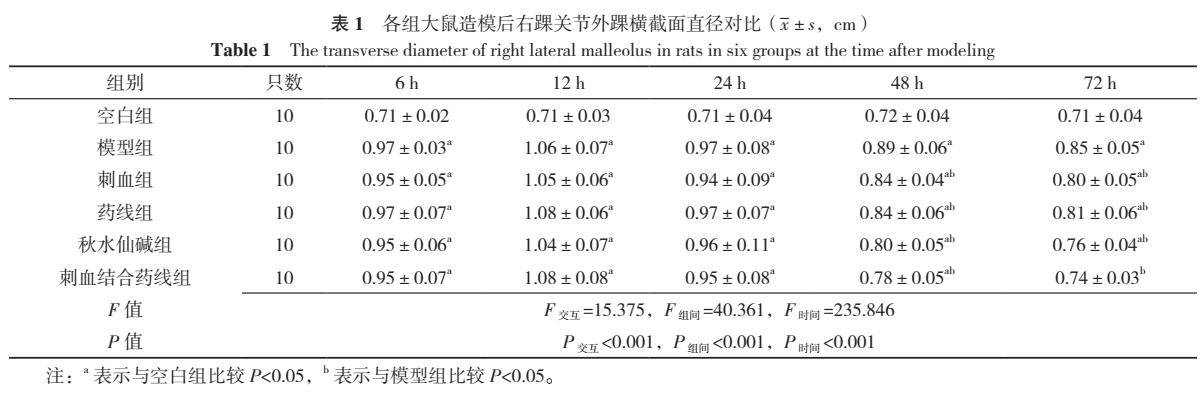
2.2 各组大鼠造模后右踝关节内外踝横截面直径 组间与时间对大鼠造模后右踝关节外踝横截面直径存在交互作用(P<0.05),组间和时间对大鼠造模后右踝关节外踝横截面直径主效应均显著(P<0.05)。6组间造模后右踝关节外踝横截面直径比较,差异有统计学意义(P<0.05);6组各时间点造模后右踝关节外踝横截面直径比较,差异均有统计学意义(P<0.05)。模型组、刺血组、药线组、秋水仙碱组造模后6、12、24、48 h、72 h右踝关节外踝横截面直径均高于空白组,刺血结合药线组造模后6、12、24、48 h右踝关节外踝横截面直径高于空白组,刺血组、药线组、秋水仙碱组、刺血结合药线组造模后48、72 h右踝关节外踝横截面直径低于模型组,差异均有统计学意义(P<0.05),见表1。
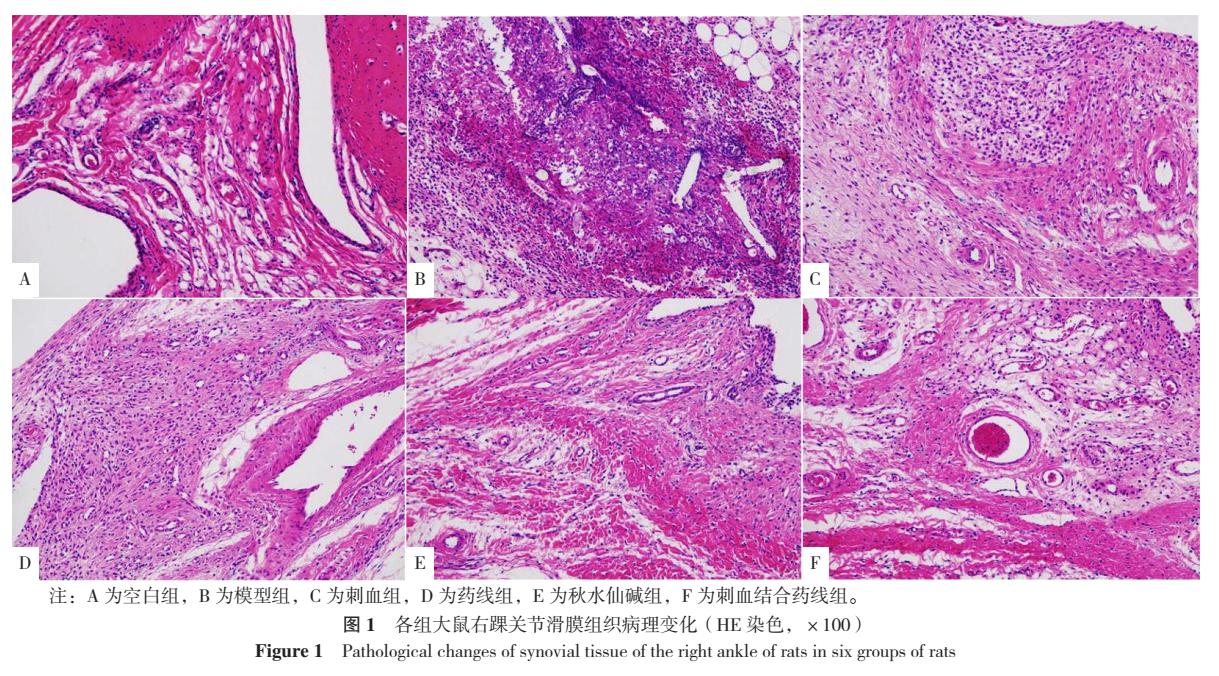
2.3 各组大鼠右踝关节滑膜组织病理变化影响 空白组大鼠右踝关节滑膜组织及细胞结构完整,胶原纤维有序排列,组织未见有明显炎性细胞;模型组大鼠右踝关节滑膜组织严重损伤,大面积坏死脱落,可见大量炎性细胞浸润。刺血组、药线组、秋水仙碱组及刺血结合药线组右踝关节其炎性细胞的浸润情况较模型组有所改善,滑膜组织结构轻度异常,炎性细胞浸润较少,详见图1。
2.4 各组大鼠血清IL-8、IL-10、COX-2水平比较 6组大鼠血清IL-8、IL-10、COX-2水平比较,差异有统计学意义(P<0.05)。模型组、刺血组、药线组、秋水仙碱组以及刺血结合药线组大鼠IL-8、COX-2水平高于空白组,IL-10水平低于空白组,秋水仙碱组、刺血结合药线组、刺血组、药线组IL-8、COX-2水平低于模型组,IL-10水平高于模型组,刺血组、药线组大鼠IL-8、COX-2水平高于秋水仙碱组,IL-10水平低于秋水仙碱组,刺血组、药线组大鼠IL-8、COX-2水平高于刺血结合药线组,IL-10水平低于刺血结合药线组,差异有统计学意义(P<0.05),见表2。

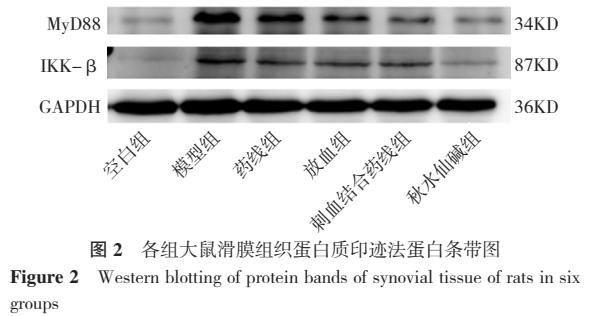
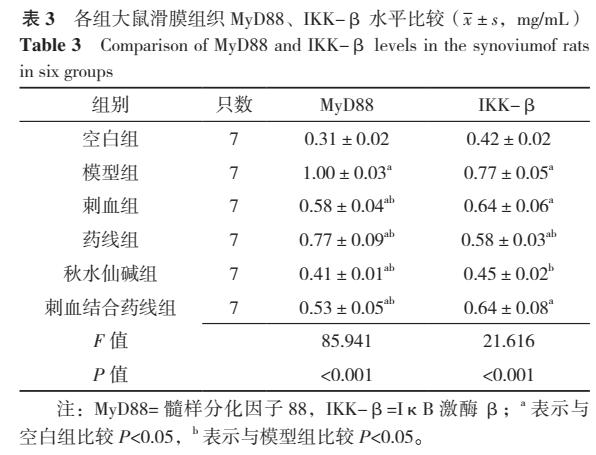
2.5 各组大鼠滑膜组织MyD88、IKK-β水平比较 6组间MyD88、IKK-β水平比较,差异有统计学意义(P<0.05)。模型组、药线组、刺血组、刺血结合药线组MyD88、IKK-β水平高于空白组,秋水仙碱组MyD88水平高于空白组,药线组、秋水仙碱组MyD88、IKK-β水平低于模型组,刺血组、刺血结合药线组MyD88水平低于模型组,差异均有统计学意义(P<0.05),见图2、表3。
3 讨论
AGA的发生和发展是饮食、遗传、环境等多种因素共同作用的结果[13],中医学认为AGA属于“痹症”“白虎历节风”等范畴,“痛风”这一概念最早是由朱丹溪提出来的,《格致余论·痛风论》中记载:“痛风者,大率因血受热……寒凉外搏,热血得寒,汗浊凝滞,所以作痛”,其病因病机主要为先天禀赋不足或机体感受外邪,邪气滞留关节,或内伤饮食,嗜食肥甘厚味,日久积而化热生痰,瘀毒痰浊相杂痹阻关节所致。而西医学上则认为MSU结晶沉积是导致AGA发生的关键因素,体内巨噬细胞可识别并吞噬MSU,激活相关炎性信号转导通路并释放炎性因子,产生强烈的炎症反应,引起剧烈疼痛,临床上一般表现为皮肤局部红肿,皮肤温度升高,剧痛拒按等症状。本研究通过将MSU注射至大鼠右踝关节制备AGA大鼠模型,其右踝表现与AGA临床症状基本相符合,结合滑膜组织病理学的改变,即滑膜组织表现不同程度损伤坏死、存在大量炎症细胞浸润,说明造模成功。在本次研究中,模型组在造模后逐渐出现右踝关节肿胀,12 h达到高峰,经治疗后,秋水仙碱组、刺血组、药线组及刺血结合药线组均能不同程度缓解关节肿胀,其中造模72 h后,空白组与刺血结合药线组大鼠右踝关节肿胀度比较,差异无统计学意义,说明刺血疗法结合壮医药线点灸在改善踝关节肿胀方面最优。秋水仙碱组大鼠在治疗期间出现腹泻,考虑为秋水仙碱引起的胃肠道反应,而余治疗各组大便正常,说明在刺血疗法及壮医药线点灸不仅能有效改善AGA关节症状,且不良反应少。
《灵枢·小针解》中指出:“满则泄之者,气口盛则当泄之也。宛陈则除之者,去血脉也”,道出了对于血实、热毒、湿热、气滞血瘀等的实证的疾病应当予刺血疗法来治疗,起到泄热、活血化瘀、调节气血、淤血去则新生等作用。在岭南地区因其特殊的地理环境气候造就了疾病多具有湿热瘀毒特征,壮医学认为“寒手热背肿在梅”,指的是肿块类型的疾病,可选择以最肿胀部位为中心,围着肿块围灸,呈梅花形分布,能软坚散结、活血消肿、解毒消炎。故从中医学结合民族医学的角度出发,刺血疗法结合壮医药线点灸可用于AGA的治疗。GA急性发作期间,MSU晶体的吞噬作用能诱导细胞膜的溶解、溶酶体和炎性递质的释放,以及单核细胞趋化蛋白1、趋化因子蛋白8、IL-8等趋化因子把中性粒细胞募集到炎性组织中,这些过程都会引起持续的炎症反应[14-15]。在免疫系统中,细胞因子在炎症和感染期间参与免疫反应,是最重要的信使分子和效应分子。TLRs参与机体的固有免疫,激活后既可促进多种炎性因子如IL-1β、IL-8等大量释放,进而在AGA炎症过程中产生炎症级联反应。故观察刺血疗法以及壮医药线点灸能否降低炎症反应,便可确定该治疗方法对AGA的应用价值。有研究表明对于内毒素致热的家兔,与单纯拔罐疗法相比,刺血疗法结合拔罐疗法能抑制粒细胞-巨噬细胞集落刺激因子、IL-1β、肿瘤坏死因子α(TNF-α)、IL-6的水平,抗炎、退热作用更优[16]。在沈谷丰等[17]研究中采用中药结合刺络放血法治疗GA患者能有效降低促炎因子TNF-α、IL-8、IL-1β水平,利于尿酸的排泄,改善GA的临床症状。在壮医药线点灸联合针刺疗法治疗膝骨性关节炎研究当中,IL-1β、IL-18水平明显下降,关节炎症得到改善,关节软骨的修复功能得到恢复[18]。在本研究当中,IL-10作为典型的抗炎细胞因子,减少炎症反应,改善临床症状[19]。IL-8是趋化因子中的一种,参与着炎症反应的整个过程。COX-2是一种诱导酶,调节着细胞的生长、迁移、增殖、自噬、凋亡和免疫反应,能促进前列腺素的合成,在组织损伤、炎症反应时表达较高,从而诱发明显的疼痛[20-21]。ELISA检测结果显示模型组大鼠中IL-8和COX-2水平升高,IL-10水平降低,说明AGA大鼠右踝关节出现过度的炎症反应,给予大鼠干预治疗后,AGA大鼠IL-8和COX-2水平降低,IL-10水平升高,提示刺血疗法及壮医药线点灸对AGA炎症反应具有一定的抑制作用,且秋水仙碱组与刺血结合药线组之间差异无统计学意义,说明在两者疗效相当,相比单纯刺血疗法或壮医药线点灸疗法,两者结合疗效最好。通过本次研究,证实了刺血疗法结合壮医药线点灸治疗AGA大鼠能有效抑制促炎因子分泌以及促进抗炎因子的释放。对于炎症反应来说,降低炎症因子,控制炎症风暴反应至关重要,本研究为刺血疗法结合壮医药线点灸治疗AGA提供了一定的可靠依据。
TLRs是一个特征明确的模式识别受体家族,在TLRs中除了TLR3外,其他TLR均需利用MyD88依赖性信号通路[22]。TLRs属于Ⅰ型跨膜蛋白,MyD88是机体内十分重要的信号传导蛋白,也是TLRs先天免疫反应信号途径和信号通路中介导的关键接头分子,其是经典激活途径中炎症递质NF-κB所必需的,而IKK-β作为NF-κB抑制物激酶复合物的主要催化亚基,又是激活NF-κB所必需的,从而诱导许多促炎因子分泌和其他免疫相关蛋白产生效应[23-24]。TLR/MyD88信号转导通路是目前GA发病机制研究最多的信号通路,GA急性发作时TLRs激活,并与通过MyD88依赖性途径触发先天免疫反应并启动下游信号通路,调节多种炎症相关基因的表达,通过MyD88的TIR结构域传递细胞内信号,进而激活转录因子,促进IL-8、IL-1β、IL-6、TNF-α等多种炎性因子的释放,产生炎症反应[25]。有研究表明痛风发作与体内MSU对Ⅰ型跨膜蛋白受体及激活其下游信号通路有关,异牡荆素可以降低关节肿胀程度,减轻炎症反应,改善AGA症状[26]。由此可知,TLRs/MyD88信号通路是改善AGA病情及减轻炎症的作用靶点。本研究刺血疗法结合壮医药线点灸能显著抑制AGA大鼠滑膜MyD88、IKK-β蛋白的表达。此外,刺血疗法结合壮医药线点灸可以抑制相关炎性因子以及促进对抗炎因子的分泌,对TLRs/MyD88信号传导通路起到抑制作用,调节炎性因子,对AGA起到治疗作用。
综上所述,本研究结果表明刺血疗法结合壮医药线点灸能更好降低关节肿胀程度,减轻炎症反应,与下调MyD88和IKK-β表达有关,TLRs/MyD88炎症反应信号转导通路的多靶点拮抗作用可能是该信号通路治疗AGA的抗炎机制之一。中医药以及民族医药是中国独有的宝库,希望通过本研究能为刺血疗法结合壮医药线点灸治疗AGA在临床工作中提供新的思路和相关理论依据,以期中医以及民族医学能得到更进一步的发展。
本文无利益冲突。
参考文献略
本文来源:朱丹萌,黄玉莹,罗统安,等. 刺血疗法结合壮医药线点灸对急性痛风性关节炎大鼠TLRs/MyD88信号通路的影响[J]. 中国全科医学,2023,26(20):2525-2531. DOI:10.12114/j.issn.1007-9572.2022.0775.