2020年的欧洲肝病学会年会(EASL2020)上,研究人员公布了关于基于RNAi靶点的乙肝在研新药VIR-2218体内外特性研究。由Vir Biotechnology研发的VIR-2218,目前已进入第2期临床试验。

乙肝新药VIR-2218,体外泛基因效应,体内持久抗病毒活性
研究人员介绍,RNAi干扰药物在全球应用广泛,通过靶向HBV-RNAs的RNAi治疗有望减少乙肝病毒抗原(包括免疫耐受期的乙肝表面抗原)的表达,促进功能性治疗。乙肝在研新药VIR-2218,是一种研究性的N-乙酰半乳糖胺(GalNAc)结合RNAi干扰类药物(研发靶点),利用增强的稳定化学作用,靶向所有HBV转录物共有的HBVx基因区。
研究人员在EASL2020发表了针对乙肝病毒研究性RNAi治疗剂VIR-2218的体外特性研究。通过转染介导的多细胞系统转染VIR-2218,检测其体外活性和特异性。使用psiCHECK2质粒中的荧光素酶读数,测定Cos7细胞中HBx基因的Pan基因型活性。检测表达HBV的HepG2.2.15细胞株的HBVmRNA、乙肝表面抗原(HBsAg)和乙肝e抗原(HBeAg)水平。
同时,研究人员还检测了VIR-2218,对HBV感染的HepG2-NTCP细胞的乙肝表面抗原(HBsAg)和乙肝e抗原(HBeAg)水平的影响。在活体内,通过单次或多次皮下注射VIR-2218,检测转染AAV8-HBV基因型D的小鼠的乙肝表面抗原(HBsAg)水平。结果表明,在体外检测转染psiCHECK2 HBV质粒(即代表HBV基因型A-J)的细胞中50 nM处的乙肝病毒-2218活性中:
显示X mRNA,对所有10种基因型均有下调(剩余仅有22.4%-51.4%)。在HepG2.2.15细胞中,乙肝在研新药VIR-2218的抑制HBVmRNA,呈剂量依赖性,例如HBsAgmRNA、HBeAg和HBsAg的IC50分别是766pm、2.21nm、499pm。这种研究结论,即达到有效抑制作用已经在HBV感染的HepG2 NTCP细胞的真实感染模型中得到证实。
在AAV-HBV小鼠模型中,使用单次SC剂量的0.3毫克/千克、1.0毫克/千克、3毫克/千克的VIR-2218,可以导致血清乙肝表面抗原(HBsAg)持续和剂量依赖性下降,对应以上3个剂量组分别是34%、72%、92%的最大降幅。此外,每隔一周6次或每月3次,或单剂量为9毫克/千克的小鼠,其血清乙肝表面抗原(HBsAg)呈剂量反应性下降,在最高剂量组中,乙肝表面抗原下降幅度最大为2.7-2.8log。
简单来讲,本研究解释了在研乙肝新药基于RNAi的VIR-2218的体内外特性研究,VIR-2218可以靶向乙肝病毒基因组的一个高度保守区域,在体外对乙肝病毒更具有泛基因型效应。另外,在体内方向,指在AAV-HBV小鼠模型中,乙肝在研新药VIR-2218表现出强大且持续的抗病毒活性。上述体外研究特性数据,支持研究人员继续在慢性乙肝新药领域对VIR-2218开发。

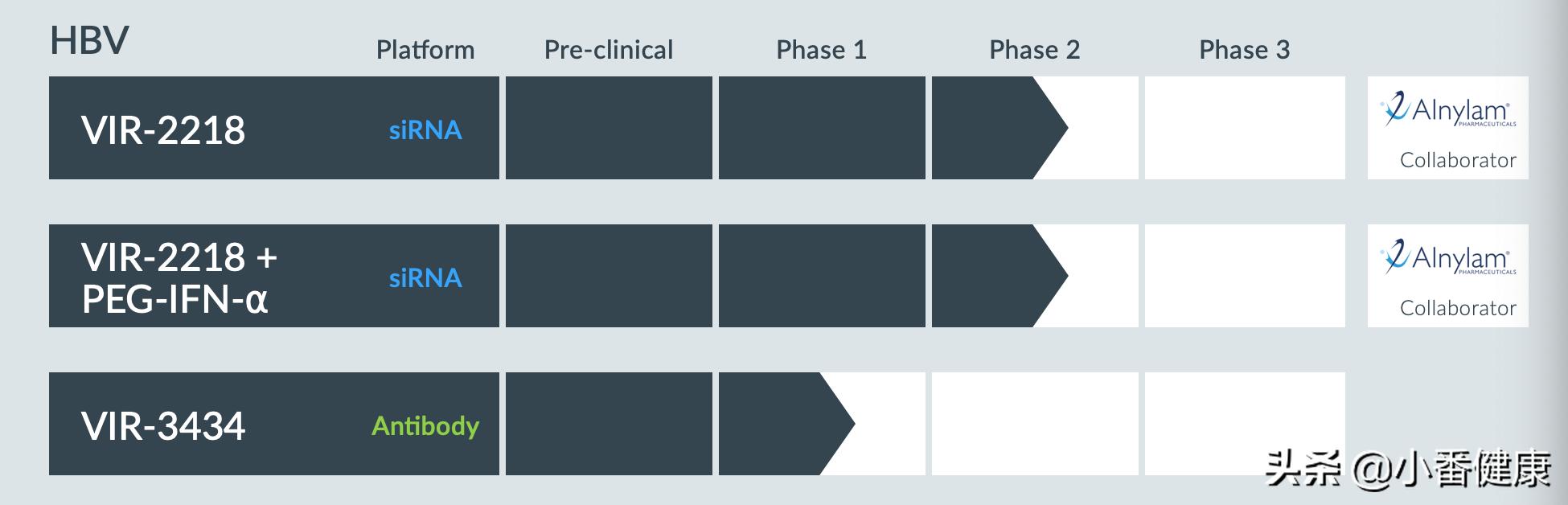
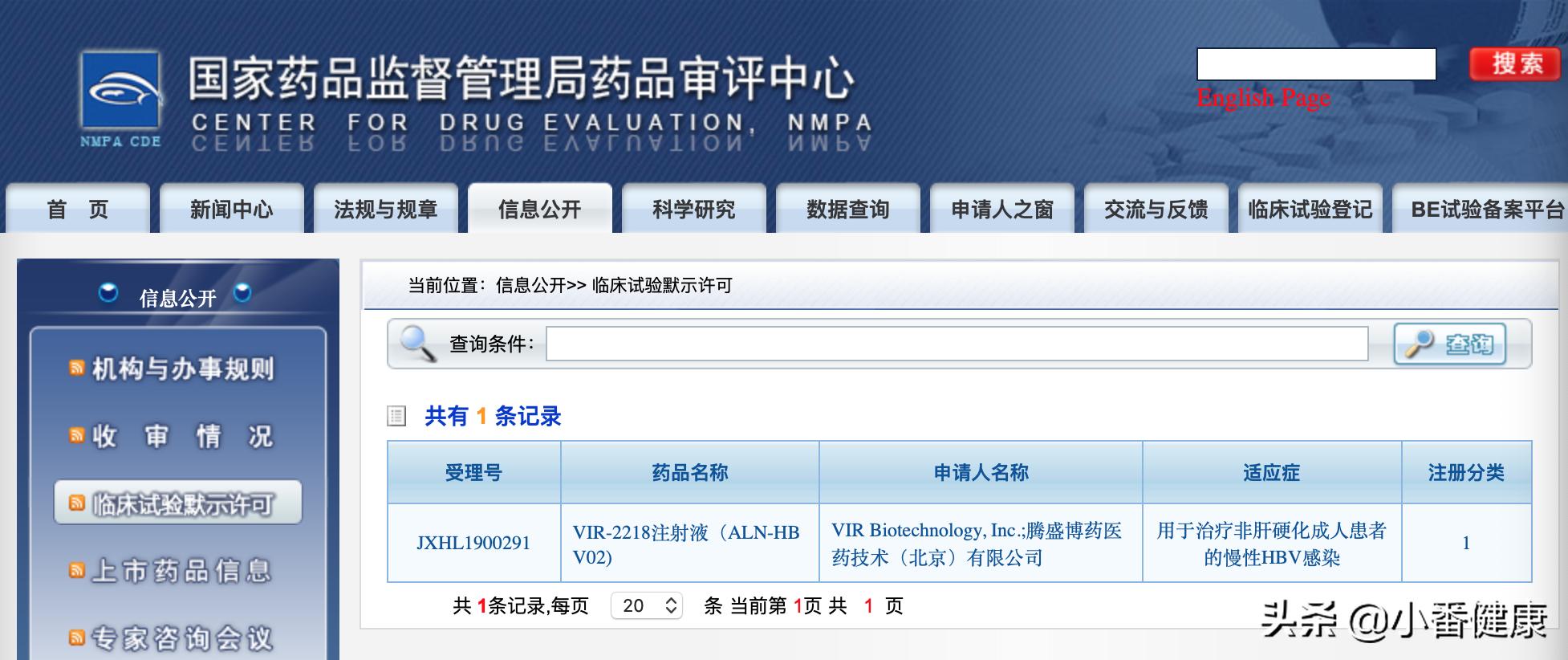
小番健康结语:可以见到,Vir Biotechnology在HBV药物研发管线中,VIR-2218已有两项进展到第2期临床试验,VIR-3434则进入第1期临床研究阶段(见上图研发管线图)。根据药监局药品审评中心,VIR-2218已获得临床试验默示许可,该药是一种RNAi治疗剂注射液。在我国该药试点医院为首都医科大学附属北京友谊医院,进展第2期临床研究;在国外该药已有两项研究进入第2期临床研究,有一项同时进行1期和2期临床研究(见上图全球和中国临床试验数据库)(本研究已发表于EASL2020)。