
作者丨常青
导读: 自2016年以来,截止2016.11.10日,CFDA公布医疗器械召回的企业达到39家,其中进口注册企业34家;国内注册企业5家(分别为:飞利浦医疗、通用电气、贝克曼库尔特、锐珂、苏州碧迪);发布召回通知121起,其中1级召回5起、II级召回33起、III级召回39起、未在中国销售的有44起。今年发布的召回产品总数达到250件。自新的《医疗器械监督管理条例》(650号令)实施以来,医疗器械产品召回的情况相对比较突出。
下面就2016年 CFDA发布的医疗器械召回情况进行分析:
2016年医疗器械召回明细▼
| 企业名称 | 召回总次数 | 召回次数明细 | 器械类别 | 注册性质 | ||||
| 序号 | I级 | II级 | III级 | 未在中国销售 | ||||
| 1 | 强生 | 26 | 0 | 6 | 5 | 15 | I/II/III类 | 进口 |
| 2 | 飞利浦(中国) | 6 | 0 | 0 | 6 | 0 | III类 | 进口 |
| 3 | 飞利浦医疗 | 5 | 0 | 0 | 5 | 0 | II/III类 | 国产 |
| 4 | 通用电气 | 8 | 0 | 4 | 0 | 4 | II/III类 | 国产 |
| 5 | 史赛克 | 8 | 0 | 0 | 2 | 6 | I/II/III类 | 进口 |
| 6 | 美敦力 | 7 | 0 | 4 | 0 | 3 | II/III类 | 进口 |
| 7 | 奥森多 | 7 | 0 | 3 | 4 | 0 | II/III类 | 进口 |
| 8 | 捷迈 | 6 | 0 | 3 | 1 | 2 | III类 | 进口 |
| 9 | 罗氏 | 4 | 0 | 1 | 1 | 2 | II类 | 进口 |
| 10 | 库克 | 4 | 0 | 0 | 0 | 3 | II/III类 | 进口 |
| 11 | 德尔格 | 3 | 2 | 1 | 0 | 0 | III类 | 进口 |
| 12 | 迈柯唯 | 3 | 2 | 1 | 0 | 0 | III类 | 进口 |
| 13 | 施乐辉 | 2 | 0 | 1 | 1 | 0 | II/III类 | 进口 |
| 14 | 雅培 | 2 | 0 | 0 | 1 | 1 | II类 | 进口 |
| 15 | 柯惠 | 2 | 0 | 0 | 0 | 2 | III类 | 进口 |
| 16 | 巴德 | 2 | 0 | 0 | 0 | 2 | II/III类 | 进口 |
| 17 | 邦美 | 2 | 0 | 0 | 0 | 2 | I/III类 | 进口 |
| 18 | 珀金埃尔默 | 2 | 0 | 1 | 0 | 1 | II/III类 | 进口 |
| 19 | 碧迪(上海) | 2 | 0 | 0 | 2 | 0 | I/II类 | 进口 |
| 20 | 爱尔康 | 1 | 0 | 0 | 1 | 0 | III类 | 进口 |
| 21 | 安科锐 | 1 | 0 | 1 | 0 | 0 | III类 | 进口 |
| 22 | 北京博士伦 | 1 | 1 | 0 | III类 | 进口 | ||
| 23 | 贝克曼库尔特 | 1 | 0 | 1 | 0 | 0 | II类 | 进口/国产 |
| 24 | 伯乐生命 | 1 | 0 | 0 | 1 | 0 | II类 | 进口 |
| 25 | 富士胶片 | 1 | 0 | 1 | 0 | 0 | III类 | 进口 |
| 26 | 豪洛捷医疗 | 1 | 0 | 0 | 1 | 0 | I类 | 进口 |
| 27 | 康蒂思 | 1 | 0 | 1 | 0 | 0 | III类 | 进口 |
| 28 | 康尔福盛 | 1 | 0 | 0 | 1 | 0 | III类 | 进口 |
| 29 | 马尼 | 1 | 0 | 0 | 1 | 0 | II类 | 进口 |
| 30 | 迈心诺 | 1 | 0 | 0 | 1 | 0 | II类 | 进口 |
| 31 | 梅里埃诊断 | 1 | 0 | 0 | 1 | 0 | III类 | 进口 |
| 32 | 日立阿洛卡 | 1 | 0 | 1 | 0 | 0 | III类 | 进口 |
| 33 | 锐珂 | 1 | 0 | 1 | 0 | 0 | II类 | 国产 |
| 34 | 赛默飞 | 1 | 0 | 0 | 1 | 0 | I类 | 进口 |
| 35 | 上海爱博才 | 1 | 0 | 1 | 0 | 0 | II类 | 进口 |
| 36 | 上海儒博 | 1 | 0 | 1 | 0 | 0 | II类 | 进口 |
| 37 | 苏州碧迪 | 1 | 0 | 0 | 1 | 0 | III类 | 国产 |
| 38 | 泰利福 | 1 | 1 | 0 | 0 | 0 | III类 | 进口 |
| 39 | 瓦里安 | 1 | 0 | 0 | 1 | 1 | III类 | 进口 |
| 合计 | 121 | 5 | 33 | 39 | 44 | —— | —— |
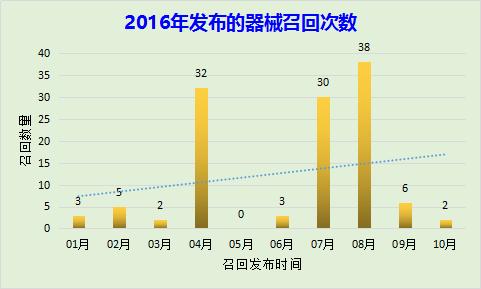
表2 2016年CFDA发布的召回器械情况▼
| 发布召回时间 | 发布召回件数 |
| 01月 | 3 |
| 02月 | 5 |
| 03月 | 2 |
| 04月 | 32 |
| 05月 | 0 |
| 06月 | 3 |
| 07月 | 30 |
| 08月 | 38 |
| 09月 | 6 |
| 10月 | 2 |
2016年器械召回原因为何?
通过今年器械情况进行汇总、分析,医疗器械召回的原因,主要分为两种情况:
1) 产品包装标签问题:标签信息与实际不符;
2) 产品生产、组装问题,导致使用过程中有潜在的功能危险。
什么是医疗器械召回?
依据《医疗器械召回管理办法(试行)》(卫生部令第82号)的规定:
医疗器械召回是指医疗器械生产企业按照规定的程序对其已上市销售的存在缺陷的某一类别、型号或者批次的产品,采取警示、检查、修理、重新标签、修改并完善说明书、软件升级、替换、收回、销毁等方式消除缺陷的行为。
医疗器械召回等级分为哪几种?
依据《医疗器械召回管理办法(试行)》(卫生部令第82号)的规定,按问题的严重等级,召回主要分为三种情况:
1)一级召回:使用该医疗器械可能或者已经引起严重健康危害的;
2)二级召回:使用该医疗器械可能或者已经引起暂时的或者可逆的健康危害的;
3)三级召回:使用该医疗器械引起危害的可能性较小但仍需要召回的。
如何评估器械即将产生的危害(缺陷)?
依据(卫生部令第82号)第十二条的规定, 对医疗器械缺陷进行评估的主要内容包括:
1)在使用医疗器械过程中是否发生过故障或者伤害;
2)在现有使用环境下是否会造成伤害,是否有科学文献、研究、相关试验或者验证能够解释伤害发生的原因;
3)伤害所涉及的地区范围和人群特点;
4)对人体健康造成的伤害程度;
5)伤害发生的概率;
6)发生伤害的短期和长期后果;
7)其他可能对人体造成伤害的因素。
注:在评估时,必须充分,不可遗漏掉相关的细节,任何疏忽都有可能造成严重的后果。
器械召回的流程是怎样的?
▼
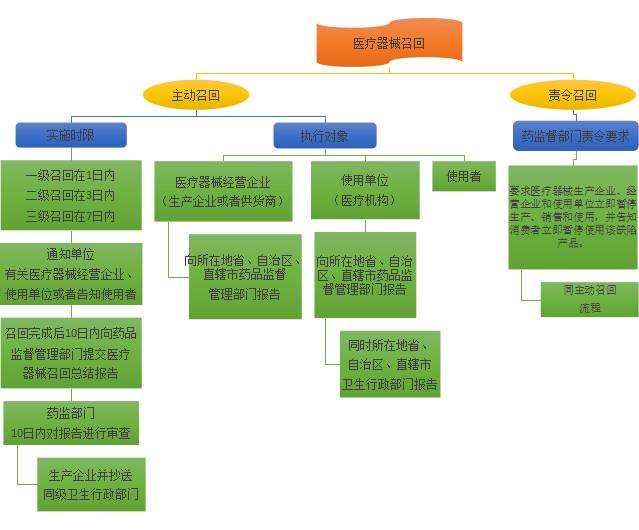
如何规避企业风险,将问题降到最低?
依据16.09.12 CFDA发布的《医疗器械召回管理办法》(征询意见稿)的规定,召回产品的范围,可分为以下四种情况:
1、正常使用情况下存在可能危及人体健康和生命安全的不合理的风险的产品;
2、不符合强制性标准、经注册或者备案的产品技术要求的产品;
3、不符合医疗器械生产、流通质量管理有关规定导致可能存在不合理风险的产品;
4、其他需要召回的产品。
当企业发现或接收到产品存在上述问题或经评估有必须进行召回时,应及时按法规的要求启动召回流程,以免产生更多的损失及危害。
转载需标注来源:弗锐达医械资讯