
阅读文章前辛苦您点下“关注”,方便讨论和分享,为了回馈您的支持,我将每日更新优质内容。
文 |不会飞的呆瓜
编辑 |不会飞的呆瓜

前言
介孔TiO2具有优良的光学性能和较大的比表面积,使其在光学检测中具有着广泛的应用。而由于介孔TiO2特殊的比表面形貌,使其对光具有极高的敏感度,因此介孔TiO2在生物传感器和对生物分子的光学检测过程中发挥了重要的作用。最近几年,基于介孔TiO2的免疫传感器的研究也得到了较快的发展。
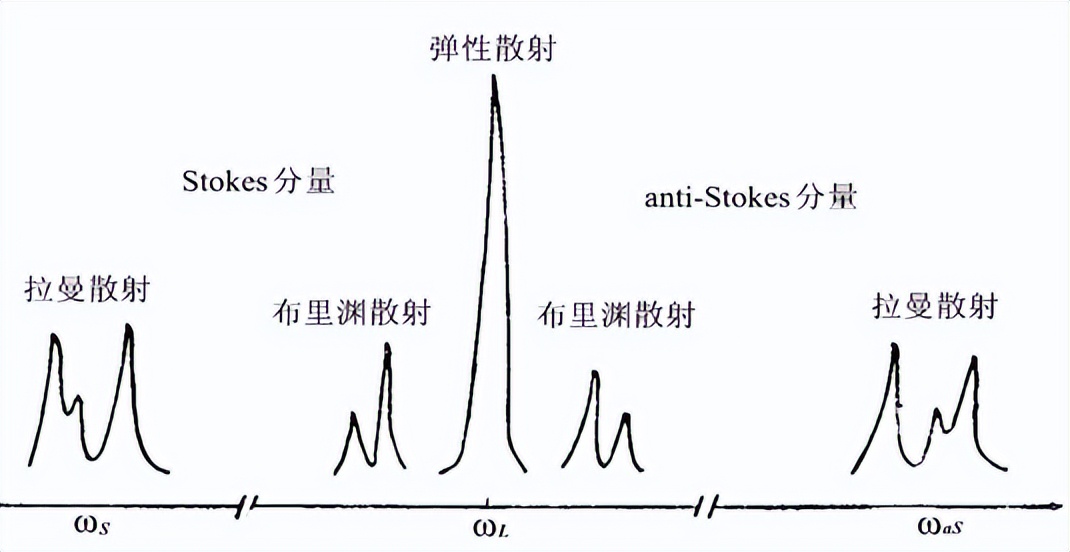
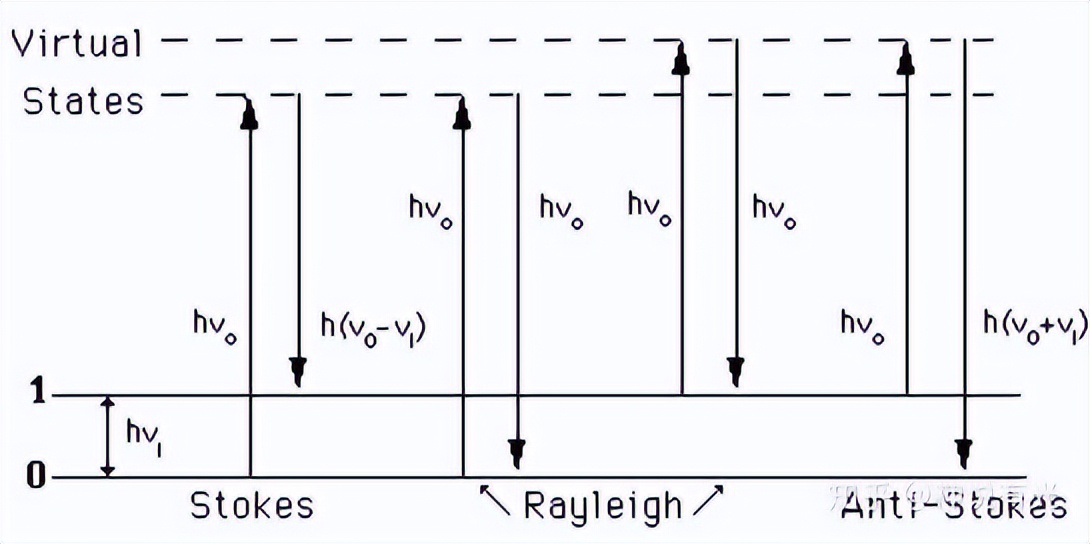
拉曼散射光谱检测,是一种重要的光学定量和定性手段。拉曼光谱作为一种分子散射光谱,通过激光照射之后产生特征的频率位移,而每一个特征频率位移对应着待检测物质分子的特征结构或成分信息。
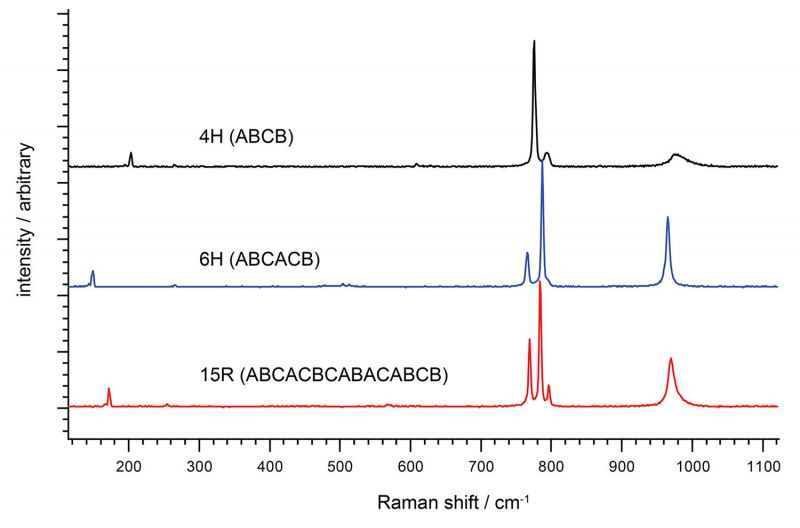
因此,通过对待检测物进行拉曼检测,特别是近红外拉曼检测,能够得到有关该检测物重要的生物学信息。拉曼检测可以作为检测抗原和抗体等生物分子之间的特殊相互作用的有效手段。
免疫分析以其独特的准确性和灵敏性,在食品安全、环境检测和医学临床诊断等领域发挥着重要的作用。
传统的免疫分析包括放射免疫分析法和酶联免疫分析法。为了进一步完善和提高免疫分析检测过程,通常将免疫分析与表面等离子共振、电化学和化学发光等技术结合,从而提高免疫分析的灵敏度。
本实验中制备的纳米介孔TiO2颗粒具有很强的拉曼散射信号,并且信号很稳定。使用纳米介孔TiO2作为拉曼标记分子,将其标记到甲胎蛋白(AFP)二抗上。
将AFP一抗固定到磁珠上,然后通过免疫反应将标记的AFP二抗、AFP抗原和AFP一抗连接到一起,进行拉曼检测,连接的AFP抗原越多,介孔TiO2越多,拉曼信号也就越强,从而实现对AFP抗原的定量检测。
本实验中使用纳米介孔TiO2作为拉曼标记物制备免疫传感器的方法还没有被报道过。TiO2的价格相当便宜,相比传统的使用昂贵的酶作为标记物的方法,大大降低了消耗,节约了成本。
钛酸四丁酯(TBOT),多巴胺(DA),牛血清白蛋白(BSA),1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(EDC)和N-羟基丁二酰亚胺(NHS)均购于上海阿拉丁试剂有限公司。
三嵌段共聚物(P123)是购于北京百灵威科技有限公司,甲胎蛋白(AFP)和甲胎蛋白抗体购于北京博奥森生物技术有限公司。磁性微球(-COOH,3,0~4,0µm,天津倍思乐色谱技术开发中心)。以上试剂均为分析纯,实验中溶液的配制均使用二次蒸馏水。
拉曼光谱仪(英国inViaRamanMicroscope),紫外可见分光光度计(Cary50,美国瓦里安公司),电子天平(北京赛多利斯仪器系统有限公司),箱式电阻炉(山东龙口先科仪器公司)。
取50mL钛酸四丁酯(TBOT)加入到20mL无水乙醇中,室温下搅拌,得到A液。取适量盐酸加入到40mL乙醇水溶液中,室温下搅拌,得到B液。将A液缓慢滴加到B液中,室温搅拌2h。
称取1.8g的三嵌段共聚物(P123),加入适量乙醇,室温下搅拌至完全溶解。取A和B的混合液加入到P123溶液中,室温下搅拌1h,得到均一透明的TiO2溶胶。
TiO2胶体先在40℃下放置12h以使溶剂挥发,在60℃下陈化24h,然后置于480℃下灼烧2h可得到纳米介孔TiO2。
量取15mL乙醇和水的混合溶液,置于50mL容量瓶中,N2保护下搅拌。称取0.03g多巴胺(DA),在氮气氛围下加入到混合溶液中,搅拌使其充分溶解。
称取0.05g介孔TiO2加入到上述溶液中,N2保护下避光搅拌3h。离心除去上清液,在40℃下干燥,得到淡黄色粉末,避光保存,备用。
称取0.001g制备好的DA/TiO2复合物,加入30µL戊二醛(5%),置于恒温振荡器中,37℃下振荡1h。离心,除去上清液,用PBS缓冲溶液清洗3次,最后离心除去上清液。
向沉淀物中加入100µL甲胎蛋白(AFP)二抗(30µg/mL),置于恒温振荡器中,37℃下振荡24h。离心,除去上清液,用PBS缓冲溶液清洗3次,最后离心除去上清液,得到介孔TiO2标记的AFP二抗。
量取100µL磁性微球于样品管中,加入300µL咪唑-盐酸(0.1M,pH=7,0)缓冲液,磁性分离之后,除去缓冲液,反复冲洗三次。
向样品管中加入100µL1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(EDC,0.8M)和100µLN-羟基丁二酰亚胺(NHS,0.2M),于恒温振荡器中,37℃下振荡1h,磁性分离,除去溶液,加入300µLPBS缓冲溶液(0.01M,pH=7.4),磁性分离之后,除去缓冲液,反复冲洗三次。

向样品管中加入100µL甲胎蛋白(AFP)一抗(20µg∙mL-1),置于恒温振荡器中,37℃下振荡24h,磁性分离之后,除去上清液,用PBS缓冲溶液清洗3次,磁性分离之后再加入200µLPBS缓冲溶液,摇匀。
向上述200µL甲胎蛋白(AFP)一抗包被的磁性微球中加入100µLBSA溶液(0.1%),置于恒温振荡器中,37℃下振荡1h,磁性分离之后,除去上清液,用PBS缓冲溶液清洗3次,磁性分离之后再加入200µLPBS缓冲溶液,摇匀。
加入100µL不同浓度的AFP抗原,置于恒温振荡器中,37℃下振荡2h,磁性分离之后,除去上清液,用PBS缓冲溶液清洗3次,磁性分离之后加入500µLPBS缓冲溶液,摇匀。
将上述500µL磁性微球悬浮液加入到介孔TiO2标记的AFP二抗中,摇匀,然后于恒温振荡器中,37℃下振荡2h。离心,用PBS缓冲溶液清洗3次,离心除去上清液。最后加入100µLPBS缓冲溶液,摇匀,用于拉曼散射检测。
本实验中进行的拉曼检测是在Pt片基底上进行的,Pt片基底的处理过程如下:先将Pt片放入二次水中超声15min,然后使用金相砂纸仔细打磨Pt片表面,使Pt片表面尽量光滑,放到乙醇溶液中超声15min,再放入*酮丙**中超声15min,重复上述过程,烘干备用。
量取1µL制备好的免疫磁性微球悬浮液,滴在干净的Pt片基底上,避光晾干,进行拉曼散射检测。

结果与讨论
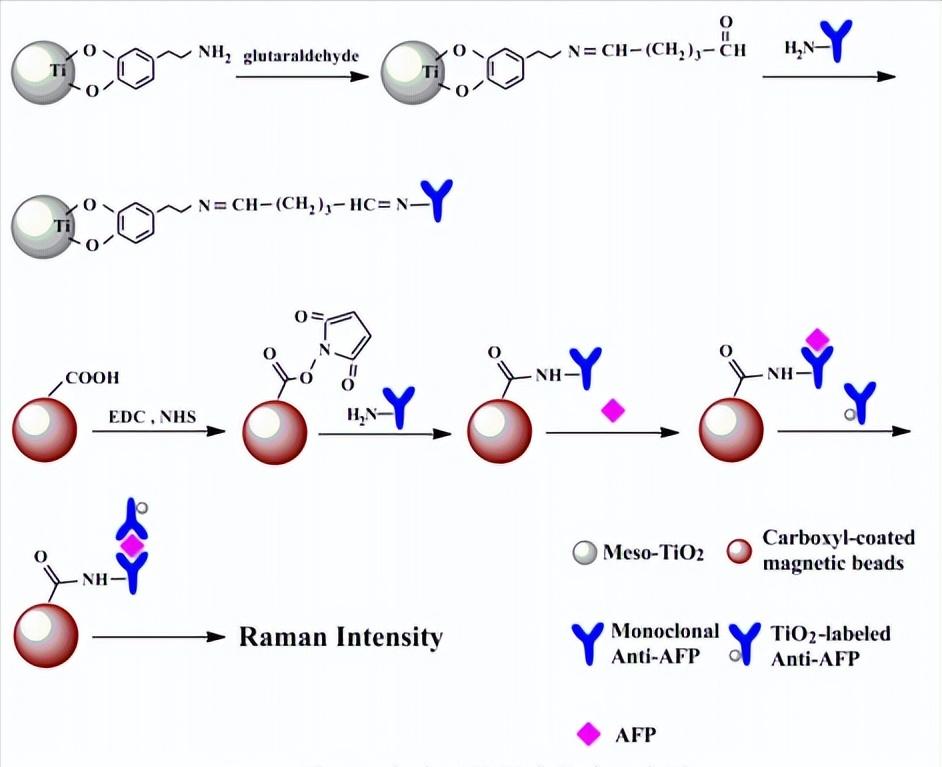
纳米介孔TiO2具有强度较高、稳定性号的拉曼散射信号,本实验基于这一现象将纳米介孔TiO2作为拉曼信号分子标记到甲胎蛋白(AFP)二抗上,通过免疫反应构建了一种双抗体夹心式的免疫磁性微球,通过拉曼散射检测,实现对AFP抗原的定量分析,构建过程如上图所示。
多巴胺(DA)与纳米介孔TiO2比较容易发生反应,通过反应可以将多巴胺上的氨基引入到纳米介孔TiO2上,实现对纳米介孔TiO2表面的*能官**团化,通过戊二醛的作用,可以将纳米介孔TiO2共价键合到AFP二抗上,实现了对AFP二抗的标记过程。
选用羧基化的磁性微球,使用1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(EDC)和N-羟基丁二酰亚胺(NHS)活化其羧基,然后将AFP一抗固定到磁性微球上,用BSA封板之后,与不同浓度的AFP抗原反应,再与纳米介孔TiO2标记的AFP二抗反应,得到免疫磁性微球,进行拉曼散射检测。
一定范围内,随着AFP抗原浓度的增加,免疫磁性微球的拉曼散射信号增强,从而实现对AFP抗原的定量检测。
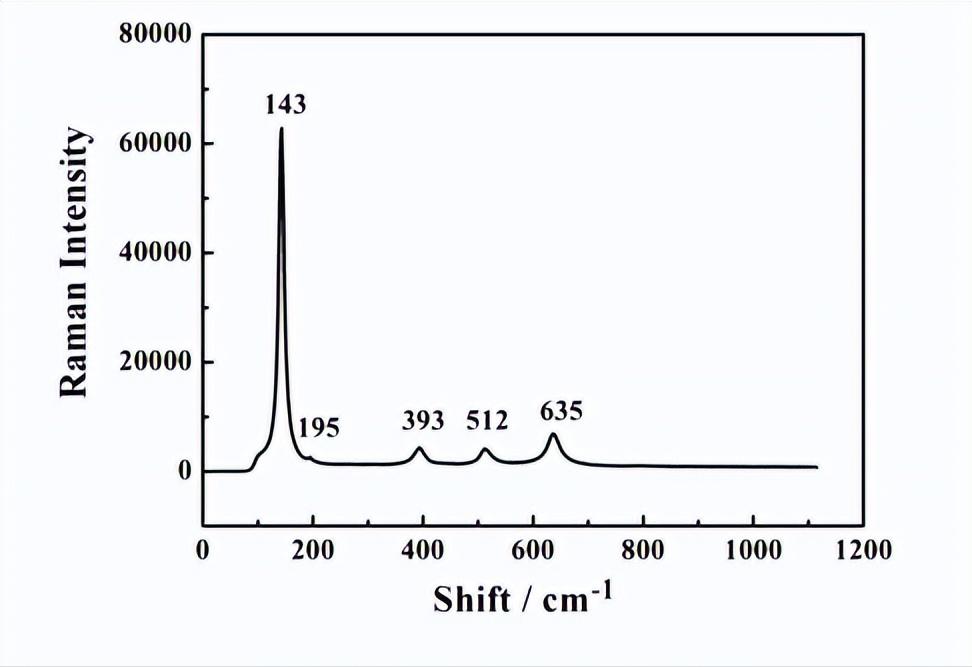
将制备好的纳米介孔TiO2颗粒均匀分散到PBS缓冲溶液(0,01M,pH=7,4)中,用移液枪取0,8µL悬浮液滴在清理干净的Pt片基底上,常温避光晾干,在波长为633nm的激光下进行拉曼散射检测。
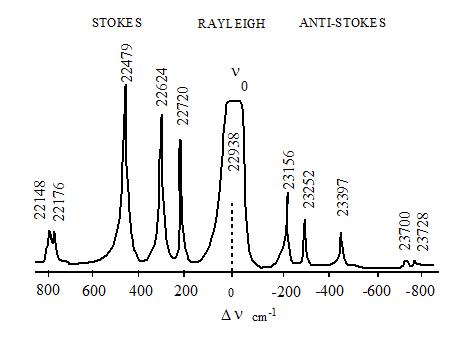
如下图所示。可以看出在143、195、393、512、635cm-1的位置出现了明显的峰,这几个峰是锐钛矿型TiO2的特征峰,说明本文介绍的方法成功制备了锐钛矿型的TiO2,而锐钛矿型的TiO2具有更加稳定和活跃的光学特性。
取适量的多巴胺(DA)溶解在PBS缓冲溶液中,取少量纳米介孔TiO2颗粒和用DA修饰之后的纳米介孔TiO2颗粒,使其充分分散在PBS缓冲溶液中
分别对这三个样品进行紫外可见光谱检测,如图4-3所示。根据报道,一定浓度的DA溶液的在210nm和280nm处有紫外吸收峰,下图中曲线a为DA溶液的紫外光谱图,在210nm和280nm处出现吸收峰,与报道一致。
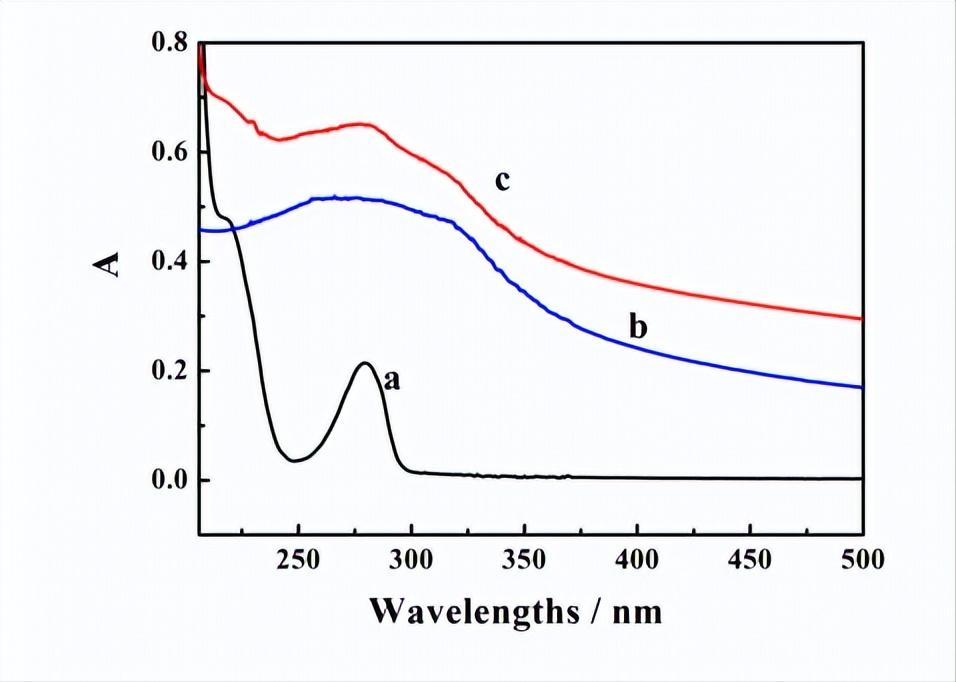
曲线b为纳米介孔TiO2颗粒的紫外光谱图,在300nm左右出现一个吸收峰,是TiO2的特征峰,与报道一致。
曲线c为DA修饰之后的纳米介孔TiO2颗粒的紫外光谱图,在210nm和280nm处有吸收峰出现,说明复合物中有DA的存在,在200nm~500nm范围内,吸收谱图变宽,这与TiO2的存在有关,而TiO2与DA的相互作用也导致大于300nm范围的吸收谱图变宽。
由此证明,本实验成功的将DA连接到介孔TiO2上,得到了DA/TiO2复合材料,从而在介孔TiO2上引入氨基。
为了对纳米介孔TiO2表面进行*能官**团化,本实验使用多巴胺(DA)与纳米介孔TiO2反应,由于DA带有氨基,因此可以在TiO2表面引入氨基。由于将DA与TiO2复合能够起到增强拉曼信号的作用,因此可以通过拉曼散射检测DA/TiO2进行表征。
对等量的纳米介孔TiO2和DA/TiO2进行拉曼散射检测,其结果如图4-4所示。下图a为DA/TiO2的拉曼散射图像,下图b为介孔TiO2的拉曼散射图像,DA/TiO2的拉曼散射信号要高于TiO2的信号,与报道一致。
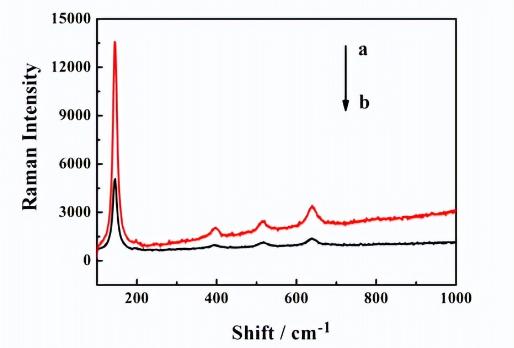
在143cm-1处有一个很强的散射峰,因此本实验根据143cm-1处的特征峰对甲胎蛋白(AFP)抗原进行定量检测。
取标记纳米介孔TiO2的甲胎蛋白(AFP)二抗和未标记纳米介孔TiO2的甲胎蛋白(AFP)二抗,经免疫反应制备免疫磁性微球,磁分离后,分别对其进行拉曼散射检测。
如下图所示, 曲线a为标记纳米介孔TiO2的AFP二抗反应制备的免疫磁性微球的拉曼散射光谱图,曲线b为未标记纳米介孔TiO2的AFP二抗反应制备的免疫磁性微球的拉曼散射光谱图。
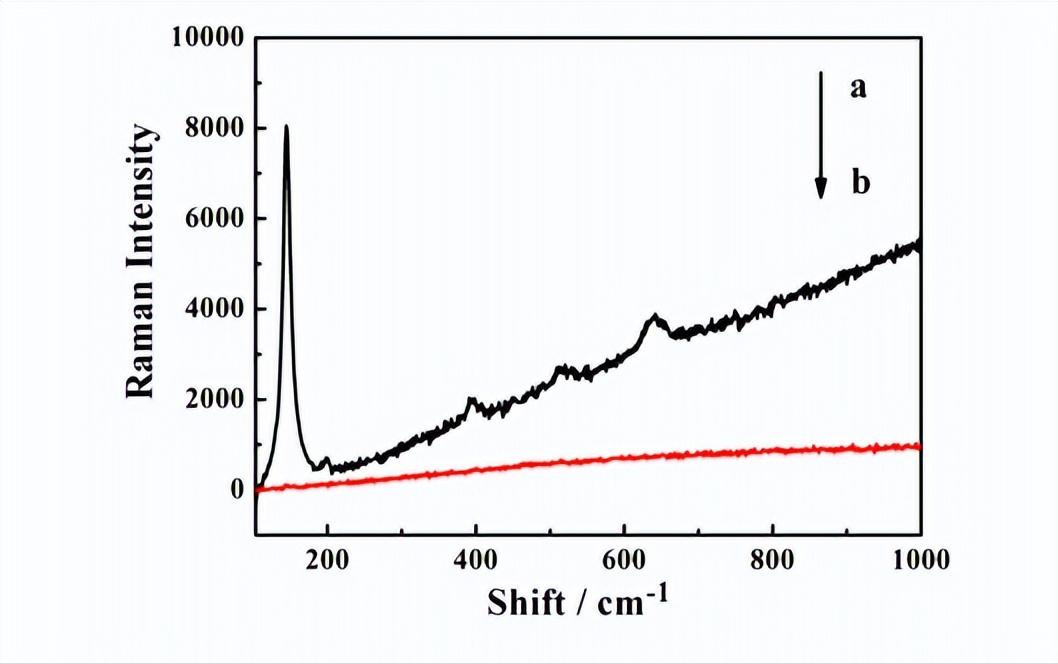
从上图中可以看出,未标记介孔TiO2的二抗反应制备的免疫磁性微球在100cm-1~1000cm-1范围内是没有拉曼信号的,而用介孔TiO2标记后,制备的免疫磁性微球上连接了介孔TiO2,因此出现了TiO2的特征拉曼散射峰,证明了该实验的可行性。
取介孔TiO2标记的甲胎蛋白(AFP)二抗和非介孔TiO2标记的甲胎蛋白(AFP)二抗,反应制备免疫磁性微球,磁性分离后,分别进行拉曼散射检测。
如下图所示,曲线a为介孔TiO2标记的AFP二抗反应制备的免疫磁性微球的拉曼散射光谱图,曲线b为非介孔TiO2标记的AFP二抗反应制备的免疫磁性微球的拉曼散射光谱图。
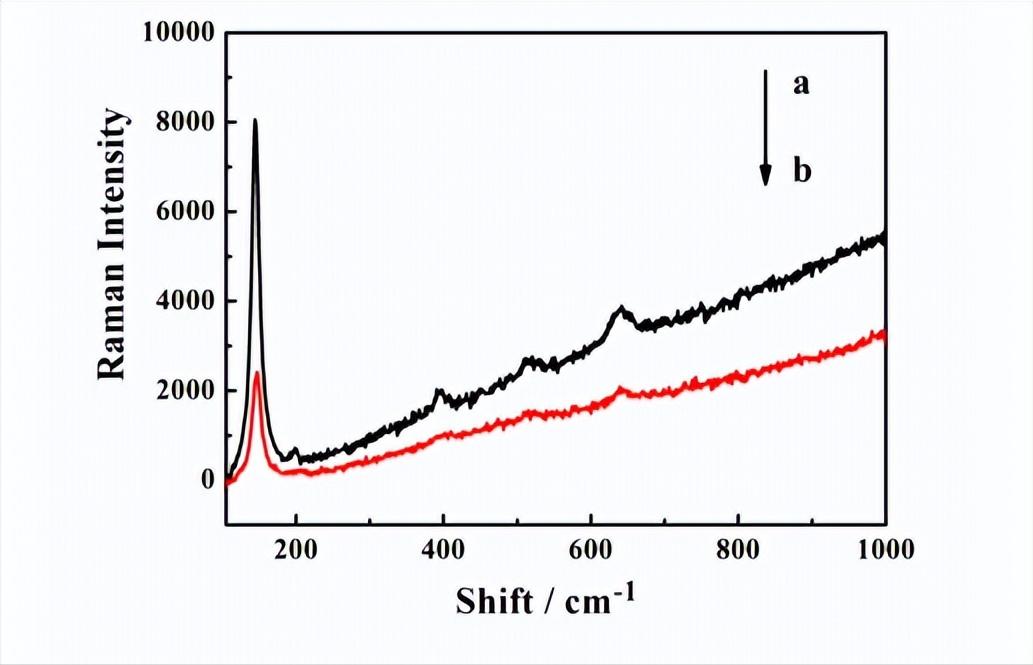
从图中可以看出,使用介孔TiO2标记二抗制备免疫磁性微球的拉曼散射信号要比使用非介孔TiO2标记二抗制备免疫磁性微球的拉曼信号要强,是因为介孔TiO2具有大的比表面积和较高的表面反应活性。
在与DA反应的过程中,介孔TiO2更容易与DA反应,从而连接上更多的氨基,得到的复合物其反应活性更强,在与AFP二抗反应的过程中,能够更多更容易的标记到二抗上,因此使用介孔TiO2标记的AFP二抗制备的免疫磁珠的拉曼信号就会更强。
结论
本实验通过多巴胺(DA)与纳米介孔TiO2反应,成功的将DA上的氨基引入到介孔TiO2,实现了对介孔TiO2的表面*能官**团化。
通过介孔TiO2表面的氨基,将介孔TiO2作为拉曼标记物标记到甲胎蛋白(AFP)二抗上,构建了一种双抗体夹心式的免疫复合磁性微球,通过拉曼检测对AFP抗原进行了定量检测,线性范围是0,05~20,0ng∙mL-1,检测限可达0,01ng∙mL-1。
由于纳米介孔TiO2的原料价格便宜,制备方法简单,因此本实验使用纳米介孔TiO2作为标记物标记二抗,取代了使用酶等蛋白质标记的传统方法,大大降低了实验成本,实现了对AFP抗原的定量检测,在生物研究和临床诊断中具有巨大的潜在应用。