临床前和临床证据表明,多巴胺和5-羟色胺部分激动剂阿立哌唑可以增强选择性5-羟色胺再摄取*制剂抑**艾司西酞普兰的抗抑郁功效。考虑到这些药物之间可能的神经化学相互作用,目前的研究调查了阿立哌唑是否改变了艾司西酞普兰的享乐和精神运动效应。
方法
雄性Sprague Dawley大鼠(n=116)接受10mg/kg/天的艾司西酞普兰(皮下),2mg/kg/天的阿立哌唑(皮下)或联合阿立哌唑+艾司西酞普兰,并检测诱导营养刺激的消耗(高果糖玉米糖浆和食物),刻板和自发运动。
在行为测试结束时,对参与奖赏过程的两个基因的mRNA进行量化:下丘脑前-黑素皮质素和海马脑源性神经营养因子。
结果
艾司西酞普兰在高果糖玉米糖浆消耗中产生了选择性但暂时的下降,阿立哌唑联合给药并未改变这一结果。艾司西酞普兰对运动没有显着影响,但阿立哌唑联合给药导致刻板印象持续增加。阿立哌唑+艾司西酞普兰组的脑源性神经营养因子和促黑素皮质素mRNA水平均低于艾司西酞普兰组。
表1 三种治疗方案下的卡路里消耗量
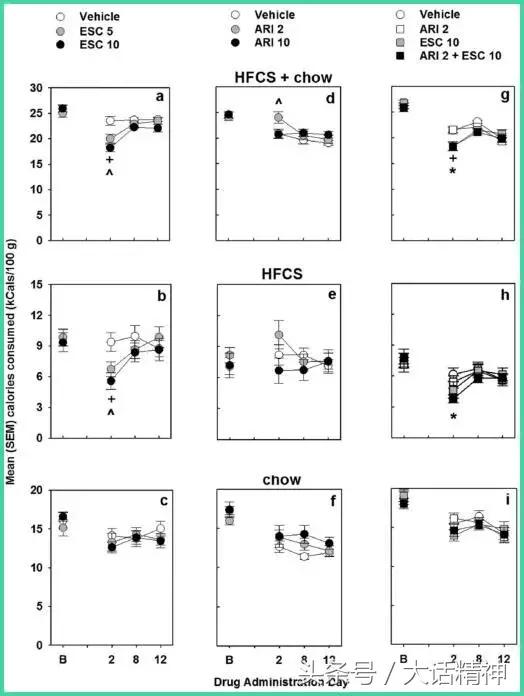
表2 试验第2、8、12天时的平均运动值
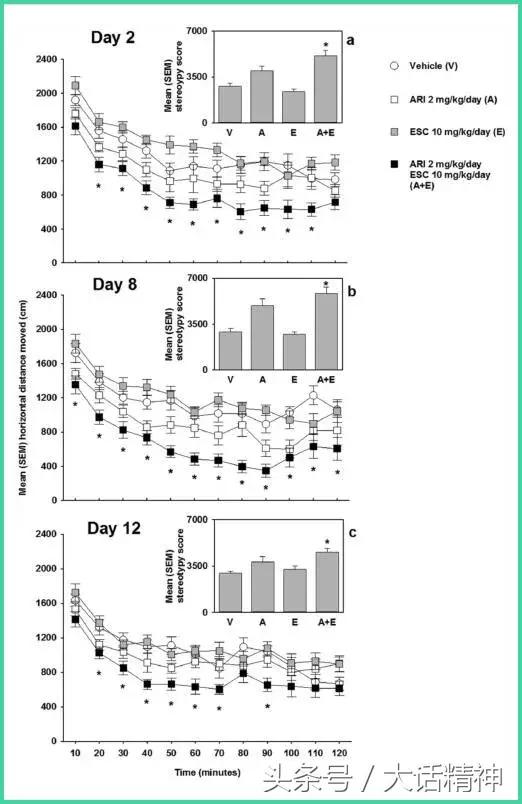
讨论
本研究调查了阿立哌唑对艾司西酞普兰享乐和精神运动功能的作用,探讨了不同治疗组对刺激、刻板印象和运动的反应,以及涉及消费美味食物,压力和抑郁的基因的表达。艾司西酞普兰单独使用时,大鼠的运动变化很小,但与阿立哌唑联合使用时,运动距离显著,行为刻板印象也随之增强。暴露于阿立哌唑+艾司西酞普兰组的大鼠的脑源性神经营养因子和促黑素皮质素mRNA水平均低于艾司西酞普兰组。研究结果表明,阿立哌唑确实可以改变艾司西酞普兰的运动激活特性,特别是在刻板领域。
在激励刺激消费的测试中,艾司西酞普兰引起的总卡路里摄入量短暂下降,这种影响并没有通过加入阿立哌唑而改变。本研究未能证明阿立哌唑诱导的艾司西酞普兰对激励营养刺激反应的增强作用。
阿立哌唑和艾司西酞普兰单独给药对运动活动的影响很小,但当联合使用时,整个给药期间存在持续显著的距离移动。同时,单独用药改变了刻板印象,但联合用药却显著增加了刻板行为。刻板行为和水平运动减少往往是联系在一起的,这表明联合用药产生的这些运动效应反映了精神运动刺激,而不是运动功能障碍。
此外,所测试药物的神经化学机制也解释了增强的运动刺激。 联合用药缓解了艾司西酞普兰对儿茶酚胺活性的抑制作用,并增加海马锥体神经元中5-HT1A受体的强直性激活,同时留下5-HT神经元放电率保持不变。另外,阿立哌唑增加了海马和前额皮质中的DA释放。
该研究中基因表达的改变似乎进一步表明,艾司西酞普兰和阿立哌唑的相互作用主要在运动水平,而不是激励功能。事实上,在给药结束后6天,联合用药组大鼠的下丘脑POMC mRNA表达显着降低,并且在海马BDNF中观察到类似的作用mRNA表达。POMC神经元的作用可能是通过阿立哌唑直接激活5-HT2C受体,或者通过由5-HT诱导的5-HT水平升高来激活相同的受体。临床和临床前的证据还表明,艾司西酞普兰治疗可以增加海马BDNF水平。因此,相对于艾司西酞普兰单独使用,联合用药大鼠中较低的表达水平与抑郁症中已知的海马BDNF表达形成对比,也进一步支持了在抑郁症动物模型中测试该药物组合的必要性。
总之,目前结果表明,在激励刺激或基因表达方面阿立哌唑对艾司西酞普兰的影响较小,相反,阿立哌唑加入到艾司西酞普兰中却能显著改善运动刺激。因此,这些大鼠的数据表明,阿立哌唑可以通过改善精神运动功能来增强艾司西酞普兰的抗抑郁功效。
参考文献
Hudson R, Zhou Y, LeriF. The combination of escitalopram and aripiprazole: Investigation ofpsychomotor effects in rats[J]. Journal of Psychopharmacology, 2017:0269881117732515.
更多精神心理资讯,可关注大话精神。
欢迎留言评论哦