
研究背景
PICC(经外周静脉穿刺中心静脉置管)在临床实践中得到了广泛应用,但也存在一些并发症和风险,如上肢深静脉血栓形成,甚至肺栓塞。静脉血栓形成的发生率为6.67% - 13.91%,其中肺栓塞发生率高达36% - 40%,死亡率为17.4%。
在血栓并发症患者中,导管相关右心房血栓在临床中很少见,但由于肺栓塞可能性较高,具有潜在的危险性。这些患者有多种治疗方案可供选择,包括手术取栓、全身抗凝、全身溶栓等,但最佳治疗方法仍存在争议。
病例报道
患者,女,52岁,因乳腺癌接受乳房切除术,术后将PICC管置于右头静脉进行化疗。3日后,患者右臂明显肿胀。采用多普勒超声检查上肢及心脏,显示右心房和PICC管周围均有血栓形成,右心房血凝块大小为2.5x2.3 cm(图2)。经心脏外科会诊后,因患者危险性高、创伤严重,不建议行心脏手术,患者随即转到血管外科治疗。
诊疗过程
患者急诊行肺动脉导管溶栓(CDT)+上腔静脉滤器植入+右锁骨下静脉CDT手术。术中血管造影显示PICC管周围右腋窝和锁骨下静脉有一长条血栓,另右心房有一血栓。上腔静脉、左右肺动脉分支血流通畅。
手术过程:研究人员首先通过右股静脉将溶栓导管植入右肺动脉干。目的是在右心房溶解血栓过程中,增加肺动脉的药物浓度以预防肺栓塞形成。经PICC导管造影证实上腔静脉无血栓形成后,经左股静脉置入上腔静脉滤器。该过滤器用于捕获溶栓过程中PICC周围右腋窝及锁骨下静脉血栓可能脱落的血块,预防肺栓塞。
其次,研究人员将PICC管替换为右锁骨下静脉溶栓导管,将导管尖置于上腔静脉(图1),分别通过两根导管注射10万IU剂量的尿激酶。术后将10万IU/24h/导管的低剂量尿激酶持续泵入导管,对导管鞘肝素化处理。每日检测血液学指标,包括血红蛋白、血小板、活化部分凝血活酶时间(APTT)和纤维蛋白原,以监测和避免出血风险。

图1 数字减影血管造影(DSA)分别显示右锁骨下静脉溶栓导管(a)、上腔静脉滤器(b)、右肺动脉干导管(c)
术后3日,右上肢和心脏多普勒超声显示导管周围无明显血栓形成,右心房血栓减小至2.3x1.3 cm大小(图2B)。术后6日,右心房血栓减小至1.3 x 0.9cm大小(图2C)。血管造影证实右腋窝及锁骨下静脉血流正常,研究人员取出右上肢导管。通过泵入低剂量尿激酶以继续肺动脉CDT。术后10日,超声心动图显示右心房血栓溶解(图2D)。
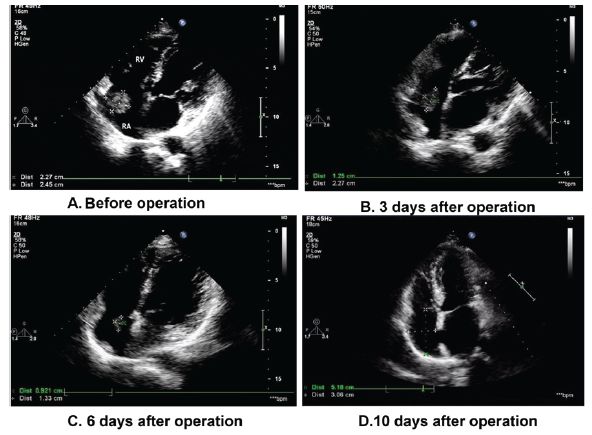
图2 术前以及术后3、6、10日心脏多普勒超声 (A)术前右心房血栓大小为2.5x2.3 cm (B)术后3日右心房血栓减小至2.3x1.3 cm (C)术后6日右心房血栓减少至1.3 x 0.9 cm (D)术后10日右心房血栓溶解
次日血管造影示上腔静脉及肺动脉血流正常,将上腔静脉滤器及肺动脉导管全部取出。研究人员在过滤器中捕获到一些血栓,经病理证实为血凝块。患者术后12日出院,出院后口服华法林持续抗凝。随访期间监测国际标准化比值(INR)和D-dimmer,以调整华法林剂量。
研究讨论
导管相关右心房血栓(CRAT)是PICC罕见的并发症。PICC管作为一种异物,造成局部损伤和血流动力学异常是血栓形成的主要原因。
一方面,导管尖端随着心脏跳动不断移动,反复摩擦会损伤右心房或血管内膜,导致凝血级联激活、血小板聚集、血栓形成。另一方面,导管尖端周围局部血流动力学异常可导致涡流和血流停滞,容易形成血栓。在以往关于CRAT的病例报道中,导管尖端大部分位于右心房。因此,心房血栓形成的主要危险因素是右心房的PICC尖端,为避免CRAT发生,我们应避免将PICC管尖端置于右心房。
结论
综上所述,对于右心房和上肢复杂血栓的治疗选择,随着血管外科和设备的发展,介入治疗可能是一种耐受性良好的治疗选择。两个用于溶栓的导管和一个用于预防肺栓塞过滤器的巧妙外科设计,突出显示这是治疗该类血栓安全可行、创伤最小的方法。
来源:Junwei Yan, Jiang Wu, Bing Liu, et al. Catheter-directed thrombolysis for thrombi in right atrium and upper extremity caused by peripherally inserted central catheters. Int J Case Rep Images 2019;10:101010Z01JY2019.