
沃森和艾博共同开发的mRNA疫苗
导读
国内新冠mRNA疫苗进展如何,恐怕很多人都在关心这个话题?
5月31日,军事医学科学院秦成峰学者等在medRxiv发表了一篇预印本文章,披露了沃森生物/艾博生物开发的新冠mRNA疫苗ARCoV(AWcorna)作为加强针的临床数据。
该疫苗由沃森生物、艾博生物和军事科学院共同研发,今年1月已在《柳叶刀·微生物》杂志上公布了其 I 期临床试验研究结果。
在奥密克戎毒株横行,新冠病毒持续变异的当下,国产mRNA疫苗ARCoV的有效性和安全性如何?它与国外研发的新冠mRNA疫苗相比,是否有优势?
业内人士指出,尽管作为加强针,艾博生物的mRNA疫苗比灭活疫苗更好,但相比国外已上市的mRNA疫苗,ARCoV疫苗产生的中和抗体浓度仍较低。
李晓韦、李安琪 | 撰文
叶水送 | 责编
新冠大流行推动了mRNA技术的发展。在国外医药公司纷纷进入mRNA疫苗赛道时,我国也没有放弃在这一领域的追逐,目前至少有10多家公司在加紧开发新冠mRNA疫苗。
近日,沃森生物/艾博生物的新冠mRNA疫苗ARCoV作为加强针的临床数据在预印本上发布,根据论文数据,其作为2针灭活疫苗之后的加强针有效性和安全性良好。
但也有业内人士表示,这一数据并不令人满意,因为引起的抗体滴度并不高。详细请见:艾博国产mRNA疫苗数据真和国外疫苗类似吗?增强针结果好吗?

01
艾博新冠mRNA疫苗加强针临床试验概况
本试验纳入了300名受试者,均为接种了2剂灭活病毒疫苗(CoronaVac或BBIBP-CorV)后6个月的成年人,并按照2:1比例接种了AWcorna mRNA疫苗或CoronaVac灭活疫苗作为加强针。

受试者基本特征
受试者中mRNA疫苗组平均年龄为43岁,灭活疫苗组为40岁,受试者中还包括了16位60岁或以上的老年人,以及27位合并基础疾病的受试者。
02
艾博新冠mRNA疫苗的有效性及安全性数据如何?
临床数据结果显示, 在接种了2剂灭活疫苗的基础上,沃森生物/艾博生物的ARCoV异源加强接种(第三针)能诱导出高于同源接种(灭活)的中和抗体,且有较好的安全性,但能否最终获批我们还不得而知。
有关疫苗的有效性和安全性数据如下:
1.两种疫苗针对原始毒株和德尔塔突变株比较

对原始新冠病毒或Delta变异株的中和抗体的GMT
ARCov异源接种诱导的中和抗体是CoronaVac同源接种的3.8倍和6.5倍。图a为两种疫苗针对新冠原始毒株,两组受试者血清的中和抗体均显著增高,第14天较第28天时高。其中ARCov组由加强接种前的4.4增高到加强接种28天时的242.4;CoronaVac组由加强接种前的4.5增高到加强接种28天时的64.3。
图b为两种疫苗针对德尔塔突变株,两组受试者血清的中和抗体亦显著增高,同样的,第14天的中和抗体浓度较第28天时高。其中ARCov组由加强接种前的4.2增高到加强接种28天时的257.8;CoronaVac组由加强接种前的4.1增高到加强接种28天时的39.8。
2.两种疫苗针对奥密克戎突变株的比较

奥密克戎变异株中和抗体的GMT
奥密克戎毒株的免疫逃逸能力强,这也是为何此前研发的新冠抗体对其无效的原因所在。此次结果显示:相比原始毒株,两种疫苗针对奥密克戎毒株,产生的中和抗体浓度都大为降低, 这也印证此前的研究,奥密克戎毒株免疫逃逸能力更强。
不过,mRNA仍比灭活疫苗效果更好一些,ARCov加强针接种诱导产生的中和抗体是CoronaVac加强针的4.4倍。 由于产生的中和抗体浓度都很低,因此行业人士指出,在真实世界中它是否有作为加强针存在的价值。
周叶斌博士在一篇文章中写道, “综合这些数据,虽然ARCoV异源增强高于灭活疫苗的同源增强,但比起已经上市的mRNA疫苗,差距明显,甚至不如国外已逐渐被mRNA疫苗取代的腺病毒疫苗”。
3.在60岁及以上老年群体中,两种疫苗比较
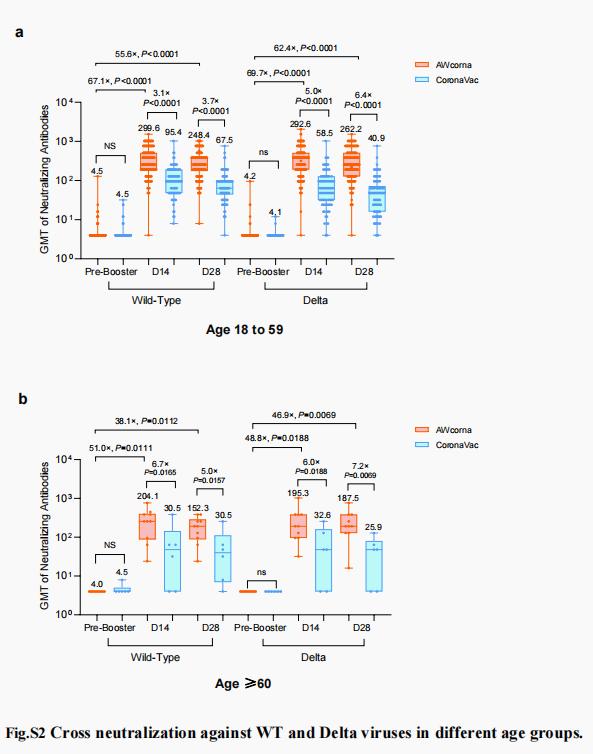
不同年龄组对原始毒株和Delta病毒的交叉中和作用
针对原始毒株,两组老年受试者接受加强针后中和抗体均显著增高,其中ARCov组由加强接种前的4.0增高到加强接种28天时的152.3;CoronaVac组由加强接种前的4.5增高到加强接种28天时的30.5,ARCov组是CoronaVac组的5倍。针对德尔塔毒株,两组老年受试者接受加强针后中和抗体同样显著增高,ARCov组在加强接种28天时中和抗体为187.5,CoronaVac组在加强接种28天时为25.9,前者是后者的7.2倍。
4.作为加强针,两种疫苗的安全性比较

在我国成年人群体中,艾博生物的mRNA疫苗异源接种安全数据
两组均未出现严重不良事件或死亡,ARCova组导致的不良事件较CoronaVac组更多。ARCova组主要的不良事件为发热和头痛,出现发热状况最多的为20μg组和25μg组,其次为10μg组,发热率超过了50%。3级全身不良事件发生率较高的为15μg组、20μg组和25μg组,为整体的30%左右。(注:所谓3级不良反应,为严重的或临床上明显的,但非立即致命的,需入院干预或延长住院时间)
03
艾博新冠mRNA疫苗开发之路
疫情初期,艾博生物便启动新冠疫苗研发工作。在2020年9月,艾博生物表示已经获批进入了I期临床试验。
2020年6月,沃森生物、艾博生物以及军事科学院军事医学研究院共同研制的ARCoV疫苗获得国内首个mRNA疫苗的临床批文。这款mRNA-LNP疫苗是一种液体制剂,封装在预充注射器中,注射前不需要解冻或溶解。可在4-25摄氏度下维持至少一周。
2021年4月19日,mRNA疫苗ARCoV(ARCoVaX) II期临床试验接近尾声,准备进入III期临床海外试验。
2021年9月,ARCoV III期临床试验分别获得了墨西哥、印度尼西亚药监部门的批准。
2022年1月24日,国内首个新冠mRNA疫苗 I期临床结果发布,评估该疫苗初步的安全性、耐受性以及免疫原性。可参见深究科学历史文章“国产首个新冠mRNA疫苗临床 I 期结果公布,10个关键信息披露重要进展”。
不过, 这一结果也让业内褒贬不一,认为与国外已上市的新冠mRNA疫苗相比要差许多。
沃森生物与艾博生物开发的ARCoV疫苗并非我国唯一的新冠mRNA疫苗,中国生物、斯微生物都在进行这方面的疫苗开发。除此之外,复星医药2020年就开始引进mRNA新冠疫苗,由于国内疫情此前控制较好,这一领域的疫苗开发就慢了下来。
今年年初,当奥密克戎毒株来袭后,当时这个开发以及审评审批策略弊端就显露出来了。目前,国内很多制药公司都投入到mRNA新冠疫苗的开发中来,希望我们距离国产新冠mRNA疫苗的过程不要太长。
参考资料
1.艾博国产mRNA疫苗数据真和国外疫苗类似吗?增强针结果好吗. 一个生物狗的科普小园.
2.重磅!国产首个新冠mRNA疫苗临床 I 期结果公布,10个关键信息披露重要进展. 深究科学
3.沃森mRNA疫苗作为加强针序贯接种,针对Omicron诱导出的中和抗体是同源加强的4.4倍. Hanson临床研究