导读: 11月2日,国家食品药品监督管理总局发布五家医疗器械生产企业的飞行检查情况公告,两家无菌,两家植入,一家体外诊断试剂,五家企业分别是:
吉林瑞尔康隐形眼镜有限公司(限期整改)
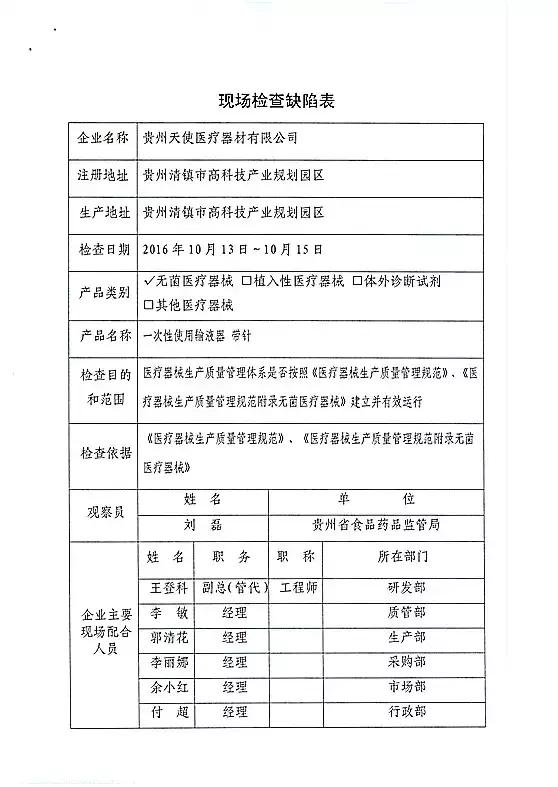
贵州天使医疗器械有限公司(限期整改)
辽宁垠艺生物科技股份有限公司(限期整改)
上海微创医疗器械(集团)有限公司(限期整改)
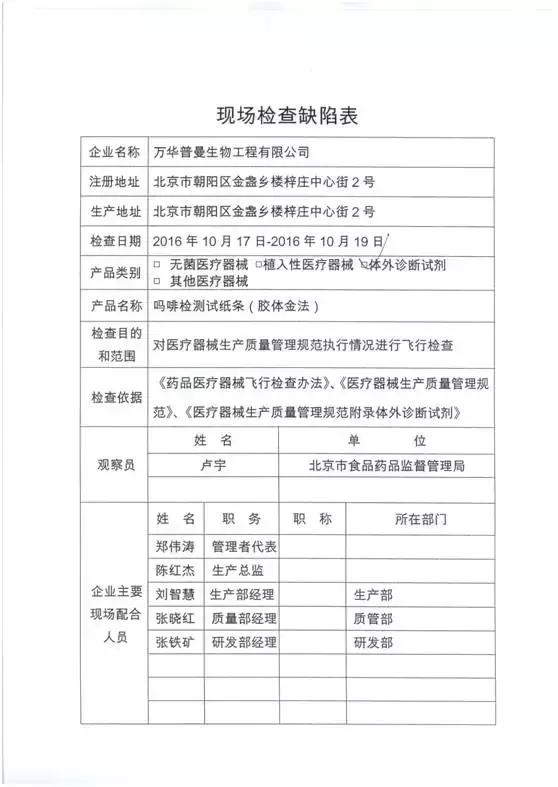
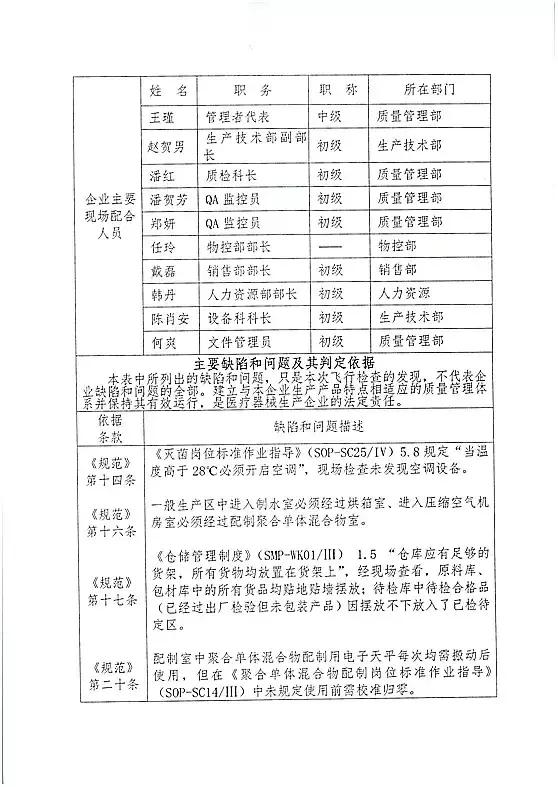
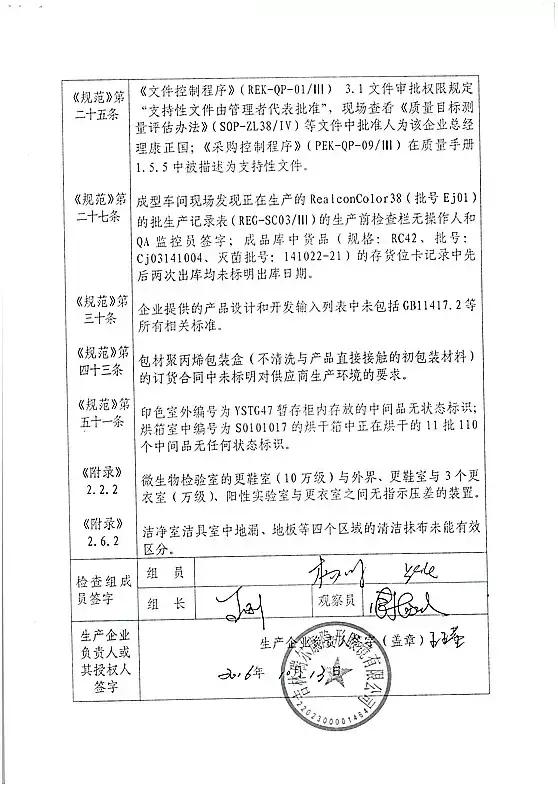
万华普曼生物工程有限公司(限期整改)
对吉林瑞尔康隐形眼镜有限公司飞行检查情况
吉林瑞尔康隐形眼镜有限公司的以下行为(见下表)不符合医疗器械生产质量管理规范相关要求,质量管理体系存在缺陷。现由吉林省食品药品监督管理局责成吉林瑞尔康隐形眼镜有限公司对上述缺陷限期整改。

对贵州天使医疗器械有限公司飞行检查情况
贵州天使医疗器材有限公司的以下行为(见下表)不符合医疗器械生产质量管理规范相关要求,质量管理体系存在缺陷。现由贵州省食品药品监督管理局责成贵州天使医疗器材有限公司对上述缺陷限期整改。

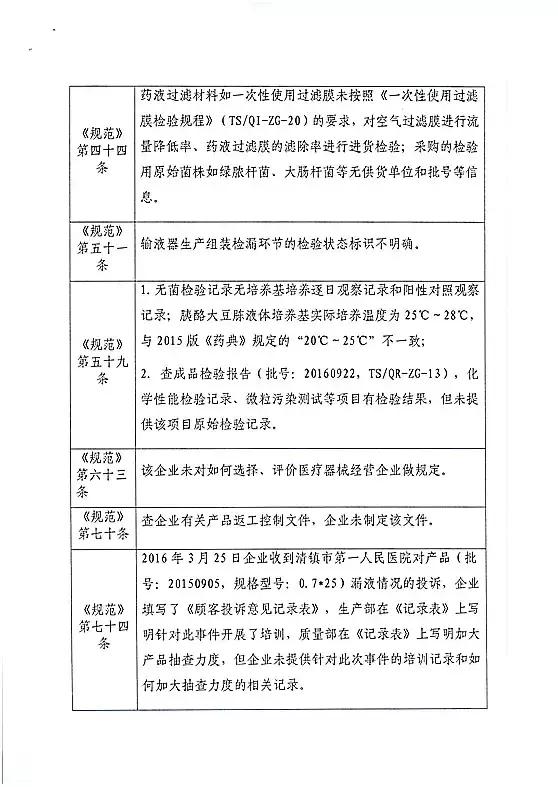
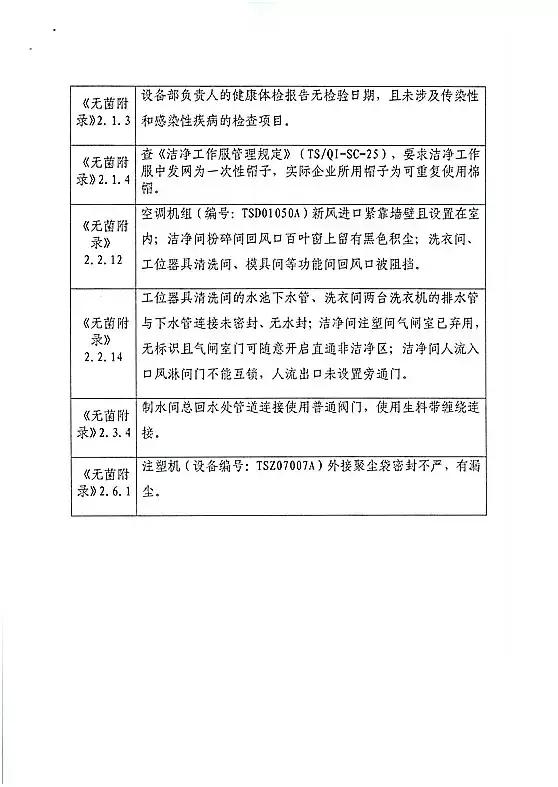

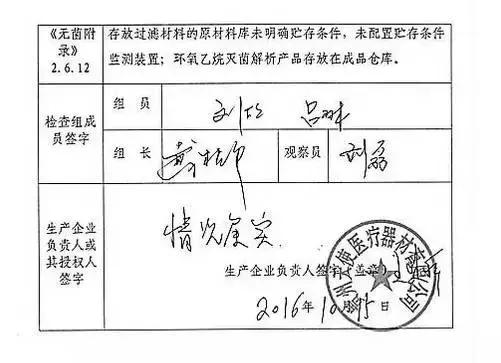
对辽宁垠艺生物科技股份有限公司飞行检查情况
辽宁垠艺生物科技股份有限公司的以下行为(见下表)不符合医疗器械生产质量管理规范相关要求,质量管理体系存在缺陷。现由辽宁省食品药品监督管理局责成辽宁垠艺生物科技股份有限公司对上述缺陷限期整改。
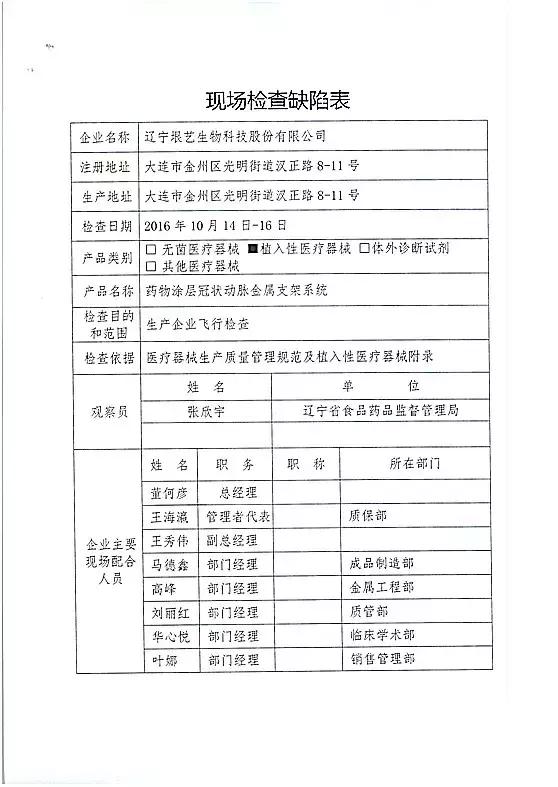



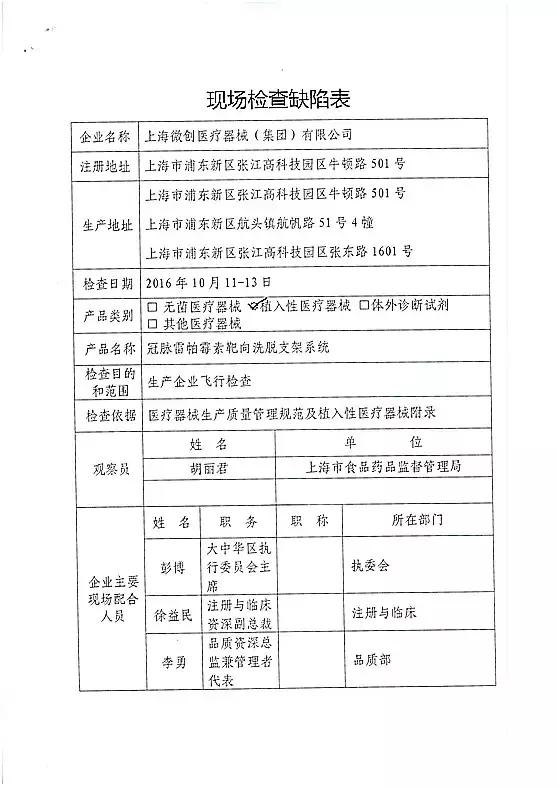
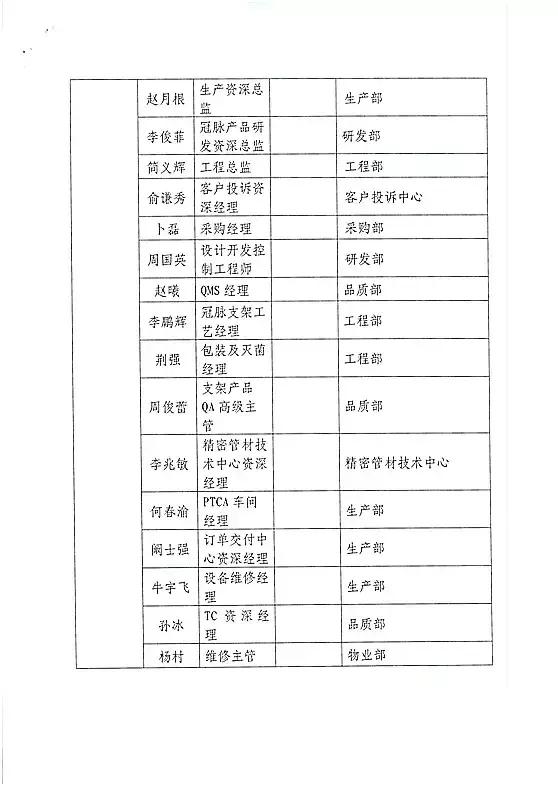
对上海微创医疗器械(集团)有限公司飞行检查情况
上海微创医疗器械(集团)有限公司的以下行为(见下表)不符合医疗器械生产质量管理规范相关要求,质量管理体系存在缺陷。现由上海市食品药品监督管理局责成上海微创医疗器械(集团)有限公司对上述缺陷限期整改。


对万华普曼生物工程有限公司飞行检查情况
万华普曼生物工程有限公司的以下行为(见下表)不符合医疗器械生产质量管理规范相关要求,质量管理体系存在缺陷。现由北京市食品药品监督管理局责成万华普曼生物工程有限公司对上述缺陷限期整改。