编者按:青春期高雄激素血症的患者,您遇到过吗?什么原因会导致高雄激素血症,您心中有数吗?在2023年(第十四届)全国内分泌代谢疾病诊治进展研讨会中,解放军总医院第一医学中心内分泌科程愈教授分享了1例青春期高雄激素血症并深入地讲解了其诊断、鉴别诊断与治疗。干货满满,快来跟小编一起学习吧~
庐山真面:回顾病情的来龙去脉
病史简介
.01
患者女性,13岁,因“月经少伴腹痛1年,闭经8月,声音变粗6月”入院。2018年,患者11岁,月经初潮,周期30天,行经5天,量中等。2019年4月,患者无诱因出现月经量减少,伴面部、胸部及背部*疮痤**,伴间断下腹疼痛,位置不固定,每次持续30分钟,屈膝位可缓解,每月发作1~2次,未予处理。患者末次月经2019年8月,伴声粗,多毛。2020年4月就诊于当地医院,具体结果如下。
体格检查
.01
体温:36.6℃,脉搏:90次/分,呼吸:18次/分,血压:120/73mmHg。身高:160cm,上部量:84cm,下部量:76cm,指间距:156cm。体重:54kg,BMI:21.4kg/㎡,腰围:68cm,臀围:74cm。上唇及颏可见毳毛生长;面部、胸部及背部散在*疮痤**。双侧乳房对称,Tanner分期 Ⅴ期,可触及乳核,未触及包块。阴毛呈菱形分布,Tanner分期 Ⅴ期,阴唇色素沉着,阴蒂肥大。
辅助检查
.01
性激素六项:
DHEA-S: 83.41ug/dl(33.90~280.0)
17OHP : 6.25ng/ml (<2.32)
皮质醇节律:
染色体核型分析: 46,XX
妇科超声:左侧附件区囊性肿物,大小约6.8×4.5×4.4cm,考虑卵巢囊肿可能性大。
骨龄片:左腕骨出现8个骨化中心,掌骨骨骺线闭合,尺桡骨远端骨骺线仍可见。
病例特点
.01
病史:继发性闭经,伴声粗、多毛,面部、胸背部*疮痤**,间断下腹疼痛,病情进展迅速。
体征:上部量大于下部量,面部、胸背部*疮痤**,乳房Tanner分期Ⅴ期, 阴毛呈菱形分布,阴唇色素沉着,阴蒂肥大。
辅助检查:染色体核型46,XX,睾酮水平升高,17OHP 轻度升高,骨骺提前闭合,左侧卵巢囊性肿物。
拨云见雾:厘清疾病的诊断思路
面对这样一个病例,该如何诊断呢?您会想到什么疾病?
继发性闭经:低促性腺激素性性腺功能减退、高促性腺激素性性腺功能减退、正常促性腺激素性性腺功能减退均可导致。
1.低促性腺激素性性腺功能减退
功能性下丘脑性闭经:神经性厌食症、营养不良、过度运动、压力、精神疾病、慢性疾病;
垂体疾病:肿瘤、囊肿、浸润性疾病、外伤、感染、手术、垂体卒中、血管病变、空泡蝶鞍、放疗;
药物:麻醉剂、抗惊厥药、抗精神病药物、阿片类药物、口服避孕药、酗酒、*洛因海**、*卡因可**、*麻大**、糖皮质激素等。
2.高促性腺激素性性腺功能减退
染色体异常:Turner综合征、46 XX性腺发育不全;
卵巢病变:自身免疫性疾病、外伤、感染、手术、放疗、化疗、半乳糖血症等。
3.正常促性腺激素性性腺功能减退
高泌乳素血症:泌乳素瘤、垂体柄压迫、药物及特发性;
高雄激素血症:多囊卵巢综合征、分泌雄激素肿瘤(卵巢、肾上腺)、ACTH依赖库欣综合征、21-羟化酶缺乏、卵巢膜细胞增生症;
非ACTH依赖库欣综合征
原发性肾上腺皮质功能不全:自身免疫、感染、外伤、出血、手术等;
甲状腺疾病:甲状腺功能亢进或甲状腺功能减退;
子宫因素:产科并发症导致子宫内膜瘢痕形成。
高雄激素血症:主要根据临床症状进行诊断。
1.多毛:常采用改良Ferriman–Gallwey (F–G) 评分系统,评估11个不同身体部位(上唇、下巴、胸部、上背部和下背部、上腹部和下腹部、手臂、前臂、大腿和小腿)的毛发生长情况进行了评分,评分范围在0(没有终毛)到4(广泛的终毛生长)之间。
2.雄激素性脱发:是指头顶、顶角和双颞区的头发弥漫性稀疏,但前额发际线一般不后移,而在额部保留一圈完整发际。
3.*疮痤**:仅存在*疮痤**症状,并不能代表具有高雄激素血症,若女性患者严重*疮痤**同时合并多毛或月经紊乱,则高度怀疑雄激素水平升高。
4.女性男性化:如声粗、肌肉含量增加、阴蒂肥大、闭经,这往往代表着显著升高的雄激素水平。
5.糖脂代谢紊乱
6.睾酮水平:需要注意的是,睾酮呈脉冲分泌,注意重复测定,且不同实验室测定的睾酮水平结果存在较大差异,难以标准化。此外,由于循环中大部分睾酮与性激素结合蛋白(SHBG)紧密结合,SHBG浓度的改变可能会影响总睾酮浓度,而不会改变游离睾酮水平。
抽丝剥茧:
明确青春期女性高雄激素血症的病因
明确了高雄激素血症以后,如何明确其病因呢?高雄激素血症常见病因有3类:(1)卵巢病变,包括多囊卵巢综合征、卵泡膜细胞增生症、雄激素分泌肿瘤;(2)肾上腺病变,包括先天性肾上腺皮质增生症、雄激素分泌肿瘤、ACTH依赖库欣综合征、高泌乳素血症。(3)其他:药物、绝经后。
青春期女性高雄激素血症最常见于多囊卵巢综合征、先天性肾上腺皮质增生症和分泌雄激素的肿瘤,它们各自有什么样的特点呢(图1)?
多囊卵巢综合征(PCOS):是青春期女性高雄激素血症最常见的原因。以雄激素增高、持续无排卵,卵巢多囊样改变为特征,临床表现为月经紊乱,伴多毛、*疮痤**、雄激素性脱发,常伴有肥胖和胰岛素抵抗。GnRH脉冲频率较高,导致LH分泌过多,从而刺激卵泡膜细胞产生雄激素。相对低水平的FSH导致卵泡发育停滞,导致多囊样改变,少排卵或无排卵。此外,胰岛素抵抗会导致高胰岛素血症,刺激GnRH分泌。
先天性肾上腺皮质增生症(CAH):是一组较为常见的常染色体隐性遗传疾病。因参与皮质醇合成的酶缺陷,皮质醇合成不足,ACTH水平升高,刺激肾上腺皮质增生,导致皮质醇前体物质堆积取决于缺陷部位,盐皮质激素和/或雄激素生成增多/减少。CAH中约90%~95%为21-羟化酶缺陷症。
分泌雄激素的肿瘤:卵巢来源及肾上腺来源。
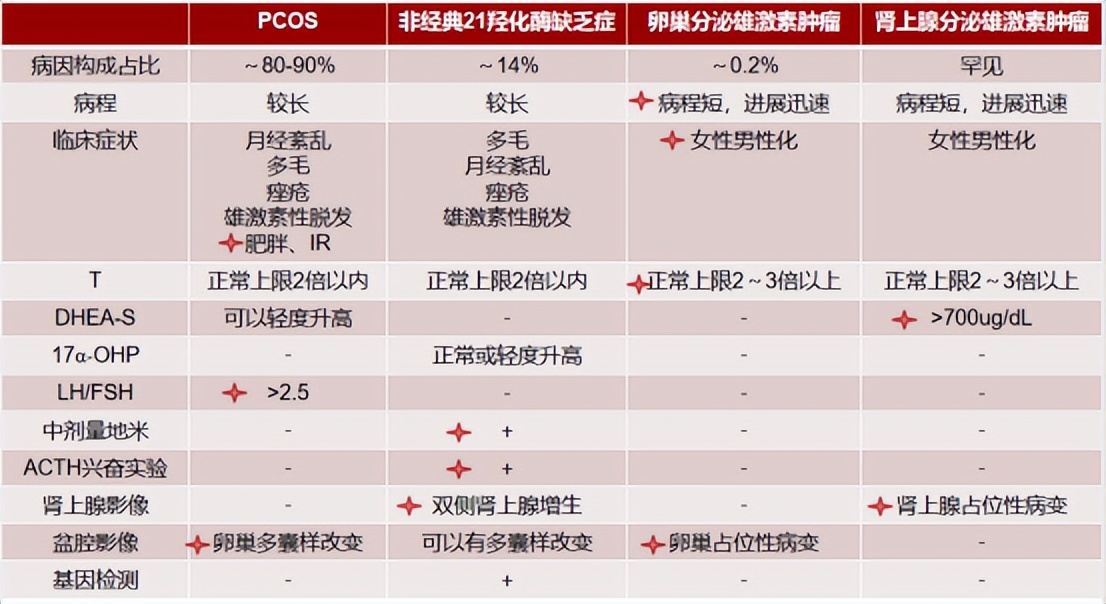
图1. 青春期女性高雄激素血症鉴别诊断
经验之谈:聚焦真实病例,提升临床思维
回到本病例,我们从病史和初步的性腺六项检查就可以排除多种疾病。患者无用药史,青春期女性,无库欣综合征临床表现,泌乳素水平正常。而卵巢间质细胞分化为黄素化间质细胞,产生大量的雄激素,多见于30~40岁女性,随年龄的增长,卵巢分泌雄激素的量逐渐增加,该患者也可排除。
但存在以下疑惑:1.患者17α-OHP 轻度升高,需进一步与21羟化酶缺乏症进行鉴别。2.外院报道左侧卵巢囊肿,而卵巢囊肿并无雄激素分泌增多的报道。进一步检查结果如下:
性激素六项:
DHEA-SO4: 36.1ug/dl(33.90-280.0)
皮质醇节律:
中剂量地塞米松抑制试验:
糖耐量试验:
经直肠妇科超声:子宫未见明显异常。左卵巢见多房囊性结构,大小约6.7×5.2×5.5cm,边界清楚,部分囊壁及分隔不规则增厚,最厚处约0.6cm,CDFI囊壁及分隔上可见较丰富血流信号,结合临床不除外分泌雄性激素的肿瘤。右卵巢显示清楚,未见异常。右附件区未见异常回声。
盆腔核磁:左侧附件区异常信号,考虑良性囊性病变可能。
基于此,我们考虑的诊断为高雄激素血症:左侧卵巢雄激素分泌瘤可能性大。糖耐量减低。遂行腹腔镜下左侧卵巢囊肿剥除术+右侧卵巢活检术,病理结果显示:左侧卵巢高-中分化,支持-间质细胞肿瘤,总大小4x3x0.6cm;右侧卵巢少许卵巢组织,间质细胞增生,可见原始卵泡。免疫组化结果:CD10(-),Calretinin(+),CD 56(+),ER (80%+),PR(弱+,局灶腺体强+),Syn(-),CgA(-),Inhibin-α(+),Ki67(+30%),CK(腺上皮+),AR(+),p53(-)。
术后患者皮肤变白,面部及后背*疮痤**明显改善,声音变细,2020/7/6(术后一月)月经来潮。于2020/7/16起行依托泊苷+顺铂+平阳霉素方案4周期。目前月经规律,肿瘤无复发。
拓宽视野:何为卵巢支持-间质细胞肿瘤?
卵巢支持-间质细胞肿瘤(SLCTs):是卵巢性索-间质肿瘤中较为罕见的类型,约占11.2%。其发病年龄多小于30岁。多为单侧,双侧极为少见,少数可分泌雌激素,或同时分泌雌激素和雄激素,呈多房囊性或囊实性,实性成分可被明显强化。Inhibin-α、Vimentin、Calretinin具有较强特异性。SLCTs可分为高分化、中分化、低分化、网状亚型及伴异源成分的SLCTs。
高分化SLCTs行患侧附件切除,其余类型I期患者,年轻未育女性对侧卵巢探查未见异常,可行保留生育能力的手术;而年龄较大、无生育需求或分期较晚的患者,应行全子宫+附件切除术,术后肿瘤分化不良者,应辅以放化疗。SLCTs的5年生存率75~90%。
结语
临床中,我们往往可以很容易通过临床症状及实验室检查明确高雄激素血症。但仍需进行详细的病史询问及体格检查,并结合病程进展、临床症状、雄激素水平、功能试验、影像学,必要时行基因检测进行病因诊断。本例中涉及的SLCTs为卵巢分泌雄激素肿瘤中常见类型,其预后良好。

程愈
解放军总医院第一医学中心
医学博士,解放军总医院第一医学中心内分泌科副主任医师,北京医学会糖尿病学分会青年委员会委员,北京内分泌代谢病学会甲状腺专业委员会常务委员。主持国家自然科学基金1项,主要研究方向为2型糖尿病及并发症的发病机制和细胞治疗。以第一作者在国内外杂志发表10余篇论著。