头条号中学物理与你携手同行!希望能在今年的中考助你一臂之力!为此!中考化学重难点轻松突破主题正在逐步推进中,敬请关注!

一、金属的化学性质
1. 金属与氧气的反应
铝镁等活泼金属在常温下就能和氧气发生反应,生成氧化物保护膜。
铁铜等在常温下几乎不与氧气反应,但在高温或点燃时能与氧气反应。
金即使在高温下也不与氧气反应,化学性质非常稳定
注意:根据金属与氧气发生反应的难易程度可大体判断金属的活泼程度。
2. 金属与酸反应
活泼金属可以与酸发生置换反应,生成盐和氢气,例如

注意:不是所有的酸都能和金属发生置换反应,生成盐和氢气。酸一般指稀硫酸和稀盐酸,而不是指浓硫酸和硝酸等酸;
金属指的是活泼金属,金属活动性顺序表中排在氢前面的金属,但一般不考虑最活泼的K、Ca、Na。
3. 金属与某些化合物溶液反应
活泼金属可以与某些化合物溶液发生置换反应,将其从溶液中置换出来。例如,铁可以和硫酸铜溶液反应,生成铜和硫酸亚铁。
二、置换反应
1. 含义
由一种单质和一种化合物反应,生成另一种单质和化合物的反应,叫做置换反应。
2. 特征
置换反应是一种基本反应类型,它是以反应物和生成物的类别来分类的。其特点为:反应物和生成物必须同时是一种单质和一种化合物。

4. 置换反应中元素化合价的问题
由于置换反应是单质与化合物反应,生成另一种单质和另一种化合物,组成单质的元素转化为生成物中组成化合物的元素,而组成化合物的元素则转化为生成物中组成单质的元素,所以在置换反应中一定有元素化合价的变化。
注意:金属铁与酸发生置换反应时,生成亚铁离子而不是铁离子。
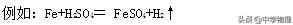
三、金属活动性顺序表
金属活动性顺序:一般是指金属在溶液中失去电子变成离子的能力的强弱。失电子能力强的金属称之为活泼金属,失电子能力弱的金属称之为不活泼金属。常见金属的活动性强弱顺序见下表:
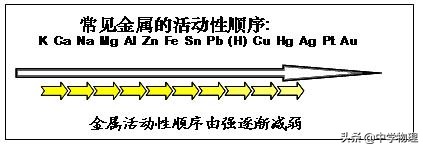
根据表中信息可总结出以下规律:
(1)金属的位置越靠前,金属的活动性越强;
(2)位于氢前面的金属可以和酸发生置换反应,生成盐和氢气;
(3)排在前面的金属可以把排在它后面的金属从其化合物溶液中置换出来。
注意:排在前面的金属不包括钾、钙、钠三种金属,它们的活动性太强,与化合物溶液发生反应时,是先和溶液中的水发生反应;也不包括铂、金,它们的活动性太弱,在自然界几乎没有化合物的形态存在。

例题 :某化学兴趣小组的同学要探究镁、铁、铜三种金属的活动性顺序,设计了如图所示的实验方案:
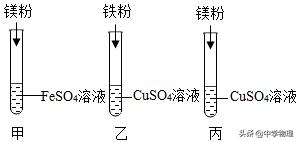
(1)试管乙中观察到的现象是_____________________________,反应的化学方程式为_____________________________。
(2)同学们经讨论后认为该方案可以优化, 试管的实验是多余的。同学们经讨论得出三种金属的活动性由强到弱的顺序为_______________________________________。
(3)去掉多余的实验,同学们将另两支试管中反应后的物质倒入同一大烧杯中,一段时间后过滤,得到不溶物和滤液,并对不溶物的成分进行如下探究:
【提出问题】烧杯中不溶物的成分是什么?
【实验探究】向过滤得到的不溶物中加稀硫酸:
①若无气泡产生,则不溶物的成分是___________________;
②若有气泡产生,则不溶物中一定含有 ,可能含有



巧解金属与酸反应图象题
对于金属与酸反应的图象题,我们解题的要领是抓住图象,一般以“三点一趋势一平台”为核心。
三 点:起点、转折点和终点(有时转折点和终点会合二为一);
一趋势:图象的变化趋势(该趋势一般能反映有关量的变化规律);
一平台:与x轴平行的那条线,平台高低即反映有关量的大小问题。
常见的有两种类型:
类型一:等质量的金属与足量的酸反应时,生成氢气的质量与其化合价以及相对原子质量有关,生成的金属化合物中化合价越高,氢气质量越多,在等化合价的前提下,还与其相对原子质量成反比,金属的相对原子质量越大,产生的氢气越少。
例题1 等质量的锌、铁两种金属与足量的盐酸反应,生成氢气的质量与时间的关系如下图所示,则下列说法正确的是( )
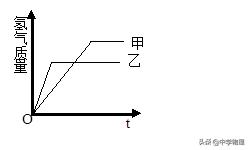
A. 甲是金属铁,乙是金属锌
B. 生成氢气的质量是甲小于乙
C. 甲金属的活动性比乙强
D. 参加反应的盐酸的质量一定相等
解析:这是一道典型的数形结合的化学图象题,用数学中的直角坐标系来反映化学反应中的有关规律。图象平台的高低反映了生成氢气质量的多少,而平台的转折点则表示反应终点,也表明了反应速度的快慢,即金属活动性的强弱。根据图示可知,金属甲生成的氢气多于金属乙,而反应速度则是甲慢于乙。据此可推断乙是锌而甲是铁,等质量的金属与足量酸反应时,生成的氢气质量与相对原子质量成反比,锌的相对原子质量大于铁的相对原子质量,所以锌放出的氢气应该少于铁,也符合图象的规律。参加反应的酸则可由氢气质量来判断。
答案:A
类型二:足量金属与等量酸反应时,生成的氢气质量是相等的(因为参加反应的酸的质量相等),此时消耗的金属的质量与其相对原子质量成正比。相对原子质量越大,参加反应的金属的质量越多。
例题2 一定量的金属甲与乙分别放入等质量、等浓度的稀硫酸中。充分反应后,放出的氢气质量与时间关系如下图所示,则下列判断正确的是( )
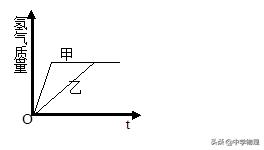

掌握的怎么样呢?自测一下试试吧!








你做对多少呢?收藏了慢慢品读吧!你会发现不一样的收获!谢谢你的支持!
