
征求意见稿
一、总局关于公开征求《医疗器械标准管理办法》(征求意见稿)意见的通知
为加强医疗器械标准管理,保障医疗器械安全有效,根据《中华人民共和国标准化法》和《医疗器械监督管理条例》,国家食品药品监督管理总局对现行《医疗器械标准管理办法(试行)》(原局令第31号)进行了修订,形成了《医疗器械标准管理办法》(征求意见稿),现向社会公开征求意见。社会各界可于2016年11月30日前,通过登录中国政府法制信息网(网址:http://www.chinalaw.gov.cn),进入首页左侧的“法规规章草案意见征集系统”提出意见和建议。
二、总局关于公开征求医疗器械不良事件监测和再评价管理办法(征求意见稿)意见的通知
为规范医疗器械不良事件监测和再评价工作,根据《医疗器械监督管理条例》,食品药品监管总局起草了《医疗器械不良事件监测和再评价管理办法(征求意见稿)》,现向社会公开征求意见。社会各界可于2016年11月30日前,通过登录中国政府法制信息网(网址:http://www.chinalaw.gov.cn),进入首页左侧的“法规规章草案意见征集系统”提出意见和建议。
械企查出
一、北京万华普曼生物工程有限公司
企业名称:北京万华普曼生物工程有限公司
检查日期:2016.10.17-2016.10.19
产品类别:体外诊断试剂
产品名称:玛啡检测试纸条(胶体金法)
缺陷和问题数:8项
二、上海微创医疗器械(集团)有限公司飞行检查情况
企业名称:上海微创医疗器械(集团)有限公司
检查日期:2016.10.11-2016.10.13
产品类别:植入性医疗器械
产品名称:冠脉雷帕霉素靶向洗脱支架系统
缺陷和问题数:10项
三、辽宁垠艺生物科技股份有限公司飞行检查情况
企业名称:辽宁垠艺生物科技股份有限公司
检查日期:2016.10.14-2016.10.16
产品类别:植入性医疗器械
产品名称:药物涂层冠状动脉金属支架系统
缺陷和问题数:18项
四、贵州天使医疗器械有限公司飞行检查情况
企业名称:贵州天使医疗器械有限公司
检查日期:2016.10.13-2016.10.15
产品类别:无菌医疗器械
产品名称:一次性使用输液器 带针
缺陷和问题数:19项
省局动态
一、广东省2016年第一批医器临床试验监督抽查项目
根据《广东省食品药品监督管理局关于开展医疗器械临床试验监督检查工作的通知》(粤食药监办许〔2016〕353号)明确的抽查范围和相关原则,广东省食品药品监督管理局抽取了广州康恩斯电子科技有限公司(受理号:0010600120150422)等10个注册申请项目,组织检查组对其临床试验数据的真实性和合规性实施回顾性监督检查。具体注册申请项目的受理号、产品名称、申请人及临床试验承担单位见附件。具体检查时间安排和抽查的临床试验机构由广东省食品药品监督管理局另行通知。
二、上海市7个医械批件监督检查抽验不合格!
为了加强对医疗器械的质量监督管理,规范市场秩序,保障医疗器械产品安全有效,上海市食品药品监督管理局2016年第三季度组织了对本市医疗器械生产、经营和使用单位的质量监督抽验,共完成检验152件。
三、福建省关于医疗器械注册及生产许可有关问题的通告
《医疗器械监督管理条例》(以下简称《条例》)已于2014年6月1日起施行,其配套的《医疗器械注册管理办法》(国家食品药品监督管理总局令第4号)、《体外诊断试剂注册管理办法》(国家食品药品监督管理总局令第5号)和《医疗器械生产监督管理办法》(国家食品药品监督管理总局令第7号)(以下统称《办法》)也于2014年10月1日起实施。
四、医疗器械“体验式销售”消费警示
湖南省食品药品监督管理局发布,医疗器械“体验式销售”消费警示,包括:
一、什么是体验方式经营医疗器械
二、免费体验方式经营医疗器械容易出现的问题
三、消费警示
行业趋势
一、第11届“十大医疗创新”年度榜单
1、“预防、诊断、治疗”疾病的微生物组2、减少心血管疾病发生和死亡的新型糖尿病药物3、治疗白血病和淋巴瘤的细胞免疫疗法4、发现循环肿瘤细胞DNA的液态活检5、汽车的自动安全和无人驾驶功能6、快捷医疗互操作资源(FHIR)7、治疗难治性抑郁症的氯胺酮8、3D可视化和增强现实技术在外科手术上的应用9、可自行使用的HPV检测10、能降解、可吸收的血管支架
二、HIV快速诊断试剂获得盖茨基金会260万资助
Atomo诊断公司获得盖茨基金会260万美元的资助,用于研发一种HIV快速诊断试剂,这有助于发展中国家人群进行快速HIV感染检测。
三、医疗投资图谱
本文根据一手调研信息对整个行业的各个环节做简要梳理,详见下图
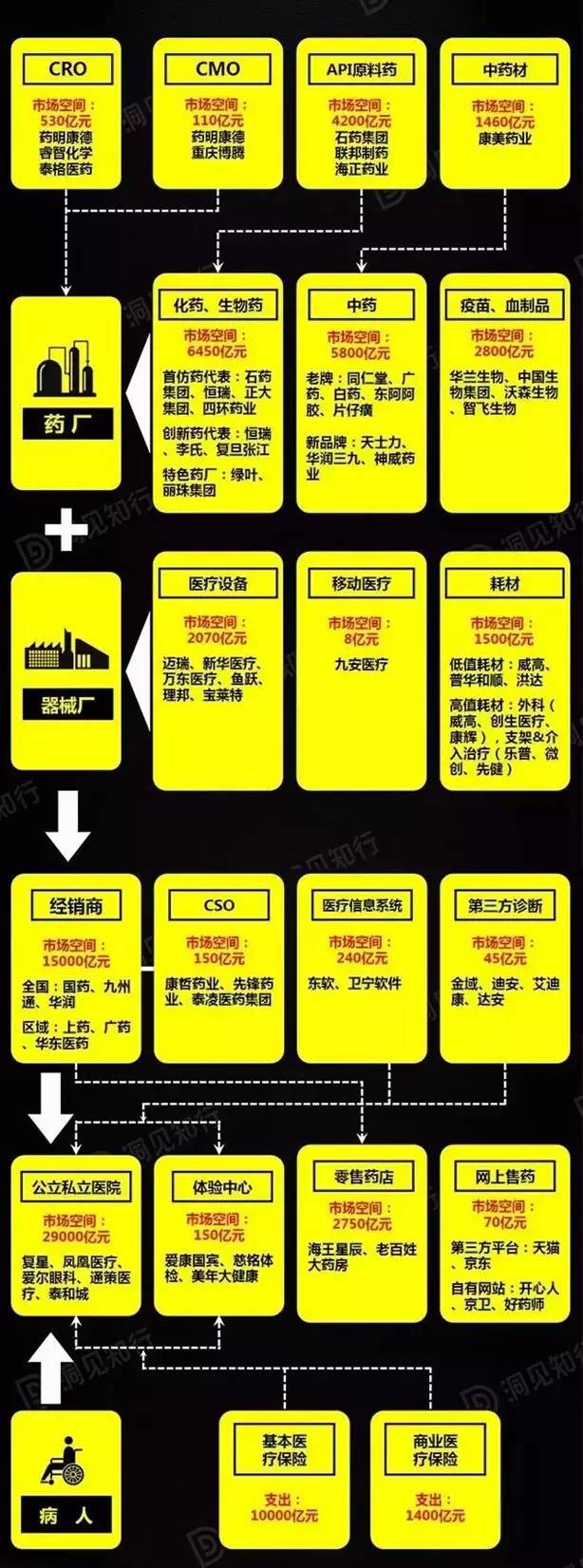
来源:弗锐达医疗器械技术服务