*仅供医学专业人士阅读参考
点击右上方“关注”, 准时接收每日精彩内容推送。
干细胞移植可以替代缺血性卒中后丢失和受损的神经元,被认为是一种潜在的卒中诊治方法。
然而,干细胞治疗面临着移植后细胞保留、存活和分化差的挑战。基于此,来自 四川大学的李正勇和王云兵 开发了一种复合水凝胶,它含有脑脱细胞外基质(dECM)和基质金属肽酶(MMPs)反应的主客体(HG)水凝胶,作为人类诱导多能干细胞来源的神经干细胞(iPSC-NSCs)输送的平台,以提高移植干细胞的存活和分化 。主要研究了HG/dECM复合水凝胶对IPSC-NSCs在水凝胶修饰的二维表面和三维水凝胶网络中存活和分化的影响。此外,在缺血性卒中模型中,将负载iPSC-NSCs的复合水凝胶注射到梗死腔中,以取代丢失和受损的神经细胞。负载于HG/dECM复合水凝胶中的iPSC-NSCs在皮质梗死区表现出较好的存活率,并且复合水凝胶促进了iPSC-NSCs向神经元的分化。 总体而言,HG/dECM复合水凝胶是一个很有前途的调节干细胞存活和分化的平台。 相关论文“A composite hydrogel improves the survival and differentiation of human iPSC-derived neural stem cells after ischemic stroke”于近期发表于杂志《Composites Part B》上。
1. dECM水凝胶的制备与表征
为了构建一个模拟自然脑中细胞外基质的生理特征的3D类脑微环境系统,对猪脑组织进行了消化和去细胞处理,以形成天然脑特定的细胞外基质成分的溶解混合物(图1A)。检测并比较了自然脑和dECM中的DNA含量,结果表明,大约95.43±1.36%的DNA被去除,避免了dECM中残留的细胞抗原,从而引起炎症反应(图1B)。还测量了自然脑和dECM中的GAG含量,以确保dECM的生物活性(图1C)。HE和Masson的三色染色显示细胞和细胞碎片缺失,而脱细胞过程后保留了天然的脑DECM结构(图1F)。免疫荧光法检测dECM中的ECM蛋白。与自然脑相比,发现脱细胞后的dECM样本中仍然保留了IV型胶原、层粘连蛋白和纤维连接蛋白(图1G)。采用扫描电子显微镜对DECM的内部结构进行了研究。图像表明,dECM是一种含有毛孔和交错纤维的3D网络结构(图1D)。此外,在37℃孵育消化和中和的dECM溶液以诱导水凝胶形成(图1E)。在不同浓度的水凝胶中测量了粘度的线性剪切变稀特性,结果表明dECM水凝胶具有合适的流动性(图1H)。不同浓度的dECM水凝胶的存储模数约为500-3500 Pa,与脑组织的存储模数相匹配(图1I)。这些结果表明,DECM可以形成具有与天然脑ECM相似的力学性能的三维网络结构,有利于细胞的存活和分化。
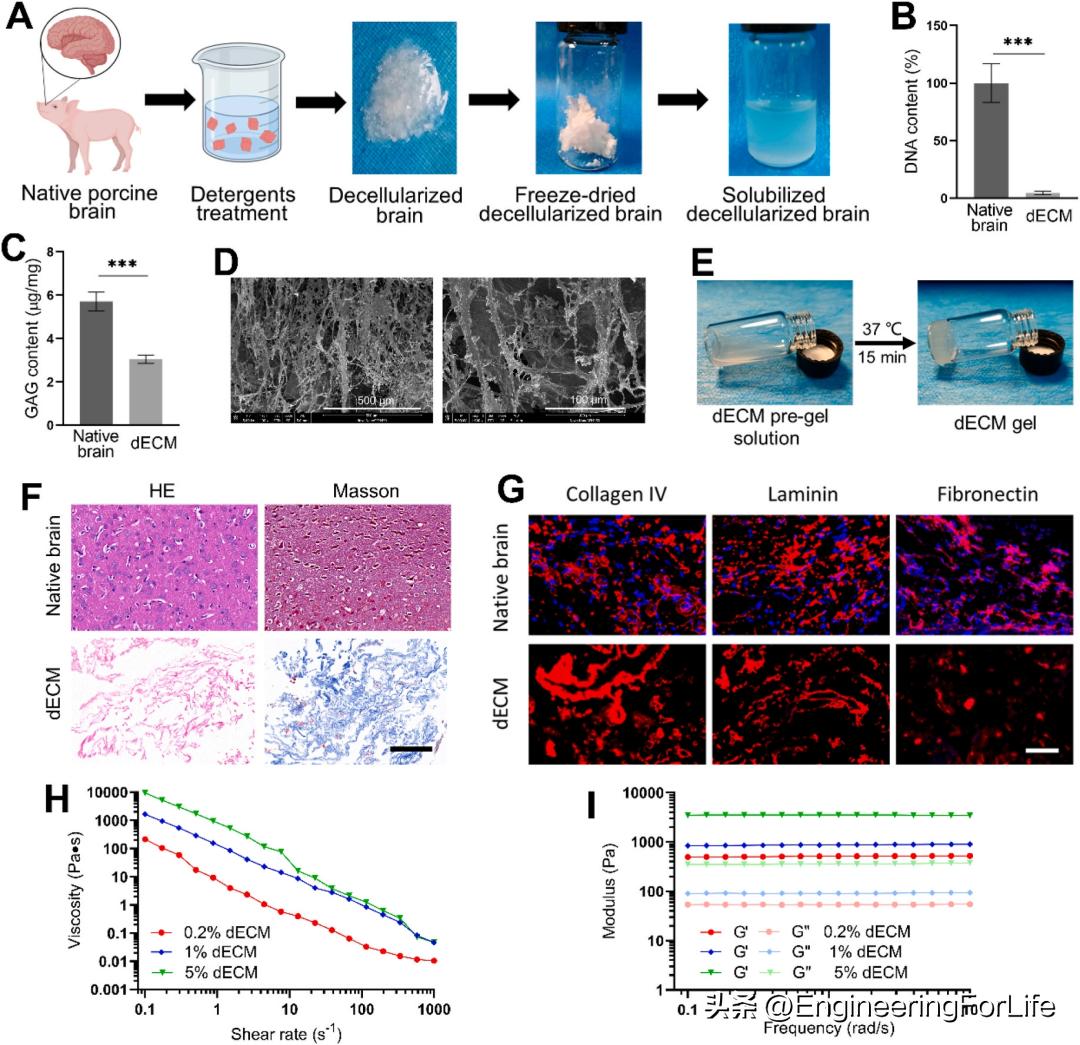
图1 dECM水凝胶的制备和表征
2. 化学改性透明质酸的合成与表征
为了避免紫外光交联对细胞的损伤,合成了与主体基团CD偶联的HA和与丙烯酸酯基团偶联的HA,并通过客体基团Ad-修饰的MMP响应肽进行了交联。首先以对甲苯磺酰氯为对甲苯磺化试剂合成CD-Tos,然后以CD-Tos为原料用1,6-己二胺合成CD-HDA(图2A)。如图2E所示,7.44和7.75ppm的典型峰可归因于TosCl中的芳香氢,而1.25-1.62 ppm的典型峰可归因于正己烷连接物的氢。由于HA在DMSO中的不溶性,首先将TBA接枝到HA上,得到HA-TBA。然后,HA-TBA与CD-HDA反应合成HA-CD(图2B)。0.87 ppm的典型峰归因于TBA甲基(图2G),1.25和1.62 ppm的典型峰归因于己烷连接物(图2H)。HA-AC的合成分两步进行,如图2D所示。首先,以透明质酸和己二肼为原料,采用EDC缩合剂,成功地合成了HA-ADH。纯化后的HA-ADH聚合物与N-琥珀酰亚胺基丙烯酸酯结合,得到HA-AC。最终产物经过纯化,然后用1H-NMR进行了表征,如图2I所示。在5.82ppm和6.26ppm处的典型峰被归因于HA-AC双键的H。如图2F所示,HA-CD和HA-AC通过CD和Ad以及双键和巯基进行交联。
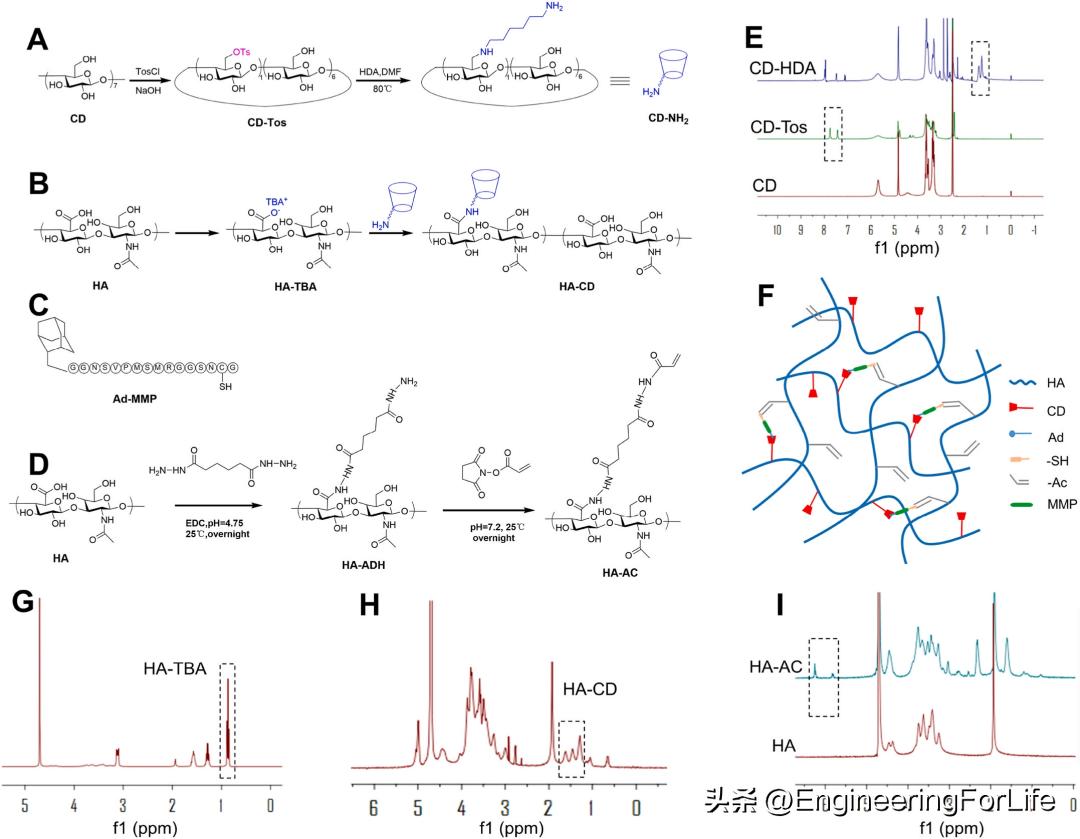
图2 CD-HDA、HA-CD和HA-AC的合成与表征
3. HG/dECM复合水凝胶的性能研究
为了研究HG/dECM复合水凝胶的自愈合性能,将两个破碎的复合水凝胶碎片接触。两块水凝胶之间的接触区愈合良好,两块水凝胶成为一个完整的水凝胶。此外,整合的水凝胶可以拉伸而不断裂,这表明HG/dECM复合水凝胶具有良好的自愈性能(图3A)。为了评价HG/dECM复合水凝胶的可注射性,用注射器将水凝胶注入水介质中。结果表明,dECM水凝胶在注射后发生碎裂,而HG和HG/dECM水凝胶具有良好的注射性能(图3C)。就其本身而言,dECM水凝胶的机械性能较弱,结构保真度较差。将dECM与HG相结合的复合水凝胶克服了dECM水凝胶的缺点,这是由于HG水凝胶具有近乎瞬时的超分子重组特性。随后,测定了不同浓度(1%dECM+1%HG、1%dECM+5%HG和1%dECM+10%HG)的HG/dECM复合水凝胶的流变性。应变扫描结果表明,当应变超过700%时,储存模数低于损失模数,这表明所有浓度的水凝胶都具有注射能力(图3D)。频率扫描结果表明,在所有浓度的水凝胶中,G’显著超过G”,频率在0.1到10 rad/s之间,这表明形成了水凝胶弹性网络(图3E)。 此外,还研究了HG/dECM复合水凝胶的几个循环的崩塌和恢复行为,结果表明复合水凝胶具有可逆和动态的交联结构(图3F)。
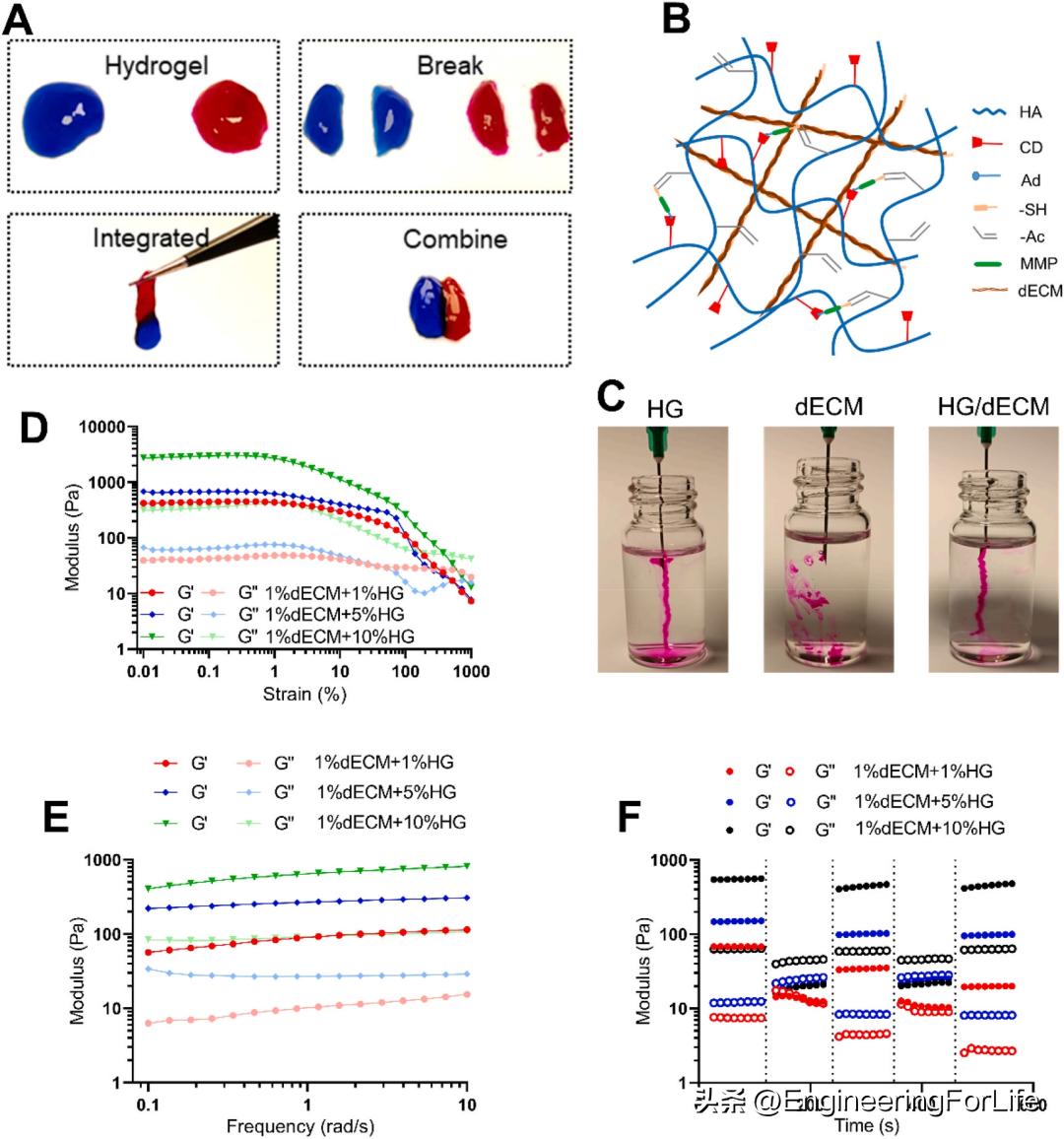
图3 HG/dECM复合水凝胶的表征
4. iPSC-NSCs的制备及最佳候选水凝胶
鉴于iPSC在治疗神经系统疾病方面的巨大潜力,开发并将iPSC来源的NSCs用于缺血性卒中的研究。神经干细胞以神经球的形式悬浮生长(图4A)。NSC标记Nestin和Sox2的染色结果确定了干细胞的表型,并证实了细胞干性的维持(图4B)。首先,将dECM预凝胶用于培养基质的表面涂层,以评估干细胞的高效分化和突起生长。在涂有不同浓度dECM的玻片上培养的iPSC-NSCs进行F-肌动蛋白染色(图4C)。在涂有0.2%、1%和5%DECM的玻片上培养3d后观察细胞形态,以确定DECM的最佳浓度。在1%dECM涂片上培养的神经干细胞的长径比高于0.2%和5%dECM上培养的细胞。同时,在1%dECM涂布的玻片上培养的NSCs的环形度低于在0.2%和5%dECM上培养的细胞(图4D和E)。然后,在涂有不同浓度HG/dECM的玻片上培养的iPSC-NSCs也进行了F-肌动蛋白染色,以确定dECM和HG水凝胶的最佳浓度比(图4F)。结果表明,在培养1天后,不同的HG和DECM浓度比之间的细胞长径比或圆形没有显著差异(图4G和H)。然而,培养7天后,在1%dECM+5%HG水凝胶前体涂层玻片上培养的神经干细胞比在其他浓度比例的复合水凝胶上培养的细胞显示出更高的细胞存活率、更高的长径比和更低的圆形(图4I、J和4K)。
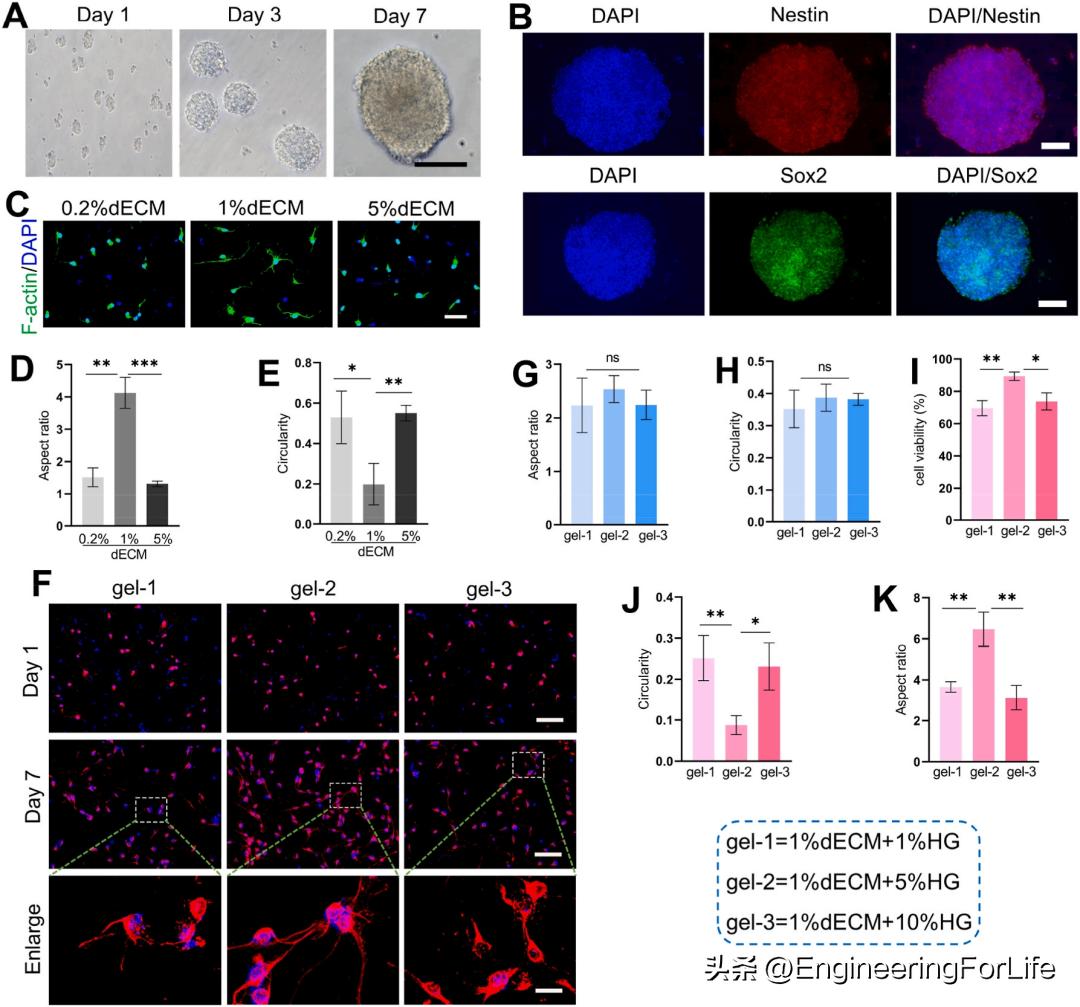
图4 水凝胶前体包被载玻片中IPSC-NSCs的2D培养
5. HG/dECM复合水凝胶促进iPSC-NSC在2D表面和3D水凝胶中的生长和分化
用CCK-8和Calcein AM/PI双染法评价HG/dECM复合水凝胶的细胞毒性(图5A)。定量分析显示,在每个时间点,每组之间的细胞死亡数量没有显著差异(图5B)。然而,HG/dECM涂层组和对照组之间的细胞活力显示出显著差异(图5C)。提示HG/dECM复合水凝胶对iPSC-NSC的存活和分化无细胞毒性。为了研究复合水凝胶对IPSC-NSC生长和分化的影响,在复合水凝胶涂层玻片上检测了细胞分化。在相差显微镜下,在复合水凝胶中培养的iPSC-NSC神经球比对照组细胞表现出更明显的径向分化(图5D)。此外,使用免疫荧光技术评估了培养7天后从iPSC-NSC神经球分化的细胞的表型。通过Nestin(干细胞标记物)和Tuj1(未成熟神经元标记物)的共同染色,研究了HG/dECM复合水凝胶在维持细胞干性和神经元分化方面的作用(图5E)。结果表明,在复合水凝胶中培养的IPSC-NSC神经球表现出比对照细胞更明显的径向分化。同时,细胞干性也得到了很好的维持。通过MAP2(神经元标记物)和GFAP(星形胶质细胞标记物)的共同染色,进一步评价HG/dECM复合水凝胶对神经元和星形胶质细胞分化的影响。结果表明, 在复合水凝胶中培养的iPSCNSC神经球可以分化为神经元和星形胶质细胞 。此外,从两个不同的IPSC-NSC神经球分化的神经元和星形胶质细胞可以相互连接(图5F)。
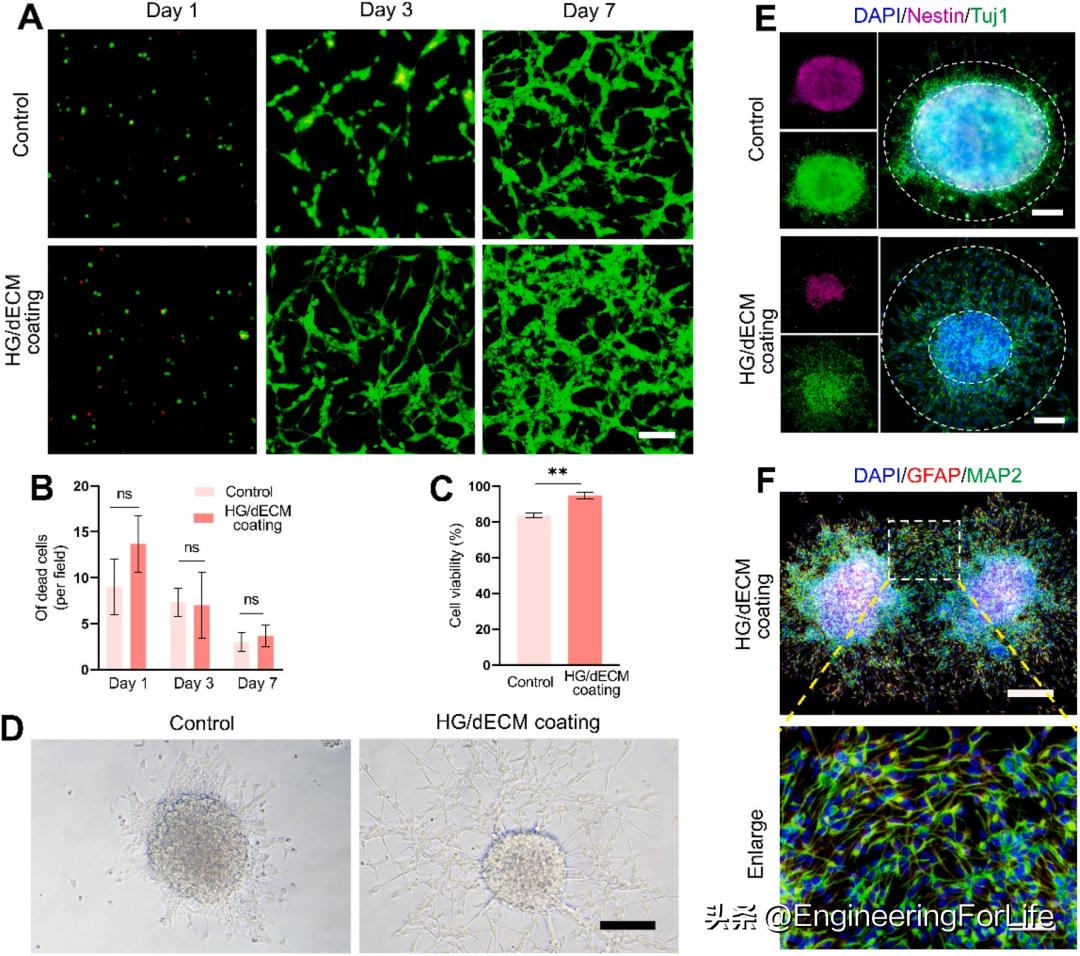
图5 iPSC-NSCs神经球在2D表面的分化
进一步研究了iPSC-NSC在3D水凝胶中的活性和分化。通过活/死染色来研究水凝胶对细胞的影响(图6A)。三维共聚焦显微镜图像显示,HG/dECM复合水凝胶的死亡细胞数少于HG水凝胶组和dECM水凝胶组。在培养1d、3d和7d后检测3D水凝胶中的细胞活性。结果表明,复合水凝胶组培养1d后细胞存活率与其他组无明显差异。然而,在复合水凝胶中培养的iPSC-NSCs在培养3天和7天后显示出比在HG水凝胶和dECM水凝胶中培养的细胞更高的细胞活力(图6B)。因此,检测了HG/dECM复合水凝胶dDECM水凝胶和HG水凝胶对iPSC-NSC分化的调节作用。用Tuj1的荧光染色研究了iPSC-NSCs向神经元的分化(图6C)。通过GFAP染色进一步评估了HG/dECM复合水凝胶对星形胶质细胞分化的影响(图6E)。结果表明,在复合水凝胶中培养的iPSC-NSCs比在DECM水凝胶和HG水凝胶中培养的细胞有更大的轴突生长(图6F)。这些数据表明, HG/dECM复合水凝胶在细胞存活和分化方面优于单一水凝胶 。
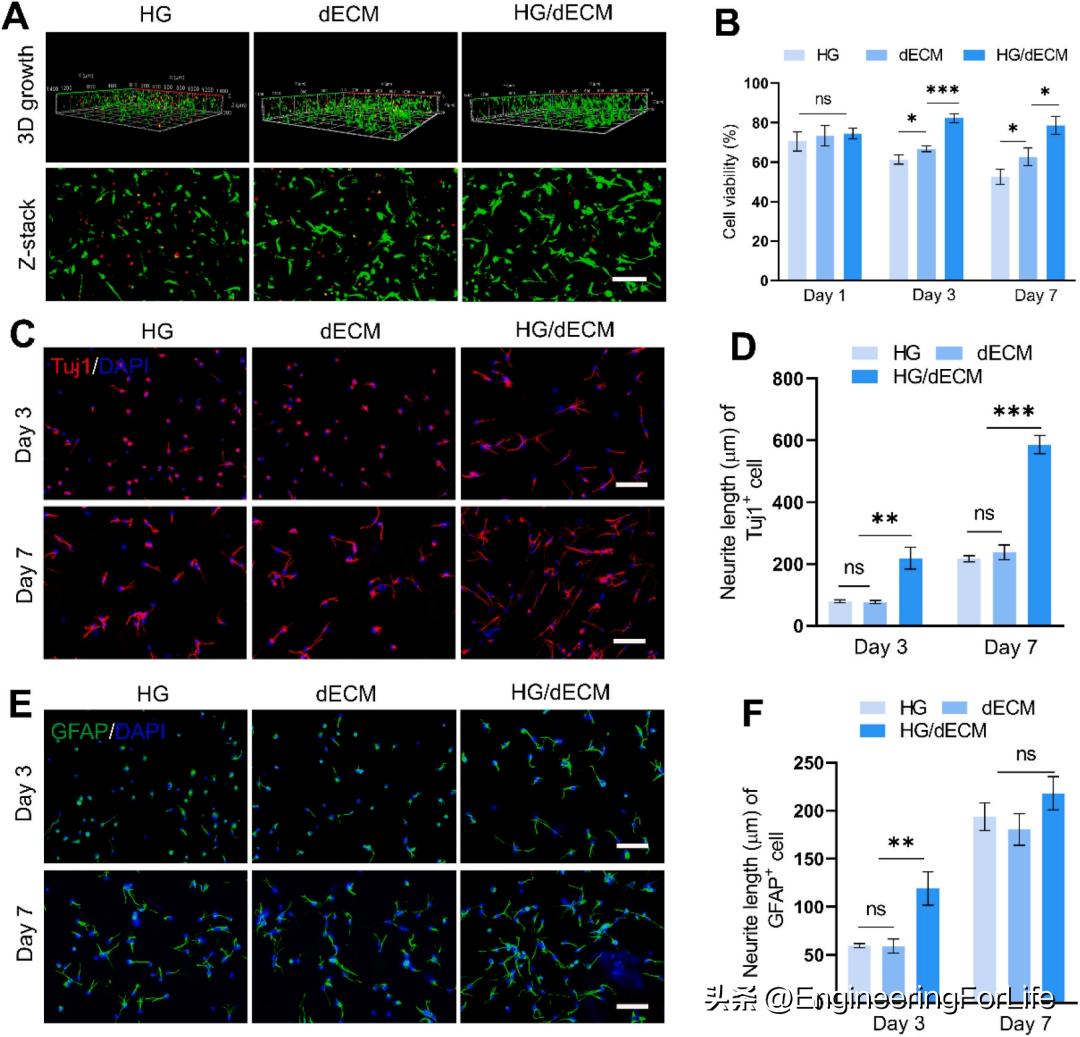
图6 iPSC-NSC神经球在3D水凝胶网络中的分化
6. HG/dECM复合水凝胶促进iPSC-NSC在缺血性中风模型中的存活和分化
在注射后7天检测了HG/dECM复合水凝胶的体内生物相容性。在HG/dECM组和PT组之间,未观察到CD3阳性T细胞或F4/80阳性巨噬细胞在脑组织中的渗透显著增加(图7A、B和7C)。通过监测GFP荧光强度来评估移植的iPSC-NSCs在梗死腔中的存活情况,结果表明HG/dECM复合水凝胶可以更好地促进干细胞的保留和存活(图7D和E)。用Tuj1免疫组织化学染色(图7F)检测移植到梗死区的iPSC-NSCs的神经元分化。结果表明,HG/dECM复合水凝胶诱导iPSC-NSCs向神经元分化,复合水凝胶中有更多的细胞表达神经元标记Tuj1(图7G)。用GFAP免疫组织化学染色检测移植到梗死区的iPSC-NSCs的星形胶质细胞分化情况。结果表明,与单独的神经干细胞相比,HG/dECM复合水凝胶不能诱导星形胶质细胞过度分化(图7I)。因此,HG/dECM复合水凝胶能更好地促进iPSC-NSC在梗死区的存活和分化。
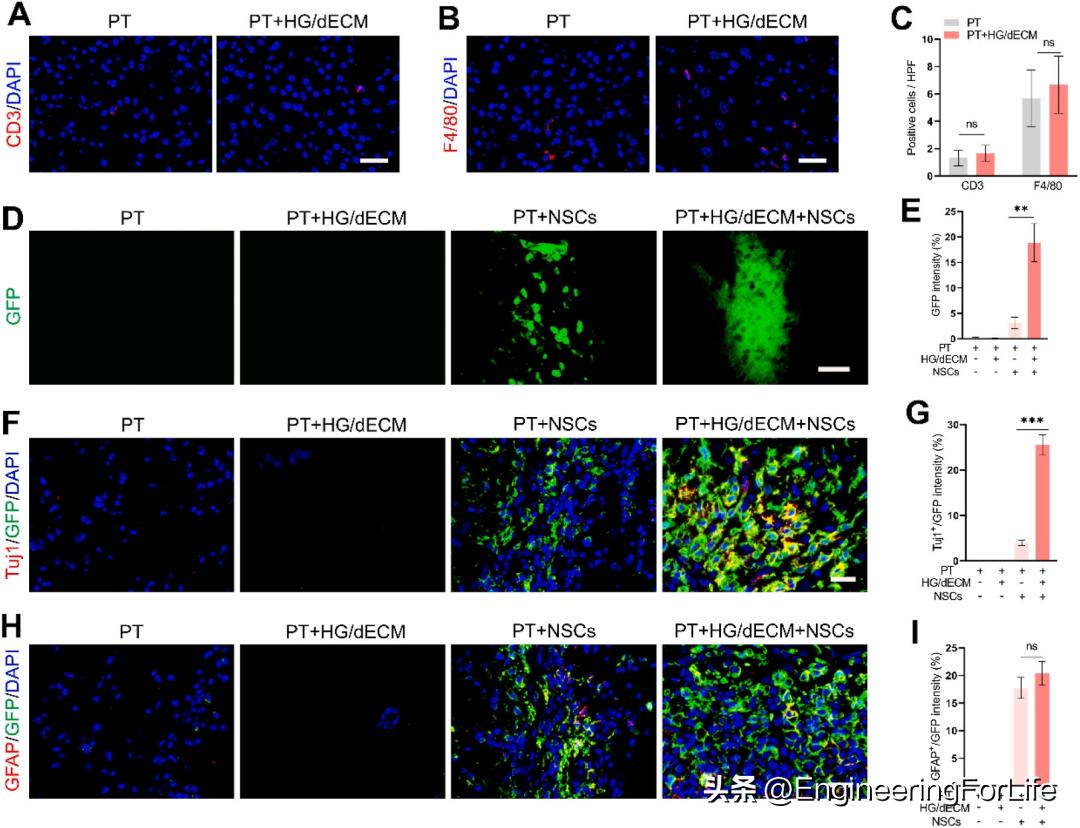
图7 HG/dECM复合水凝胶促进了IPSC-NSCs的体内存活和分化
综上所述,本文通过结合脑脱细胞外基质(dECM)和MMPs反应的主客体(HG)水凝胶的复合水凝胶输送系统,可以有效地解决缺血性卒中后移植干细胞的细胞保留、存活和分化不良的问题。 复合水凝胶中的ECM可以模拟自然脑微环境中独特的复杂生化特征,为细胞的生存和分化提供某些必需的脑内细胞外基质蛋白。同时,具有可调应力松弛的HG基透明质酸水凝胶能够适应细胞生长过程中的体积膨胀。总体而言,这种复合水凝胶策略可以与其他脱细胞ECM来源一起应用于组织特异性再生疗法的开发。
了解更多
关注“EngineeringForLife”,了解更多前沿科研资讯~
