干眼(DED)是临床上极为常见的眼表疾病,典型特征是持续存在干涩、刺痛、疲劳、畏光,甚至视力波动、视功能障碍等异常感觉。
罹患干眼者长期处于慢性应激状态,出现焦虑、抑郁等负面情绪,进一步加重干眼症状形成恶性循环,严重影响患者生活质量,引发社会问题。
干眼病因复杂,发病机制尚不明确,治疗以缓解症状、保护视功能为主。
亚洲干眼学会提出,干眼最初被分为蒸发过强型和水液缺乏型两大类,其中水液缺乏型干眼(ATD)作为干眼的第一大分型,主要是由泪腺损伤或功能障碍而导致的泪液生成不足所造成,治疗包括补充水液和促进泪液分泌。

目前干眼主流的治疗方式是对症治疗,即使用人工泪液局部滴用,以缓解眼部的不适,但存在重复给药、治标不治本等问题。
针刺治疗干眼历史悠久,疗效持久,但作用机制尚不完全明确。
现代研究认为,针灸主要能够从减轻炎性反应、促进泪液蛋白分泌、增加泪腺中乙酰胆碱含量、调节激素水平、泪液代谢和血管活性肠肽(VIP)等多个角度干预疾病进程。
VIP是一种免疫神经肽,有学者认为针灸可以通过神经体液调节方式对血管活性肠肽的产生和表达水平产生影响。
也有研究表明针刺能促进泪腺中VIP含量升高,使其直接与分泌细胞相互作用刺激泪腺分泌泪液,并与G蛋白偶联跨膜受体结合促进环磷酸腺苷(cAMP)释放,cAMP与蛋白激酶A(PKA)的调节亚基结合,促使PKA磷酸化,形成完整的VIP/cAMP-PKA活化通路。
水通道蛋白5(AQP5)是一种水通道蛋白,在角膜上皮和泪腺组织中高表达,与眼病密切相关。
研究证实,泪腺中AQP5的表达或分布异常,均会导致其功能结构的破坏,从而导致干眼发生,尤其是ATD。
因此AQP5在ATD的发病机制中扮演重要的效应蛋白角色,而AQP5是VIP/cAMP-PKA通路的下游主要靶蛋白之一。
VIP/cAMP-PKA/AQP5是一条完整的上下游信号通路,目前关于针刺调控此信号通路治疗干眼的研究较少,本研究通过观察针刺对ATD模型豚鼠眼表症状、泪腺组织病理变化及泪腺中VIP、cAMP、PKA、磷酸化蛋白激酶A(p-PKA)及AQP5表达的影响,探讨针刺是否可以通过激活VIP/cAMP-PKA通路,促进AQP5的表达,从而促进泪腺分泌,改善干眼症状。
普通级健康雄性英国短毛三色豚鼠40只,体质量300~350g,由南京中医药大学动物实验中心提供,动物生产许可证号:SCXK(苏)2019-0005。
饲养于南京中医药大学附属医院基础药理实验室,温度(21±2)℃,12h明暗交替光照周期,自由饮水和摄食,适应性饲养1周后实验。
裂隙灯检查眼前节无异常,酚红棉线泪液分泌试验(PRT)≥10mm/20s的豚鼠入组,随机分为空白组、模型组、针刺组、假针组和西药组,每组8只。
实验中对动物的处理遵循中华人民共和国科学技术部2006年颁布的《关于善待实验动物的指导性意见》,并通过南京中医药大学附属医院伦理委员会批准(批号:2021DW-02-01)。

LS-1B型手持裂隙灯显微镜(重庆上邦),FA1004电子分析天平(上海舜宇恒平)一次性无菌针灸针(0.18mm×13mm,苏州医疗用品厂有限公司),荧光素钠染色试纸、泪液分泌酚红棉线(南京杰力康),包埋机、石蜡切片机、脱水机(美国莱卡),组织摊片机(东莞科迪),光学显微镜、荧光显微镜(日本奥林巴斯),多功能酶标仪(山东云唐),高速冷冻离心机(德国Eppendorf),垂直电泳仪、蛋白转膜系统(美国Bio-Rad),凝胶成像系统(上海天能)。

氢溴酸东莨菪碱(成都普菲德),玻璃酸钠滴眼液(江西珍视明),4%多聚甲醛(武汉白鲨),苏木精-伊红染色试剂盒(武汉Boster),BCA蛋白质试剂盒(北京碧云天),VIP、cAMP、PKA、AQP5抗体(武汉ABclonal),p-PKA抗体(美国CST),二抗(美国Jackson),RIPA裂解液、磷酸酶*制剂抑**、蛋白Marker(美国ThermoFisher),Cocktail蛋白酶*制剂抑**(美国Selleck),豚鼠VIP、AQP5ELISA测定试剂盒(南京精仁生物)。
适应性饲养1周后,除空白组外其余各组豚鼠于每日8:00am、11:00am、14:00pm和17:00pm于后肢外侧皮下注射氢溴酸东莨菪碱每次0.6mg,连续10d后,PRT<7mm/20s,角膜荧光染色阳性为ATD模型复制成功。
实验第11天开始干预,使用布袋束缚豚鼠,操作者手指轻扶其颈背以固定。
空白组不作任何处理。
针刺组针刺双侧“睛明”“攒竹”“丝竹空”“瞳子髎”“太阳”,穴位定位参考《实验针灸学》,留针15min,每日1次,连续14d;假针组用钝头针点压以上穴位1次,每日1次,连续14d;西药组予玻璃酸钠滴眼液滴眼,每次1滴,3次/d,连续14d。
除空白组外,其余各组豚鼠继续皮下注射氢溴酸东莨菪碱溶液维持模型直至实验结束。
泪膜破裂时间(BUT)测定:分别于造模前、造模后及干预后进行测定。
先将荧光素钠染色滤纸条的着色端用0.9%氯化钠溶液润湿,湿润的着色端轻点豚鼠的下眼睑穹窿部2—3次后,使豚鼠眨眼数次,荧光素钠充分弥散分布在角膜上。
在手持式裂隙灯显微镜的钴蓝灯照射下观察,计时器记录下出现第1个角膜干燥斑所用的时间,反复测量3次,取其均值即为BUT。

角膜荧光素钠染色及评分(FLS)测定:观察BUT后,使豚鼠眨眼数次让荧光素钠均匀地分布在角膜上。
在手持裂隙灯显微镜的钴蓝灯照射下观察角膜上皮损伤并进行染色评分。
评分标准:通过角膜中央做垂直和平行两条线,将角膜平均分为4个象限,每个象限评分为0—3分。
无荧光染色斑点为0分;荧光染色少于30个斑点为1分;荧光染色超过30个,但没有融合成片的斑点为2分;融合成片的染色斑点为3分。
最后计4个象限分数的总和为该侧FLS评分。

PRT测定:FLS测定结束后,将酚红棉线着色端反折,轻置于豚鼠下眼睑内靠近外眦部约1/3处,使其闭目,持续20s后取下棉线,测量棉线被泪液湿润酚红浸染的长度。
泪腺指数检测:治疗结束后,各组大鼠深度麻醉处死,即刻取出双侧泪腺组织,用4℃PBS漂去组织血液,滤纸吸干残留的PBS。
泪腺称重并计算泪腺指数。
泪腺指数(mg/g)=双侧泪腺质量(mg)/豚鼠体质量(g)。

HE染色观察泪腺组织病理变化:每组8只豚鼠的一侧泪腺组织固定于10%甲醛溶液中24h,石蜡包埋后切片(厚度5μm),进行HE染色,通过光学显微镜观察各组泪腺病理变化。
免疫荧光技术检测泪腺组织AQP5的表达:每组8只豚鼠泪腺组织石蜡切片脱蜡至水后,置于盛满EDTA抗原修复缓冲液(pH8.0)的修复盒中抗原修复,随后将切片在PBS(pH7.4)中晃动洗涤3次,每次5min,稍甩干后用组化笔在组织周围画圈防止抗体流走,滴加3%BSA封闭30min。

轻轻甩掉封闭液,加AQP5一抗(1:200)4℃孵育过夜,PBS晃动洗涤3次,每次5min。
滴加免疫荧光二抗(1:500),避光室温孵育50min。
PBS液漂洗3次,每次5min;滴加DAPI染液,避光室温孵育10min。
PBS晃动洗涤3次,每次5min。
加入自发荧光淬灭剂5min,流水冲洗10min。
用抗荧光淬灭封片剂封片,荧光显微镜下观察并采集图像,分析AQP5表达强度,计算阳性表达百分比。

ELISA法检测泪腺组织中VIP和AQP5的含量:每组3只豚鼠,分别取一侧泪腺组织300mg,在冰浴中充分匀浆后加300μL0.9%氯化钠溶液进行稀释,离心后取上清液,标准品设置完成后,按说明书要求分别用VIP和AQP5试剂盒进行检测,用酶标仪在450nm波长测量各孔的吸光度值,计算出各样品的实际含量。
Westernblot法检测泪腺组织中VIP、cAMP、PKA、p-PKA、AQP5蛋白表达:取每组3只豚鼠另一侧泪腺组织50mg于冰上剪碎匀浆,加入RIPA裂解液300µL及蛋白酶*制剂抑**PMSF混合液(100∶1)于冰上裂解20min,于4℃离心5min,吸取上清转移至新预冷的微量离心管中置于冰上,即为蛋白样本,弃沉淀。

用BCA试剂盒测定样品总蛋白含量,计算上样量,蛋白上样进行分离胶(浓度12%、8%)、浓缩胶(5%)凝胶电泳后转至PVDF膜。
5%脱脂奶粉室温摇床封闭2h,PBST洗膜15min×3次后,加入一抗VIP、cAMP、p-PKA、PKA、AQP5、GAPDH(1:1000),置于4℃摇床孵育过夜。
次日,PBST洗膜15min×3次后,加入二抗(1:5000),室温孵育90min。
PBST洗膜10min×3次后用ECL发光试剂盒A、B溶液等量混合,滴加于PVDF膜上,凝胶成像系统曝光显影。
采用ImageJ图像分析软件对显影的条带进行灰度值分析,以目的蛋白与内参蛋白条带灰度值的比值作为目的蛋白的相对表达量。

采用SPSS25.0软件分析处理,计量资料采用均数±标准差(x−±s)表示,本实验数据经检验呈正态分布,多组间比较采用单因素方差分析,进一步两两比较时,若方差齐则采用LSD检验,若方差不齐则采用TamhaneT2检验。
以P≤0.05为差异有统计学意义的标准。

造模前,各组豚鼠PRT、BUT和FLS差异均无统计学意义。
造模后,与空白组比较,模型组、针刺组、假针组和西药组PRT、BUT降低(P<0.01,P<0.05),FLS升高(P<0.01,P<0.05)。
干预后,与模型组比较,针刺组和西药组PRT、BUT升高(P<0.01,P<0.05),FLS降低(P<0.01,P<0.05)。
与假针组比较,针刺组和西药组PRT、BUT升高(P<0.01,P<0.05),FLS降低(P<0.01,P<0.05)。
与西药组比较,针刺组PRT升高(P<0.05)。

与空白组比较,模型组的泪腺指数降低(P<0.01)。
与模型组比较,针刺组和西药组的泪腺指数升高(P<0.05)。
空白组泪腺结构无明显异常,上皮细胞大小均匀,胞质丰富,排列紧密规则,未见明显腺泡萎缩或炎性反应;模型组和假针组泪腺上皮细胞可见明显萎缩,排列无规律,腺腔扩张,局灶可见淋巴细胞浸润;针刺组泪腺上皮细胞结构基本正常,部分腺腔扩张,可见少量淋巴细胞浸润;西药组泪腺部分上皮细胞萎缩、腺腔扩张,可见部分淋巴细胞浸润。
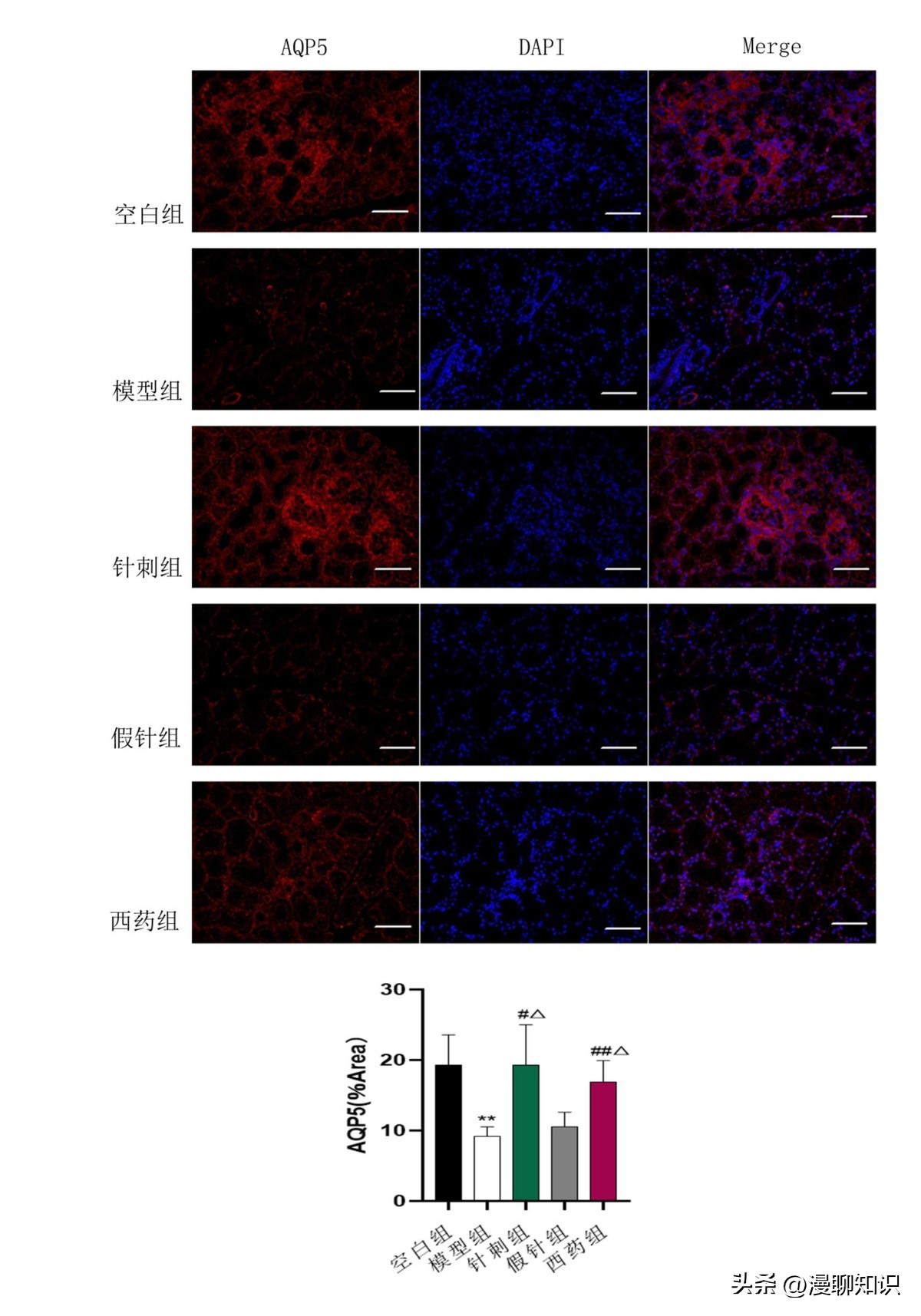
与空白组比较,模型组中AQP5荧光表达降低(P<0.01)。
与模型组和假针组比较,针刺组和西药组中AQP5荧光表达升高(P<0.05,P<0.01)。
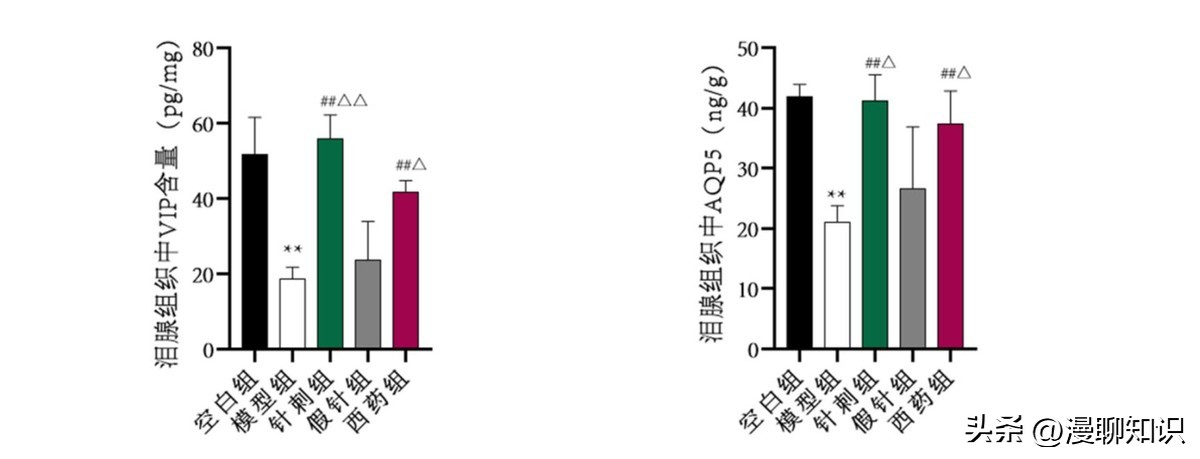
与空白组比较,模型组豚鼠泪腺组织VIP和AQP5含量降低(P<0.01)。
与模型组和假针组比较,针刺组与西药组泪腺组织VIP和AQP5含量升高(P<0.01,P<0.05)。
与空白组比较,模型组豚鼠泪腺组织VIP、cAMP、PKA、p-PKA、AQP5蛋白表达降低(P<0.01,P<0.05)。
与模型组比较,针刺组VIP、cAMP、PKA、P-PKA、AQP5的蛋白表达升高(P<0.05,P<0.01);西药组VIP、AQP5蛋白表达升高(P<0.05)。
与假针组比较,针刺组AQP5、VIP、cAMP和PKA的蛋白表达升高(P<0.01,P<0.05),西药组AQP5的蛋白表达升高(P<0.05)。
泪腺是泪液中水、蛋白质及电解质的主要来源,参与泪膜形成,润滑眼表。
当泪腺受影响时,会引起泪液分泌量减少,导致ATD,破坏眼表完整性[20],临床多采用人工泪液替代以缓解症状,但很难解决根本问题。
针刺治疗干眼由来已久,在临床上广泛应用。
多项随机临床对照试验显示,相较于人工泪液,针刺可以促进泪腺分泌,显著提高泪液分泌量,改善患者眼部干痒痛及视力波动等症状,对于ATD患者尤为适用。
在本研究中,连续针刺氢溴酸东莨菪碱诱导的ATD豚鼠14d后,与模型组相比,针刺组PRT、BUT升高,FLS降低,证明针刺可以促进泪液分泌,同时改善眼表症状,与西药组使用玻璃酸钠组相比,针刺组PRT升高,同样也证实了单纯使用人工泪液治疗干眼,只能补充水分和润滑眼表,而针刺能在促进泪液分泌方面发挥作用,做到治病求本。
炎性反应和细胞凋亡都被认为是干眼发病机制中的关键环节,HE染色的泪腺切片结果显示,与模型组比较,针刺组泪腺上皮细胞结构相对完整,淋巴细胞浸润较少,也说明针刺可以抑制炎性反应,改善泪腺细胞形态学变化,对ATD豚鼠模型的泪腺有明显的保护作用。
水通道蛋白家族(AQPs)作为一类特异性跨膜转运水的蛋白,能显著增加细胞膜水通透性,参与水的分泌、吸收及细胞内外水的平衡,广泛存在于细菌、植物和动物细胞膜上。
截至目前共发现13种亚型,其中AQP5主要在泪腺上皮、涎腺、角膜上皮、肺泡上皮和胃肠道中表达。
Wood等在研究中证实了AQP5在泪腺等外分泌腺分泌中的作用,当AQP5表达、分布或转运发生异常时,均可导致泪腺结构紊乱及功能异常,导致泪液分泌下降,而泪液分泌减少是ATD发生发展的关键。
本研究在观察氢溴酸东莨菪碱诱导的ATD豚鼠泪腺时,同样发现模型组泪腺上皮细胞可见明显萎缩,腺腔扩张,局灶可见淋巴细胞浸润,并且免疫荧光技术检测到模型组泪腺中AQP5表达降低。
空白组和针刺组泪腺的AQP5荧光染色较强,且主要表达在泪腺的导管和腺泡细胞的顶质膜上,说明AQP5在ATD的发病中扮演相当重要的效应蛋白角色。
VIP是一种神经内分泌免疫调节肽,具有调节免疫、血管舒张及激素分泌等多种作用。
在眼部主要由眼表、泪腺和睑板腺的副交感神经自主神经元产生。
Orsolya等研究显示,VIP(100nM)刺激会引起小鼠泪腺导管强烈而连续的液体分泌,并导致体内cAMP含量升高。
VIP可以与G蛋白偶联跨膜受体结合,激活腺苷酸环化酶从而促进cAMP释放,cAMP与PKA的调节亚基相结合,从而促使PKA磷酸化,形成完整的VIP/cAMP/PKA活化通路。
cAMP/PKA的活化可以增强AQP5的表达,VIP/cAMP/PKA的激活会增强AQP5的水液转运能力。
Nahid等也在体外实验中证实了AQP5是VIP/cAMP-PKA通路的下游主要靶蛋白之一。
本研究结果显示,针刺可以升高水液缺乏干眼豚鼠泪腺中VIP、cAMP、PKA、p-PKA及AQP5的表达。
综上所述,针刺可以改善ATD豚鼠模型泪腺组织结构,减少淋巴细胞浸润,促进泪液分泌,缓解干眼症状,从而治疗干眼,以上作用可能与激活VIP/cAMP-PKA/AQP5信号通路有关。