
01
要点概括
1. 表型变异甚至存在于源于单个祖细胞的克隆群。表型变异可以产生不同特征的细胞亚群(例如,某些细胞可能对某些药物产生耐药性)。若要量化变异细胞的动态变化,需要以高时空分辨率跟踪单个细胞。
2. 一些活细胞成像技术(例如高内涵成像)允许跟踪单个细胞,但同时需要对细胞进行荧光标记,因此会产生光毒性,从而限制实验的持续时间或成像频率。Nanolive成像不基于荧光,从而避免了这些限制。Nanolive测量细胞组分的折射率,允许在不影响空间分辨率和不受时间限制的情况下高频监测细胞。因此在群体水平上跟踪单个细胞的状态、行为、表型和功能。
3. 在此功能应用中,我们展示了Nanolive成像在单细胞表征方面的巨大潜力。首先,我们在未受干扰细胞群和时间水平上分析微观异质性(案例研究一)。然后,在研究细胞内转运(案例研究三)和呼吸扰动(案例研究四)如何影响细胞形态的微观异质性之前,我们将我们的分析扩展到包括脂滴动力学的定量评估(案例研究二)。
4. 希望本应用能够激励研究人员使用Nanolive活细胞成像技术改变他们的研究,并通过捕获随时间变化的复杂的细胞状态和群体环境中细胞亚群的相互关联性来改进单细胞分析。
02
案例
案例一:未受干扰细胞表型变异的量化
背景
表型变异是所有生物系统普遍存在的特征。它支持复杂的动态系统(如免疫反应)和生物过程(如干细胞分化)。测量细胞表型变异需要保持高空间和时间分辨率的多重成像平台,如Nanolive的CX-A型号。在这里,我们首次对未受干扰细胞群体中单个细胞的表型变异性进行定量分析。
实验方法
使用Nanolive CX-A上的10x10网格扫描模式(每8.5分钟拍摄一张图像),对未受干扰的3T3前脂肪细胞群进行90小时成像。生成的图像进行最大强度Z投影,使用内部开发的标准操作方法进行分割和量化。
实验结果
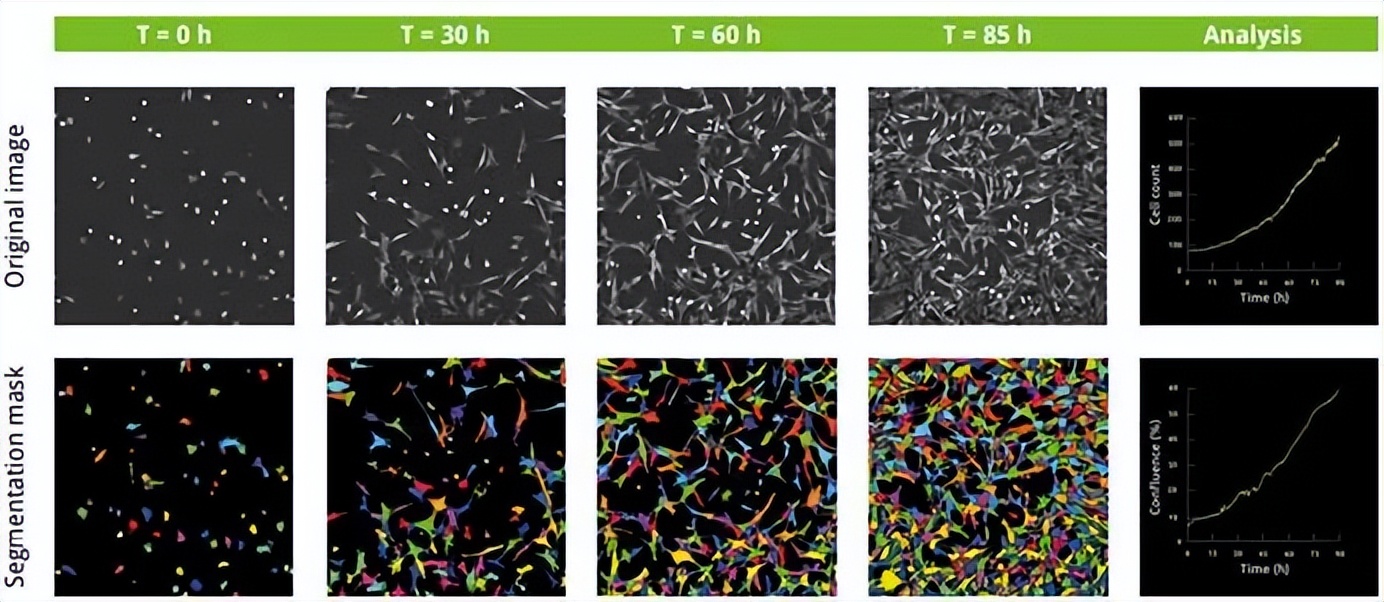
图-1. 在整个实验过程中,细胞融合率增加了10倍,从实验开始时的6%(74个细胞)增加到实验结束时的60%(521个细胞)
1. 群体水平上可视化表型变异分析
在每个时间点,计算每个细胞(共150650个细胞)的六个指标(单元面积、周长、紧凑度、范围、干物质量和粒度)。数据被可视化为相对频率直方图,用于测量群体中的微观异质性,并比较指标差异。单元面积(A)、压实度(B)和干质量(C)如下所示:
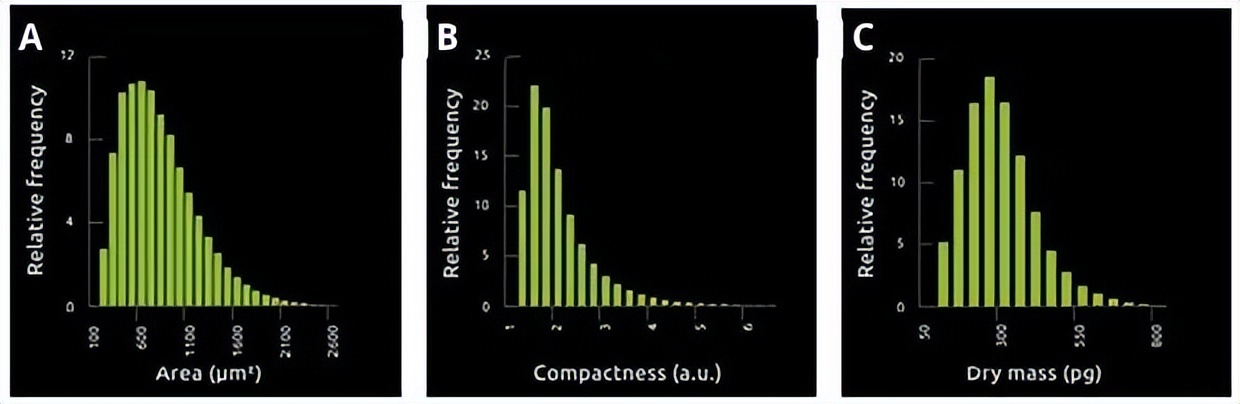
图-2. 所有指标高度可变,并呈正偏态(峰偏左)
2. 单细胞的时间响应分析
下图显示了随时间变化的细胞面积和紧凑度,首先是显示平均±标准误差(SE)的线形图,然后是变异系数(CV)。
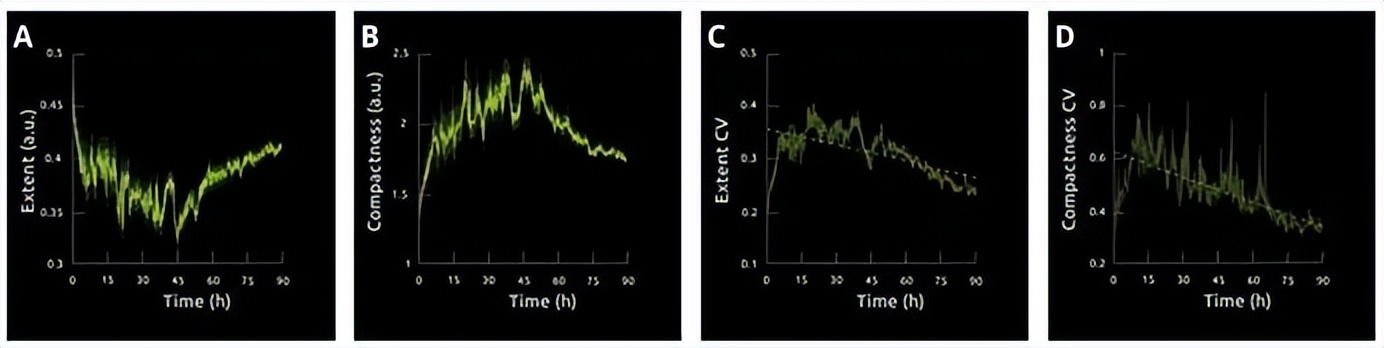
图-3. 在前48小时内,观察到平均范围减少了31%,但在实验的后半部分,观察到平均范围稳步增加(A)。在平均压实度(B)中观察到相反结果。有趣的是,这两个指标的变异性随时间的推移而减少,如SE(A,B)和CV(C,D)值的减少
3. 导致群体水平上的表型变异的原因
微观异质性的成因可分为内在和外在因素。内在因素是指生物噪音,外在因素与细胞周围环境中的空间不平等或细胞-细胞/细胞-基质相互作用有关。为了测试在群体水平上观察到的变异是否由内在因素或外在因素驱动,我们比较了群体水平上的细胞(外在因素发生函数变化)和孤立的单个细胞(外在因素稳定)。彩色轮廓与直方图中的颜色有关。
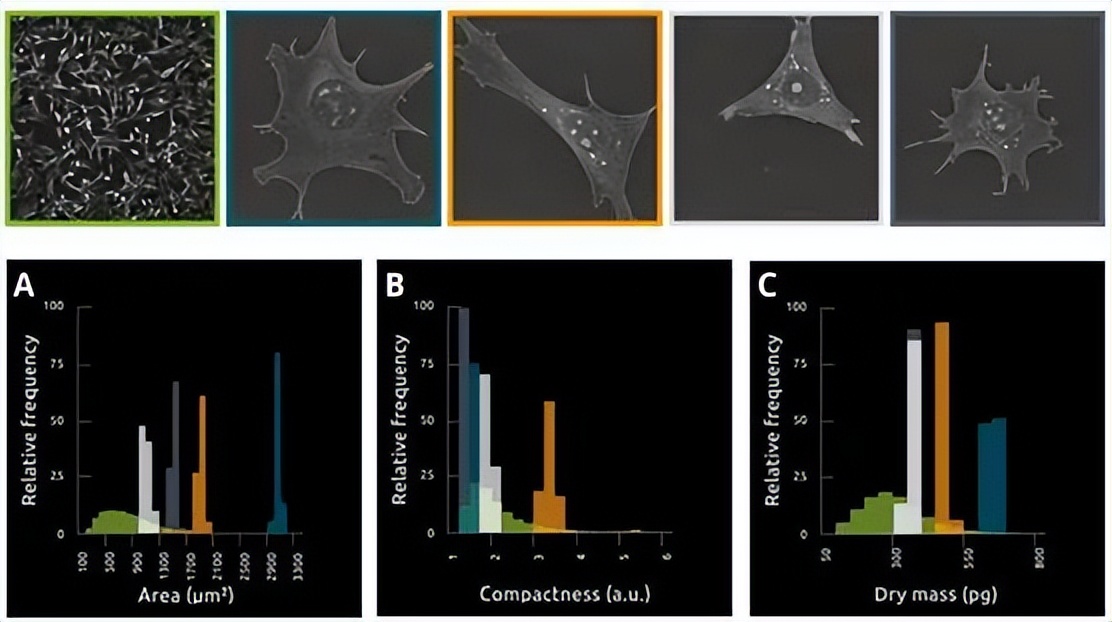
图-4. 尽管表型不同,但分离的单个细胞比群体水平(A、B、C)的细胞变化较小,这表明群体水平的变化受外部因素影响,最有可能是细胞拥挤,因为细胞必须适应日益有限的空间。这种方法提供了一种测试表型变异的机制基础的方法
案例二:未受干扰细胞中脂滴动力学的定量研究
背景
了解脂滴(LD)动力学对于健康、食品等行业非常重要。Nanolive无标记成像克服了光毒性和光漂白性缺点,并且完全定量,确保总体、单细胞和单个LD水平上不会遗漏细节。
实验方法
使用Nanolive CX-A上的10x10网格扫描模式(每8.5分钟拍摄一张图像),对未受干扰的3T3来源的前脂肪细胞群进行30小时成像。最终的图像进行了分析最大强度Z投影,分割成单个细胞和LDs,并使用内部软件进行分析。
实验结果
1. 在总体水平上量化LD动态
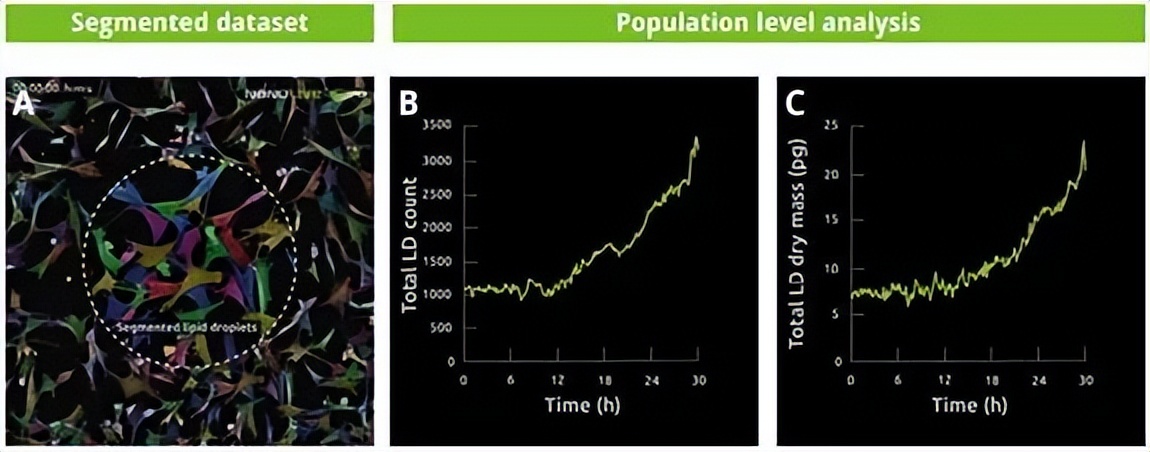
图-5. 在实验过程中,LD观测非常精确(A),增加了26.7%(细胞从278个增加到518个)。右图显示总LD计数(B)和总LD干物质量(C)的分析。在试验的前12小时内,这两个指标相对稳定,然后逐渐增加。这两个指标的增长幅度相似。LDs的总数增加了187%(B),而总LD干物质量在同一时期增加了202%(C)
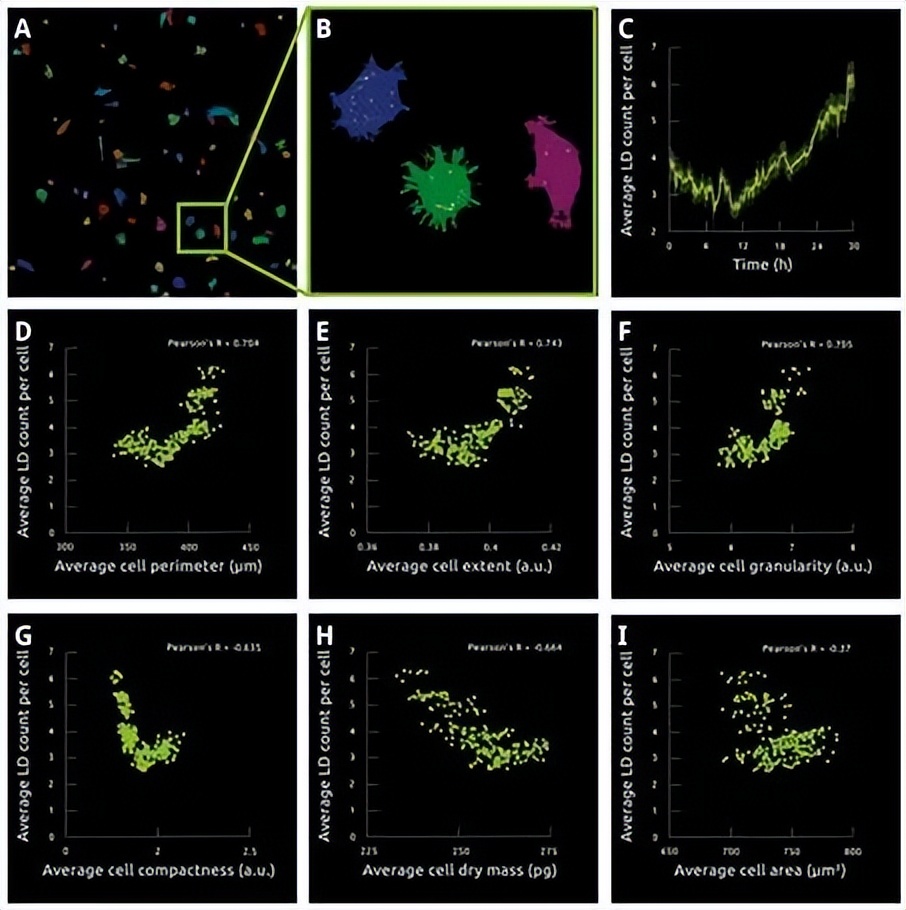
图-6. 从总体水平(A)到单细胞水平(B)进一步分析,发现在最初的12小时内,每个细胞的LDs平均数量减少,随后增加(C)。这种增加可能与细胞衰老有关,有研究报道LD在老细胞中的积累。也可能反映了能量的变化。将LDs的平均数量与其他细胞指标关联,表明包含更多LDs的细胞往往具有更大周长(D)、更大面积(E)和更高粒度(F),但紧凑性较差(G),干物质量较少(H)。而关于干物质量,发现在含有较多LDs的细胞中,单个LDs较小,或者含有较少LDs的细胞具有较多的胞质和核干物质
2. 在单个LD水平上量化LD动态
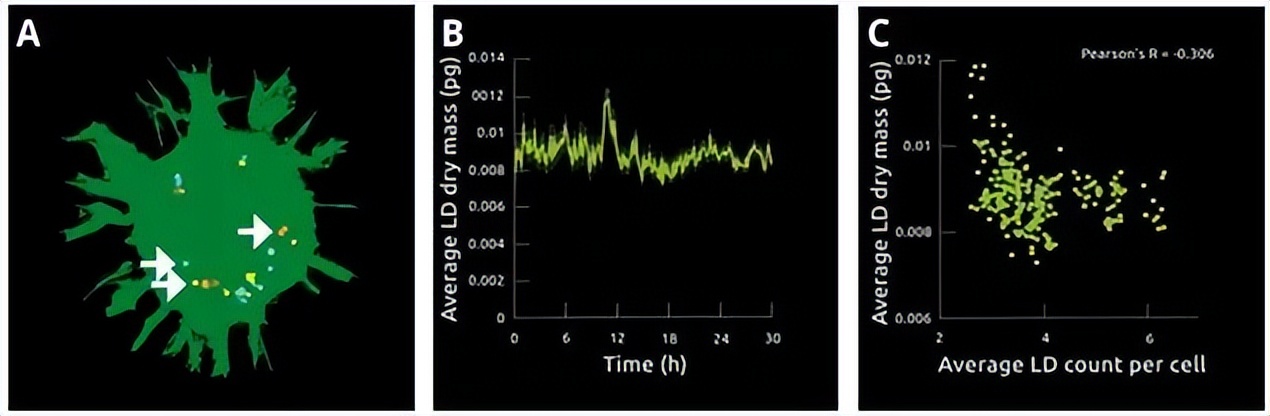
图-7. 描述单个LDs的形态(A;白色箭头)。计算LD的平均干物质量随时间的变化。在本例中,我们看到干物质量波动,但在实验过程中不会发生剧烈变化(B)。根据每个细胞的平均LD计数绘制单个LD干物质量,表明如果细胞含更多LD,则单个LD往往更小
案例三:扰动胞内运输后的表型变异
背景
胆固醇转运的改变在阿尔茨海默病、艾滋病等多种疾病中起到重要作用。U18666A(一种胆固醇的带电衍生物)抑制溶酶体中胆固醇的释放,触发内吞过程中脂质和胆固醇积累(详见图A)。因此,我们调查了U18666A的存在对表型变异的影响。
实验方法
1. 3T3衍生的前脂肪细胞与U18666A一起孵育,并在Nanolive的CX-A上使用10x10网格扫描模式成像24小时(每8.5分钟拍摄一张图像)。生成的图像经过最大强度的Z投影,使用内部开发的标准操作进行分割和量化。
2. 测量六个指标:面积、周长、紧凑度、范围、干物质量和粒度。计算U18666A扰动细胞的变异系数(CV),并将其与相同融合处的未扰动细胞(案例研究1)进行比较。细胞面积和粒度显示的结果如下:
实验结果
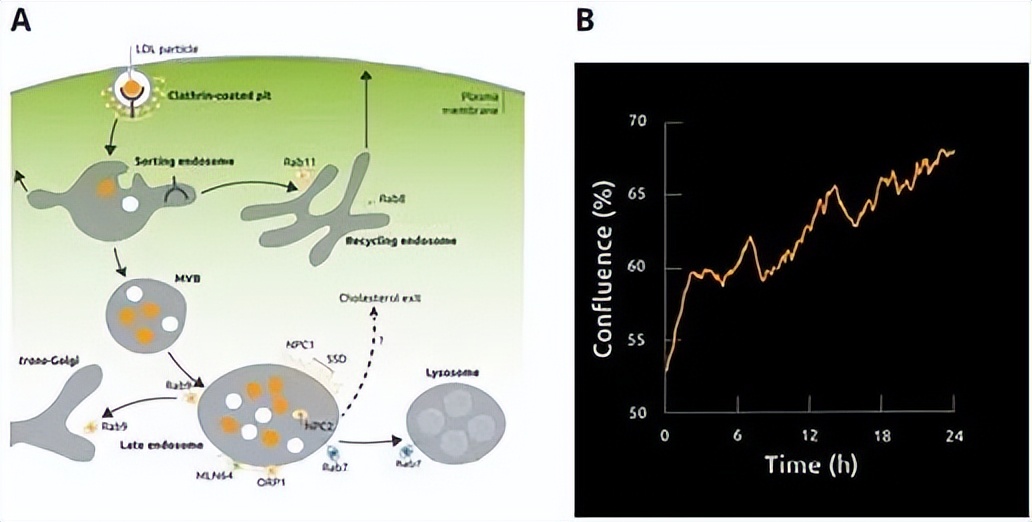
图-8. 在实验过程中,细胞融合率增加了15%,从53%的细胞增加到68%。略低于在类似时间段内未受干扰细胞中观察到的融合增加率(20%;案例研究1)
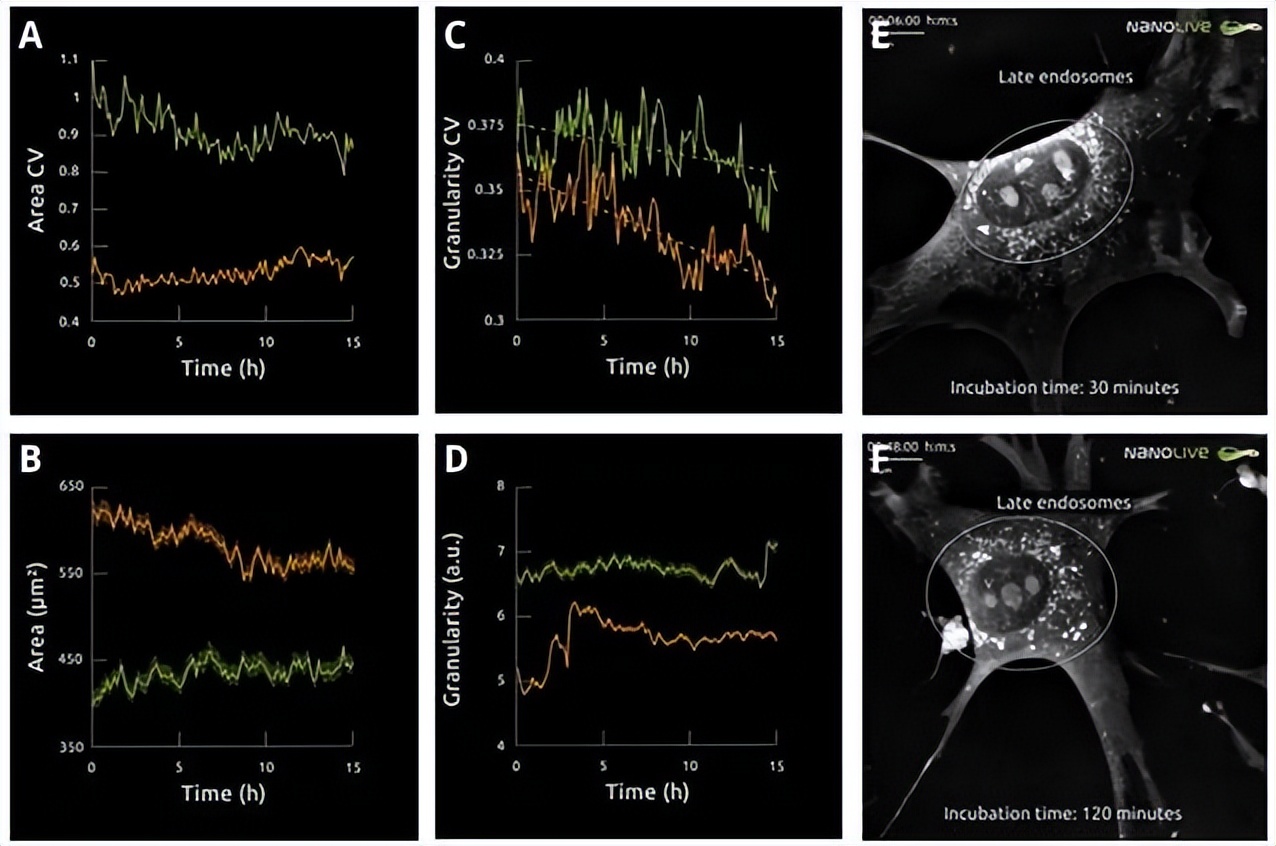
图-9. 与未受干扰的单元(A)相比,U18666A细胞面积降低了50%。时间变化的面积图显示U18666A扰动细胞的表面积大于未扰动细胞(B)。粒度是影响变异的其他指标,随着时间推移,变异性降低了16%(C)。在未受干扰的细胞中观察到类似的减少,表明细胞的内部成分随着时间的推移变得更相似。随时间变化的粒度图显示粒度在稳定之前的前4小时内急剧增加(D)。详细地分析粒度,显示晚期内体分布的差异可能是U18666A扰动细胞粒度早期增加的原因。晚期内体(细胞3中的亮点)在孵育30分钟后(E)呈核周分布,但在孵育120分钟后(F)贯穿整个细胞分布
案例四:呼吸扰动后的表型变异
背景
呼吸的改变导致许多疾病。了解细胞对刺激和压力的反应所经历的动态变化,需要实时捕捉细胞反应。在本案例研究中,我们使用鱼藤酮(电子传递链复合物I中的一种化学*制剂抑**电子转移)干扰呼吸,然后使用Nanolive的自动显微镜CX-A对细胞反应进行成像。量化随时间变化的表型变化,并将其与未受干扰的细胞进行比较(案例研究一)确定扰动呼吸是否诱导或减少异质性。
实验方法
3T3衍生的前脂肪细胞与鱼藤酮一起孵育,并在Nanolive的CX-A上使用10x10网格扫描模式成像24小时(每8.5分钟拍摄一张图像)。生成的图像经过最大强度的Z投影,使用内部开发的标准操作步骤进行分割和量化。
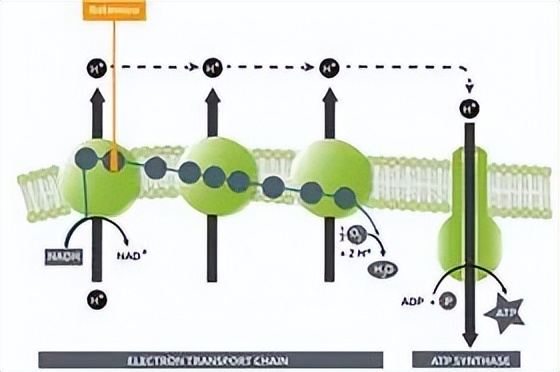
图-10. 鱼藤酮的作用
实验结果
1. 量化细胞对鱼藤酮干扰的反应
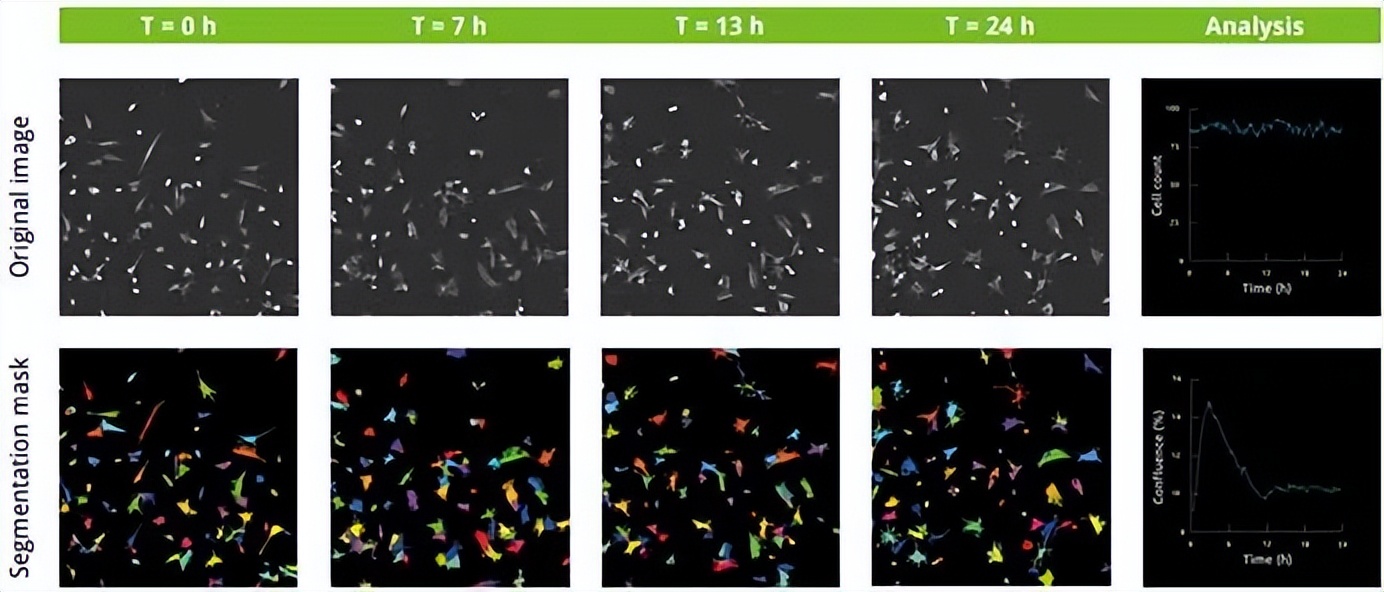
图-11. 细胞对鱼藤酮扰动立即反应。细胞融合率在最初的3小时内增加,在接下来的9小时内恢复到起始水平,之后稳定下来
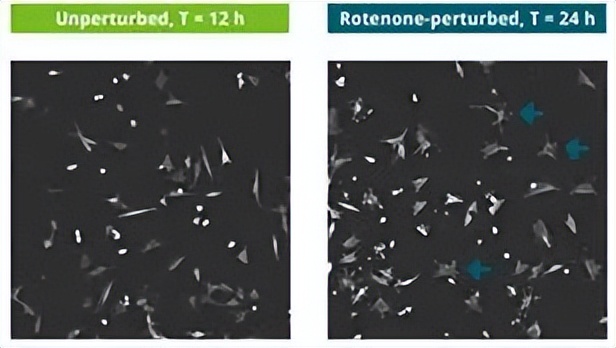
图-12. 鱼藤酮干扰细胞在同一融合处显示出与未干扰细胞明显不同的形态(案例研究1)。许多细胞形成额外的或拉长的突起(蓝色箭头)
2. 鱼藤酮对表型的影响
测量六个指标:面积、周长、紧凑度、范围、干物质量和粒度。计算鱼藤酮扰动细胞的变异系数(CV),然后在同一细胞融合处将其与未扰动细胞(案例研究1)进行比较。细胞面积、范围、干物质量和粒度这四个指标显示以下结果:
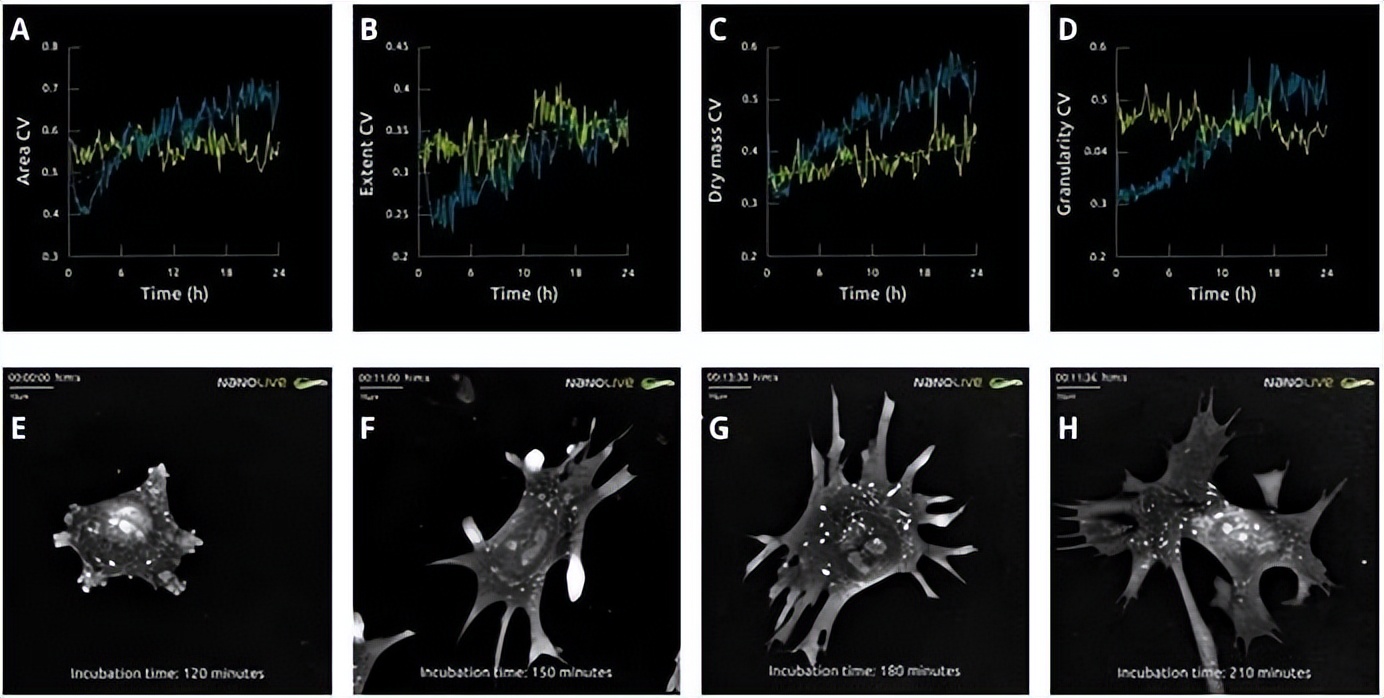
图-13. 鱼藤酮扰动在恢复阶段(即在实验的前4小时;A)诱导细胞面积的变异性增加75%。在范围(B)、干物质量含量(C)和粒度(D)中也观察到了类似增加。显然,呼吸扰动会在群体中产生大量噪音。在恢复过程(E-F)的不同阶段检查单个细胞,发现存在广泛的形态,随着时间的推移,这些形态变得越来越突出。这可能反映了不同细胞间内在因子的差异;一些细胞可能或多或少具有可塑性,这与它们能够应付的压力水平有关
03
参考文献
1.Gurr, M.I. et al. 2016. Lipids: biochemistry,biotechnology and health. John Wiley & Sons.
2.Laissue PP. et al. 2017. Nat. Meth. 14(7):657-61.
3.Folick A. et al. 2011. Curr. Opin. Gen. Develop.1;21(5):585-90.
4.Flor, AC. et al. 2017. Cell Death Discov.30;3(1):1-2.
5.Lizardo, DY. et al. 2017. Mol. BioSyst.13:498–509.
6.Olzmann, JA. and Carvalho, P. 2019. Nat. Rev.Mol. Cell Biol. 20(3):137-55.
7.Cenedella, RJ. Lipids, 44(6), 477-487 (2009),
8.Ikonen E. Nat. Rev. Mol. Cell Biol. 9(2):125-38(2008)
9.Sandoz PA et al. PLoS Biol. 19;17(12):e3000553(2019)
10.Radad K et al. Neurochem Int. 1;49(4):379-86(2006)


昆明纳瑞科技有限公司