单用内分泌治疗或联合CDK4/6*制剂抑**,对HR+ BC女性的认知功能有何影响?
编者按: 辅助内分泌治疗(ET)是激素受体阳性(HR+)乳腺癌治疗的基石,而且ET联合“细胞周期蛋白依赖性激酶4和6”(CDK4/6)*制剂抑**的方案越来越普遍。由于雌激素对神经系统具有保护作用,细胞周期蛋白D又会影响海马细胞增殖,因而ET联合CDK4/6*制剂抑**疗法可能会影响人的认知功能,但目前的相关研究较少。本文综述了ET联合CDK4/6*制剂抑**对绝经前、围绝经期和绝经后乳腺癌患者认知功能的影响。
背景
大约每8名美国女性中就有1人会被诊断出浸润性乳腺癌(BC)[1],其中约有75%为激素受体阳性(HR+)[2]。建议患原发性HR+ BC女性接受(新)辅助全身治疗(如内分泌治疗)以降低疾病复发风险;内分泌治疗(ET)的首选疗程为5年,高危患者则可延长至7~10年。目前,新的治疗策略为内分泌药物(如选择性雌激素受体(SER)调节剂如他莫昔芬、SER下调剂如氟维司群、类固醇和非类固醇芳香化酶*制剂抑**)联合“哺乳动物雷帕霉素靶点(mTOR)”*制剂抑**、CDK4/6*制剂抑**和“磷酸肌醇3-激酶(PI3K)”*制剂抑**。这些靶向药物增加了可选的ET治疗方案,有望延长治疗持续时间。
BC患者在化疗期间及化疗后经常报告认知能力下降:超过一半的BC患者报告认知发生变化(主要是记忆力和注意力方面);纵向研究发现,从化疗前到化疗后1年,高达61%的BC患者在标准化神经心理学测试中表现较差[3]。发生化疗相关认知能力下降的危险因素多种多样:年龄较大、基因多态性(如载脂蛋白E)以及化疗类型(含蒽环类药物方案)均与风险增加相关[4,5]。研究表明认知能力下降的严重程度似乎与剂量和持续时间相关,在其他肿瘤中也是如此[6-8]。然而这些风险因素未能准确预测风险。
目前认为化疗相关的认知能力下降的最重要机制是神经回路失调、脑源性神经营养因子下调、神经炎症以及氧化应激增加[9]。神经影像学研究表明,从化疗前到化疗后,患者的灰质密度降低,大脑激活和脑循环发生变化,白质完整性降低,结构连接性和形态学发生变化[10];与没有癌症史的女性相比,接受过化疗的BC女性甚至在治疗后20年仍存在大脑结构差异[11]。
与化疗相关认知能力下降的研究相比,辅助治疗及转移性乳腺癌ET治疗的相关认知功能研究较少,ET联合方案对认知影响的研究则几乎没有。由于雌激素在维持大脑功能完整性方面发挥着重要作用,因此总结ET对绝经前、围绝经期和绝经后BC患者认知的影响具有重要意义。ET持续时间的延长(辅助治疗已长达10年),以及ET与CDK4/6*制剂抑**联合使用的迅速增加,使得这些疗法对认知影响的研究变得愈发重要。
激素受体阳性乳腺癌
当组织病理学检查显示≥1%(美国)或>9%(荷兰)的肿瘤细胞中存在激素受体时,BC被定义为HR+。在HR+ BC中,雌激素通过与癌细胞的激素受体结合,在癌细胞的发育和生长中发挥着最重要的作用。雌激素通过与位于细胞核或细胞壁上的雌激素受体(ER)结合来影响细胞功能,结合之后ER发生二聚化和磷酸化,从而与ER靶基因的DNA结合。与上述雌激素反应元件(ERE)结合可导致靶基因的激活,然后诱导癌细胞生长、分化、凋亡和血管生成。此外,雌激素还可通过蛋白质与蛋白质相互作用来激活靶基因(独立于ERE结合),例如通过酪氨酸激酶途径(例如EGFR、HER2、IGFR)[12]。生长因子也可促进ER磷酸化,从而增加蛋白激酶的激活,引起基因转录。
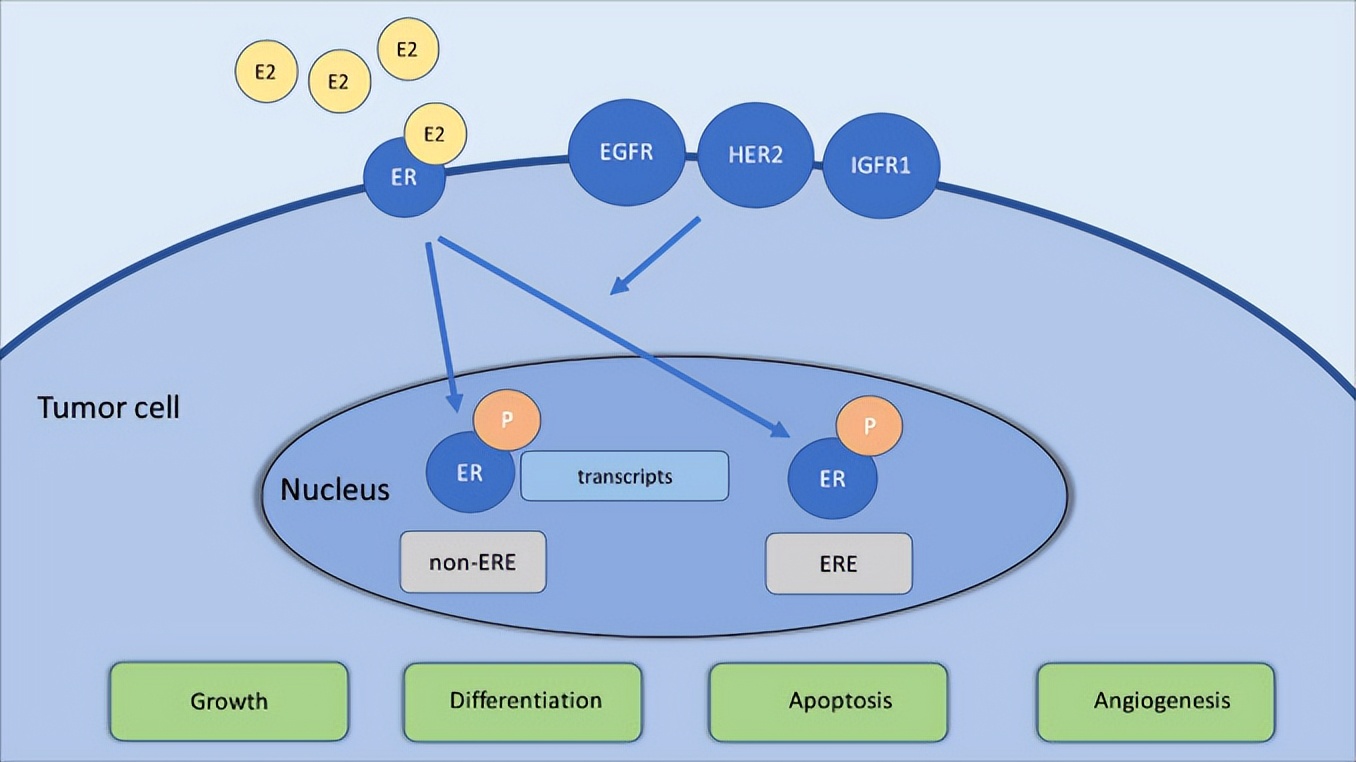
△ 雌激素和生长因子受体间的相互作用
内分泌治疗
ET具有多种类型,主要根据患者的绝经状态、疾病阶段以及既往ET治疗来选择后续方案。在临床实践中,芳香化酶*制剂抑**(阿那曲唑、依西美坦和来曲唑)、他莫昔芬、氟维司群和黄体生成素释放激素(LHRH)类似物是最常见的ET类型[13]。除氟维司群外,所有药物均可在(新)辅助治疗和转移性乳腺癌中使用。
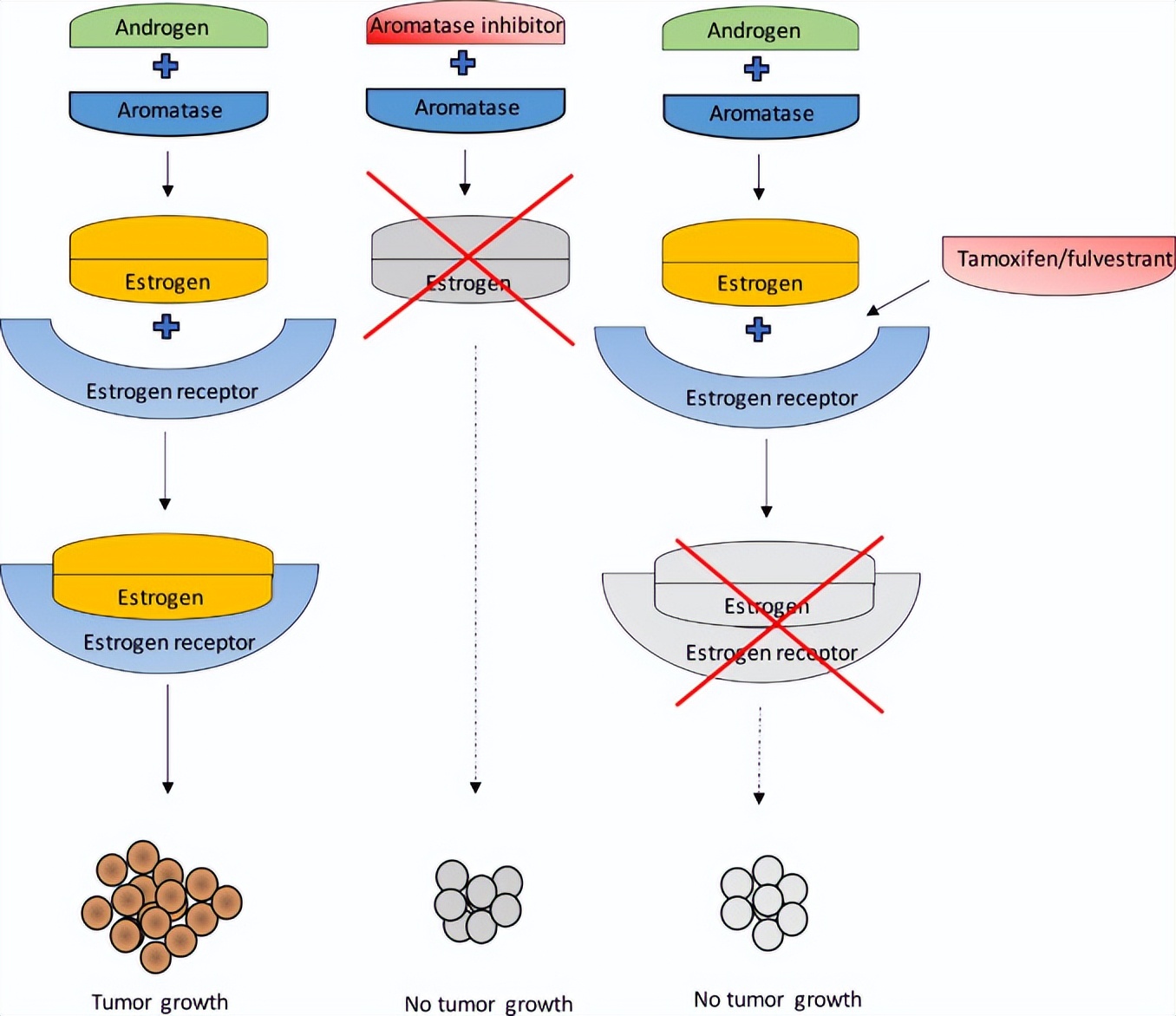
△ 芳香化酶*制剂抑**、他莫昔芬和氟维司群治疗BC的作用机制
他莫昔芬是所有SERM中最常用的药物,具有雌激素和抗雌激素效应,并且是已知治疗BC时间最长的ET。他莫昔芬可通过与ER结合,并根据不同组织而发挥抑制或刺激雌激素作用,如他莫昔芬对子宫内膜和骨组织有刺激作用,但对乳腺组织有抑制作用[14]。
芳香化酶*制剂抑**可通过灭活外周脂肪组织中的芳香化酶来抑制雌激素的产生。然而芳香化酶失活就导致雌激素前体转化为雌激素受阻(雌激素前体即使在绝经后仍然在肾上腺中产生),进而导致严重的雌激素过低[15]。类固醇和非类固醇芳香化酶*制剂抑**存在区别:类固醇*制剂抑**通过形成共价键不可逆地灭活芳香化酶;而非类固醇芳香化酶*制剂抑**可逆结合,从而降低酶活性。类固醇(如依西美坦)和非类固醇芳香化酶*制剂抑**(如阿那曲唑和来曲唑)主要用于绝经后妇女。而在卵巢功能完整时,严重的低雌激素状态会刺激垂体腺,使卵巢产生雌激素;因此当使用芳香化酶*制剂抑**治疗绝经前女性时,需要通过手术切除卵巢,或同时使用LHRH类似物(戈舍瑞林、布舍瑞林和亮脯氨酸等)来抑制卵巢功能[16]。
氟维司群是一种“选择性雌激素受体下调剂”(SERD),通过下调肿瘤组织中的ER来抑制雌激素的作用。氟维司群通过与ER结合来抑制其二聚化,并抑制其易位至细胞核,然后ER被降解[17,18]。
在辅助治疗中,多项荟萃分析表明他莫昔芬治疗5年可将前5年内的疾病复发风险降低一半,在停用他莫昔芬的第5~10年中可将疾病复发的风险降低1/3。死亡风险也降低了1/3。在高危女性中,他莫昔芬辅助用药延长至10年的死亡率绝对值进一步降低近3%[19]。与他莫昔芬相比,用芳香化酶*制剂抑**(部分)替代他莫昔芬可将疾病复发风险额外降低30%[20]。在转移性HR+ BC的一线治疗中,芳香化酶*制剂抑**单药治疗可将无进展间隔延长13~16个月[21]。
ET如何影响认知功能?
随着雌激素在认知功能中的作用逐步清晰,雌激素相关的ET疗法可能与认知能力下降有关。目前已发现雌激素在多种生物系统中发挥作用,并对正常的认知功能至关重要。既往研究表明,雌激素会影响健康女性在月经周期、绝经过渡期和更年期的认知能力[22]。而且雌激素在神经可塑性和神经保护方面具有积极作用[23,24]。此外,雌激素可与神经递质相互作用,包括大脑的胆碱能和血清素能系统,它们在认知和情绪过程中发挥着重要作用[25,26]。由于常见的疲劳、失眠和情绪障碍等副作用,ET可能会引起间接的认知障碍[27]。这些副作用可分别对认知功能产生影响,也可相互加强而对认知产生不利影响。
芳香化酶*制剂抑**和他莫昔芬均可穿过血脑屏障[28-30]。考虑到前文描述的药物作用机制(芳香化酶*制剂抑**导致雌激素浓度下降,而他莫昔芬则阻断乳腺组织中的ER),芳香化酶*制剂抑**和他莫昔芬对认知功能产生不同影响似乎合理。此外,芳香化酶*制剂抑**对所有组织都具有抗雌激素作用,而他莫昔芬(根据组织类型)也可能对ER具有刺激作用。大脑区域对两种独特ER(ERα和ERβ)之间的平衡也有所不同,如海马区和颞叶皮质中的ERβ数量多于ERα,而杏仁核和下丘脑中的ERα数量多于ERβ[31]。
内分泌治疗影响认知,我们又了解多少?
几项横断面和前瞻性神经心理学研究探讨了ET对认知功能的影响。尽管多数研究设计不完美且研究结果各不相同,但数据似乎表明内分泌治疗BC患者对认知功能存在不利影响,包括自我报告的认知主诉和测试减值[32,33]。例如Boele等人研究发现,与未患癌症及未接受全身治疗的BC患者相比,使用他莫昔芬的绝经后BC患者言语记忆得分较低,且认知主诉频率较高[34]。
ET影响认知领域较为一致的意见是言语记忆(言语信息编码、存储和检索,如购物清单或报纸文章)。一项荟萃分析表明,基于9项横断面研究,接受ET(他莫昔芬或芳香化酶*制剂抑**)治疗BC患者的言语记忆测试得分低于未接受ET治疗的BC患者和健康对照组[35]。言语记忆与大脑区域广泛表达的ER相关[36]。
几项随机对照试验表明,与芳香化酶*制剂抑**相比,使用他莫昔芬更常出现认知能力的下降。TEAM试验对绝经后BC患者进行了神经心理学测试,发现他莫昔芬组的言语记忆和EF得分低于非癌症对照组[33],但依西美坦组的得分并不低于对照组。IBIS II研究对BC高风险的绝经后妇女进行了神经心理学测试,结果显示阿那曲唑组与对照组的得分相似[37]。此外,在BIG 1-98研究中,使用来曲唑的绝经后患者在治疗第五年的神经心理学测试中得分优于他莫昔芬组[38]。
绝经状态可能在ET影响认知方面发挥了重要作用,然而相关研究数据很少[39]。在TAILORx的一项侧面研究发现,相较于绝经后女性,接受ET治疗的绝经前女性更容易出现认知下降[40]。这可能是由于ET治疗后雌激素水平发生相对较大且突然的变化,因此对绝经前患者的影响可能更强。而另一方面,绝经后患者可能更容易出现认知能力下降,因为年龄越大,患BC的风险越大,认知功能受损也越大。
什么是CDK4/6*制剂抑**?
CDK4/6*制剂抑**最近才应用于BC治疗,主要联合内分泌治疗用于HR+、人表皮生长因子受体2阴性(HER2-)的转移性BC。至2021年,已有3种CDK4/6*制剂抑**(哌柏西利、瑞波西利和阿贝西利)应用于临床[41],其(新)辅助治疗的研究也正在进行。
CDK4/6*制剂抑**可通过抑制CDK4/6-细胞周期蛋白D1信号转导途径来干扰细胞周期。细胞周期分为4个阶段:G1期、S期、G2期和M期。CDK4-6/细胞周期蛋白D1信号转导通路调节G1期向S期的转变。细胞周期蛋白D1与CDK4/6结合,导致视网膜母细胞瘤(Rb)蛋白磷酸化并释放E2转录因子,这些因子激活可调节G1期向S期转变的基因。CDK4/6*制剂抑**通过抑制细胞周期蛋白D和CDK4/6发挥作用,从而阻止转录因子的释放并实现细胞分裂的停滞[42]。研究还表明,CDK4/6*制剂抑**通过增加抗原呈递而直接作用于肿瘤细胞,并通过激活肿瘤微环境中的免疫细胞来激活免疫系统[43]。
多项随机对照试验表明,ET联合CDK4/6*制剂抑**治疗HR+/HER2-转移性BC患者可延长无进展生存期(PFS)并改善患者预后[44-49]。与单独使用ET相比,联合CDK4/6*制剂抑**可显著改善PFS(一线的平均中位PFS为13.6~23.4个月,二线的平均中位PFS为8.9~15.5个月)和生存期(37.3~46.7个月)[50]。
CDK4/6*制剂抑**对认知功能的影响
CDK4/6*制剂抑**似乎会影响认知相关的生物系统。CDK4/6*制剂抑**诱导的细胞分裂停滞会增加细胞因子分泌,已证实与认知障碍和疲劳相关[51-54];疲劳是CDK4/6*制剂抑**常见的副作用,可能对认知功能存在间接的负面影响[54,55]。
CDK4/6*制剂抑**不具有细胞特异性,意味着这些药物不仅可能干扰癌细胞的细胞周期,还可能干扰健康细胞的细胞周期(尤其快速生长的健康细胞,如大脑中的祖细胞)[56]。大脑中的祖细胞在神经发生、新神经元产生方面发挥着重要作用。细胞周期蛋白D似乎也在神经发生中发挥作用,特别是在神经分化过程中[57]。CDK4/6*制剂抑**可抑制细胞周期蛋白D,这可能导致神经发生受损以及随后的认知障碍,例如学习和记忆困难。
在其他非恶性疾病中,尚未观察到泛CDK*制剂抑**对认知的不利影响。非恶性动物模型的临床前研究表明,第一代泛CDK*制剂抑**对认知具有积极作用。在创伤性脑损伤中,发现CDK*制剂抑**(CR8、夫拉平度、罗可维汀和olomoucin)可以通过减少神经损失以及星形胶质细胞和小胶质细胞激活来减轻空间记忆障碍[58,59]。在多发性硬化症和精神分裂症中,CDK*制剂抑**(夫拉平度)已被证明可通过抑制小胶质细胞激活来促进髓鞘再生以减少工作记忆障碍[60]。
CDK4/6*制剂抑**如何影响认知,我们又了解多少?
部分原因是CDK4/6*制剂抑**最近才得到广泛应用,因此CDK4/6*制剂抑**对BC患者的认知影响几乎没有被研究过。最近的2项RCT(哌柏西利PALOMA-3和阿贝西利MONARCH 2)对主观认知进行了分析,表明CDK4/6*制剂抑**对绝经前和绝经后转移性BC患者没有额外影响。在PALOMA-3中,CDK4/6*制剂抑**联合ET组和ET组均报告注意力和记忆力存在下降,但组间没有差异[61]。在MONARCH-2中,联合组报告认知障碍的时间明显晚于ET组[62]。但应谨慎理解这些研究,因为其仅通过欧洲认知量表(2个问题)进行评估,而欧洲癌症治疗研究组织的生活质量问卷为30个问题(EORTC-QLQ-C30)。
结论
尽管还不能得出结论,但越来越多的研究似乎表明ET对绝经前、围绝经期和绝经后BC患者的认知功能存在不良影响,包括自我报告和测试认知等。言语记忆力下降是最常见的现象。ET类型似乎也有一定影响,他莫昔芬可能最为有害。需要研究不同绝经状态下ET对认知的影响,因为绝经前和绝经后的严重程度可能有所不同。
对临床实践的影响
在对内分泌治疗或联合CDK4/6*制剂抑**影响认知功能的理解更深入之前,建议临床实践中考虑它们对BC患者以及其他疾病领域认知功能的潜在有害影响。当患者在日常生活中出现认知问题时,可转诊至临床神经心理学家。临床神经心理学家将分析医学背景,进行神经心理学测试,并使用访谈和各种患者报告结果来确定认知障碍以及认知模式和程度的优势和劣势。这种神经心理学评估对于选择最佳的治疗方案至关重要(针对问题的生物学和/或心理基础治疗)。癌症和认知领域正在积极研究干预认知问题的方法,使用补偿策略和生活方式干预(如运动)进行认知康复的前景广阔[11]。
参考文献
1. Siegel RL, Miller KD, Fuchs HE, Jemal A. Cancer statistics, 2021. CA Cancer J Clin. 2021;71:7–33.
2. Osborne CK, Schiff R. Mechanisms of endocrine resistance in breast cancer. Annu Rev Med. 2011;62:233–247.
3. Wefel JS, Saleeba AK, Buzdar AU, Meyers CAJC. Acute and late onset cognitive dysfunction associated with chemotherapy in women with breast cancer. Cancer. 2010;116:3348–3356.
4. Sleurs C, Madoe A, Lagae L, et al. Genetic modulation of neurocognitive development in cancer patients throughout the lifespan: a systematic review. Neuropsychol Rev. 2019;29:190–219.
5. Kesler SR, Blayney DW. Neurotoxic effects of anthracycline-vs nonanthracycline-based chemotherapy on cognition in breast cancer survivors. JAMA Oncol.2016;2:185–192.
6. Wefel JS, Vidrine DJ, Marani SK, et al. A prospective study of cognitive function in men with non-seminomatous germ cell tumors. Psycho-Oncol. 2014;23:626–633.
7. Collins B, MacKenzie J, Tasca GA, Scherling C, Smith A. Cognitive effects of chemotherapy in breast cancer patients: a dose–response study. Psycho-Oncol.2013;22:1517–1527.
8. Schagen SB, Wefel JS. Chemotherapy-related changes in cognitive functioning. EJC. 2013;11:225 Suppl.
9. Gibson EM, Monje M. Emerging mechanistic underpinnings and therapeutic targets for chemotherapy-related cognitive impairment. Curr Opin Oncol. 2019;31:531–539.
10. Li M, Caeyenberghs K. Longitudinal assessment of chemotherapy-induced changes in brain and cognitive functioning: a systematic review. Neurosci Biobehav Rev. 2018;92:304–317.
11. Wefel JS, Kesler SR, Noll KR, et al. Clinical characteristics, pathophysiology, and management of noncentral nervous system cancer-related cognitive impairment in adults. CA Cancer J Clin. 2015;65:123–138.
12. Pietras RJ, Márquez-Garbán DC. Membrane-associated estrogen receptor signaling pathways in human cancers. Clin Cancer Res. 2007;13:4672–4676.
13. Burstein HJ, Temin S, Anderson H, et al. Adjuvant endocrine therapy for women with hormone receptor–positive breast cancer: American Society of Clinical Oncology clinical practice guideline focused update. J Clin Oncol. 2014;32:2255.
14. Zwart W, de Leeuw R, Rondaij M, Neefjes J, Mancini MA, Michalides RJ. The hinge region of the human estrogen receptor determines functional synergy between AF-1 and AF-2 in the quantitative response to estradiol and tamoxifen. J Cell Sc. 2010;123:1253–1261.
15. Carpenter R, Miller W. Role of aromatase inhibitors in breast cancer. Br J Cancer. 2005;93:S1–S5.
16. Stocco C. Tissue physiology and pathology of aromatase. Steroids. 2012;77:27–35.
17. Gombos A. Selective oestrogen receptor degraders in breast cancer: a review and perspectives. Curr Opin Oncol. 2019;31:424–429.
18. Carlson RW. The history and mechanism of action of fulvestrant. Clin Breast Cancer. 2005;6:S5–S8.
19. Davies C, Pan H, Godwin J, et al. Long-term effects of continuing adjuvant tamoxifen to 10 years versus stopping at 5 years after diagnosis of oestrogen receptor-positive breast cancer: ATLAS, a randomised trial. Lancet. 2013;381:805–816.
20. Early Breast Cancer Trialists’ Collaborative GroupAromatase inhibitors versus tamoxifen in early breast cancer: patient-level meta-analysis of the randomized trials. Lancet. 2015;386:1341–1352.
21. Reinert T, Debiasi M, Bines J, Barrios CH. Trends in progression-free survival (PFS) and time to progression (TTP) over time within first-line aromatase inhibitors trials in hormone receptor-positive advanced breast cancer. Breast Cancer Res Treat. 2018;168:457–465.
22. Luine VN. Estradiol and cognitive function: past, present and future. Horm Behav. 2014;66:602–618.
23. Arevalo M-A, Azcoitia I, Garcia-Segura LM. The neuroprotective actions of oestradiol and oestrogen receptors. Nat Rev Neurosci. 2015;16:17.
24. Fester L, Prange-Kiel J, Jarry H, Rune GM. Estrogen synthesis in the hippocampus. Cell Tissue Res. 2011;345:285.
25. Dumas J, Hancur-Bucci C, Naylor M, Sites C, Newhouse P. Estrogen treatment effects on anticholinergic-induced cognitive dysfunction in normal postmenopausal women. Neuropsychopharmacology. 2006;31:2065–2078.
26. Henderson JA, Bethea CL. Differential effects of ovarian steroids and raloxifeneon serotonin 1A and 2C receptor protein expression in macaques. Endocr J. 2008;33:285–293.
27. Cella D, Fallowfield LJ. Recognition and management of treatment-related side effects for breast cancer patients receiving adjuvant endocrine therapy. Breast Cancer Res Treat. 2008;107:167–180.
28. Ki Ito, Ito T, Okada T, et al. A case of brain metastases from breast cancer that responded to anastrozole monotherapy. Breast. 2009;15:435–437.
29. Kil K-E, Biegon A, Ding Y-S, et al. Synthesis and PET studies of [11C-cyano] letrozole (Femara), an aromatase inhibitor drug. Nucl Med Biol. 2009;36:215–223.
30. Lien EA, Solheim E, Ueland PM. Distribution of tamoxifen and its metabolites in rat and human tissues during steady-state treatment. Cancer Res. 1991;51:4837–4844.
31. Azcoitia I, Yague J, Garcia-Segura LM. Estradiol synthesis within the human brain. J Neurosci. 2011;191:139–147.
32. Ganz PA, Petersen L, Castellon SA, et al. Cognitive function after the initiation of adjuvant endocrine therapy in early-stage breast cancer: an observational cohort study. J Clin Oncol. 2014;32:3559.
33. Schilder CM, Seynaeve C, Beex LV, et al. Effects of tamoxifen and exemestane on cognitive functioning of postmenopausal patients with breast cancer: results from the neuropsychological side study of the tamoxifen and exemestane adjuvant multinational trial. J Clin Oncol. 2010;28:1294–1300.
34. Boele FW, Schilder CM, de Roode M-L, Deijen JB, Schagen SB. Cognitive functioning during long-term tamoxifen treatment in postmenopausal women with breast cancer. Menopause. 2015;22:17–25.
35. Underwood E, Rochon P, Moineddin R, et al. Cognitive sequelae of endocrine therapy in women treated for breast cancer: a meta-analysis. Breast Cancer Res Treat. 2018;168:299–310.
36. Deroo BJ, Korach KS. Estrogen receptors and human disease.. J Clin Investig. 2006;116(3):561–570.
37. Jenkins VA, Ambroisine LM, Atkins L, Cuzick J, Howell A, Fallowfield LJ. Effects of anastrozole on cognitive performance in postmenopausal women: a randomised, double-blind chemoprevention trial (IBIS II). Lancet Oncol. 2008;9:953–961.
38. Phillips K-A, Ribi K, Sun Z, et al. Cognitive function in postmenopausal women receiving adjuvant letrozole or tamoxifen for breast cancer in the BIG 1-98 randomized trial. Breast J. 2010;19:388–395.
39. Ganz PA, Van Dyk K. Cognitive impairment in patients with breast cancer: understanding the impact of chemotherapy and endocrine therapy. J Clin Oncol. 2020;38:1871–1874.
40. LI Wagner, RJ Gray, JA Sparano, et al.Patient-reported cognitive impairment among women with early breast cancer randomly assigned to endocrine therapy alone versus chemoendocrine therapy: results from TAILORx. J Clin Oncol, 38 (2020), pp. 1875-1886
41. De Groot A, Kuijpers C, Kroep J. CDK4/6 inhibition in early and metastatic breast cancer: a review. Cancer Treat Rev. 2017;60:130–138.
42. Hamilton E, Infante JR. Targeting CDK4/6 in patients with cancer. Cancer Treat Rev. 2016;45:129–138.
43. Chaikovsky AC, Sage J. Beyond the cell cycle: enhancing the immune surveillance of tumors via CDK4/6 inhibition. Mol Cancer Res. 2018;16:1454–1457.
44. Finn RS, Crown JP, Lang I, et al. The cyclin-dependent kinase 4/6 inhibitor palbociclib in combination with letrozole versus letrozole alone as first–line treatment of oestrogen receptor-positive, HER2-negative, advanced breast cancer (PALOMA-1/TRIO-18): a randomised phase 2 study. Lancet Oncol. 2015;16:25–35.
45. Finn RS, Martin M, Rugo HS, et al. Palbociclib and letrozole in advanced breast cancer. N Engl J Med. 2016;375:1925–1936.
46. Hortobagyi GN, Stemmer SM, Burris HA, et al. Updated results from MONALEESA-2, a phase III trial of first-line ribociclib plus letrozole versus placebo plus letrozole in hormone receptor-positive, HER2-negative advanced breast cancer. Ann Oncol. 2018;29:1541–1547.
47. Cristofanilli M, Turner NC, Bondarenko I, et al. Fulvestrant plus palbociclib versus fulvestrant plus placebo for treatment of hormone-receptor-positive, HER2-negative metastatic breast cancer that progressed on previous endocrine therapy (PALOMA-3): final analysis of the multicentre, double-blind, phase 3 randomised controlled trial. Lancet Oncol. 2016;17:425–439.
48. Sledge Jr GW, Toi M, Neven P, et al. MONARCH 2: abemaciclib in combination with fulvestrant in women with HR+/HER2− advanced breast cancer who had progressed while receiving endocrine therapy. J Clin Oncol. 2017;35:2875–2884.
49. Slamon DJ, Neven P, Chia S, et al. Phase III randomized study of ribociclib and fulvestrant in hormone receptor-positive, human epidermal growth factor receptor 2-negative advanced breast cancer: MONALEESA-3. J Clin Oncol. 2018;36:2465–2472.
50. Sledge G, Toi M, Neven P, et al. MONARCH 2: overall survival of abemaciclib plus fulvestrant in patients with HR+, HER2-advanced breast cancer. Ann Oncol. 2019;30:v856.
51. Klein ME, Kovatcheva M, Davis LE, Tap WD, Koff A. CDK4/6 inhibitors: the mechanism of action may not be as simple as once thought. Cancer Cell. 2018;34:9–20.
52. Ohtani N, Takahashi A, Mann DJ, Hara E. Cellular senescence: a double-edged sword in the fight against cancer. Exp Dermatol. 2012;21:1–4.
53. Wardill HR, Mander KA, Van Sebille YZ, et al. Cytokine-mediated blood brain barrier disruption as a conduit for cancer/chemotherapy-associated neurotoxicity and cognitive dysfunction. Int J Cancer. 2016;139:2635–2645.
54. Joly F, Lange M, Dos Santos M, Vaz-Luis I, Di Meglio A. Long-term fatigue and cognitive disorders in breast cancer survivors. Cancers. 2019;11:1896.
55. Lasheen S, Shohdy KS, Kassem L, Abdel-Rahman O. Fatigue, alopecia and stomatitis among patients with breast cancer receiving cyclin-dependent kinase 4 and 6 inhibitors: a systematic review and meta-analysis. Expert Rev Anticancer Ther. 2017;17:851–856.
56. Liu D-Z, Ander BP. Cell cycle inhibition without disruption of neurogenesis is a strategy for treatment of aberrant cell cycle diseases: an update. Sci World J. 2012;2012.
57. Urbach A, Witte OW. Divide or commit–revisiting the role of cell cycle regulators in adult hippocampal neurogenesis. Front Cell Dev Biol. 2019;7:55.
58. Skovira JW, Wu J, Matyas JJ, et al. Cell cycle inhibition reduces inflammatory responses, neuronal loss, and cognitive deficits induced by hypobaria exposure following traumatic brain injury. J Neuroinflammation. 2016;13:299.
59. Di Giovanni S, Movsesyan V, Ahmed F, et al. Cell cycle inhibition provides neuroprotection and reduces glial proliferation and scar formation after traumatic brain injury. Proc NatI Acad Sci U S A. 2005;102:8333–8338.
60. Mi G, Gao Y, Liu S, et al. Cyclin-dependent kinase inhibitor flavopiridol promotes remyelination in a cuprizone induced demyelination model. Cell Cycle. 2016;15:2780–2791.
61. Harbeck N, Iyer S, Turner N, et al. Quality of life with palbociclib plus fulvestrant in previously treated hormone receptor-positive, HER2-negative metastatic breast cancer: patient-reported outcomes from the PALOMA-3 trial. Ann Oncol. 2016;27:1047–1054.
62. Kaufman PA, Toi M, Neven P, et al. Health-related quality of life in MONARCH 2: Abemaciclib plus fulvestrant in hormone receptor-positive, HER2-negative advanced breast cancer after endocrine therapy. Oncologist. 2020;25:e243.
审批号: CN-120489
有效期至: 2024-8-21
声明: 本材料由阿斯利康支持,仅供医疗卫生专业人士参考