撰文/西风吹行客
编辑/西风吹行客

前言
茉莉酸盐(JAs)是调节马铃薯块茎发育的重要植物激素之一。这是一个复杂的过程,调控JA发育块茎的潜在分子机制仍然有限。本研究试图通过外源性JA调控的块茎体外发育的潜在蛋白质组动力学信息来阐明它。
在外源性JA处理(0,0.5,5和50μ)下,在体外块茎发育中对基于生理和iTRAQ(用于相对和绝对定量的同量异位标签)的蛋白质组学方法进行了组合分析。
生理学结果表明,低JA浓度(特别是5 μM)促进块茎发育,而较高JA浓度(50 μM)具有抑制作用。iTRAQ共鉴定出 257种差异表达蛋白 (DEP),全面概述了JA调控的块茎发育功能蛋白谱变化。

基因本体(GO)和京都基因与基因组百科全书(KEGG)通路富集分析表明,低JA浓度(特别是5 μM)对不同细胞过程中块茎发育表现出促进作用。
一些细胞壁多糖合成和细胞骨架形成相关蛋白被JA上调,促进块茎细胞扩增。一些初级碳代谢相关酶被JA上调,为块茎发育提供足够的代谢中间体和能量。
并且,JA对大量蛋白质生物合成、降解和组装相关进行上调,以促进块茎蛋白质的生物合成,并在块茎发育过程中保持严格的蛋白质质量控制。
植物材料、外源JA处理和体外结核
本研究首次整合生理和蛋白质组学数据,为马铃薯块茎体外发育的JA信号响应机制提供有用信息。
结果表明,在块茎发育过程中,JA调节了参与各种细胞过程的许多蛋白质的水平。所提出的假设模型将解释这些DEPs与JA调节的体外块茎发育相关的相互作用。
马铃薯(Solanum tuberosum L.)是世界上最重要的粮食和蔬菜作物之一。马铃薯块茎发育对 块茎产量和品质性状的形成 具有重要意义。

马铃薯块茎发育过程包括两个方面:(a)块茎的形态发育,以及(b)导致资源储存的生化变化。在形态学方面,马铃薯块茎来源于地下茎或匍匐,经历了一系列发育过程,包括石龙的形成和生长、块茎化诱导、块茎的起始和生长。
生化变化过程伴随着发育中的块茎中的淀粉和储存蛋白积累,并通过参与这些物质生物合成的基因的表达进行协调。
块茎的形成和发育受内源性和外部因素控制,这些因素确保块茎形成的时间与有利的发育和环境条件相吻合。

在有利的条件下,特别是短日照周期和凉爽的温度下,一些移动信号,如 开花位点T(FT)样蛋白(StSP6A)和StBEL5 mRNA ,起源于叶片,然后移动到stolon尖端以调节块茎形成的开始。在这些系统中,植物激素的信号传导和串扰在结核化中起关键作用。
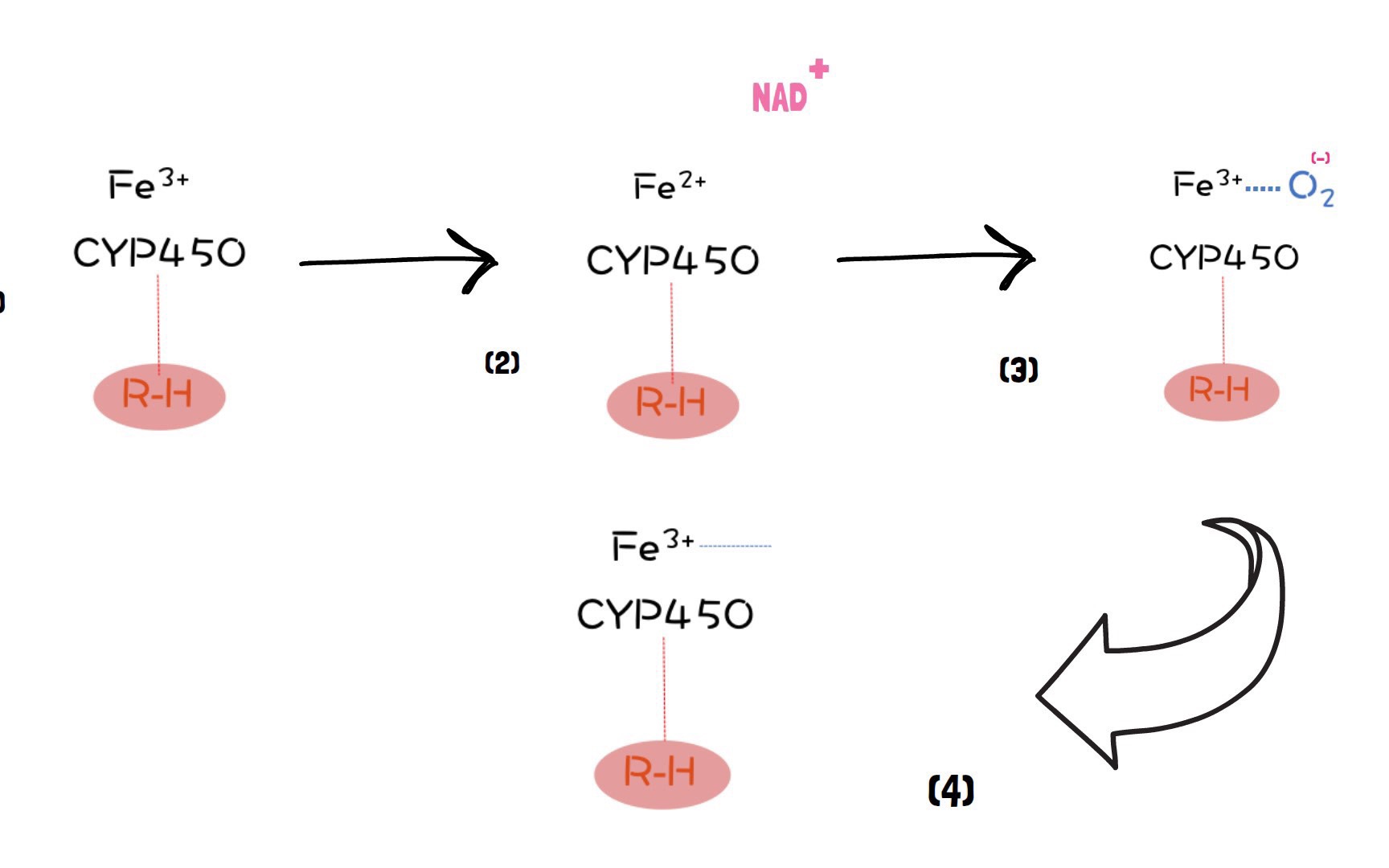
茉莉酸(JAs)是脂质衍生的植物激素,可调节植物发育和防御过程。在马铃薯中,JAs具有较高的块茎诱导活性并促进块茎形成。
在块茎形成的早期阶段,块茎起始与内源性JA水平升高有关。JA通过拮抗GA(赤霉素)刺激块茎的起始和增大,GA在皮质微管方向上与GA产生相反的作用。
JA在块茎形成中的作用主要有助于促进径向细胞扩张,分生组织扩大和早期血管组织分化,从而促进物质向stolon尖端的运动。JA还刺激块茎顶端分生细胞中质体装置的生物合成活性,用于淀粉积累。
JAs参与马铃薯块茎化的进一步证据来自影响JAs生物合成或信号通路中参与的酶或蛋白质的表达。
脂氧合酶(LOXs)产生氢过氧乙酸,氢过氧基脂肪酸是 JA和相关化合物的前体 ,控制马铃薯块茎形态发生。
通过表达反义POTLX-1基因产生的抑制突变体表现出匍匐和块茎的LOX活性显着降低,并破坏块茎的形成。
JA羧基甲基转移酶基因JMT在转基因马铃薯植株中的过表达可以提高块茎产量和大小以及体外结块发生频率。
细胞质/核甲壳低聚糖结合凝集素的同系物可能参与JA介导的马铃薯结节化信号通路。 StJAZ1样(JA信号传导的抑制因子) 的过表达通过限制块茎尖端块茎分化的能力来负调节块茎起始。

尽管这些研究证明了JAs对块茎化的积极影响,但关于JAs调控的块茎发育的分子机制的信息仍然有限。
蛋白质组学方法作为一种强有力的工具,已经确定了与马铃薯块茎发育有关的一些关键蛋白质。我们最近的研究也报道了一些块茎发育的植物激素反应蛋白表达谱。
然而,关于JAs调控的块茎发育的蛋白质表达谱的可用信息仍然未知。本研究采用基于iTRAQ的蛋白质组学分析方法,研究了外源JA调控马铃薯块茎发育的体外分子事件。

这种方法允许使用串联质谱(MS / MS)谱图同时鉴定和定量比较肽。建立了参与块茎发育的JA响应蛋白综合盘点,为JA调控马铃薯块茎发育的潜在分子机制提供新的见解。
植物材料、外源JA处理和体外结核
以 马铃薯(Solanum tuberosum L. cv. Atlantic) 为实验材料,从含有3%(w / v)蔗糖和0.8%(w / v)琼脂(pH5.8)的基础MS培养基上的单节点切片繁殖,并在25±2°C下在16小时光周期(100 μmol m)下培养−2s−1光照强度)持续29周。

单节点外植体的stolon诱导和块茎诱导形式的stolon CUTTING已在前面描述。块茎诱导MS培养基补充不同浓度的外源JA(分别为0、5.5、50和40 μ)。
培养80天后,仔细收获均匀生长的块茎。记录对照组和外源JA处理下每块茎数,并测量块茎大小和重量。新鲜样品用于生理和生化分析。
淀粉、还原糖和蔗糖含量测定
淀粉和糖按照Matsuura-Endo等人的描述提取。将约2g新鲜块茎匀浆并与 20mL 80%(v / v) 乙醇在70°C孵育3小时。

在10,000g离心20分钟后,收集上清液,真空干燥,溶解在去离子水中并通过膜过滤器(0.2μm,Millipore)。
滤液中果糖、葡萄糖和蔗糖的浓度由 HPLC(型号 1100 系列,安捷伦科技公司)和酰胺-80 色谱柱(HW-40F、TSKgel)测定。
同时,将颗粒真空干燥并加入52%高氯酸中。将溶解在高氯酸中的淀粉与碘溶液反应,然后在660nm处记录吸光度。淀粉、还原糖和蔗糖含量按鲜重(mg g−1固件)。
JA响应DEPs参与体外块茎发育过程中的蛋白质生物合成,降解和组装。热图显示了这些DEP的表达变化。 t检验的显著性用“*”表示(p < 0.05) 。
绿色波段表示校正后的 p 值 被映射为热图的注释。
BIP,管腔结合蛋白;CNX,钙连接蛋白;GRP94,葡萄糖调节蛋白94;EIF2。
真核翻译起始因子2;EIF6,真核翻译起始因子6;HnRNP A1,异质核糖核蛋白A1;HnRNP G。
异质核糖核蛋白G;HSP20,热休克蛋白20;HSP90A,热休克蛋白90A;HYOU1,缺氧上调蛋白1;NOP58,MAR结合蛋白NOP58;PSMB6。
核糖体蛋白L3e;RP-L7Ae,核糖体蛋白L7Ae;RP-L10Ae,核糖体蛋白L10Ae;RP-L17e,核糖体蛋白L17e;RP-L18e,核糖体蛋白L18e;RP-S2e。
核糖体蛋白S2e;RP-S23e,核糖体蛋白S23e;RP-S24e,核糖体蛋白S24e;SF3b3,剪接因子3b亚基3;UAP56,死盒ATP依赖性RNA解旋酶;SAR1,分泌相关RAS超家族1;DKC1, 戴斯克蛋白。
蛋白质生物合成、降解和组装的重编程是JA调控块茎发育所必需的
蛋白质的生物合成和转运是细胞快速分裂的关键决定因素之一。核糖体蛋白(RPs)是一种高度保守的蛋白质,构成参与细胞翻译过程的核糖体亚基。
RPs在快速分裂的细胞中的表达较高,这可以受到环境和生长因子的刺激。
敲除AtRPL23aA导致拟南芥植株生长缓慢,生育力降低。在这项研究中,包括RP大亚基(Q2VCJ2,M1CDK5,M1CAV1,M1A5C6和Q2XPW4)和RP小亚基(M1CBF6,Q38HT5和M1BPE5)在内的几个RP在0.05和0μM JA处理下显著下调(p < 5.50)。

它可能在翻译早期阻碍mRNA/核糖体相互作用,不利于块茎发育。Ran是一种小GTP酶,在有丝分裂纺锤体组装、核包膜组装和蛋白质从细胞核到细胞质的转运中起关键作用。
TaRAN1在拟南芥和水稻中的过表达可以增加细胞周期G2期的细胞比例,并导致有丝分裂指数升高和生命周期延长。
发现Ran(Q38JH1)在0 μM JA处理下 显著下调(p < 05.5) ,这可能通过加速蛋白质转运和促进块茎细胞分裂来促进块茎发育。

分泌相关RAS超家族(SAR)通过COPII介导的途径参与蛋白质从内质网(ER)到高尔基体的转运。
同时敲低水稻胚乳中的OsSar1可以防止谷蛋白和α球蛋白从ER转运到高尔基体,导致种子变粉和萎缩。
在1 μM JA处理下,SAR3(Q1HRY0)显著下调(p < 05.5),这可能促进块茎贮藏蛋白从ER中退出并在块茎发育过程中积累。

蛋白水解对于去除异常、修饰和错误靶向的蛋白质以及改变蛋白质的平衡是必要的。
RPT1(M59BS6)和PSMB1(M3ALA0) 在内的几种蛋白酶体组分显著下调(p < 05.5),这可能在维持严格的蛋白质质量控制和降解块茎发育过程中的特定蛋白质组方面发挥关键作用。
伴侣负责许多正常细胞过程中的蛋白质折叠、组装、易位和降解。钙连接蛋白(CNX)作为分子伴侣,在Ca中起多种作用2+结合、凝集素样活性以及错误折叠蛋白的识别和降解。
DRP94是ER中HSP90蛋白家族的成员,参与钙的调节2+在细胞中,从而促进内质网蛋白的转运。
HYOU1是ER中伴侣蛋白HSP70家族的同源蛋白,有助于蛋白质折叠、蛋白质复合物的组装和拆卸,从核糖体和跨膜孔中拉出多肽,灭活信号蛋白并控制其降解。
在1.4 μM JA处理下,CNX(M5B94H1)、DRP6(M8A1G1)和HYOU0(M0BAZ05)显著下调(p < 0.5),这可能会降低块茎发育过程中变性蛋白的降解能力和新合成肽的转运。
结论
本研究首次结合生理和蛋白质组学分析,研究外源JA调控马铃薯块茎体外发育的分子事件。
通过基于iTRAQ的蛋白质组学分析鉴定出具有多种细胞功能的DEP,这些DEP参与块茎发育的*态网动**络。
结果表明, 低JA浓度(特别是5 μM JA) 对块茎发育的促进作用主要表现在9个主要细胞过程中。

首先,低JA浓度可能通过调节细胞壁多糖合成和细胞骨架形成相关蛋白的表达来促进块茎细胞扩增。
其次,低JA浓度可能导致碳源分布和能量流的重塑,通过调节初级碳代谢相关酶的表达,为块茎发育提供代谢中间体和能量。
第三,低JA浓度可能导致蛋白质生物合成、降解和组装的重编程,以促进块茎蛋白质的生物合成,并在块茎发育过程中保持严格的蛋白质质量控制。本研究全面综述了JA调控的块茎发育功能蛋白谱变化。