
【研究背景】
锂硫(Li-S)电池被认为是一种有潜力的替代锂离子电池(LIBs)的技术,具有高能量密度、低毒性和低成本等优势。Li-S电池使用硫(S8)作为阴极材料、金属锂作为阳极材料,能够实现比LIBs更高的能量密度(三倍以上)。然而,传统Li-S电池由于使用金属锂作为阳极存在一些安全问题。为了解决这个问题,可以使用Li2S与无金属锂阳极配对来构建Li-S电池,这可以避免使用锂阳极带来的安全隐患,并具有较高的理论容量和稳定的结构。然而,Li2S的首次充电的活化仍然是一个挑战。已经开发了各种基于Li2S的高级阴极材料解决这个问题。但是这些解决方案都只能在常温下运行,这对于需要在低温下使用的电动汽车来说并不友好。虽然Li-S电池所使用的电解液可以在低温下工作,但是Li2S在低温条件下的电化学活化仍需要进一步的研究。迄今为止,还没有关于在-10°C下成功实现传统Li-S电池中Li2S/S8的电化学完全活化的报道。
【内容简介】
本文介绍了电解液添加剂NH4NO3在Li2S中实现-10°C下电化学活法方面所发挥的关键作用。NH4NO3中的NH4+与Li2S发生强烈相互作用,改变了Li2S的脱锂途径。通过降低Li2S的活化势垒,NH4NO3使得Li2S即使在-10°C的低温条件,也能在*醚乙**类电解液的电化学稳定窗口内有效利用,并且具有良好的容量和循环性能(图1)。

图1.基于Li2S的Li-S全电池在-10°C时含/不含有NH4NO3添加剂的插图。
【主要内容】
由于固相Li2S的绝缘性,提高其导电性是关键问题。采用商用石墨烯和Li2S混合制备复合粉末,并通过球磨工艺制备Li2S/石墨烯复合阴极,可以改善Li2S的脱锂动力学和锂的电化学利用率。复合阴极具有紧凑的二维几何形态和增强的电子网络。采用0.5 M LiTFSI + 0.8 M LiNO3溶于DME: DOL=1:1(v/v)作为基线电解液。在电解液中添加NH4NO3,制备了改性电解液,进一步优化Li-S电池的性能。
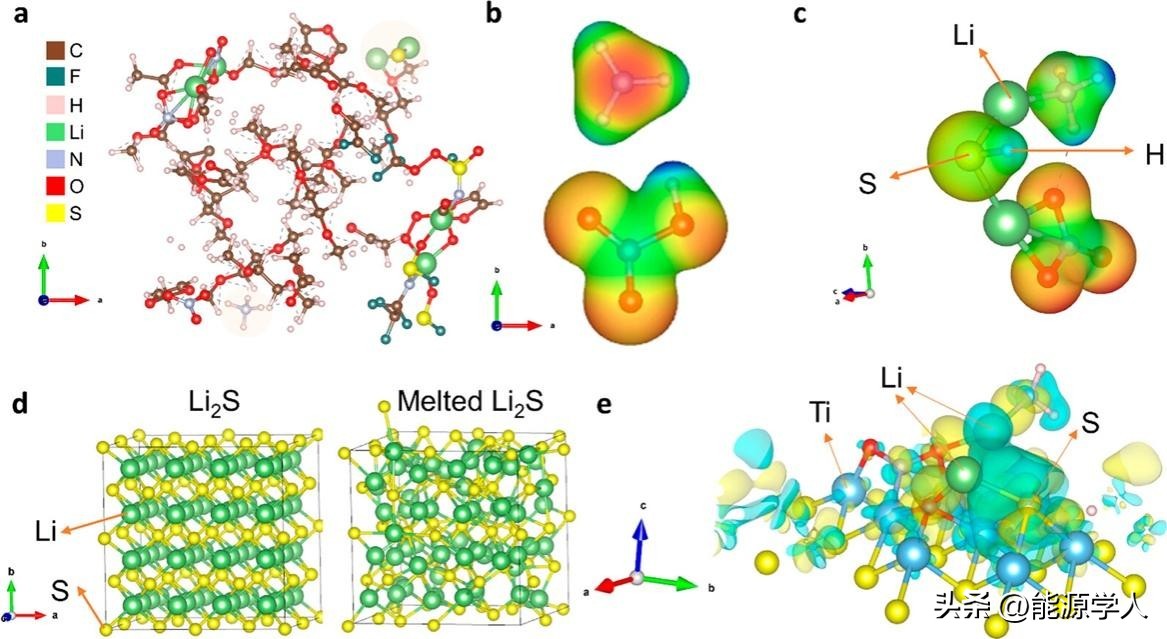
图2.NH4NO3添加剂功能的计算研究。
为深入了解NH4NO3添加剂在Li-S电池中的功能,使用密度泛函理论(DFT)进行了理论研究。通过模拟324个原子进行溶解过程的计算,发现NH4+和Li2S与分子的结合能为-5.44 eV,表明它们在热力学上有利(图2a)。NH4+与周围分子之间的氢键相互作用以及含氧分子与Li+的相互作用促进了溶质和添加剂在溶剂中的溶解趋势。分子静电势(MESP)计算揭示了与分子相互作用相关的有价值信息(图2b)。NO3-阴离子与Li+相互作用,S2-与H+相互作用(图2c)。Li和S之间的相互作用弱于它们各自与周围分子的相互作用,从而促进了Li-S键的断裂,使得Li2S颗粒表面从固相溶解到液相。通过建立晶体模型和熔融模型并进行比较(图2d),发现在存在NH4NO3时,熔融相完成8Li2S→16Li+S8反应所需能量所需能量较低,进一步证明不同的Li2S相对电化学反应有不同的影响。这些理论研究结果为后续的实验结果提供了直接验证的依据。
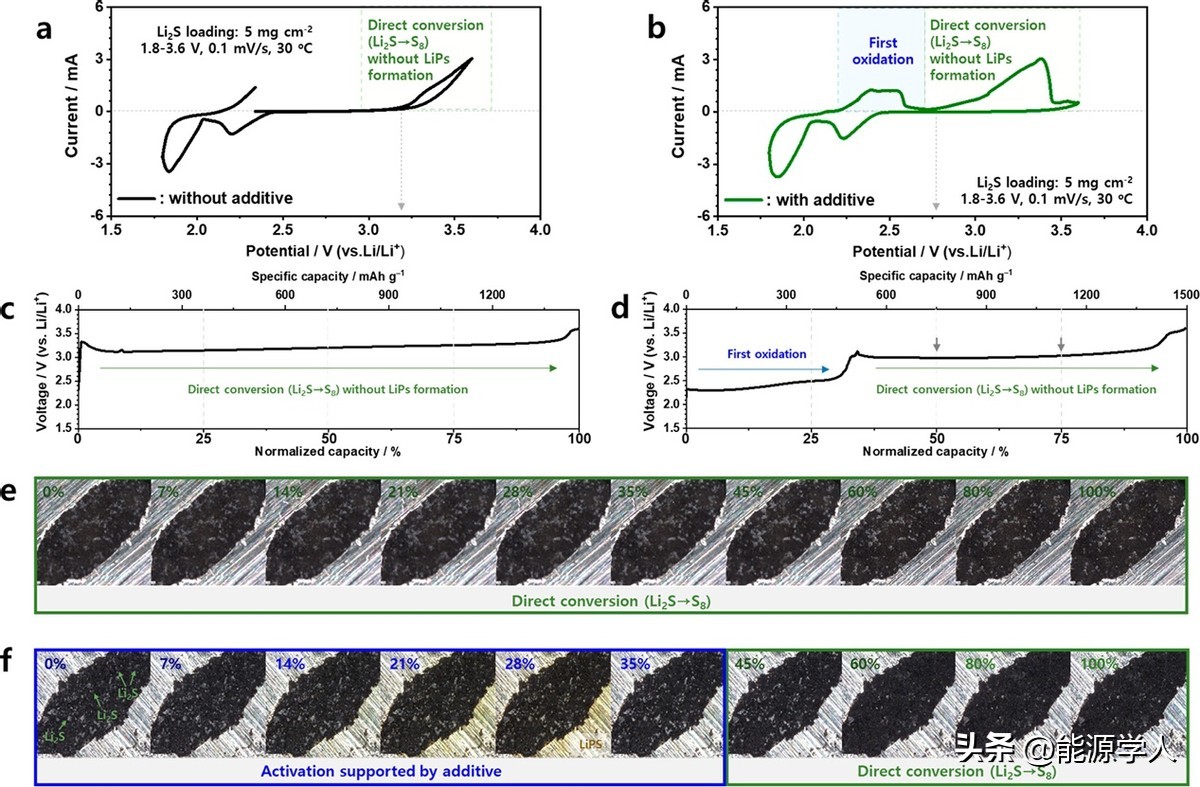
图3.循环伏安法和operando光学显微镜分析电解液中含/不含有NH4NO3添加剂的复合阴极。
为了验证NH4NO3改善电化学性能的功能,使用金属锂为阳极,复合Li2S为阴极,0.5 M LiTFSI + 0.8 M LiNO3(基线)或0.5 M LiTFSI + 0.55 M LiNO3 + 0.25 M NH4NO3溶于DME:DOL = 1:1 (v/v)电解液(改良),组装了Li-S电池。30°C下对Li-S电池进行了首圈的CV测试。基线电解液只能观察到一个氧化峰,对应于Li2S通过直接转化反应脱锂(图3a)。改良电解液在第一次阳极扫描中观察到了两个明显的氧化峰,其中一个峰出现在改良电解液中液相Li2S的化学氧化范围内(图3b)。使用改良电解液的Li-S电池还参与了直接转化反应,但在活化电位上显示出比基线电解液更低的活化(图3c和d)。接下来的阴极扫描显示出典型的硫还原反应(图3a和b中的CV图)。通过Operando光学显微镜(o-OM),确认了NH4NO3添加剂在形成液相Li2S以及在脱锂化过程中触发Li2S/石墨烯复合阴极低电位活化的功能。图3c-f显示了在第一次充电过程中,从o-OM中获得的Li2S/石墨烯复合阴极的电压曲线及照片。通过o-OM观察到在不添加NH4NO3的情况下,复合阴极的初始活化电位较高,并在第一次充电过程中显示出Li2S直接转化为S8的电压平台(图3c)。基线电解液下的复合阴极在脱锂过程中没有形成LiPS(图3e)。使用添加剂后,复合阴极的电压曲线发生了明显变化(图3f)。NH4NO3添加剂产生了较低的OCV电位(约2.2 V),并在第一次充电的早期阶段将复合阴极的活化势垒降至2.5 V以下,触发了两步脱锂。在充电过程至35%阶段(第一步),复合正极中Li2S更容易脱锂和形成LiPS的。液相LiPS在充电约14%时从复合阴极中洗脱出来,然后持续到28%的充电过程(图3f)。最终,液相锂离子逐渐消失,在35%的充电过程后没有观察到可见的液相锂离子。在接下来的的充电过程(第二步),使用添加剂的复合阴极可能表现出Li2S向S8的直接转化反应,这表明液相Li2S暂时形成,并具有催化作用,提高了Li2S的脱锂动力学。此外,与基线电解液相比,使用0.25 M NH4NO3添加剂后,复合阴极中的Li2S颗粒在充电40%后明显消失,表明Li2S对S8的脱锂化反应更好。原位电化学阻抗谱分析也反映了这些观察结果,使用NH4NO3添加剂后,液相Li2S的形成降低了在完全放电状态下的总电阻,改善了高达70% SoC的电荷转移动力学。NH4NO3添加剂刺激了液相Li2S的形成,并改善了Li2S在第一次充电过程中的电荷转移动力学。
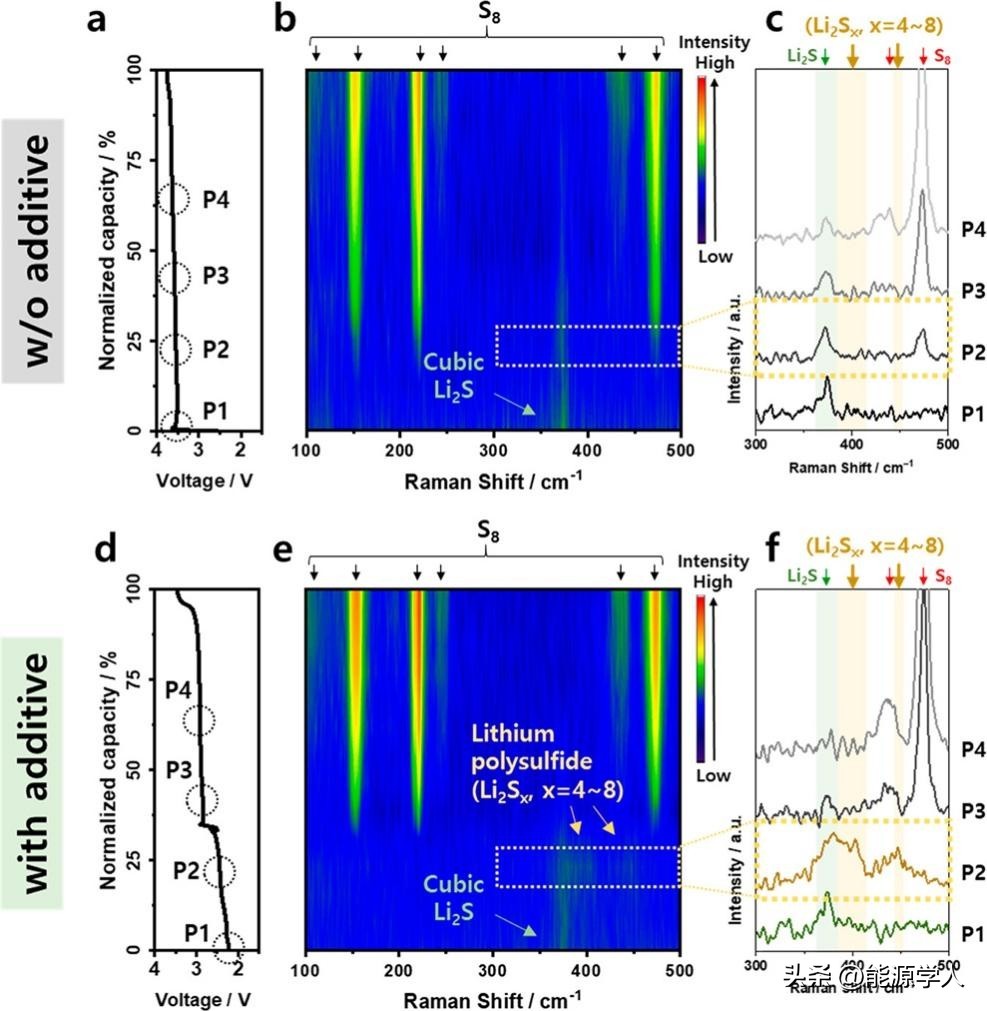
图4.含/不含NH4NO3添加剂的电解液中复合阴极的Operando 拉曼分析。
operando 拉曼光谱 (o-OM)分析详细说明了复合阴极在第一次充电过程中Li2S转化为S8的不同脱锂行为与电解液中是否添加NH4NO3的关系,将得到的拉曼光谱峰强度以等值线图的形式呈现在图4中。在基线电解液中中未观察到可溶性多硫化物Sn2-(n≥4)的特征拉曼光谱表明Li2S直接转化为S8(图4a-c)。充电开始时,在395和448 cm-1处出现了微弱但可分辨的信号,分别对应于S8n-和S42-,并持续到20%的充电过程(图4d-f)。含有NH4NO3添加剂的复合阴极中S8的强度较高,这进一步证明了Li2S/石墨烯复合阴极在使用NH4NO3时具有更好的脱锂动力学。

图5.在含/不含NH4NO3添加剂的电解液中首次充电期间Li2S的形态分析。
通过使用透射电子显微镜(TEM)在室温和低温条件下(30°C和-10°C),研究了在有/无NH4NO3添加剂的Li-S电池中Li2S的形态变化,并在0.1C电流密度下取出Li2S/石墨烯复合阴极进行观察。充电过程停在图6中标记的点上。在基线电解液中充入的Li2S显示为结晶形态,如图5a、c所示。在改良电解液中充入的Li2S在30°C和-10°C时表现出非晶化的表面,如图5b、d和e所示。这些晶体学特征的改变表明Li2S通过与NH4NO3添加剂相互作用并形成无定形LiPS层来脱锂
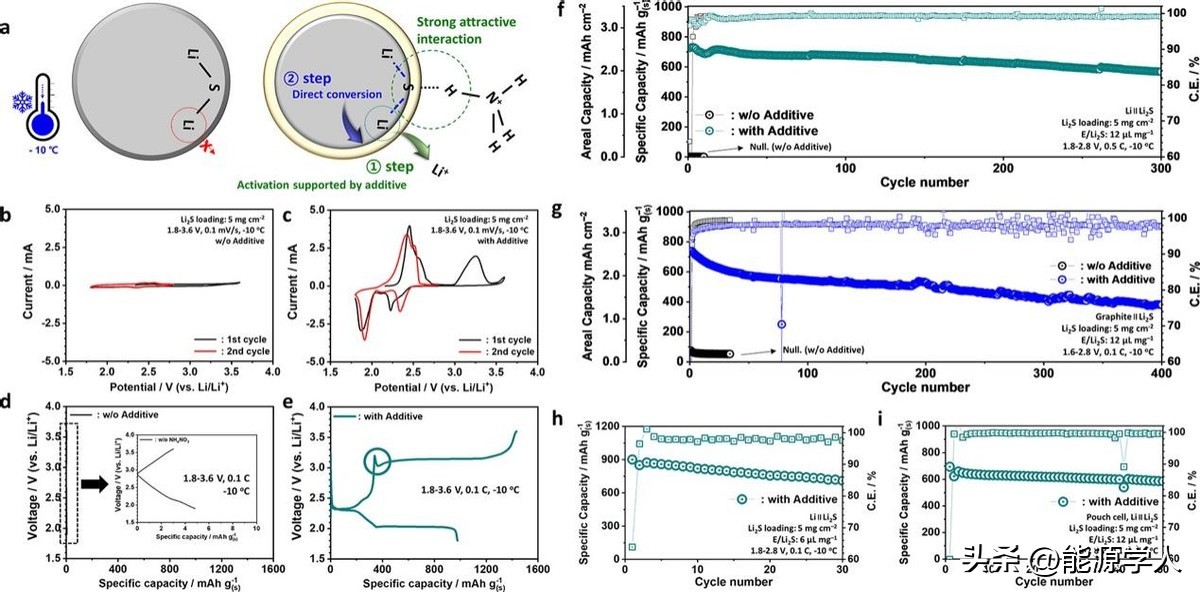
图6.在−10°C下,含/不含NH4NO3添加剂的电解液中的Li2S/石墨烯复合阴极的电化学性能。
通过添加0.25 M NH4NO3的方法,成功改善了Li2S/石墨烯复合正极在-10℃超低温条件下的性能(图6a)。图6比较了带有0.25 M NH4NO3添加剂和不带添加剂的复合阴极在低温(-10℃)下的电化学性能。添加了NH4NO3添加剂的Li2S/石墨烯复合阴极的电化学阻抗谱(EIS)数据显示在-10 ℃的OCV状态下电阻较低,这表明添加剂的化学作用降低了Li2S阴极的电阻值。基线电解液中的复合阴极在最初的两个循环中未观察到氧化/还原峰(图6b)。在含有0.25 M NH4NO3的电解液中,复合阴极显示出较高的电化学活性和明显的氧化/还原峰(图6c)。即使在-10 ℃下,0.25 M NH4NO3添加剂也使Li2S与S8发生了两步脱锂反应。在第一次阴极扫描和第二次阳/阴极扫描中,观察到了硫与Li+的电化学还原/氧化反应。与基线电解液相比,含有0.25 M NH4NO3的电解液中复合阴极在-10 ℃下的充放电电压曲线几乎相同(图6e)。经过NH4NO3电解液活化为S8的Li2S颗粒上,经过25%充电后,其具有较高的放电容量(978 mAh/g),并在0.5 C的电流密度下显示出726 mAh/g的高容量和长期循环稳定性,300个循环后容量保持率为78%(图6f)。尽管在-10 °C下动力学反应缓慢,但使用0.25 M NH4NO3改性电解液的Li2S阴极在稳定电压窗口内被完全活化。复合阴极和石墨阳极构建了Li-S全电池,该电池可以在-10 °C的极低工作温度下存活。在0.1 C的条件下经过400次循环后,放电容量高达736 mAh g-1(图6g)。最后,在贫电解液和-10 °C条件的软包电池中验证了NH4NO3添加剂的实际可行性(图6h和i)。
【结论和展望】
本研究通过引入NH4NO3添加剂到电解液溶液中,成功实现了在-10°C下Li-S全电池的可靠运行。NH4NO3添加剂的引入导致液相Li2S的形成,使得在低温下Li2S容易发生反应。通过这一策略,Li2S/石墨烯复合阴极展现出高能量密度和稳定的循环性能。这是一项突破性的发现,只需少量的NH4NO3添加剂即可完全激活Li-S电池,在极端低温条件下存活,这在之前的研究中尚未报道。这些发现为Li-S电池的实际应用提供了新的启示,使其能够在全球各地的各种温度环境下运行。
Turning on Lithium–Sulfur Full Batteries at −10 °C, Hun Kim, Jang-Yeon Hwang, Young-Geun Ham, Ha-Neul Choi, Muhammad Hilmy Alfaruqi, Jaekook Kim, Chong Seung Yoon, and Yang-Kook Sun, ACS Nano Article ASAP, DOI: 10.1021/acsnano.3c04213
https://pubs.acs.org/doi/full/10.1021/acsnano.3c04213