最近写啥来说,昨天的文章CLDN18.2单抗胃癌率先撞线,ADC/双抗紧随,胰腺癌在望相较于今天的重磅新闻,极其应景。但对于我这种悲观主义者来说。面临被收购阴云笼罩的AZ,在Biotech行业整体低迷行情下的康诺亚,在后PD-1时代最具成功可能的CLDN18.2靶点上进行ADC的合作,有诸多不确定性。但也有合理性,毕竟AZ错失了ICBs赛道红利,全力押注ADC赛道,DS-8201的强效结果更是让罗氏退避三舍,CLDN18.2 单抗已获成功,吸取ICBs错失先机的教训,提前布局CLDN18.2 ADC 也是合情合理。但11.88亿美元的BD,绝对还是玩的国内Biotech企业炒作的戏码。但对于这一点,我心态也发生了变化,创新药的研发需要社会资本的介入,对于韭菜们,我不能同情心泛滥。命运早已注定,沉浮滚打都是自己决定的,我就关注我在意的目标赛道的近况好了。
——快 讯——
2月23日,康诺亚欣然宣布该公司非全资附属公司KYM Biosciences(康诺亚拥有70%权益)与AstraZeneca AB(阿斯利康)已订立全球独家许可协议,以开发及商业化CMG901。

AstraZeneca将获得CMG901的研究、开发、注册、生产及商业化的独家全球许可,并根据许可协议负责与其进一步开发及商业化相关的所有成本及活动。
KYM Biosciences将收取6300万美元的预付款,并在达成若干开发、监管及商业里程碑后,收取最多11.25亿美元的额外潜在付款。KYM亦有权从AstraZeneca收取销售净额的分级特许权使用费。KYM有责任提供协助和人员以促进技术及专业知识转让。除另有协定外,AstraZeneca将负责承担与就CMG901正在进行的实验有关的开发及监管事务活动的所有费用。
——Claudin 18.2 靶点研发加速内卷——
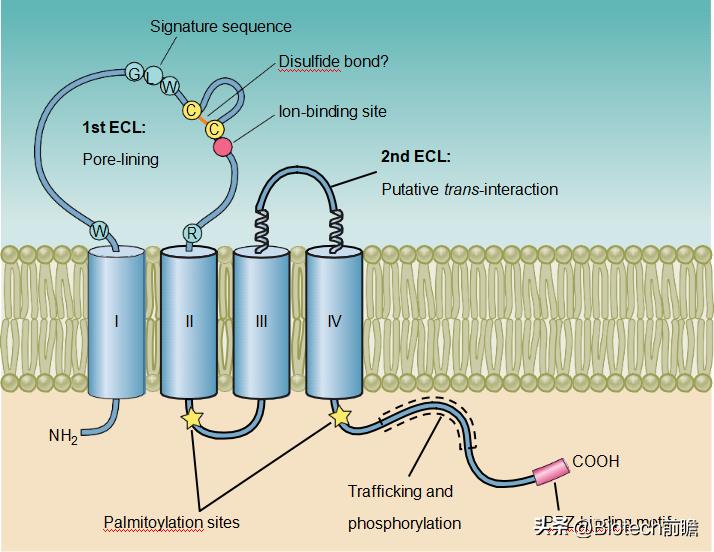
Claudin 蛋白结构
在介绍Claudin 18.2(CLDN 18.2)靶点前,首先得介绍Claudins,Claudins是一类存在于上皮和内皮紧密连接中的整合素膜蛋白,最早由Shoichiro Tsukita等于1998年发现。Claudins蛋白家族共有24个成员,具有4个跨膜结构域。其中,NH2端和COOH端位于胞内,具有两个胞外环。这种结构使得Claudins紧密蛋白家族能够有效维持上皮细胞和内皮细胞的极性,从而有效调控细胞旁通透性和电导。
有研究表明,Claudin蛋白表达的改变会导致紧密连接功能受损,影响信号传导途径,并在某些上皮癌中起到促肿瘤作用。正常组织由于细胞间紧密粘连, 抗体药物极难与其结合。然而, 癌细胞组织间隙的松散结构却使CLDN18.2暴露于蛋白类大分子药物下变成可能, 因此CLDN18.2是一个理想的新一代抗肿瘤治疗靶点。此外,不同的Claudin蛋白在正常组织中的表达谱也有差异。 以胃癌为例,Claudin 18.2特异地表达在分化的胃黏膜上皮细胞,但在胃干细胞区不表达。虽然基于HER2的胃癌靶向药物已获批多款,但胃癌患者的HER2阳性突变率很低,大约只有10%~20%。而Claudin 18.2在所有胃癌患者中的阳性率可以达到近60%,具有更广泛的患者获益可能。所以,Claudin 18.2靶点竞争激烈,是有原因的。
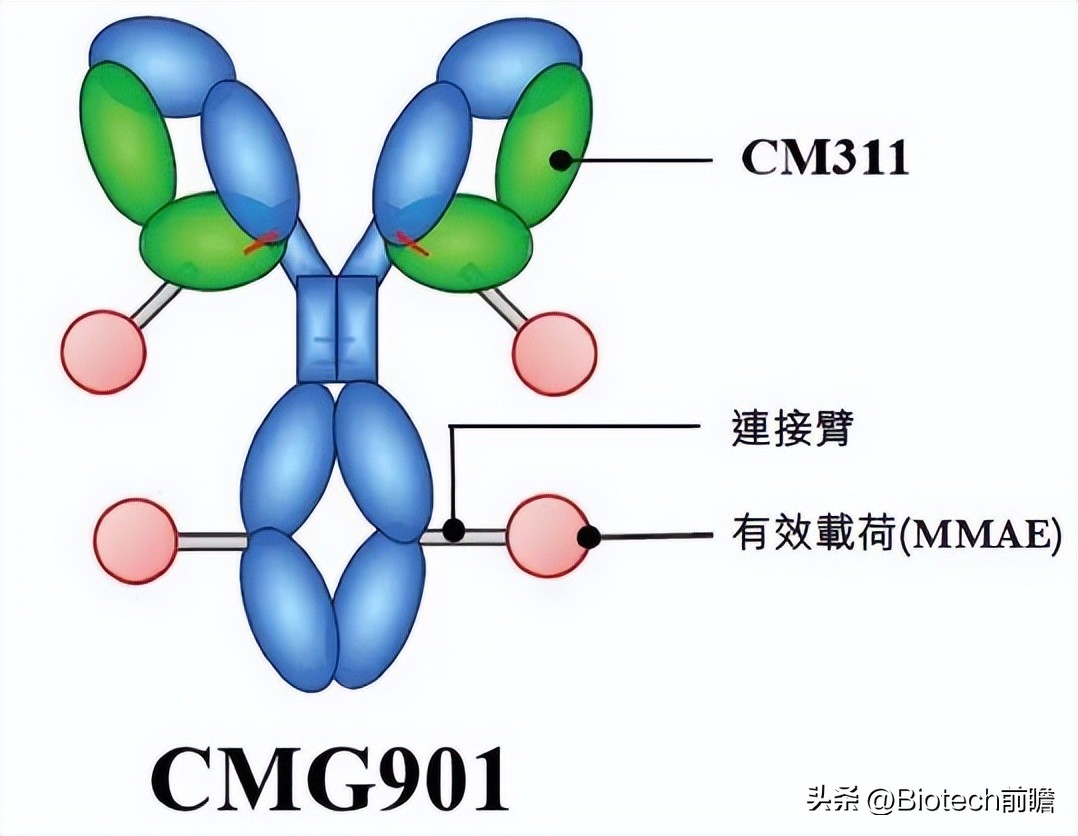
2021年7月8日,专注于自免及肿瘤疾病领域的Biotech企业—康诺亚生物,正式在港交所上市。研发管线中的CMG901,为为全球首个Claudin 18.2 ADC药物,由康诺亚与乐普生物旗下美雅珂联合研发。
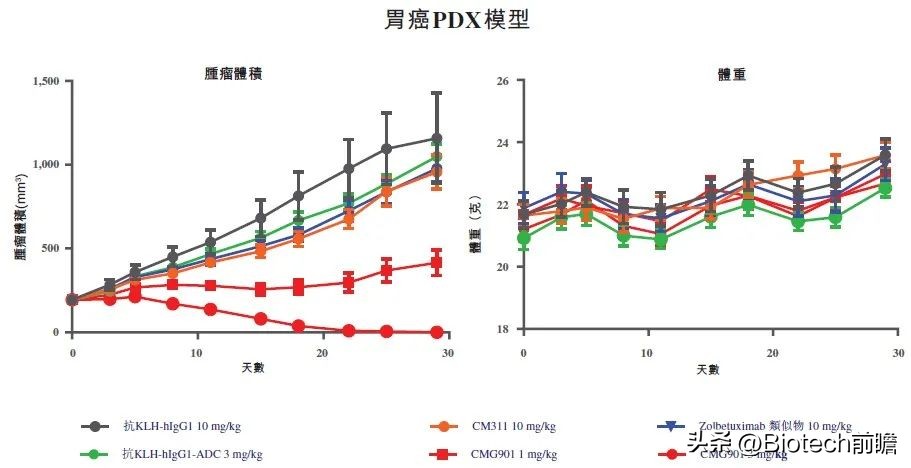
小鼠胃癌PDX模型研究中,CMG901表现出远远优于Claudin 18.2抗体的抗肿瘤活性。
下表汇总了目前为止Claudin 18.2在研项目信息:
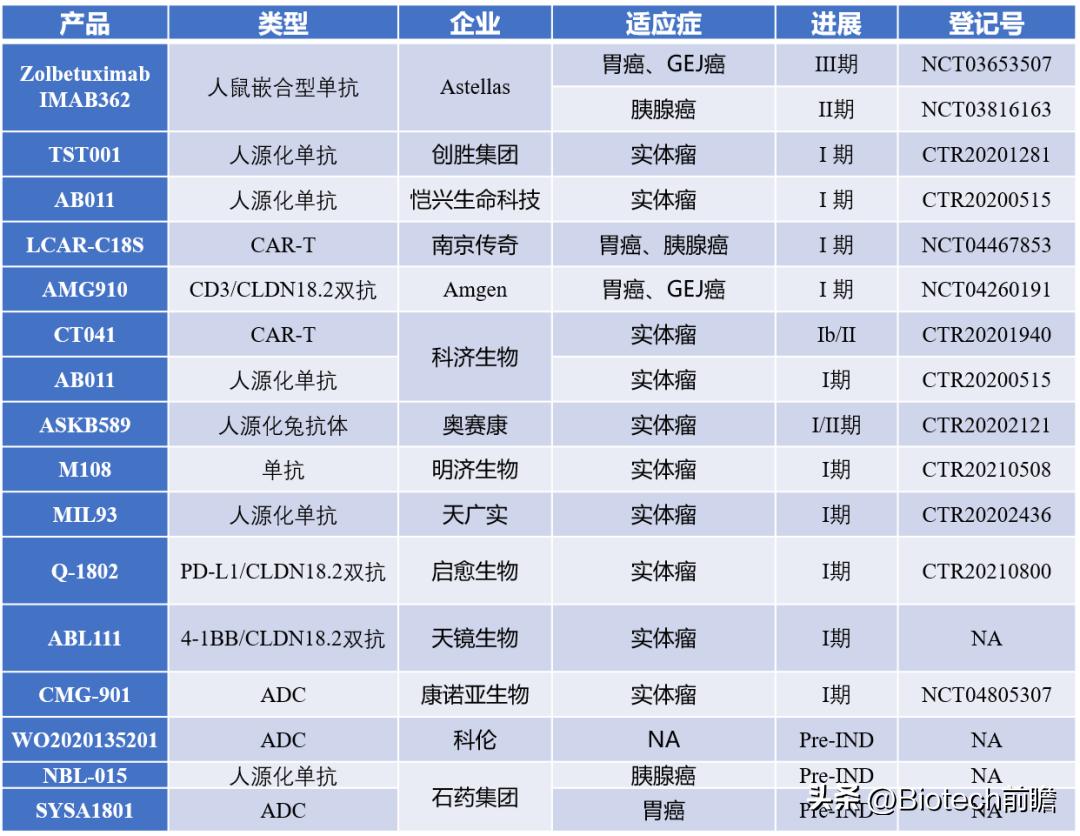
资料来源:ClinicalTrials,CDE,各公司官网
——你所不知的ADC研发坎坷——
对于抗体偶联药物(ADC)研发的难度,深有体会,毕竟差点没毕业的重要原因就是各个难点太难了。印象中,三次全合成20步反应,关关通过,总在最后一步功亏一篑,一度抑郁到对实验室有无名的恐惧感,而这才是ADC linker中最基础需要打通的一关,还有抗体、payload等三元素的搭配和连接,都是难关。但在资本助推和部分实体瘤领域迎来重磅ADC产品,毫无疑问,ADC成为近年来肿瘤治疗的热门赛道。
也有必要将既往对于ADC领域的研发难点向有志于在此领域学有所长的人以启示,毕竟创新药的投资,没相关知识储备,是不行的。
ADC通常由单克隆抗体(mAb)通过化学合成的连接子(linker)与细胞毒*药性**物(payload)共价连接。ADC结合了高度特异性靶向能力和高效*伤杀**作用的优点,实现了对癌细胞的精确高效清除。
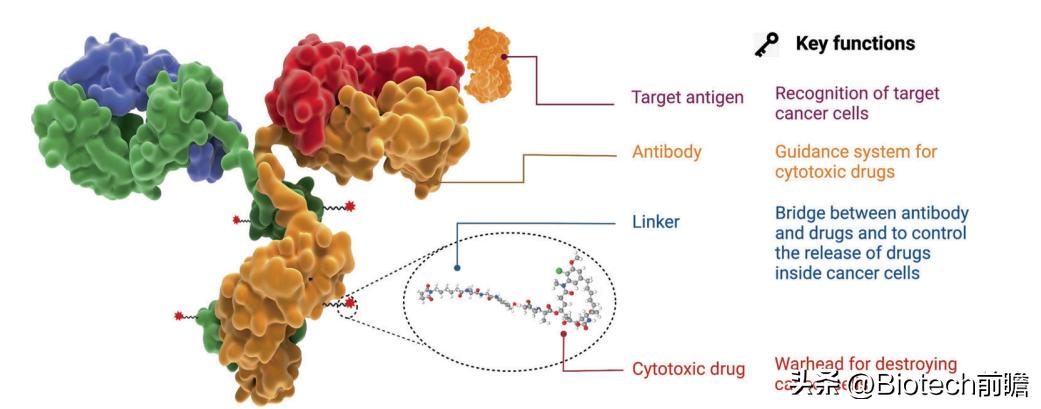
ADC药物的结构和特性
自2000年FDA批准第一款ADC产品Mylotarg®(gemtuzumab ozogamicin)以来,截至2021年12月,全球共有14种ADC获得市场批准用于血液系统恶性肿瘤和实体瘤,此外,目前还有100多个ADC候选产品处于临床试验的不同阶段。
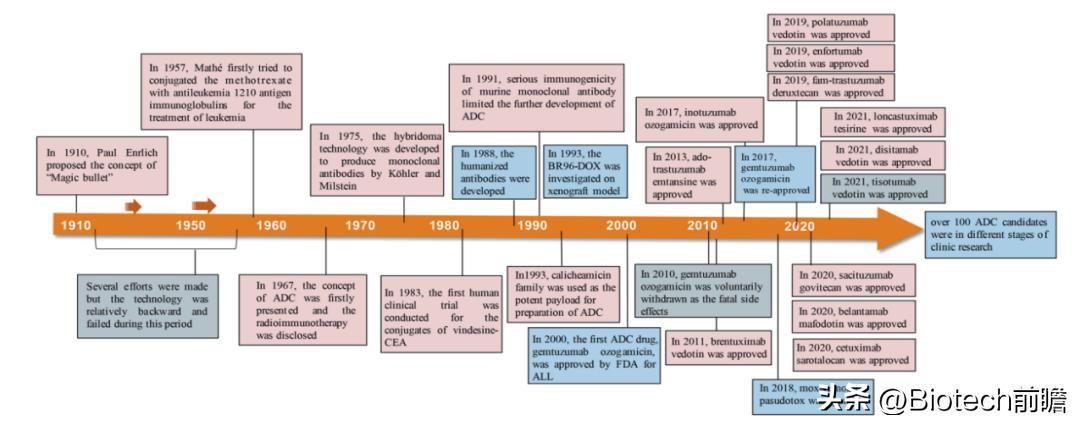
ADC药物开发和批准过程中的重要事件
但创新肿瘤产品的研发之路并非是一路坦途,ADC赛道亦如此。
针对ADC中的抗原选择,抗体选择,linker、payload等的选择,在ADC技术报告:下一代ADC发展前景预测 一文中有详细梳理,本文主要探索未来发展方向。
ADC的潜在发展方向
随着共轭技术的不断优化,抗体工程技术的进步,更多的靶向于其他靶点的ADC产品正在临床探索中。如Trop2 ADC、Claudin18.2 ADC;其中,PD-L1 ADC也有不少企业在探索中。
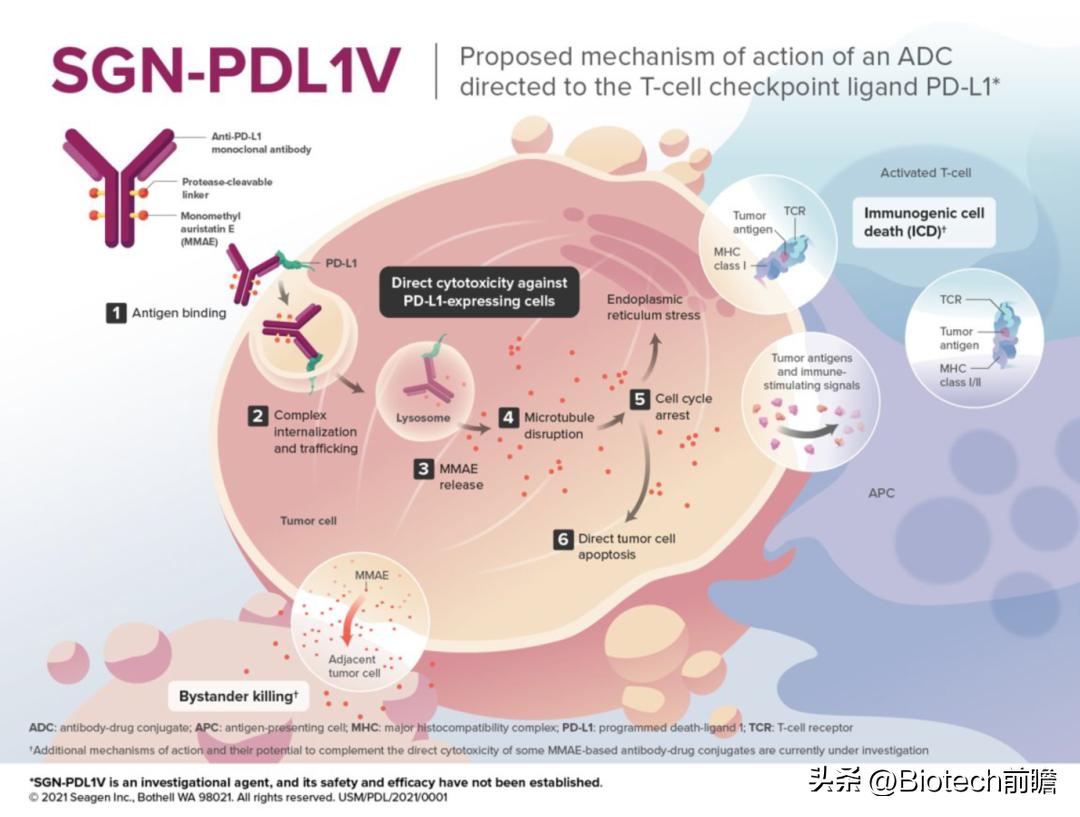
SGN-PDL1V 作用机制(来源:2021SITC)
例如,Seagen管线中处于研发早期阶段的SGN-PDL1V,靶向PD-L1的新型ADC产品, Payload采用的是MMAE, MMAE(一甲基澳瑞他汀E)是ADC使用最广泛的有效载荷,约占总数的30%,主要通过抑制微管蛋白聚合而起到有效的有丝分裂抑制作用。
ADC在肿瘤组织中显示>100倍的药物浓度,大大扩大了细胞毒素的治疗窗口,能够有效减少全身化疗导致的毒副反应,从而有效实现ADC与其他肿瘤治疗手段的连用探索。
其次,SGN-PDL1V的连接子为蛋白酶可切割型。抗体为全人源的抗PD-L1单克隆抗体(Seagen PD-L1单抗)。Seagen PD-L1单克隆抗体利用人类IgG1-Fc骨架,经过工程化改造,消除了Fc段的效应器功能,包括补体依赖性细胞毒性(CDC)、抗体依赖性细胞毒性(ADCC)和抗体依赖性细胞吞噬作用(ADCP)。
另外,鉴于单靶点抗体往往具有高耐药率,双靶点双抗作为ADC的抗体也有企业在探索中。
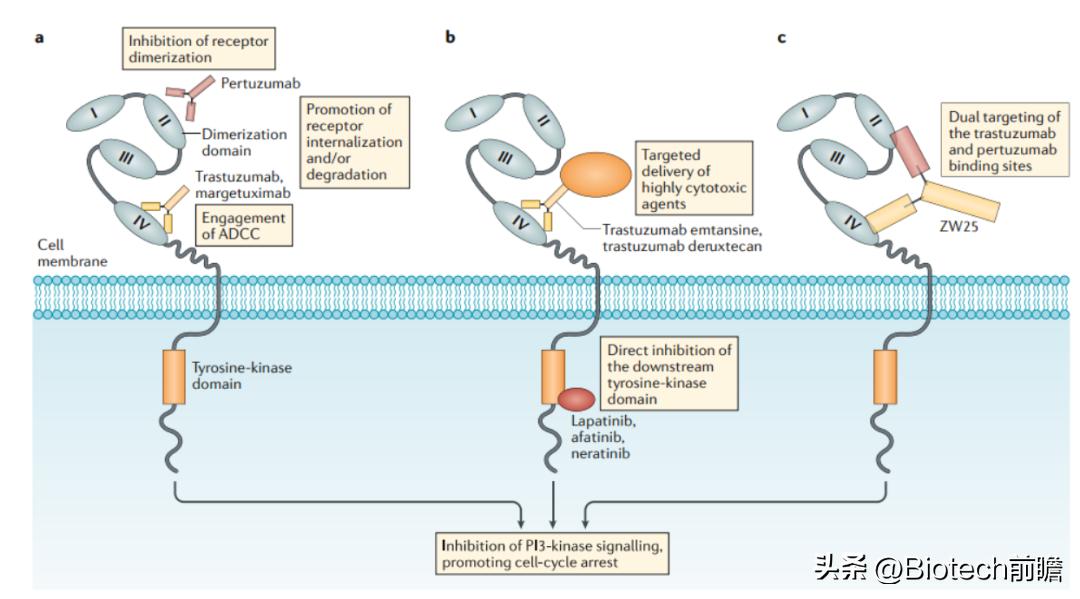
靶向HER2的药物的作用机制
该领域目前研究尚处于早期探索阶段,进展最快的是ZW-49,是Zymeworks利用其专有的Azymetric™ Bispecifics和ZymeLink™ ADCs平台共同开发得到的双特异性抗体ADC药物。能够同时特异性结合HER2受体的两个非重叠表位,即帕妥珠单抗结合位点和曲妥珠单抗结合位点。以期在临床应用中,对于曲妥珠单抗、帕妥珠单抗,甚至TDM-1等新型ADC药物耐药的患者,起到良好治疗效果。
期待未来有更多新型ADC不断商业化上市,惠及更广泛的实体瘤和血液肿瘤领域的患者。
参考资料
1. Signal Transduction and Targeted Therapy (2022) 7:93
2. Bioorg Chem. 2021 Nov;116:105366.
3. Oh DY, et al. Nat Rev Clin Oncol. 2019;10.1038/s41571-019-0268-3.
4. Mark D. Pegram, et al. Mol Cancer Ther; 20(8) August 2021.