强强联合,一周内多家制药公司合资入华,是行业传说中的“狼”来了吗?
一起来了解一下:
2019年7月16日,印度制药巨头“西普拉”已合资入华!
7月16日,印度制药巨头西普拉(Cipla)欧洲分公司 CiplaEU 宣布,将和江苏创诺制药有限公司成立合资公司,作为西普拉在华的分公司。而其主要的业务领域也不无意外的,是西普拉所最擅长的呼吸领域产品。按照协议,双方共同投资3000万美元,其中西普拉欧洲分公司持股80%,江苏创诺制药持股20%。
2019年7月19日,韩国巨头生物合资入华!
7月19日,韩国生物仿制药巨头赛尔群(Celltrion)昨天宣布,其香港分公司将与总部位于香港的南丰集团合作,在上海成立合资公司鼎赛医药(Vcell Healthcare),专注在中国开发、生产及商业化单克隆抗体生物类似药。
2019年7月29日,四环医药联合印度Strides成立合资公司!
7月29日,四环医药宣布,公司全资子公司耀忠国际已与印度Strides Limited全资子公司Strides新加坡子公司成立合资公司。合资公司将主要从事药品的注册申报及销售业务,分别由耀忠国际及Strides新加坡子公司各占51%及49%股权。Strides Limited将会向合资公司授权该等产品,并可选择随后扩大产品组合。Strides Limited将通过其在印度和新加坡的制造工厂向合资公司供应该等产品。
2019年7月30日,辉瑞普强和印度迈蓝合并开创“仿制药帝国”!
7月30日讯,全球最大药企辉瑞与最大仿制药企迈兰(Mylan)联合宣布达成最终协议,将辉瑞的非专利品牌和成熟药品业务部门普强和迈兰合并,建立一个新的跨国制药企业。辉瑞和迈兰的董事会已经一致批准了这项交易,辉瑞股东将持有合并后新公司57%的股份,迈兰股东持有合并后新公司43%的股份。辉瑞普强将把立普妥(阿托伐他汀钙)、西乐葆(塞来昔布)和伟哥(西地那非)等知名品牌带入新公司。预计这家新公司将在2020年收入达到190~200亿美元。新公司将重新命名,在美国特拉华州注册成立,并将在宾夕法尼亚州匹茨堡、中国上海和印度海德拉巴建立全球运营中心。
“4+7集中采购”或可让优秀仿制药,涌入中国市场
2018年开始,国家出台一系列的药监新政改革,为进口仿制药进入中国创造了越来越有利的条件。4月,国务院办公厅印发《关于改革完善仿制药供应保障及使用政策的意见》,明确提出完善支持政策,促进仿制药替代,推动仿制药产业国际化,鼓励境外企业在我国建立研发中心和生产基地。5月,国家药监局、卫健委发布《关于优化药品注册审评审批有关事宜的公告》,进一步优化了对于罕见病药、急需药进口审批制度,大大缩短其在国内上市时间。5月1日,国内进口抗癌药开始实施零关税,同时,对部分药品则降至3%的费率征收进口环节增值税。7月,国家药监局发布《接受药品境外临床试验数据的技术指导原则》,境外完成的仿制药生物等效性试验数据,研究质量好,具备真实性、完整性、准确性和可溯源性的,也可用于在我国的注册申请。
从去年连续出来的政策来看,国家政策对进口药物注册标准正逐步放开,审批流程逐步简化,国外的优质药品进入中国将越发变得更加便捷。加之关税的减、免,未来大批进口仿制药涌入中国市场也不足为怪。
随着第一批“4+7”带量采购的中选品种公布,是否通过一致性评价已经成为仿制药参加带量采购的准入门槛。为了获得参与带量采购竞标的资格,将会有更多的进口仿制药参与一致性评价。
对于进口仿制药来说,想快速抢占中国市场最好的途径之一或可以是参加国家集中采购。
进口仿制药冲击,中国药企面临压力与机遇并存

有专业人士分析,面对竞争,中国仿制药压力与机遇并存,不仅需要注重自身提高“专业战斗力”,更需要有清晰的洞察和远见,合理布局品种管线非常重要。
相比于国内仿制药,印度仿制药在价格和监管体系方面拥有其自身的优势。
在价格方面,印度的人力成本、时间成本、固定资产投资等成本均比中国低,从而导致在印度生产的药品,整体成本比中国低,售价就势必会比中国低。就拿印度全球药房来举例,印度全球药房是印度本土的一家药店,借助移动互联网时代,开启了跨境电商,打通了和中国、美国等发达国家之间的买药鸿沟,以在线的形式把印度低廉的仿制药销售给中国、美国等患者。让中国没有医保或者是支付不起医保的患者可以足不出户从印度全球药房商城上就能购买到物美价廉的印度药房直邮的仿制药。
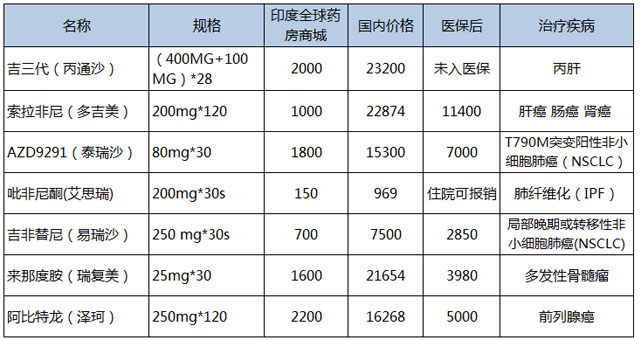
当然,在中国可能就没法做到如此低的价格,如果印度药企和中国药企合资,那么所销售的药品价格势必会高于印度本土药房的价格。因为其中会涉及到相关手续、税等等。
其次,在监管方面,由于长期出口欧美市场,印度的监管体系也更加国际化和高效。据资料显示,印度自行研制的药物有110 项得到美国FDA的批准,欧盟批准有75 项,南非等其他非洲国家有100 项。印度是除美国以外拥有经美国FDA 批准的工厂数量最多的国家。
在中国,从目前政府部门近来对推动仿制药产业发展的一系列动作来看,“提质”与“降价”是贯穿其中的关键词。“质优价廉”是长久以来政府对仿制药提出的标准, 在此环境下,若印度及来自其他国家的“仿制药高手”大批进入中国市场,将会对国内仿制药生产企业带来一定的压力。
虽然要面临巨大的产业发展压力,但从另外一方面看,一旦放开印度仿制药进入中国市场,将带动国产仿制药产业质量的整个提升,同时进一步加速原研药及国产仿制药的降价。
此外,也有专业人士向药谷君透露,由于印度、韩国、日本等国外进口仿制药企对中国市场环境缺乏较深入的了解,进入中国后想要与原研药企和本土企业展开正面竞争,还需要营销推广等多个维度的配合,才能在大变迁中成为最后赢家。这对国内药品代理商来说,或许带来了新的市场机遇。
这样一来,国内代理商如何提前进行品种布局就显得更加迫在眉睫。
从国家用药结构来看,目前国内市场进口仿制药较少,因此,在国内部分危重疾病、罕见病等原研药缺失的用药领域,进口仿制药更有可能被加快引进。
参考目前进口仿制药在国内的申报和过评情况来看,治疗癌症、乙肝、肿瘤、阿尔兹海默症、帕金森病、静脉血栓等病的药物。相对其他药物,这些药国内仿制厂家较少、价格比原研药更便宜、利润空间更大、行业集中度较高,这些品种极有可能成为进口仿制药入华的先遣部队。
文章来源文献:http://www.yddrug.com/