来 源:司晓菲,孙昱,李艳杰,葛妍秀,姜典卓.哌甲酯类药品治疗注意缺陷多动障碍药学研究的一般考虑 [J]. 药物评价研究, 2022, 45(4): 611-617 .
注意缺陷多动障碍(attention deficit hyperactivity disorder,ADHD)是一种常见的神经发育性障碍,主要特征为与发育水平不相称的注意缺陷和(或)多动冲动,多发病于童年期,在世界范围内儿童发病率达7%。作为一种常见的儿童精神障碍疾病,患者通常存在一种及以上共患病,严重影响患者的学习、家庭和社会生活,并带来沉重的负担。针对ADHD的治疗包括药物治疗和非药物治疗,近年来也出现了神经疗法等研究方法,目前通常采用药物治疗为主的治疗模式。但是临床治疗药物非常有限,主要为中枢兴奋剂和非中枢兴奋剂,常见的中枢兴奋剂包括盐酸哌甲酯类、安非他明类、匹莫林等,非中枢兴奋剂中代表*药性**物包括选择性去甲肾上腺素再摄取*制剂抑**(如托莫西汀)和α2肾上腺素能受体激动剂(如可乐定、胍法辛)等。
近年来国内监管部门探索完善儿童用药的全生命周期管理,陆续出台了多项儿童用药的相关法规和指导原则。2019年8月,新修订的《药品管理法》明确规定:国家采取有效措施,鼓励儿童用药的研制和创新,支持开发符合儿童生理特征的儿童用药新品种、剂型和规格,对儿童用药予以优先审评审批。2021年6月1日,国家药品监督管理局药品审评中心在官方网站开通了“儿童用药专栏”,将儿童用药相关政策法规、指导原则和培训资料等予以集中公开,开通儿童用药审评审批绿色通道,提高审评审批效率。
目前我国儿童药研发仍处于早期阶段,ADHD治疗药物的监管仍在不断完善。近年来上市了各种剂型的哌甲酯类药品,剂型包括普通片、口服溶液、缓释片、缓释胶囊、咀嚼片、透皮贴剂等。本文主要介绍美国、欧洲和日本、中国上市的哌甲酯类药品。
1 美国
哌甲酯类是应用最广泛的一线用药,针对哌甲酯类药物,美国食品药品管理局(FDA)已批准多种制剂上市,剂型包括普通片、口服溶液、缓释片、缓释胶囊、咀嚼片、透皮贴剂等,各种制剂较为丰富,供医务人员和患者选择使用的空间较大。
口服速释片剂通常1日给药2~3次,通常最后1次给药时间是在下午。口服液体制剂则更有利于不方便吞咽完整药片的儿童使用。2021年FDA批准了复方速释制剂(商品名AZSTARYS),该胶囊中盐酸右哌甲酯和氯化羟甲基哌甲酯2种药物物质的量比为3∶7。对于调释制剂,1日给药1次的调释制剂包括缓释片CONCERTA、缓释胶囊METADATE CD、RITALIN LA和FOCALIN XR等,但是不同调释制剂的释药机制可能明显不同,药动学数据中的血药浓度达峰时间和药时曲线下面积(AUC)存在不同。
目前上市的缓释胶囊品种较多,例如METADATE CD胶囊中含30%速释微丸和70%迟释微丸。RITALIN LA和FOCALIN XR均采用口服小丸药物吸收系统(spheroidal oral drug absorption system,SODASTM)技术,硬胶囊中速释微丸和肠溶包衣的迟释微丸各占1/2,速释微丸可以口服后迅速释放,缓释微丸在口服几小时后开始释放(约5 h后释药),人体药动学显示为双峰释放(bimodal release),同时具有速释和迟释的效果,且可以有效减少峰谷血药浓度波动。另外,也上市了体外给药的透皮贴剂(商品名DAYTRANA),其FDA说明书显示此贴剂包括3层,为背衬层、含药物的压敏胶和保护层,通常在早上使用,在起效时间前2 h贴于臀部,并在使用9 h后移除,应严格按照说明书的使用方法使用。
笔者将1955—2019年FDA批准上市的部分哌甲酯类药品的活性成分、剂型、商品名、参比制剂(RLD)或对照标准制剂(RS)编码、特殊给药方式、用法用量等内容归纳出来,见表1。
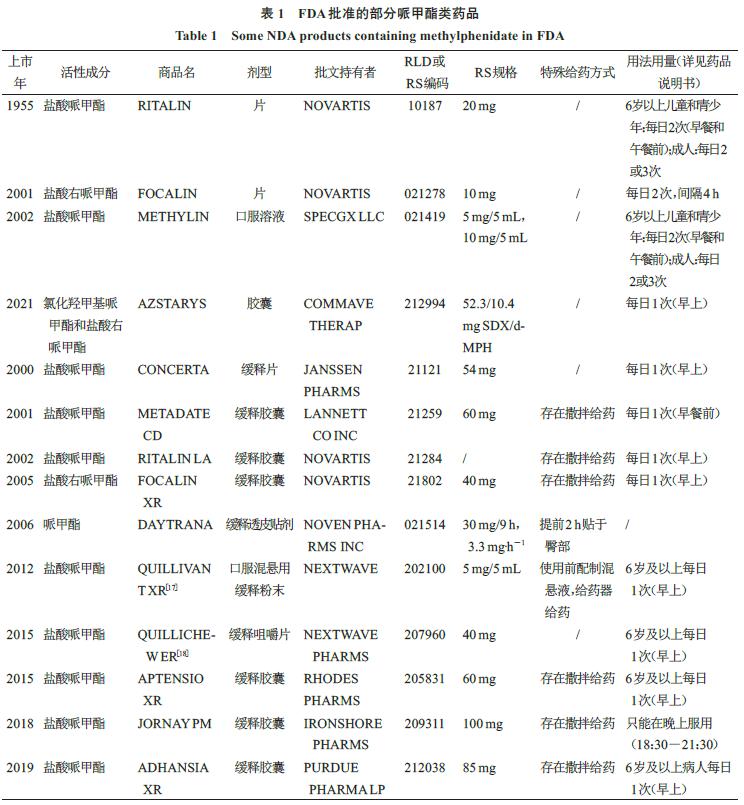
2 欧洲和日本
欧洲上市的有普通片、缓释片、缓释胶囊等,通过欧洲药品管理局(EMA)的集中审批程序或者药品局总部(HMA)的互认可程序(mutualrecognized procedure,MRP)和分权程序(decentralisedprocedure,DCP)上市。在欧盟范围内同一产品在各个国家可能有不同的商品名,主要上市产品包括RITALIN、RITALIN LA、CONCERTA、Equasym、Equasym XL、Medikinet(仿制药)和Rubifen(仿制药)等。日本药品与医疗器械管理局(PMDA)批准上市的主要为普通片(RITALIN)和缓释片(CONCERTA)。
3 中国
中国上市的哌甲酯类药品包括片剂、缓释片和注射用无菌粉末3种剂型,上市产品相较于FDA的品种略显单一。暂未检索到近3年的哌甲酯类制剂国内申报上市信息,2016年曾有企业申报盐酸苏右旋哌甲酯缓释胶囊,故仅汇总了中国已上市哌甲酯类药品,见表2。盐酸哌甲酯在国内属于第一类精神类药品,需结合相应管理条例,实行定点生产制度。目前国内进口的哌甲酯调释药物仅有盐酸哌甲酯缓释片(商品名CONCERTA),于2015年获批进口,规格为18、36 mg。此品种2000年在FDA获批,规格为18、27、36、54 mg。
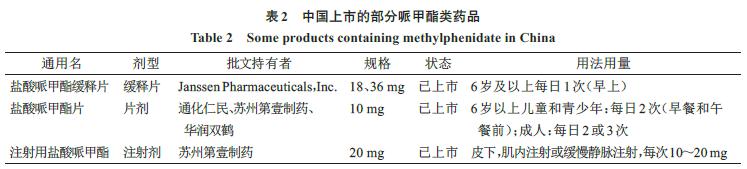
汇总结果显示FDA近年来批准了多个通过505b(2)形式申报的新药品种,例如JORNAY PM、ADHANSIA XR等,在已知主成分基础上对其制剂进行优化,该申报形式对应国内的化药药品注册分类中改良型新药的概念。通过开发新型的缓控释制剂,使其具有明显的临床优势。改良型新药可以借鉴已知主成分的研究数据,缩短临床研发周期,且更加符合对个体化用药的趋势要求。国内目前ADHD用药相对较单一,可以借鉴改良型新药的研发思路进一步研究与申报。
针对儿童用药的给药途径和剂型选择方面,考虑儿童用药的安全性和依从性,药物研发时可以参考口服给药剂型决策树选定合理的剂型,如胶囊剂考虑使用时是否可将胶囊内容物与食物混合服用,口服液体制剂考虑多剂量包装的稳定性和量取装置的准确性,口服调释制剂考虑被儿童咀嚼的风险等。另外透皮贴剂考虑结合目标年龄和品种特性合理设计制剂的尺寸、形状和使用部位,明确是否涉及切割给药使用等。随着制药界技术水平的提高、药监机构各种政策法规和指导原则的及时发布,国内对儿童用药的监管将更加科学与规范,将极大地促进开发出适宜儿童使用的新剂型药品。