
【注册圈】百问百答系列3期——参比制剂
问题1:参比制剂必须要通过一次性进口进来吗?
回答:少量可以直接购买,大量需要一次性进口;因为通关时需要进口通关单,进口通关单需要一次性进口批件办理。国内已上市的参比制剂不用,国内未上市的需要清关。
问题2:有法规规定附条件批准的药品不能作为参比制剂么?
回答:没有,2019年的25号文没有提到。2022年2月18日CDE发布的《化学药品注册受理审查指南修订稿(征求意见稿)》第二部分注册分类3、4、5.2类第13条:如申请人选择的参比制剂中存在附条件批准的适应症,申请人应当在“其他特别申明事项”中对其附条件批准的适应症进行说明。由此分析附条件批准的药品可以作为参比制剂。
问题3:如果参比制剂是通过贸易商购买,都需要哪些证明材料?指的是模块一中对照药来源证明文件。
回答:官方网站的批准信息,所购参比制剂的实物和包装标签(包括内包装和外包装)照片,购买发票、说明书,采购合同,入库单、供应商资质、生产商资质。如果是赠予,那么要弄一个赠予证明。
问题4:生物制品没有标准品,在报上市时,自制的参比品需要送中检院标定或备案吗?
回答:可以明确,在申报上市的时候,一般来讲要准备好标准物质备案。当申报资料递交之后,审评中心在审评 3 个月之后发通知,做标准物质备案。一般来讲,如果工艺和其他产品的工艺差距很大,应该用你的原液中的标准物质。所以说标准物质的备案是要等 CDE 的审评人通知你。
问题5:美国上市的药品参比制剂如何查询?
回答:在橙皮书输你要查询的药品,搜出来列表里面标RLD的是参比制剂。
https://www.accessdata.fda.gov/scripts/cder/ob/index.cfm
问题6:仿制药研发,购进参比制剂是买一批还是三批?
回答:指南只是建议多批。一般情况下是三批。
问题7:我司有一个品种选择的参比制剂和自己研究的不是一个规格,这种情况能被受理吗?因为我司研究的规格暂时还没有参比制剂,参比制剂申请过但是没有被批准(审议未通过)
回答:两种情况:第一种比较特殊,就是中国和国外的用法用量多年以来就完全不一样,你拿国外的原研做参比,一是可能涉及到3类药的临床;二是就算做了,在国内的临床上也很难推广开来,这种情况就是跟CDE申请看看能不能拿原研做质量参照,然后规格还是国产规格。第二种是审议没通过的,那就直接找CDE开会复核,多开几次会说不定就过了。总之得找参比制剂专业开会复核,现在没参比不受理的。
依据:《药品注册受理审查指南(试行)(征求意见稿)》,申请人应选择国家药监局《化学仿制药参比制剂目录》已公布的参比制剂开展研究,并在仿制药注册申请表中“参比制剂信息(仿制药适用)”项填写研究中所用参比的相应信息。
化学药品3、4、5.2类注册申报资料自查表需要填写1.1 是否具有与参比制剂相同的活性成份、剂型、 规格、适应症、给药途径和用法用量。
问题8:参比制剂有3个规格,均已收录在参比制剂目录,其中1个规格原研进口,另外2个规格在国外上市,我们想报3个规格,能否均按4类申报?还是另外2个规格需按3类申报?
回答1:可以具体看下一般性技术问答里面第6条,不管规格,主要看原研有没有在国内上市。
回答2:可以,前提是另两个规格的适应症在国内被批准。
问题9:参比FDA登记的持有人发生变更,和参比制剂目录上出现了不一致。新发的四十九批参比目录更新了之前发布过参比的信息,体现为在备注2中描述了持证商变更,增加变更后的持证商。这种情况下,如何更新参比持证商信息,是重新提交参比遴选资料,还是有其他途径补充新持证商的相关信息?
回答:重新提交参比制剂遴选资料,资料里面说明增加变更后的持证商。
问题10:仿制药参比制剂如果没有公布,是不是要备案?如果不行,是不是研究工作都白做了?备案后药审中心不认可参比,现在手上有个品种药审中心无法推荐参比制剂。
回答1:仿制药参比制剂没有公布,按照流程来,就是要进行参比制剂备案的。
回答2:不认可参比的话,你这个品种在注册申报时就不给受理。
问题11:我们一次性进口一个参比制剂,包装盒上写的是made in Italy,我们通过FEI号查询到的地址却是USA,后面再去查参比制剂的审评历史,发现参比制剂发生了变更,我们查到的信息是变更后的,我们买到的产品可能也就是变更批准附近做的。有两个问题:1、FDA包装盒上面写的made in Italy是指制剂产品的产地吗?2、若确实是指制剂的产地,如何去确认变更前产地是在意大利,能查到变更前的地址吗?若查不到怎么排除是假药,在申报和核查的时候如何进行解释呢?
回答:FDA的批准页面那里有Approve history,你可以去那里找找变更前的label,label最后有生产信息。
问题12:如果参比制剂买不同批号,需要具体每个批号多少量吗,还是写个总量就可以?
回答:按批号,能追踪。
问题13:日本的参比制剂一次性进口申请,NMPA网站要求提供的“提供上市国家药品监管部门核发的批准证明文件”,应该提供什么文件呢?
回答:我们写的批准信息和批准文号和批准日期,最好写明在哪个里面查的。
问题14:5.2类注册,关于参比制剂的选择,有要求一定选择公布的国内上市的进行质量对比吗?是否有要求选择参比制剂进行稳定性放样研究呢?
回答:参比制剂稳定性见CDE一般性技术问题解答建议参照稳定性研究指导原则,对申报产品进行稳定性研究,并未强制要求一定要与参比制剂进行稳定性对比研究。要么选择国内参比制剂,要么备案你们选择的国外上市参比制剂。
问题15:国内申报,如果参比制剂没有提供COA,是不是申报企业需要自己检测后出一份COA?
回答:国内上市申请前做BE时,参比制剂要全检。申报企业自检或委托检验,一般自检即可),并出具COA。如果是上市申请时质量对比研究用,可不全检,也不必出具COA.
问题16:不推荐参比的药学研制信息表里参比制剂那儿用写成对照制剂吗?还是不写?
回答:不写。特别说明事项里面说一下,根据xxx本品为不推荐参比制剂,我公司根据xxx进行了全面的药学研究,申请本品的上市许可。参比制剂那里可以写不适用。
问题17:如果我们资料中写了同一持有人,不同生厂商的参比,一个是德国上市,一个是原研进口,都作为参比制剂,现在审评老师要求我们证明这两个参比的等同性,请问需要怎么证明呢?
回答1:处方,用法用量,适应症,给药途径等。
回答2:处方应该是比较初级的要求,能把生产工艺和产品质量汇报下更好。
回答3:从质量和疗效一致上进行等同比较,质量可以自己研究,疗效可以用文献。
问题18:一个品种有两个规格,只想申请其中一个规格为参比制剂,遴选资料里是不是只用体现拟申请规格的内容呢?
回答:体现你选的即可。
问题19:一个已有批文的口服溶液,想要变更规格,从10ml变更为5ml,是否需要有参比制剂呢?如果按照补充申请,不是以一致性评价为目的,这种情况是否需要参比制剂呢。
回答:看你这个规格是装量还是浓度。如果是装量,是按照变更走即可,变更研究是变更前后产品对比研究。看变更指导原则,变更浓度的话,也可以走变更,但是有如下要求“新增规格应为原研药品增加的新规格或仿制药增加目前原研药品/参比制剂已有的规格,同时不得改变药品原批准的适应症、用法用量或者适用人群”。
问题20:参比制剂备案,如果产品在欧盟是通过互认程序获批的,这个表格里面需要把原研在欧盟各个国家的批准信息都要列出来吗?还是列几个就可以,我们要做的这个产品在欧盟20多个国家批准,需要都写上吗?
回答:都列出来。
问题21:关于CDE发布的《化学仿制药参比制剂目录(第四十六批)》(征求意见稿)中《已发布化学仿制药参比制剂调出品种目录》中包含盐酸氨溴索吸入溶液、吸入用硫酸沙丁胺醇溶液,其调出情况说明为“经一致性评价专家委员会审议,拟调出参比制剂因不符合中国药典吸入制剂通则关于“吸入液体制剂应为无菌制剂”的要求,予以调出”。查阅欧洲药典对于吸入液体制剂的要求,是未要求无菌。难道以后欧盟上市的剂型为吸入制剂的原研产品均不可以作为参比制剂了吗?
回答:根据上述参比制剂调出理由,理论上是这样。
问题22:所用的参比制剂如果持证商发生了变更,还需要重新提交遴选资料吗?
回答:反馈给遴选委员会,让他们修改参比制剂目录。
问题23:参比制剂的规格和适应症数量和国内已上市多年的制剂不一致,仿制时候,可以按国内的规格和适应症报吗?如果这么报需不需要做临床实验啊?剂型是注射剂。
回答:不可以,仿制是仿原研,不管三类还是四类。仿制药需具有与参比制剂相同的活性成份、剂型、规格、适应症、给药途径和用法用量。
问题24:如仿制药,公布的参比制剂为1g,且临床用法1g-2g/次,而国内现有规格均为0.5g,医保规格也为0.5g。这种情况能仿制0.5g吗?
回答:按照法规,这种情况应该不能仿制0.5g。
问题25:参比制剂可以不用办理一次性进口,包括临床用的?
回答1:要自行购买的,代理的都要提供一次性进口证。
回答2:根据100号公告,申请人自行购买参比制剂的适用范围为一致性评价品种。
总局关于仿制药质量和疗效一致性评价工作有关事项的公告(2017年第100号)
(https://www.nmpa.gov.cn/xxgk/ggtg/qtggtg/20170825205601306.html)
回答3:可以走代购,用到临床就需要批件了,一次性进口。
问题26:除了购买参比制剂外,哪里能找到参比制剂最新更新的说明书?
回答:美国的话 dailymed;欧盟的话EMA或HMA都可以;日本 PMDA。药智网、丁香园用药助手、戊戌数据等都可以。
问题27:现在单独申报原料药的话还必须和参比制剂对比吗?
回答:原料药没有要求必须和参比制剂对比。
问题28:对于BE临床样品参比制剂那些是获批后几年可以销毁?有法规出处吗?
回答:GCP,Sponsor保存到批准,试验机构保存2年。具体看《药物临床试验质量管理规范》第21条和45条。临床试验机构至少保存留样至药品上市后2年。临床试验机构可将留存样品委托具备条件的独立的第三方保存,但不得返还申办者或者与其利益相关的第三方。申办者应当采取措施确保试验期间试验用药品的稳定性。试验用药品的留存样品保存期限,在试验用药品贮存时限内,应当保存至临床试验数据分析结束或者相关法规要求的时限,两者不一致时取其中较长的时限。
问题29:我公司预开发一个品种,为缓释片剂,目前国外仅印度上市了该缓释片,但是查不到任何相关的信息,安全有效性数据查不到。其原研为日本上市的普通片剂,我们开发的缓释片注册分类应属于2类(改良型新药)吗?还是仿制印度的仿制药?印度不在ICH成员国里,可以作为参比制剂吗?
回答:做不了参比制剂,欧美市场有完整的安全性有效性数据才行。注册分类是2类,印度上市的不应该会有参比地位,去备案估计也不会批准。
问题30:国家公布的参比制剂目录没有收载的品种,怎么确定原研到底是哪家的?
回答:戊戌数据可以查到,如果戊戌数据没有就去美国orange book看看。
问题31:日本已上市的产品是仿制药不是原研药品无法作为参比制剂,根据药审中心19年发的25号文提到【在原研药品停止生产或因质量等原因所致原研药品不适合作为参比制剂的情况下,可选择在美国、日本或欧盟等管理规范的国家获准上市的国际公认的同种药品、经审核确定的在中国境内生产或经技术转移生产的国际公认的同种药品】,所以是否日本已上市的同类型产品曾经遴选过参比制剂,但是未获批准,一般审评中心对这个审评的尺度基于什么?毕竟这个药品按照指导原则的概念是可以作为参比制剂遴选的啊。
回答:日本上市的这个因为是仿制药,药审中心不批准做为参比制剂。
问题32:原研参比制剂的包装,除了实物拍照,有其他途径可以获得吗?
回答:如果是境外原研可以上这个网站*载下** https://www.drugs.com。
问题33:一致性评价可以没有参比制剂吗?
回答:有那种临床价值明确但不推荐参比制剂的, 出了药学研究指导意见那种可以没有。基本都有。名字就是质量和疗效一致性评价,没参比就没标杆,没法评价。
问题34:国家尚未推荐参比的口固制剂,可否进行一致性评价?可用注射剂作为参比做一致性评价吗?
回答:基于风险,先进行参比备案,国家批准了再进行一致性,不可以用注射剂做参比制剂。
问题35:美国的膳食补充剂能作为我国药品(非处方药)的参比制剂吗?
回答:美国膳食补充剂那就是属于食品级的东西,不能做药品的参比制剂。
问题36:未进口中国的德国参比制剂说明书,在哪里*载下**呢?EMA上搜索不到。
回答:https://www.drugs.com。关键词搜索化合物和商品名。
问题37: 对于临床价值明确,无法推荐参比制剂的化学药品应该按几类报?审评通过后会给通过一致性评价的标识吗?
回答:按原法规,无参比制剂的,由药品生产企业进行临床有效性试验。国办发〔2016〕8号里面写的比较清楚,所以企业肯定需要会开会确认参比制剂。受理审查指南(2020年第10号)第5页有写。
2022年2月18日,CDE发布《药品注册受理审查指南》(征求意见稿)删除了原有“不推荐参比制剂的情形”按该版本的受理审查指南,临床价值明确但原研不明确,无法确定参比制剂的品种可能将不能按仿制药申报。
问题38:仿制药4类,工艺验证批做稳定性考察的时候需要同时放参比制剂做对比研究吗?
回答:法规没有强制要求一定要放参比的稳定性。建议按一致性评价的放吧。
问题39:某注射剂品种,2019年CDE受理其国内2.2类的申请,同年FDA批准该注射剂的上市申请,今年CDE公布了FDA上市的为参比制剂。2019年受理的国内2.2类申请(目前在审评过程中),审评的时候会不会要求其按照现公布参比进行一致性的对比研究?会按照2.2类批准吗?
回答:药品上市申请审评审批期间,药品注册分类和技术要求不因相同活性成份的制剂在境内外获准上市而发生变化。药品注册分类在提出上市申请时确定。
问题40:我们现在想报推荐参比,但是境外持证商已经更换成新的了,和我们用的已经不一样了,这种情况报原来的持证商还可以接受吗,还是两个持证商都报呢?
回答: 建议两个持证商都报,并做情况说明。
问题41:大家的公司仿制药品种,参比制剂会和自制制剂同步放影响因素试验吗?
回答:同步。
问题42:美国的参比一次性进口注册,标签和说明书上都没有生产商信息,都是怎么确认生产商的啊?中介说就写标签上的公司名称就可以了,结果上海局没通过,要求重新确认并提供证明。
回答:需要证明的话,只能写邮件给生产商,一般国外没有公章,一些老师不认可生产商反馈的邮件,所以还得自己写一个说明。
问题43:参比制剂持有人是美国,产地在法国,申请一次性进口时,生产企业没有,只知道在法国,这种情况如何申请一次性进口?说明书上面只有持证人的地址,产地法国只有药外盒上面贴了,现在是省局有这个疑问。
回答:联系卖参比制剂的公司帮忙查,或者查药盒,标签,旧版本的说明书,特别是最早的版本,如果生产厂家没有变化。或者查Dailymed,有时候会有。有时候会写原料、制剂、包装的厂家的。Dailymed上还有之前旧版本的标签说明书。真的查不到生产商,和卖参比的公司沟通好,只要保证通关没有问题,省局能发批件就行。
问题44:参比制剂一次性进口,不同规格的可以放在一起申请一次吗?
回答:不同包装可以。不同规格应该不行,因为涉及到你对应的一次性进口批件的评审,一个评审就1个规格。
问题45:临床价值明确,无法推荐参比制剂的化学药品,是否还会存在? 如果存在,是否一定会找一个“参比”作为标杆,供企业参照开展研究对比? 如果不存在,“药学技术要求”的作用就是指导 企业开展研究吗? 那52-55批参比目录中,推荐了 之前无法推荐参比目录中的品种,标注的是“原研”,是否说明之前那117个品种中,无法推荐参比,这个信息是不准确的?
回答:2020年8月27日 国家药品监督管理局药品审评中心发布“临床价值明确,无法推荐参比制剂的化学药品目录(第一批)(征求意见稿)”;2021年2月20日 国家药品监督管理局药品审评中心组织起草了《第一批拟不推荐参比制剂化药品种药学研究技术要求》(征求意见稿),经专家会讨论,目前已完成30个品种的药学研究技术要求,并在中心网站予以公示;目前这两个均为征求意见稿,所以无法确定无法推荐参比制剂的化学药品是否还会存在;“药学技术要求”的作用就是指导企业开展研究。参比制剂的推荐是一个渐进的过程,无论是药品生产企业还是国家监管部门和审评部门对参比制剂的了解和认知都是个渐进的过程,2021-11-19发布第52批参比制剂,距离2020.8.27发布的“临床价值明确,无法推荐参比制剂的化学药品目录(第一批)(征求意见稿)”已经有一年多时间,信息发生改变也很正常。
对于临床价值明确,无法推荐参比制剂的化学药品,目前均为征求意见稿, 2022年2月18日,CDE发布《药品注册受理审查指南》(征求意见稿)删除了原有“不推荐参比制剂的情形”,按该版本的受理审查指南,临床价值明确但原研不明确,无法确定参比制剂的品种是否还会存在也是无法确定的。
问题46:根据化药注册分类,3类和4类的仿制对象都是原研药品,如果原研已退市,但参比制剂目录公布了该品种国际公认同种药物,可以参照该同种药物进行仿制吗?参比制剂是已经明确列在参比制剂目录里了,但其不是原研制剂,而是国际公认同种药物,能否参照该参比制剂进行3类或4类仿制申报?
回答1:按照参比制剂遴选原则来筛选。与国家局公布的参比制剂对比一致就OK。
回答2:可以,注册分类里面3类和4类需要和参比制剂的质量和疗效一致,选用列入参比制剂目录里面的就好了。

之前我们申报的有个产品也是原研退市,选用被公认的参比,没问题。
问题47:收录到上市药品目录集品种,指定为参比制剂,但未收录到参比制剂目录,是否要进行参比制剂遴选?
回答:需要进行参比制剂遴选。
问题48:原研在美国和欧盟都上市,都进入国内的参比制剂目录,是不是哪家有渠道可以随便选?
回答:采用“发布参比制剂有关事宜说明”判定其等同性。
问题49:假如仿制药参比制剂目录公布的参比制剂写的是欧盟上市,但是看持证商应该是法国的,这个原研如果在欧盟多个成员国都有上市,是欧盟上市所有的原研都可以当参比,还是只能选法国的

回答:欧洲多国上市的情况持证商一致就行,不一定要在法国买,如果变了最好走个目录增订。目录增订流程跟报参比制剂类似,CDE申请人之窗交异议申请表。
问题50:做仿制药3类一定要用国家局公布的《仿制药参比制剂目录》里有的参比制剂吗?那如果一个品种不在《仿制药参比制剂目录》里,我们可以直接买原研产品作为参比制剂吗?

回答:最好参比制剂备案,万一后面CDE不认可。你通过了,后期CDE就会把它加入目录
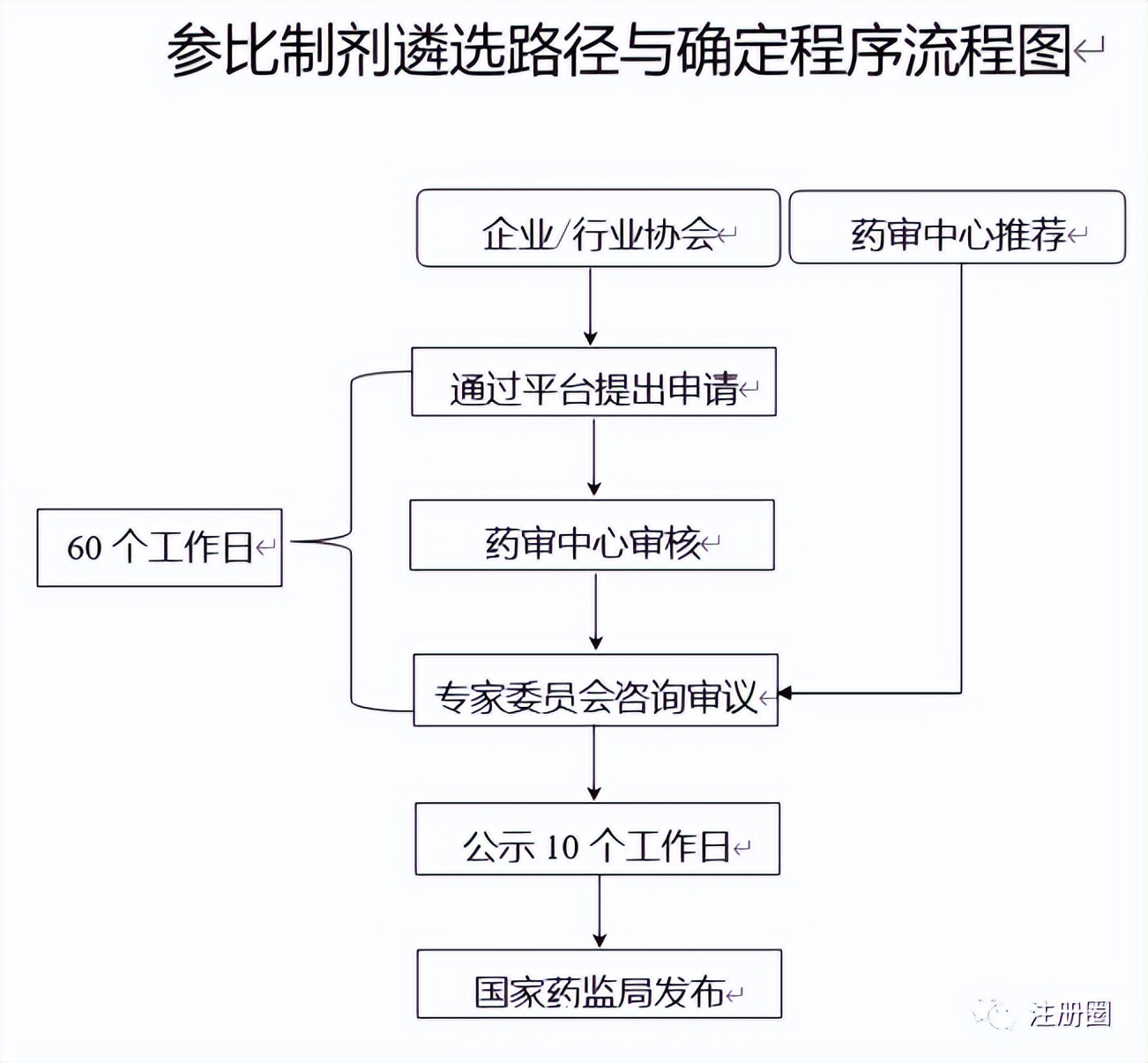
问题51:化学药品真3类申请临床时,参比可以是未公示的吗?就是参比制剂信息那里可以不填吗?
回答:不可以,参比制剂如果未公示需要自己提交参比制剂遴选申请。
问题52:有一个参比制剂,持证商变化了,新的持证商未被列入参比制剂目录,这样的话,只能走参比制剂遴选渠道把新持证商申请列入吗?
回答:是的。
问题53:苯磺酸左氨氯地平片好像没有查到有参比制剂,但是又有仿制药申报,参比怎么确认?
回答1:目前国内一致性评价获批的苯磺酸左氨氯地平片均以辉瑞制药有限公司生产的苯磺酸氨氯地平片为参比制剂,选择“施慧达” 为参比制剂的仿制药企业和一致性评价企业均以失败告终,以石家庄四药有限公司为例,BE试验登记的信息显示(登记号:CTR20160387),该公司选择的对照药是商品名为“施慧达”的苯磺酸左旋氨氯地平片。

回答2:参比是苯磺酸氨氯地平片,没有带左旋的,苯磺酸左氨氯地平片是国内特色品种。
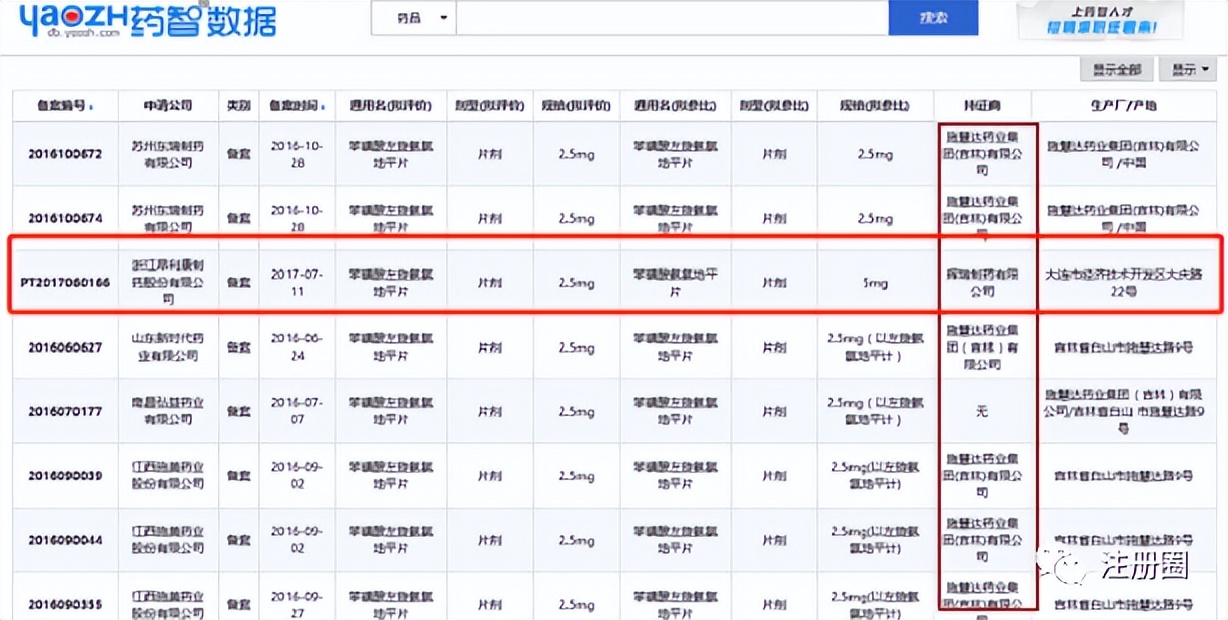
红框这个是可行的,左旋算是国内施慧达的原研,但是国家局不列为参比,这个品种国家局就是以辉瑞没有消旋的作为参比。
问题54:参比制剂一次性进口批件是否可以由MAH委托的生产企业申请?
回答::参比制剂一次性进口没有特别规定,谁申请都可以,只要有合法来源就行,你可以理解生产企业申请然后转给MAH一样的,证明性材料齐全就行了。
问题55:参比制剂目录中既收载了欧盟上市原研,又收载了美国橙皮书中的国际公认同种药品(美国原研已撤市),仿制药开发选择美国橙皮书中的国际公认药品作为参比制剂是否合适?会被CDE认可么?
回答:推荐目录中的都可以。在国内、欧美、日本上市的原研都可以用。
该问答为注册圈汇总而成,对以上观点,有任何不妥之处,欢迎大家积极斧正,评论留言交流。
更多其他资讯与服务请关注:注册圈。
注册圈,让注册人不再孤单!齐聚各层制药人,加入交流圈一起分享行业知识吧~