不想错过界哥的推送?
戳上方蓝字“医学界肿瘤频道”关注我们
并点击右上角“···”菜单,选择“设为星标”

“神药”阿司匹林能预防胰腺癌吗?Necitumumab联合化疗一线治疗晚期肺鳞癌对亚洲人群有用吗?广谱抗癌药”拉罗替尼在1期研究中的表现如何?让我们一起来揭晓这些疑问!
文丨Sharon
来源丨医学界肿瘤频 道
01
“神药”阿司匹林能预防胰腺癌吗?
有证据表明,“神药”阿司匹林可降低多种癌症的发病率。对于“癌中之王”胰腺癌,其是否能同样起到预防作用呢?来自韩国嘉泉大学医学院的In Cheol Hwang等[1]为我们解答了这一问题。
然而,非常遗憾的是,答案是:不能!
从机制上讲,阿司匹林可能通过抑制环氧化酶-2或其他促凋亡作用来降低癌症风险。流行病学研究也显示,阿司匹林能够降低结直肠癌和几种其他癌症风险。
有两项病例对照研究报告,阿司匹林能够降低胰腺癌风险,然而Queensland胰腺癌研究中没有发现该获益。由于这些研究中阿司匹林使用情况都是由患者自己报告的,所以可能存在重大缺陷。
而且,近期一项美国两个大型队列(测定阿司匹林代谢物水杨酸的血浆水平)进行的前瞻性分析也发现,定期使用阿司匹林和未来胰腺癌风险无关。
为了进一步确认两者之间的关系,Hwang等采用韩国国民健康保险服务(NHIS)系统数据进行了分析。
NHIS系统几乎囊括了全部韩国人群,而且NHIS还对所有≥40岁的人群提供两年一次的健康检查。因此来自NHIS索赔数据库的处方数据(药物识别码、剂量和持续时间)能够准确测定药物暴露情况。
本研究中,研究人员从一个标准化12年纵向队列(健康检查队列)中获取了NHIS数据,该队列由在2002年1月1日至2003年12月31日之间接受过≥1次每两年一次的体检的个体构成。
前5年(2002年1月1日至2006年12月31日)的数据用于确定队列纳入和排除标准,以及阿司匹林使用和胰腺癌相关的暴露和潜在混杂因子。
观察期延至2013年12月31日,在避免永恒时间偏倚的同时,识别新诊断胰腺癌病例。
该分析最终共纳入461 489例受试者。
结果显示:
-
在这项用药信息可靠的队列研究中,阿司匹林使用与新发胰腺癌之间没有显著关联。
-
在根据可用变量分层进行亚组评估时,也得到一致结果。
-
这与之前研究报告的使用阿司匹林可以降低糖尿病患者中胰腺癌发病率的结果相反。
表1 与胰腺癌相关的因素
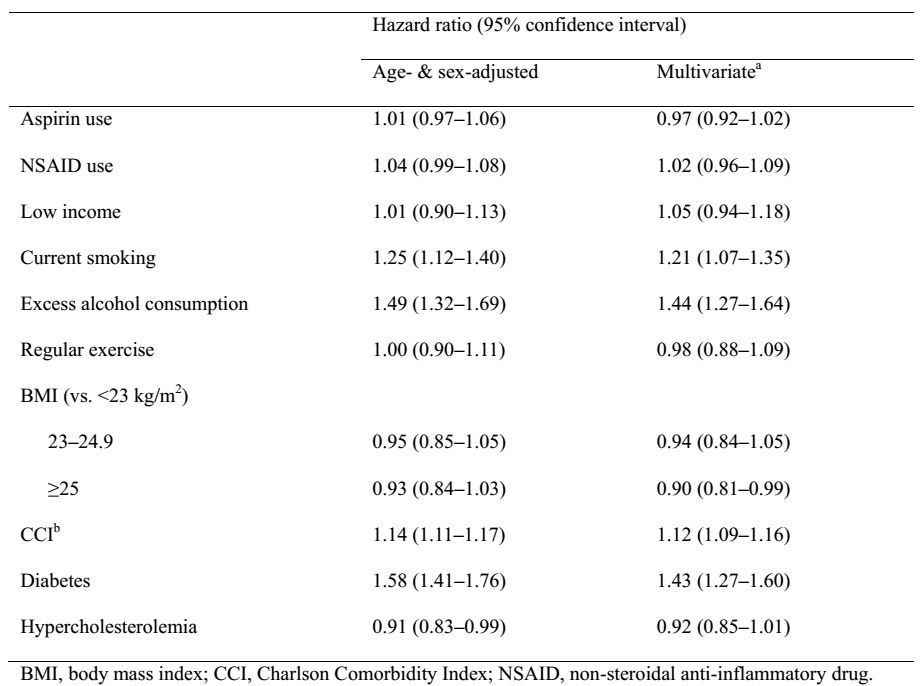
研究人员表示,该研究为使用阿司匹林不能预防胰腺癌提供了新的有力证据。
02
日本人群研究:Necitumumab+化疗一线治疗晚期肺鳞癌可改善生存
近日,Lung Cancer杂志上发表的一项日本1b/2期研究[2]结果显示,Necitumumab+吉西他滨+顺铂(GC+N方案)相比吉西他滨+顺铂(GC方案),一线治疗IV期鳞状非小细胞肺癌(NSCLC)患者,可带来显著临床获益且耐受良好。
Necitumumab是一种重组人源性lgG1单克隆抗体,能够与人表皮生长因子受体(EGFR)结合,阻断其与配体结合,从而抑制细胞增殖。由于在3期SQUIRE研究中,GC+N较GC带来显著的生存获益,2015年美国食品药品监督管理局(FDA)已批准该方案用于一线治疗转移性鳞状NSCLC。
那么该方案是否也同样适用于亚洲人群呢?
这项研究于2013年5月7日至2017年6月28日在日本的39家中心开展,所选患者为初治的鳞状NSCLC,ECOG PS为0-1分。
其中1b期部分为单臂、剂量递增研究,旨在为2期部分确定吉西他滨的剂量,共纳入9名患者;2期部分纳入181名患者,按照1:1随机分至GC+N组(n=90)和GC组(n=91)。
药物剂量为:吉西他滨1250mg/m2(d1、d8),顺铂75mg/m2(d1,每3周为1周期,最多4周期),Necitumumab 800mg(d1、d8,每3周重复,直至病情进展或出现不可耐受的毒性)。
首先看看下2b部分的主要终点总生存(OS)数据:
-
在研究数据截止时,GC+N组和GC组分别发生63例(70%)和74例(81%)死亡;
-
GC+N相比GC显著改善OS,两组中位OS分别为14.9个月和10.8个月(分层HR 0.66;95%CI 0.47-0.93;P=0.0161);
-
而且在根据年龄(<70岁:HR 0.68;≥70岁:HR 0.482)和ECOG PS评分(ECOG PS 0: HR 0.46;ECOG PS 1: HR 0.74)进行的亚组分析中,GC+N组的OS改善均更多。
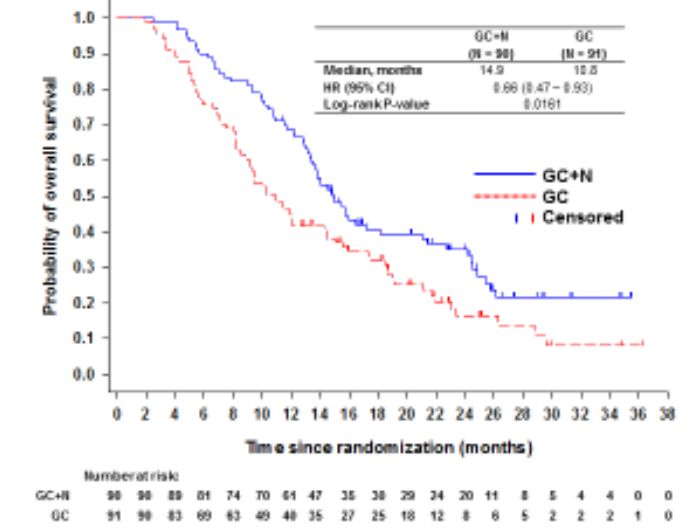
图1:两组患者OS的Kaplan-Meier曲线
在次要终点方面:
-
同样,GC+N组相比GC组观察到显著的无进展生存(PFS)改善,两组中位PFS分别为4.2个月和4.0个月(分层HR 0.56;95%CI 0.41-0.78;P=0.0004)。在预先设定的亚组中亦观察到相似结果;
-
GC+N组客观缓解率(51% vs 21%;P<0.0001)和治疗失败事件(TTF)也有所改善;
-
对平均症状负荷指数(ASBI)和肺癌症状量表(LCSS)总评分恶化时间HR(分别为0.47和0.27)的分析也更有利于GC+N组;表明GC+N方案能够延缓症状和生活质量恶化的时间。
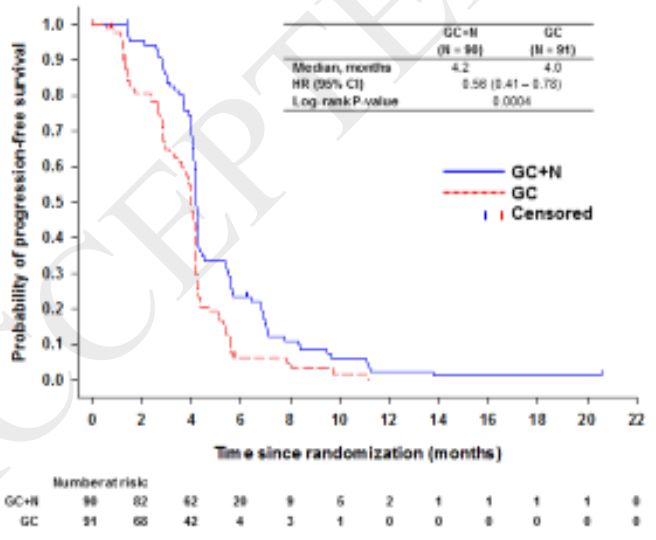
图2:两组患者PFS的Kaplan-Meier曲线
此外,在EGFR阳性的患者中 ,与GC相比,GC+N显著延长中位OS(14.8个月 vs 9.4个月;HR 0.62;P=0.011)和中位PFS(4.2个月 vs 3.9个月;HR 0.54;P<0.001),ORR也更高(54% vs 18%;P<0.001)。在EGFR阴性患者中,两组之间OS、PFS、ORR无显著差异。
安全性方面,研究Ib期部分没有观察到剂量限制性毒性。在2期部分,以下≥3级的治疗相关不良事件的发生率,GC+N相比GC组多5%以上:中性粒细胞计数降低(42% vs 35%)、发热性中性粒细胞减少(12% vs 3%)、食欲下降(11% vs 4%)和*疮痤**样皮炎(6% vs 0%)。
总体上,GC+N联合用药方案表现出良好的获益-风险特征。
03
广谱抗癌药”拉罗替尼1期研究:耐受良好且抗肿瘤活性持久
TRK融合蛋白是癌细胞中NTRK基因融合后引发的异常表现,能够驱动肿瘤的发生,且TRK融合蛋白存在于多种不同类型的肿瘤。“广谱抗癌药”拉罗替尼(Larotrectinib)作为首个强效、高选择性的TRK*制剂抑**,近期报告的其对存在TRK融合的实体瘤高达81%的总有效率,让其得到了广泛关注。美国FDA也加速批准其用于携带NTRK基因融合的局部晚期或转移性实体瘤患者。
那么,拉罗替尼在1期研究中所展现出的安全性、耐受性、药代动力学特征和活性如何呢?大家一起来了解下近日在Annals of Oncology发表的这项研究[3]。
这是一项多中心、1期、剂量递增研究,纳入转移性实体瘤成人患者,无论NTRK基因融合状态。关键入选标准包括:疾病价和(或)可测量、ECOG PS评分0-2分和足够的器官功能。
给药方式:拉罗替尼口服给药,每天1次或2次,持续28天,根据标准3+3剂量递增方案逐渐增加剂量水平。
主要终点为拉罗替尼的安全性,包括剂量限制性毒性。
结果显示:
从2014年5月1日至2017年8月24日,本研究共纳入70名转移性实体瘤患者,其中8名存在NTRK基因融合,62例无NTRK基因融合,共分为6个剂量队列。
-
队列1:50mg QD,n=4;
-
队列2:100mg QD,n=5;
-
队列3:100mg BID,n=43;
-
队列3a:200mg QD,n=5;
-
队列4:150mg BID,n=7;
-
队列5:200mg BID,n=6;
在剂量递增阶段,前两个剂量水平没有发生剂量限制性毒性;接受100mg BID治疗的前6名患者中有1名报告剂量限制性毒性(头晕),200mg QD治疗患者没有报告;接受100mg BID治疗的7名患者中有1名发生剂量限制性毒性(丙氨酸转氨酶和天冬氨酸转氨酶升高);接受200mg BID治疗的6名患者中有1名报告,为头晕。
也就是说,共发现4个剂量限制性毒性,但没有毒性导致停药研究药物。
另外,该研究中拉罗替尼未达到最大耐受剂量;根据耐受性和对NTRK基因融合患者的有效持续时间,研究人员推荐2期研究采用的拉罗替尼剂量为100mg BID。
拉罗替尼相关不良事件主要为1级,没有4-5级事件;最常见的3级拉罗替尼相关不良事件为贫血(6%;4/70)。
根据研究者评估的结果,总体ORR为12%(8/67),其中7名为NTRK基因融合患者,1名为NTRK基因扩增患者。在存在NTRK基因融合的患者中,独立审查委员会评估的ORR为100%(8/8),其中2名完全缓解,6名部分缓解。
所有NTRK基因融合患者都观察到肿瘤负荷减小。中位随访时间为26.9个月,拉罗替尼中位缓解时间未达到。
另外,药代动力学分析显示,拉罗替尼的暴露剂量一般与给药剂量成正比。
总而言之,拉罗替尼在TRK融合癌症成人中,耐受良好且抗肿瘤活性持久。
参考文献
[1]Min-Hyung Kim, Sang Min Park, Young Ho Yun, In Cheol Hwang. Aspirin does not prevent pancreatic cancer in a large Asian cohort. Cancer Epidemiol Biomarkers Prev January 14 2019 DOI:10.1158/1055-9965.EPI-18-1325
[2]Watanabe S, Yoshioka H, Sakai H, et al. Necitumumab plus gemcitabine and cisplatin versus gemcitabine and cisplatin alone as first-line treatment for stage IV squamous non-small cell lung cancer: a phase 1b and randomized, open-label, multicenter, phase 2 trial in Japan, Lung Cancer(2019), https://doi.org/10.1016/j.lungcan.2019.01.005
[3]D S Hong, T M Bauer, J J Lee A Dowlati, et al. Larotrectinib in adult patients with solid tumours: a multicentre, open-label, phase I dose-escalation study. Annals of Oncology, DOL: 10.1093/annonc/mdy539.
(本文为医学界肿瘤频道原创文章,转载需经授权并标明作者和来源。)
觉得好看,请点这里
↓↓↓↓