
受COVID-19疫情影响,第62届美国血液学年会(ASH)将首次以线上形式于2020年12月5日-8日召开。一年一度的ASH年会可谓是全球最顶级的血液学领域国际盛会,是全球上百个国家的上万名血液学专家获悉领域最新进展、交流学习的盛大平台。今年ASH年会上在多发性骨髓瘤和轻链(AL)淀粉样变性领域将有哪些研究成果精彩亮相呢?本次特邀上海交通大学医学院附属瑞金医院血液科糜坚青教授对这些重磅研究进行汇总,带大家先睹为快!
1. CARTITUDE-1:Cilta-cel治疗复发/难治性多发性骨髓瘤(R/R MM)的Ib/II期临床研究
摘要号:177
Cilta-cel(LCAR-B38M;JNJ-68284528)是一种靶向B细胞成熟抗原的嵌合抗原受体T(CAR-T)细胞疗法。在中国的LEGEND-2 I期研究中,Cilta-cel对患有R/R MM的患者产生了深度、持久的缓解,并具有可控的安全性。本研究报告了来自Ib期的部分更新数据以及II期的初始数据。
截至2020年5月20日,97例R/R MM患者接受了Cilta-cel治疗(29例Ib期,68例II期)。中位随访时间为8.8个月。总缓解率( Overall Response Rate,ORR,主要终点)为94.8%(95%CI 88.4–98.3),严格意义的完全缓解(sCR)率为55.7%(95%CI 45.2-65.8),非常好的部分缓解(VGPR)率为32.0%(95%CI 22.9–42.2),部分缓解(PR)率为7.2%(95%CI 3.0–14.3)。所有患者的M蛋白水平均降低。至首次缓解(第一次达到≥PR)的中位时间为1.0个月(范围0.9-5.8;80.4%≤1.0个月),至大于等于完全缓解(≥CR)的中位时间为1.8个月(范围0.9-12.5;74.1%≤3.0个月)。缓解深度随着时间而加深,中位缓解持续时间未达到(NR)。在52例微小残留病(MRD)可评估的患者中,94.2%的患者MRD阴性(阈值为10-5)。6个月无进展生存(PFS)率和总生存(OS)率分别为87.4%(95%CI 78.9-92.7)和93.8%(95%CI 86.7-97.2),中位PFS和OS为NR(图1)。
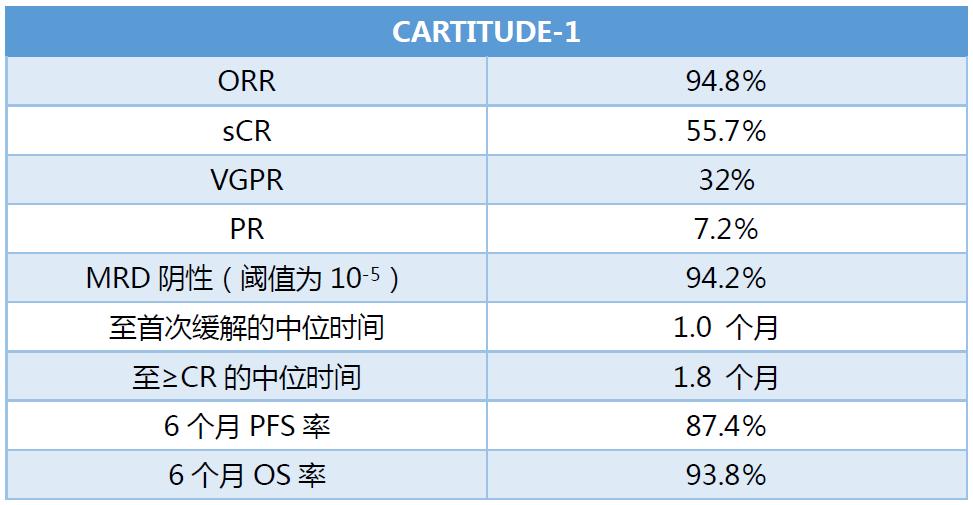
图1 CARTITUDE-1的Ib/II期临床疗效
来自CARTITUDE-1的Ib/II期初步数据表明,在经过多线治疗的MM患者中,一次低剂量的Cilta-cel输注可带来早期、深度和持久的缓解,其安全性与LEGEND-2一致。此外,CARTITUDE-1在其他MM人群中的研究正在进行中。
2. Teclistamab,一种B细胞成熟抗原(BCMA) x CD3双特异性抗体,用于R/R MM I期的最新研究结果
摘要号:180
Teclistamab(JNJ-64007957)是一种结合BCMA和CD3的人源化IgG-4双特异性抗体,在临床前研究中,Teclistamab将CD3+T细胞重定向至表达BCMA的骨髓瘤细胞,从而诱导靶细胞的细胞毒性。正在进行的Teclistamab治疗R/R MM的研究(NCT03145181)显示,静脉注射(IV)270 µg/kg剂量的客观缓解率(Objective Response Rate,ORR)为67%,可评估MRD的患者中,80%的患者为MRD阴性。本研究同时报道了皮下给药的最新结果。
截至2020年7月20日,分别有84例和44例患者接受Teclistamab IV(0.3–720 µg/kg)和皮下注射(SC,80–3000 µg/kg)。结合每周一次IV 270 µg/kg,IV 720 µg/kg,SC 720 µg/kg,SC 1500 µg/kg这4种剂量水平,客观缓解率为30/47(63.8%)。选择1500 µg/kg SC为推荐的第2阶段剂量(RP2D)。目前在此剂量下,6例患者均出现了不同程度的缓解(3例PR,1例VGPR,2例sCR),且随着时间的推移,缓解程度逐渐加深。
在所有IV和SC队列的48例缓解患者中,首次缓解的中位时间为1个月(范围0.3-4.2),中位缓解持续时间尚未达到。在MRD可评估的完全缓解(CR)患者中,IV队列中4/5的患者和SC队列中2/2的患者MRD为阴性(阈值为10-6)。
Teclistamab安全性可控,细胞因子释放综合征(CRS)发生级别低(无≥3级别事件),IV和SC发生严重感染率和神经毒性率低,并且均可观察到深而持久的缓解。Teclistamab令人鼓舞的耐受性和疗效支持计划中的第II期单药治疗(1500 µg/kg SC)试验和未来的联合研究。
3. 达雷妥尤单抗联合来那度胺、硼替佐米和地塞米松(D-RVd)治疗适合移植的新诊断多发性骨髓瘤(NDMM):GRIFFIN研究最新随访数据
摘要号:549
GRIFFIN II期研究(NCT02874742)评价了D-RVd在适合移植NDMM患者中的疗效。GRIFFIN的随机试验结果达到了其预先设定的主要终点,sCR有所提高(D-RVd,42.4% vs. RVd,32.0%;P=0.068)(Voorhees P, et al. Blood 2020);但中位随访时间有限(13.5个月),本研究通过分析GRIFFIN最新随访数据,以评估达雷妥尤单抗(DARA)联合来那度胺(DR)维持治疗的作用。
该研究入组了207例NDMM患者,分为两组(D-RVd;RVd)。维持治疗12个月时,D-RVd组的sCR率仍明显高于RVd组(63.6% vs. 47.4%,P=0.0253)。D-RVd组的MRD阴性率(10-5或10-6)均仍高于RVd组。并且,相比巩固治疗结束时,DR维持进一步增加了sCR和MRD阴性率(图2)。随着随访时间的延长,未观察到新的安全问题。

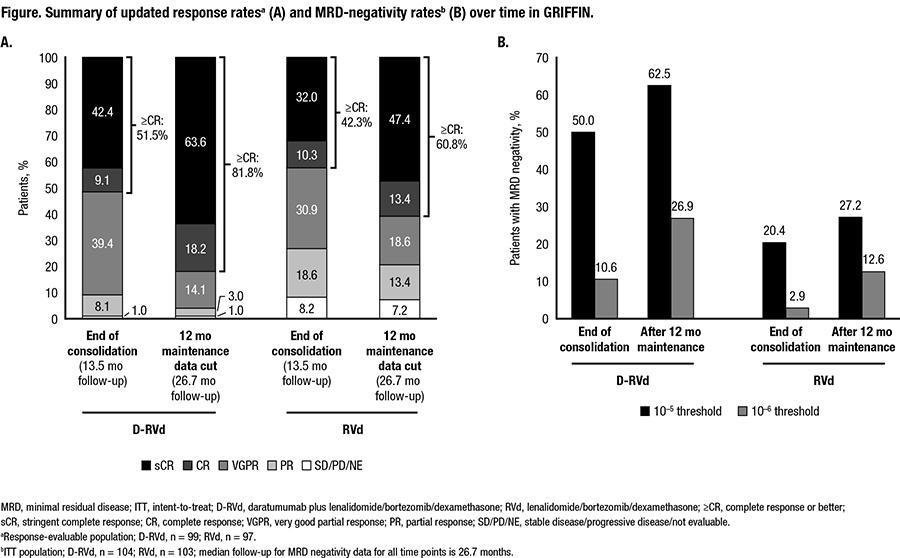
图2. D-RVd和RVd疗效的最新随访数据
4. 达雷妥尤单抗+硼替佐米+地塞米松(D-Vd)与硼替佐米+地塞米松(Vd)治疗R/R MM:LEPUS和CASTOR合并亚组分析
摘要号:2290
LEPUS(MMY3009)研究是在中国开展的III期临床试验,其结果与全球进行的CASTOR研究相比,D-Vd方案在中国MM患者人群中,CR率、VGPR率略有提高;与已知的D-Vd方案安全性一致,未发现新的不良事件。本研究报告了合并亚组分析的结果,包括LEPUS研究的中国患者和CASTOR研究的全球患者,以评估D-Vd与Vd在不同亚组人群中(年龄、细胞遗传学风险和肾功能)的疗效,中位随访时间为7.5个月。
结果显示,与Vd组相比,D-Vd组在各年龄(<65,65-74,≥75岁)、细胞遗传学状态(标危/高危)、肾功能(肌酐清除率≤60 mL/min和>60 mL/min)的不同亚组人群中,PFS与缓解深度(ORR/≥CR/≥VGPR)均获得更显著的临床获益(图3)。这些数据将支持中国R/R MM患者接受D-Vd方案的治疗。ASH会议报告将公布其他亚组数据,比如PFS2。
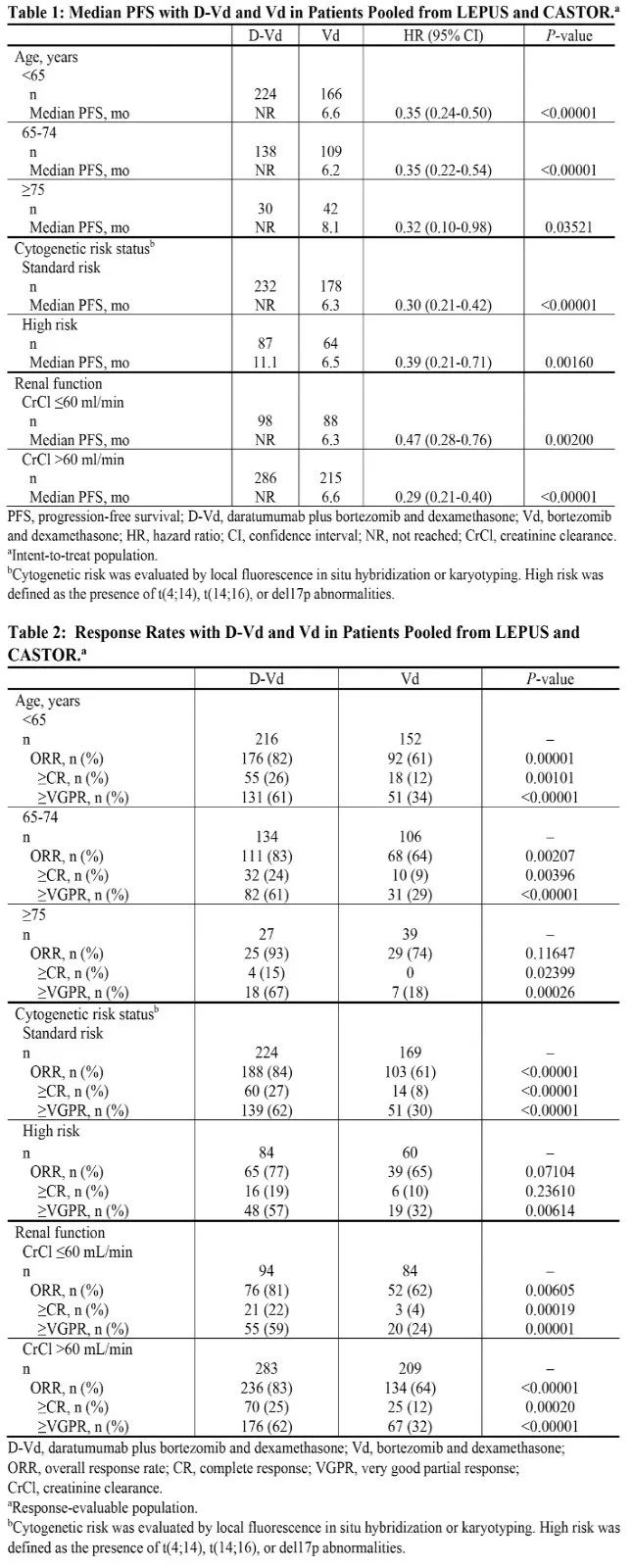
图3. D-Vd和Vd在LEPUS和CASTOR合并亚组的中位PFS、ORR
5. 通过MRD指导临床决策可改善MM的临床预后
摘要号:2237
MM中的MRD检测在临床试验中越来越多地用于评估疾病缓解,并作为预测缓解持续时间的预后工具。这项研究回顾性分析了根据MM患者的MRD状态来改变临床决策对临床预后的影响。
本研究对3个医疗中心的373例MM患者进行了回顾性分析。纳入研究的患者至少接受了一项MRD评估。在以下3个方面进行了基于MRD的临床治疗决策改变:1. MRD阴性后停止或减少治疗;2. MRD阳性后增加治疗强度;3. MRD阳性后开始新的治疗。
在373例患者中,其中57例(16%)做出了改变治疗的临床决策。24例患者在MRD阴性后减少或停止了治疗(第1组),20例患者在MRD阳性后增加了治疗强度(第2组),13例患者在MRD阳性后接受了新的治疗方案(第3组)。与未改变治疗决策的患者(n=312)相比,根据MRD改变临床治疗决策的患者(n=57)的PFS显著延长(中位PFS:97个月 vs. 75个月,p=0.006)(图4)。此外,本研究再次证实,与未达到MRD阴性的患者相比,达到MRD阴性患者的PFS显著延长(中位PFS:97个月 vs. 57个月,p=0.0001)。
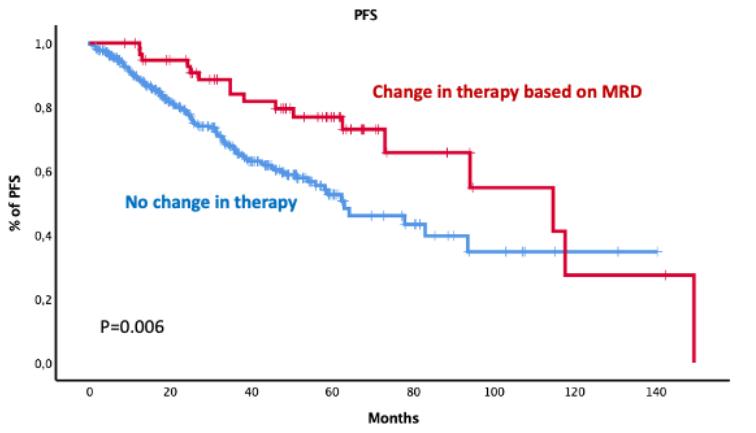
图4 根据MRD改变临床治疗决策和未改变治疗决策的患者的PFS
6. 皮下注射达雷妥尤单抗(DARA SC)联合硼替佐米、环磷酰胺和地塞米松(VCd)治疗新诊断轻链(AL)淀粉样变性患者:3期ANDROMEDA研究的亚洲人群分析
摘要号:1409
在3期ANDROMEDA研究中,与VCd组相比,DARA联合VCd(D-VCd)方案可以显著改善AL淀粉样变性的预后,D-VCd vs. VCd:血液学达到CR率:53.3% vs. 18.1%(P<0.0001);6个月心脏缓解率:42% vs. 22%(P=0.0029);6个月肾脏缓解率:54% vs. 27%(P<0.0001)。本研究报告了ANDROMEDA研究亚洲人群(中国、日本和韩国)的亚组分析结果。
388例随机分组的患者中,60例是亚洲人(D-VCd,n=29;VCd,n=31)。中位随访时间为9.4个月。D-VCd组和VCd组的总体血液学CR率分别为59%和10%(优势比 13.2;95%CI 3.3-53.7;P<0.0001)。与VCd组相比,D-VCd组的非常好或更好的部分缓解率更高(≥VGPR;93% vs. 61%)。D-VCd组患者的主要器官恶化-无进展生存期(MOD-PFS)更优(HR 0.21;95%CI 0.06-0.75,P=0.0079)(图5)。
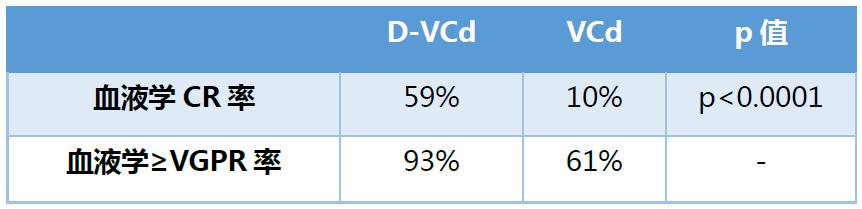
图5. D-VCd与VCd在亚洲人群中的血液学缓解
相比VCd,D-VCd方案能为患者带来更深的血液学缓解并改善其临床结局,安全性与总体研究人群一致。这些数据将支持D-VCd在新诊断为AL淀粉样变性的亚洲患者人群中的使用。
糜坚青教授总结
在目前整个血液肿瘤治疗领域中,靶向免疫治疗非常重要,2020 ASH公布了许多相关研究进展。其中单抗治疗如达雷妥尤单抗,研究显示在适合移植NDMM患者治疗方案中加入达雷妥尤单抗可使MM患者达到深度且持久的缓解,没有发现新的安全性事件。新诊断AL型淀粉样变性患者亚洲人群数据显示,VCd联合达雷妥尤单抗同样可获得更深层的血液学缓解,改善临床预后,且安全性与整体研究人群一致。双抗治疗如BCMA x CD3双特异性抗体Teclistamab,最新I期研究结果显示,其用于治疗R/R MM患者具有良好的疗效和安全性。除此之外,CAR-T治疗如Cilta-cel,CARTITUDE-1的Ib/II期研究显示,其可使经过多线治疗的MM患者产生早期、深度和持久的缓解。与此同时,MRD检测与免疫疗法相辅相成,研究显示在MM患者中,通过MRD指导临床决策可以显著改善患者临床预后,由此可见,免疫治疗联合MRD检测将如虎添翼,为多发性骨髓瘤患者带来更多的临床获益。


糜坚青 教授
-
教授,主任医师,博士生导师
-
上海交通大学医学院附属瑞金医院血液科行政副主任
-
上海血液学研究所*党**支部书记,血液中心病区主任
-
上海医药行业协会血液医学转化专业委员会主任委员
-
上海抗癌协会理事、血液肿瘤分会副主任委员
-
中华医学会血液分会委员、上海医学会血液分会委员
-
中国抗癌协会血液转化医学专业委员会常务委员
-
中国老年医学会血液分会常务委员
-
中国抗癌协会血液肿瘤专业委员会委员
-
中国初级卫生保健基金会血液病专家委员会主任委员
-
亚太医学生物免疫学会血液分会主任委员
-
亚洲骨髓瘤工作组成员
-
卫生部临床途径技术审核专家委员会评审专家
-
上海市浦江人才、上海领军人才、上海市优秀学科带头人
