
表位标记是用于研究蛋白质功能的一种方法,可以对感兴趣的蛋白质进行标记或修饰。 传统的方法是使用外源质粒过表达标记蛋白质,但这种方法通常会导致一些不良副作用,如蛋白质定位、比例和细胞生理的改变。在CRISPR/Cas9技术出现后,科学家们尝试使用CRISPR/Cas9 技术,利用同源定向修复 (HDR) 机制的方法来引入蛋白质表位标签。但 HDR 在细胞有丝分裂后效率低下,并且容易受非同源末端连接 (NHEJ) 途径的干扰。
为了规避外显子中indel形成的负面影响,最近,美国俄勒冈健康与科技大学Vollum研究所钟海宁团队开发了一种新的方法—— CRISPR介导的外显子插入 (CRISPR-mediated Insertion of Exon)简称CRISPIE。CRISPIE采用了靶向内含子序列的策略,该策略将所需的表位标签包含在一个设计的外显子模块中,外显子两端分别以内含子序列为基础。当将该供体模块插入到靶向位点的内含子序列中时,表位标签通过RNA剪接包含在内源性转录本中,同时基本消除了插入处的indel事件。因此,CRISPIE过程在mRNA水平和蛋白质水平上实现了近乎无误差的内源性蛋白质表位标记。
CRISPIE技术具有简便、高效、无需外源性蛋白质、可在大多数细胞类型中使用等优点。本篇protocol向我们展示了利用CRISPIE技术在人类U-2 OS细胞中实现人类β-肌动蛋白(ACTB)N-端标记的详细步骤。相关工作于2022年3月以“Labeling Endogenous Proteins Using CRISPR-mediated Insertion of Exon (CRISPIE)”为题发表于 Bio-protocol 。

一、材料与试剂
1. 10 cm表面处理组织培养皿( FisherbrandTM ,目录号:FB012924) 2. 1.7 mL微量离心管(Thermo Scientific,目录号:21-402-903) 3. 35 mm细胞培养皿( FalconTM ,目录号:353001) 4. 无菌聚苯乙烯一次性分装移液管 (FisherbrandTM,目录号: 13-678-11 [25 mL]; 13-678-11E [10 mL]; 13-678-11D [5 mL])
5. 一次性硼硅酸盐玻璃巴斯德移液管 (FisherbrandTM,目录号: 13-678-20C)
6. 人类 U-2 OS 细胞 (ATCC,目录号: HTB-96)
7. pX330-U6-Chimeric_BB-CBh-hSpCas9 质粒 (Addgene,目录号: 42230)
8. pKanCMV_mRuby3 质粒 (Addgene,目录号: 172854)
9. 脂质体转染试剂 Lipofectamine 2000 (Invitrogen,目录号: 11668019)
10. McCoy's 5A 培养基 (ATCC,目录号: 30-2007)
11. Opti-MEM 培养基 (Gibco,目录号: 31985062)
12. 胰酶/EDTA 消化液 (Gibco,目录号: 25300062) 13. 胎牛血清 (FBS) (Hyclone,目录号: 26140079)
14. 70% 乙醇溶液(去离子水制备)
15. BbsI-HF 酶 (New England Biolabs,目录号: R3539S)
16. 多聚核苷酸激酶 (PNK) (New England Biolabs,目录号: M0201S)
17. 牛肠碱性磷酸酶 (CIP) (New England Biolabs,目录号: M0290S)
18. 10× Cut Smart 缓冲液 (New England Biolabs,目录号: B6004S)
19. T4 DNA 连接酶缓冲液 (New England Biolabs,目录号: B0202S)
20. Quick 连接试剂盒 (New England Biolabs,目录号: M2200S)
21. 分子生物学级水 (HyClone,目录号: SH30538.03)
22. Carbenicillin (Sigma,目录号: C1389-5G)
23. Ampicillin (Sigma,目录号: A9518-25G)
24. Kanamycin (Sigma,目录号: 11815024)
25. DH5α 感受态细胞 (ThermoFisher Scientific,目录号: 18265017)
26. Luria-Bertani (LB) 培养基胶囊 (制作平板用) (Sigma,目录号: 113002231)
27. Kanamycin LB 平板 (30 μg/mL;自制)
28. Ampicillin LB 平板 (50 μg/mL;自制)
29. 胰蛋白胨 (Tryptone) (Fisher Scientific,目录号: BP9726-500)
30. 氯化钠 (Sodium chloride) (Thermo Scientific,目录号: J2161836)
31. 酵母提取物 (Yeast extract) (Gibco,目录号: 211929)
32. 大肠杆菌增强培养基 (Terrific Broth, TB) 粉末 (Sigma,目录号: 1016290500)
33. 甘油 (Glycerol) (Sigma,目录号: G5516-500ML)
34. 玻璃珠 (Fisher Scientific,目录号: 11-312C)
35. 冰桶
36. QiaQuick 纯化试剂盒 (Qiagen,目录号: 28706)
37. Qiagen Miniprep Kit (Qiagen,目录号: 27104)
38. SOC 培养基 (详见配方)
39. TB 培养基 (详见配方)
40. 添加 FBS 的 McCoy's 5A 培养基 (详见配方)
二、仪器与软件
实验仪器
1. 水浴锅(37°C和42°C)
2. 组织培养箱
3. 细菌培养箱
4. 制冰机
5. 涡旋混合器(Fisher)
6. 移液器(Drummond)
7. 生物安全柜
8. 真空源(如真空泵)
9. 真空分离器(Vac-ManTM真空分离器,Promega,目录号:A7231)
10. 热循环扩增仪(PCR仪)
11. 桌面离心机
12. 荧光显微镜
实验软件
1. SnapGene( SnapGene 软件;https ://snapgene.com ) 2. CRISPick(Broad研究所, https: //portals.broadinstitute.org/gppx/crispick/public )
三、实验流程
A. 使用 CRISPick 设计 Cas9 sgRNA
1. 首先需要的 CRISPIE 质粒是一个表达 Cas9 和目标特异性 sgRNA 的表达质粒。这允许 Cas9 特异性地切割目标基因组位置。在通过 in silico 方法设计 sgRNA 后,将其合并到空白的 Cas9-sgRNA 表达载体 pX330(Addgene #42230)中。
2. 为了选择一个 sgRNA 目标序列,我们使用 Broad Institute 的 CRISPick(https://portals.broadinstitute.org/gppx/crispick/public;请注意,其他 sgRNA 设计网站/软件也可能有效)。
3. 在起始页面上,选择所需的参考基因组、CRISPR 机制和 Cas9 酶的来源物种(图1)。
注意:在我们的协议中,我们使用“Human GRCh38”参考基因组、CRISPRko 和 SpyoCas9。
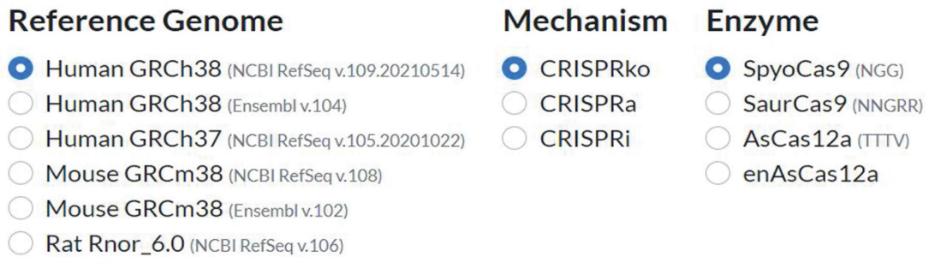
图1. 指定CRISPick参数,用于CRISPIE
4. 点击“bulk mode”并将目标序列粘贴到“Target(s)”框中,或使用网站上列出的接受的目标格式引用target。
a. 批量模式允许将大型/多个目标序列粘贴进去(图2)

图2. 将target序列(FASTA格式)粘贴到批量模式输入框中
b. 我们建议创建包含注释sgRNA结合位点的target序列SnapGene文件。这在设计多个要筛选的sgRNA以及分析最终插入序列时非常有用。
c. 将target序列的5'和3'端各包含约200个碱基,以确保考虑了所有的sgRNA选项。
d. Target序列需要位于基因内含子中。CRISPIE的内在优势在于剪切点在内含子区域内的插入连接处的插入缺陷会被剪切掉,而当插入缺陷位于外显子中时,这是不可能的。当靶向基因内含子时,选择一个不会在引入供体模块后破坏蛋白质结构的内含子是很重要的。N和C末端标签分别嵌入到基因的第一个或最后一个内含子中。如果基因的第一个外显子中存在大量编码序列,CRISPIE将难以标记其N末端。在基因内或C末端处进行靶向可以作为替代方案。此外,为了在感兴趣基因的C-末端进行标记,需要将该基因的最后一个外显子的编码序列包含在给体模块中。这些都是在使用CRISPIE时需要考虑的约束条件。然而,与基于HDR的插入相比,CRISPIE需要包含的序列通常要短得多。
5. 选择所需的“CRISPick配额”。
注意:如果希望从输出中手动选择所需的 sgRNA,请跳过此步骤。否则,此工具会使用算法根据设定的标准(例如脱靶效应、切割位置等)推荐前几个最佳的 sgRNA(请确认翻译是否准确?the top sgRNA)。
6. 选中“report unpicked sequences?”框(图 3)。

图3. 通过设置CRISPick配额指定潜在sgRNA位点的数量
勾选“Report unpicked sequences”以获取所有潜在的sgRNA及其特性(由CRISPick算法确定)的文件。
7. 输出结果显示后,*载下**所需的文件:
a. “Picking Results”显示根据“CRISPick Quota”算法选出的最佳sgRNA。
b. “Picking Summary” 以表格格式提供了一个包含所有可能的sgRNA及其相关信息的全面列表。
c. “Input Target Sequence” 包含了您使用的输入文件,供您查阅。
8. 请注意,如果所选的序列将被合并到供体质粒中(用于切除模块,以便将其插入到目标基因组区域中),则可能需要包含“context sequence”(也列在Picking Results中)。context sequence是指环绕sgRNA靶向序列的一组序列,它们可能影响Cas9的结合和靶向序列的内切酶活性(见图4)。
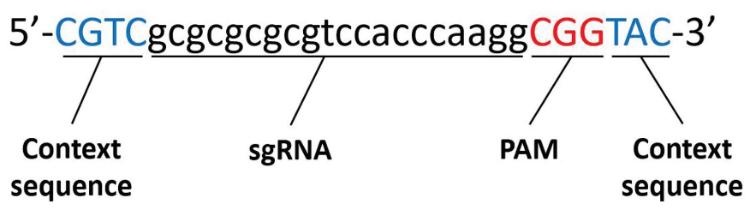
图4. 一个包含其上下文序列的sgRNA靶向序列示例
我们经验证实,在图中显示的特定上下文序列基础上,CRISPick算法可以获得高的Azimuth分数。
9. 使用 DNA 设计软件(我们使用 SnapGene),创建一个包含所需基因的文件,以便使用 CRISPIE 进行编辑。注释目标基因中的目标位点。
B. Cas9质粒的体外构建
1. 从CRISPick(或其他sgRNA设计软件)选择sgRNA序列。
2. 为了通过内置的BbsI位点将sgRNA合并到pX330质粒中,请在正向寡核苷酸的5'端添加4个碱基序列:CACC,并在反向寡核苷酸的5'端添加AAAC。
需要在体外构建具有兼容末端序列的寡核苷酸,以实现将其定向克隆至经BbsI酶消化的pX330质粒中。
3. 另外,如果sgRNA不以G开头,则在sgRNA的5'端添加一个G,这是由U6启动子启动转录所必需的。为了更清晰明了,下面提供了一个示例(图5B)。
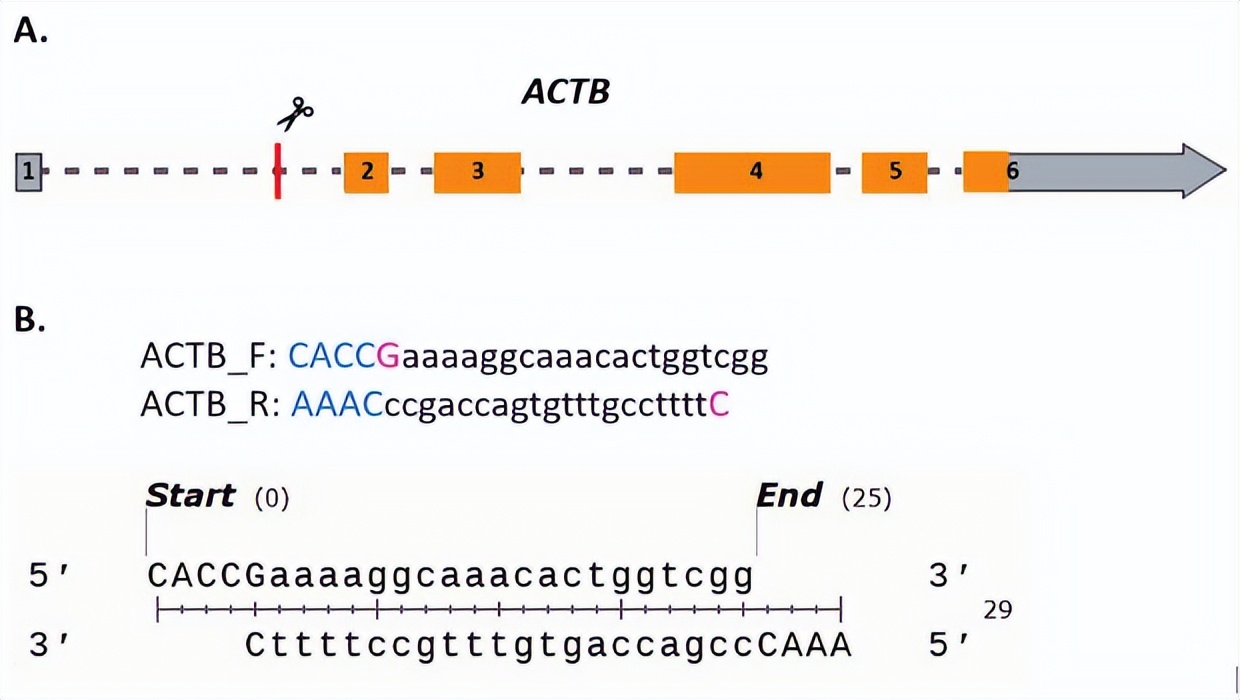
图5. sgRNA的体外设计
(A)人类 β-actin基因示意图,其中外显子编号为1-6。红色条形图示CRISPIE sgRNA的大致靶向位点。ACTB的编码序列用橙色突出显示。(B)展示了克隆针对人类ACTB内含子1的sgRNA质粒的正向和反向引物序列。sgRNA序列(黑色,小写字母),用于连接到目标载体的相邻序列(蓝色大写字母)和转录起始G(品红色)被不同方式突出显示。下部分展示了退火的引物,它将被连接到pX330载体中。
C. 将sgRNA序列克隆到pX330中
1. 将载体消化、去磷酸化和纯化
a. 在37℃下进行25 μL的反应,持续3小时或隔夜消化pX330质粒(Addgene#42230)。

b. 消化后,加入0.6 μL的牛肠碱性磷酸酶(CIP),在37°C下孵育30分钟。
c. 纯化消化后的质粒。我们通常使用Qiaquick纯化试剂盒。
注意:我们建议使用HF版本的BbsI。非HF版本可能会随着时间的推移在-20℃下存储而失去效力。
2. sgRNA寡核苷酸的磷酸化和退火
a. 在PCR管中设置以下反应,以便在PCR中一步完成多核苷酸激酶(PNK)反应和退火:

b. 执行以下反应步骤:

c. 将2 μL的退火反应液稀释在198 μL的分子级水中,以便在连接反应中使用。
3. 连接退火寡核苷酸到消化的pX330质粒中
使用NEB快速连接试剂盒,制备以下反应物并在室温下孵育25分钟:

4. 使用标准方案转化和扩增含连接质粒的DH5α细胞。
a. 我们使用自制的DH5α感受态细胞。在所有冰上预冷的离心管中,将1-2 μL的连接反应加入30 μL的DH5α细胞中。在冰上放置20-30分钟。在42°C的水浴中孵育离心管恰好1分钟,然后立即在冰上放置5分钟。加入300 μL的SOC培养基,将离心管在37°C摇动250 rpm下孵育1小时。将转化反应的约200 μL平板培养在LB琼脂平板上(50 μg/mL Carbenicillin),并用玻璃珠扩散。在37°C下孵育过夜。
b. 使用所需的质粒小提技术(例如,Qiagen Miniprep质粒试剂盒)选择要扩增的菌落。
c. 对小提质粒进行测序以检查sgRNA的正确插入。我们实验室使用Azenta Life Sciences(以前是Genewiz)的sanger测序服务。
D. 选择 CRISPIE 供体质粒和转染标记
1. 从 Addgene 存储库中选择哪个 CRISPIE 供体取决于目标内含子两侧的外显子的翻译阅读框。RNA 剪接可以发生在基因的单个密码子内部和之间。外显子具有剪接位点,可以位于密码子的第一,第二或第三个碱基之前(分别表示为0、1和2;图6)。

图 6. 外显子的阅读框
如图展示了两个外显子之间三种可能的剪接位点。每个三联密码子都被下划线标出,虚线下划线表示跨越内含子的密码子。
选择与插入的内含子的读码框架匹配的供体模块非常重要。根据目标位点,需要选择0-0、1-1或2-2的转移相供体外显子。在ACTB的情况下,起始密码子位于第一个(0)读码框架的外显子2上。因此,0-0供体模块是ACTB内含子1所需的理想质粒。
a. Addgene #172848(供体 B7)包含一个具有 0-0 翻译相的mEGFP
b. Addgene #172849(供体 B8)包含一个具有 1-1 翻译相的mEGFP
c. Addgene #172850(供体 B9)包含一个具有 2-2 个翻译相的mEGFP
拓展:translational phase是指外显子和内含子在翻译过程中的相对位置关系。可以翻译为“转移相”、“翻译相”。翻译过程是将mRNA转化为蛋白质的过程,该过程依赖于mRNA的读码框架。每个外显子都被视为具有读码框架的一部分,并且在该外显子中包含的第一个密码子决定了该外显子的翻译起始点。当一个内含子插入到两个外显子之间时,它会影响外显子的相对位置,因此影响翻译过程中的相对读码框架位置。translational phase用于描述两个相邻外显子在内含子插入之后的相对位置关系,其值表示两个外显子在翻译过程中的相对位移量,以三联密码子为单位。例如,0-0 translational phase表示两个外显子的相对位置没有改变,1-1 translational phase表示第二个外显子在翻译过程中相对于第一个外显子向前移动了一个密码子。
2. 上述列出的供体质粒是自我剪切质粒:它们表达一个设计的sgRNA,其靶位点与同一质粒内的供体模块相邻。然而,我们通过实验证明,一个由与基因组编辑位点相同的sgRNA位点夹杂的供体模块,但处于相反的方向,与通用供体相比可以获得大约50-100%更高的标记效率。可能是因为当目标特异性序列以相反方向定位时,它可以促进供体向前插入,从而增加成功编辑的比率(图7)。
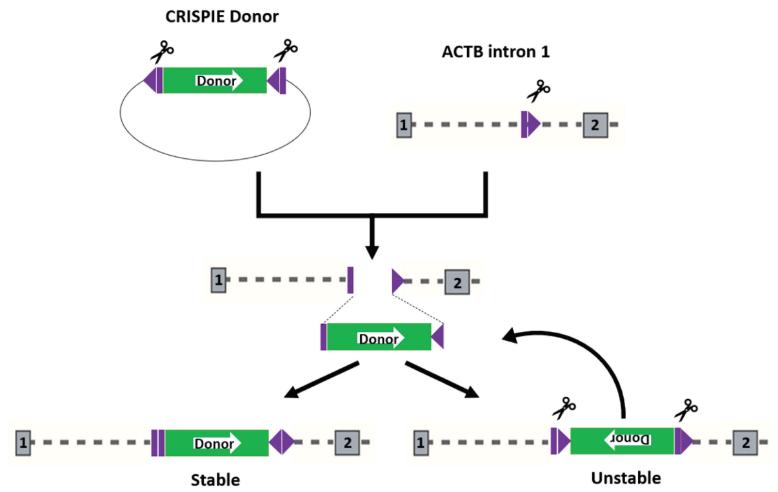
图 7. 基因组位点和供体上sgRNA靶位点的相反方向有利于将供体向前定向插入
在Cas9在基因组位点中产生双链断裂后,供体模块可以向前或向后插入。由于夹在供体模块两侧的sgRNA靶点与基因组位点上的sgRNA靶点方向相反,将供体模块向前插入会破坏夹在供体两侧的sgRNA靶点,从而形成一个稳定的插入。而将供体模块向后插入则会形成功能性的sgRNA靶点,可以进一步受到Cas9的切割,因此形成不稳定的插入(除非在插入接合点上发生了INDELs)。sgRNA 结合位点以紫色显示,Cas9 切割位点表示为紫色矩形和三角形之间的细白线。供体模块内的白色箭头表示供体模块的方向。
a. Addgene编号#172842是一个针对ACTB第一外显子特异性的mEGFP供体,用于图2所示的sgRNA。
b. 原始供体质粒是通过基因合成(使用Azenta Life Sciences,前身为Genewiz)生成的。
c. 可以通过用适当的目标特异性sgRNA序列(包括PAM和上下文序列)替换供体质粒的当前靶向位点,并使用可用的限制酶位点,生成其他靶向特异性的供体模块。通过这种方式,研究人员可以瞄准其他基因的内含子位置。可以通过替换现有供体的FP来生成具有不同标签(如不同荧光蛋白)的给体。
d. 供体序列包括标签编码外显子,其两侧是剪接和从质粒中切除供体所需的重要相邻序列(图 8)。
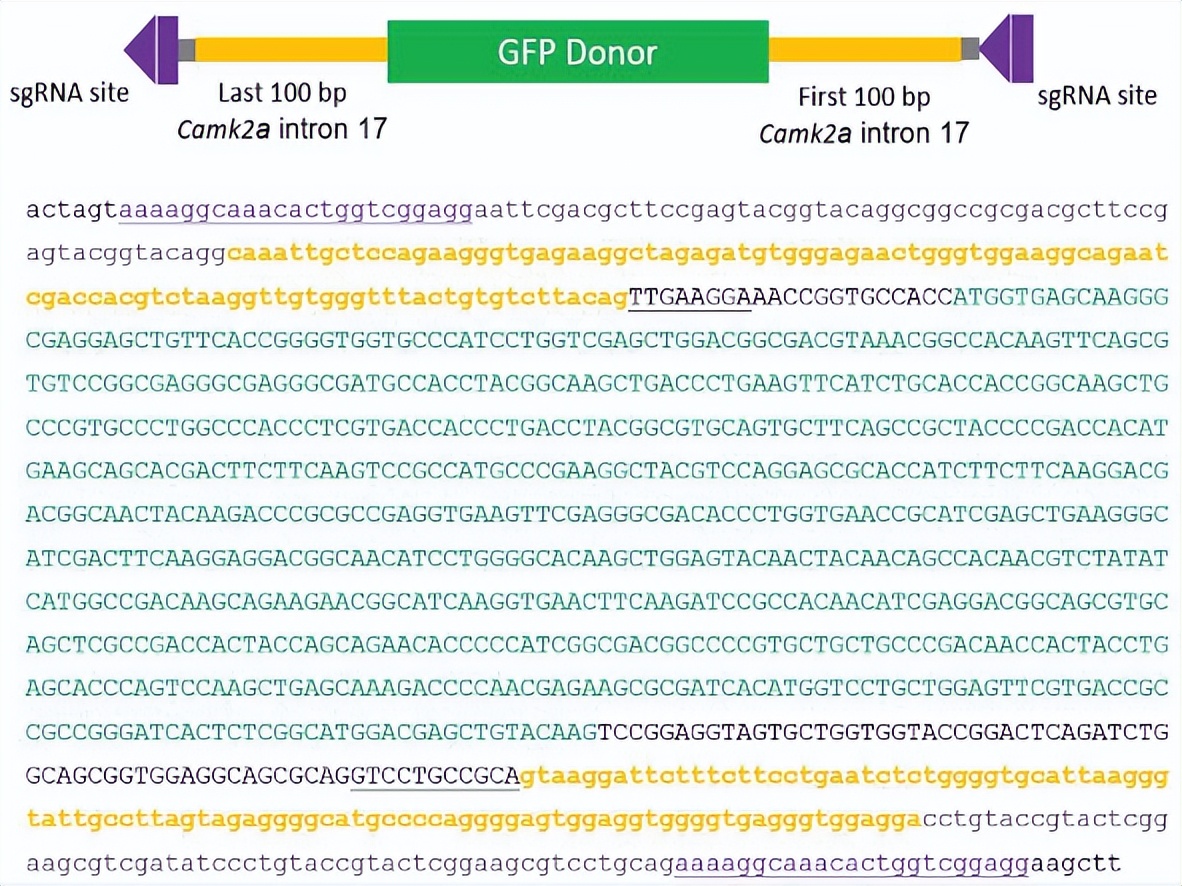
图8. 代表性CRISPIE供体模块的5'到3'序列
如图显示了供体B1 (Addgene#172842; phase 0-0)的序列。大写字母:外显子序列;小写字母:内含子序列;黄色:来自小鼠CaMKIIα(Camk2a)的内含子序列;下划线:相邻于Camk2a内含子17的外显子序列;紫色:sgRNA靶向位点;绿色:EGFP。请注意,只有外显子序列将被整合到最终的mRNA中。
3. 我们还使用mRuby表达载体 ( Addgene #172854) 作为转染标记。其他转染标记应在纳入 CRISPIE 程序之前进行表征和优化。
E. U-2 OS Lipofectamine 2000 转染
1. 在McCoy's 5A培养基(10%FBS)中培养U-2 OS细胞。将培养箱设置为37℃和5%CO 。当细胞达到约90%密度时,应每2-3天传代一次。
2. 在转染前24小时,在含2毫升McCoy's 5A培养基(10%FBS)的35毫米培养皿中播种约1.25×105个细胞,并让其过夜附着。顺时针旋转细胞五次,逆时针旋转五次,上下移动五次,左右移动五次。这确保细胞均匀涂覆在培养皿底部。我们不使用抗生素,但我们未测试抗生素是否会影响细胞生长或标记效率。
3. 开始转染前,请确保细胞达到30-50%的密度。在此范围之外生长可能会降低转染效率。
4. 对于每个转染反应,将5 μL Lipofectamine 2000与145 μL Opti-MEM培养基混合。通过涡旋混合充分混合。在室温下孵育混合物5分钟。
注意:在执行多次转染时创建一个总混合液。
5. 根据生产厂家的方案,这种lipofectamine 2000 / Opti-MEM总混合物的孵育时间可长达20分钟。
6. 对于每个转染反应,将0.2 μg的转染标记物(mRuby3;从Addgene获得)、1.0 μg的sgRNA / Cas9质粒(在上面的A-C步骤中创建)和1.0 μg的含有供体模块的质粒(从Addgene获得)分别混合到150 μL的Opti-MEM中的单独管中。可以通过从反应中排除sgRNA / Cas9质粒或含有供体模块的质粒之一来制作阴性对照。
注意:只使用微量(0.2 μg)的转染标记物是非常重要的,以防止转染标记物掩盖来自GFP标记的细胞的荧光。大多数红色荧光蛋白,包括mRuby3,会在绿色通道中产生透漏,部分原因是由于荧光团的分支成熟。同时,内源标记蛋白的荧光信号通常很暗,因此很容易被高表达的红色荧光蛋白的透漏遮挡。
7. 在5分钟的脂质体lipofectamine/Opti-MEM孵育完成后,将此混合物与DNA/Opti-MEM混合物结合,然后充分上下移液并涡旋混合。在室温下孵育20分钟。充分混合对于最佳的转染效率非常重要。
8. 将每个转染混合物(300 µL)分配到一个包含U-2 OS细胞的35毫米培养皿中,这些细胞在24小时前被传代。
9. 转染后5.5小时,小心地吸去转染培养基,向每个培养皿中加入2 mL预热的McCoy's 5A培养基(10% FBS)。在37℃和5.0% CO2下孵育30分钟。
注意:注意吸力并从培养皿的侧面添加培养基,以最小化对底部细胞的干扰。
10. 吸出培养基,向细胞中加入 2 mL 预热的 McCoy's 5A 培养基(10% FBS),然后将它们置于 37°C 和 5.0% CO2的培养箱中。
注意:这些洗涤步骤是必不可少的,因为长时间暴露于 lipofectamine 2000 会损害 U-2 OS 细胞健康。
11. 可以在转染后 72 小时评估蛋白质表达。
F. U-2 OS 细胞计数用于确定转染效率。
1. 使用 100 × 放大倍率的明场视图(10× 空气物镜 [0.3 NA] 和 10 × 目镜),选择具有规则、均匀分布生长的细胞区域。
2. 一旦找到视野,将X和Y方向置零,然后切换到400×放大倍率(40× 水浸入式物镜[0.8 NA]和10× 目镜)。
3. 切换到红色荧光蛋白(RFP)滤光片,并计算表达mRuby的任何细胞数量。仍处于相同的视野中,切换到GFP滤光片。计算表达GFP的细胞数量。
注意:我们使用奥林巴斯BW51XI直立显微镜。然而,大多数标准的荧光显微镜(如Chroma ET49002和ET49005)都应该能够工作。仅计数具有所需蛋白GFP标记的细胞是很重要的。在肌动蛋白的情况下,应清晰可见GFP-肌动蛋白的纤维(见图9),避免计数具有非特异性GFP荧光的细胞(例如,荧光渗透整个细胞),这种情况偶尔会发生,可能是由于Cas9编辑的有限特异性导致的。
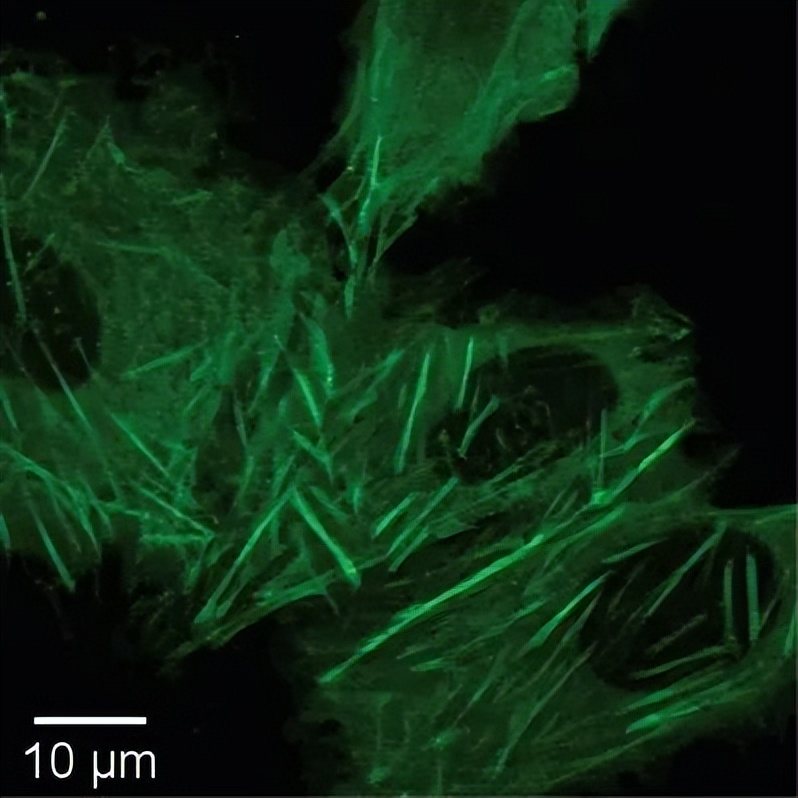
图9. 成功标记的U-2 OS细胞示例
请注意,GFP标记的肌动蛋白丝和细胞核中没有GFP。只计算具有符合所标记蛋白质特征形态分布的GFP荧光的细胞。
4. 重复上述计数方法,对12个视场进行计数,使用预先确定的、在所有样品中保持一致的光栅图案。为了减少变异,我们排除任何具有<10个mRuby阳性细胞的视场,并用额外的预定视场替换它们。
5. 可以使用可用的 Epi、共聚焦或双光子荧光显微镜对这些细胞进行活体或固定成像。
6. 标记效率由成功标记的细胞数(例如绿色)除以FOV中转染细胞(红色)的总数计算。
如果需要确定每个基因位点的标记效率,可以使用以下公式从标记效率和每个细胞的目标位点数计算得出,假设每个位点的编辑是独立的事件。
细胞标记效率 = 1 - (1 - 等位基因标记效率)拷贝数
7. 评估CRISPIE编辑在基因组中的准确性可以通过多种方法实现。我们通常使用下一代测序(NGS)。通过荧光激活细胞分选(FACS),富集GFP阳性细胞的基因组DNA和mRNA,然后使用适当的引物进行RT-PCR和PCR,以检测插入结合点。在需要的情况下,可以使用巢式PCR来提高特异性。PCR产物随后被送到NGS进行分析(我们使用Azenta Life Sciences,前身为Genewiz)。如原始出版物[6]所示,通常的结果是INDELs在基因组DNA序列中丰富存在,但在mRNA序列中几乎不存在。
a. 在供体模块的 5' 和 3' 插入连接处跨越约 2-300 bp的跨度。这确保了 PCR 将检测到相对较大的插入和缺失。
b. 我们实验室使用自定义的MATLAB代码对序列进行比对和编辑结果鉴定。但是,这可以通过使用现有的软件包或与NGS专家合作来完成。
四、配方
1. SOC培养基
将以下成分与搅拌棒(建议使用)混合在450 mL去离子水中:
10 g 胰蛋白胨
2.5 g 酵母提取物
0.25 g NaCl
成分混合均匀后,加入5 mL 250 mM KCl。
使用10 N NaOH调整溶液pH为7(大约100 μL)。
确保总体积为500 mL后,在液体循环下自动消毒30分钟,20 psi。
加入2.5 mL过滤灭菌的2 M MgCl2溶液。
加入10 mL过滤灭菌的1 M葡萄糖溶液。
2. TB培养基
根据瓶子上的制造商说明:
将47.6 g TB颗粒物混合在1 L的水中。
加入4 mL甘油。
一旦溶解,以20 psi的压力自动消毒30分钟。
3. McCoy's 5A培养基添加FBS(10% v/v)
将55 mL FBS加入500 mL McCoy's 5A培养基中。
注:尽管500 mL中的10%为50 mL,但添加55 mL以考虑FBS在培养基最终体积中的额外体积。这很重要,因为改变血清浓度可能会对U-2 OS细胞生长产生显着影响。
五、原文信息
Wilson, E. A., Mao, T. and Zhong, H. (2022). Labeling Endogenous Proteins Using CRISPR-mediated Insertion of Exon (CRISPIE). Bio-protocol 12(5): e4343. DOI: 10.21769/BioProtoc.4343. (点击链接,查阅原文: https://s.bio-protocol.org/56005221ebd0d081 )
六、参考文献
Cold Spring Harbor. (2018). SOC Medium. Cold Spring Harbor Laboratory Press.
Fortin, D. A., Tillo, S. E., Yang, G., Rah, J. C., Melander, J. B., Bai, S., Soler-Cedeño, O., Qin, M., Zemelman, B. V. and Guo, C. (2014). Live imaging of endogenous PSD-95 using ENABLED: a conditional strategy to fluorescently label endogenous proteins. J Neurosci 34(50): 16698-712.
Melander, J. B., Nayebi, A., Jongbloets, B. C., Fortin, D. A., Qin, M., Ganguli, S., Mao, T. and Zhong, H. (2021). Distinct in vivo Dynamics of Excitatory Synapses Onto Cortical Pyramidal Neurons and Inhibitory Interneurons. SSRN Electron J . doi:10.2139/ssrn.3837634.
Nishiyama, J., Mikuni, T. and Yasuda, R. (2017). Virus-Mediated Genome Editing via Homology-Directed Repair in Mitotic and Postmitotic Cells in Mammalian Brain. Neuron 96(4): 755-768 e755.
Roberts, B., Haupt, A., Tucker, A., Grancharova, T., Arakaki, J., Fuqua, M. A., Nelson, A., Hookway, C., Ludmann, S. A. and Mueller, I. A. (2017). Systematic gene tagging using CRISPR/Cas9 in human stem cells to illuminate cell organization. Mol Biol Cell 28(21): 2854-2874.
Zhong, H., Ceballos, C. C., Massengill, C. I., Muniak, M. A., Ma, L., Qin, M., Petrie, S. K. and Mao, T. (2021). High-fidelity, efficient, and reversible labeling of endogenous proteins using CRISPR-based designer exon insertion. Elife 10: e64911.

Bio-protocol 简介
Bio-protocol于2011年在斯坦福大学创建, 致力于搭建全球权威的、高质量的生物实验方案分享平台,以助力科学发现。 Bio-protocol 期刊是Bio-protocol旗下的一份同行评审的国际学术期刊,发表高质量的生命科学实验方案,旨在提高科研的可重复性。至今, Bio-protocol 已发表了来自全球上万名优秀科研工作者(包括多名诺贝尔奖获得者)的5000多篇实验方案,并且同 Science 、 eLife 等12家国际权威科学杂志建立长期合作关系,共同促进生命科学研究的可重复性。2019年 Bio-protocol 期刊已被PubMed Central,ESCI收录。