欢迎点击「科学网」↑关注我们!

图片来源:http://zlab.mit.edu/team.html
张锋 CRISPR-Cas9基因编辑技术的专利官司今天出结果了。美国专利局法庭(注一)宣布张锋获胜。

众所周知,Doudna在2012年六月发表论文,首次报道运用CRISPR-Cas9在试管中实现DN*片A**段的切割。6个月后的2013年1月,张锋的研究小组发表论文,在人类细胞中用CRISPR-Cas9实现基因编辑,并很快申请了专利。2016年3月,Doudna提出专利干扰诉讼,称张锋的发明显然是在她的专利基础上的事情。据报道,双方为了专利诉讼花了千万美元的律师费。
在此之前,我对张锋的了解仅仅是在韩春雨事件中听过其名而已,而且似乎有人对他的名气还存在疑问。在阅读相关资料后,我发现张锋才是CRISPR -Cas9技术的集大成者。围绕双方的争议,我写了若干博文。介绍了CRISPR-Cas9基因编辑技术,也分析了张锋与DOUDNA在CRISPR-Cas9的专利官司。相关介绍参见:《张峰专利官司科普及案情发展-叛逃者将被UC传讯》、《CRISPR基因编辑技术及张锋的贡献》、《CRISPR基因编辑技术的显然性分析》、《CRISPR基因编辑研究秘辛大起底》、《发自张锋实验室的四封CRISPR邮件》。(相关内容请点击下方 阅读原文 移步作者科学网博客了解)
在《CRISPR基因编辑技术及张锋的贡献》(见下)一文中,我结论到 【张锋首次将CRISPR-Cas9成功用于高等生物的基因编辑,其主要成果是基于2011年Charpentier的tracrRNA发现】。在2012年初,也就是Doudna论文发表前半年,张锋就已经提交了完整的真核细胞基因编辑设计。张后来的论文结果基本是基于这个设计。
事件中,张锋实验室还出了一个中国留学生背叛者,向DOUDNA提供内部消息。但这个学生提供的电子邮件等信息恰恰证明张锋在 2012年初就开始了相关真核细胞的基因编辑研究,并且明显找到了关键。而DOUDNA在其2012年论文发表之后数个月仍未能成功实现真核细胞的基因编辑,直到张锋合作伙伴CHURCH提供了真核编辑的数据之后才获得成功。
根据张锋所在布罗德研究院的声明,美国专利局法庭在2月15日宣布,Doudna针对张锋的真核细胞CRISPR-Cas9基因编辑技术的专利干扰诉求不成立。美国专利局判决称:
➤Doudna与Vilnius的专利申请只是在试管中剪切DN*片A**段,没有涉及细胞、基因组,也没有基因编辑。(The applications filed in 2012 by the Vilnius team and the Berkeley team each showed only that purified Cas9 protein and a certain purified RNA could cut a short piece of DNA in a solution in a test tube. In both cases, the applications in 2012 contained no cells, no genomes, and no editing.)
➤Vilnius的专利申请只是自然系统不能申请专利(专利必须是人脑的创造,自然现象不能申请专利)(The USPTO rejected the Vilnius application as not having significantly more than a study of the natural system and failing to describe invention.)
➤张锋的真核细胞基因编辑专利不受Doudna专利影响。
对相关技术感兴趣的读者可以参阅《CRISPR基因编辑技术的显然性分析》等博文。另外,科技时代,科学技术是财富。据报道,去年 Doudna 专利官司启动后,张锋的 EDITAS 公司股价从 $42 开始大跌,最低只有13。今天 EDITAS 大涨 30%,达到 $24。张锋的财富量在10年内可能超过到处捣房地产的美国总统川普家族。
虽然科学研究的目的是为人类文明做贡献,而不是获取,但能用科技智慧创造财富也许更能够激励人们进行科学探索。
科学网的生物学家们都有希望。加油!
注一:读者可能问,专利局怎么有法庭,这个问题我在之前解释过——这叫administrative law court.
附件:

转载本文请联系原作者获取授权,同时请注明本文来自岳东晓科学网博客。
链接地址:http://blog.sciencenet.cn/blog-684007-1033916.html
CRISPR 基因编辑技术及张锋的贡献
地球上所有细胞生物的遗传信息都储存在数字化的DNA序列中。今天,基因测序技术已经非常发达,DNA序列可以非常廉价迅速的确定。但测序只是读取数据,近年生物学最大的发现与发明之一是可编程的基因编辑技术:CRISPR-Cas9。这个技术类似于 WORD的搜索替换功能:用户输入一串字符串,程序找到匹配的字符串,然后进行删除或者替换。CRISPR-Cas9的编辑技术里,搜索匹配字符串由实验人员通过一段RNA表示,叫做导引RNA——gRNA,编辑由一个称为Cas9的蛋白根据gRNA定位完成。这个编辑系统的灵活性显而易见。Cas9蛋白是固定的,你只需要改变导引就能在不同位置对DNA进行编辑(注一)。
CRISPR-Cas9技术的来源是细菌的自然免疫系统。某些细菌在遭到病毒入侵后,能够把病毒基因的一小段存储到自身的DNA里一个称为CRISPR的存储空间。当再次遇到病毒入侵时,细菌能够根据存写的片段识别病毒,将病毒的DNA切断而使之失效。有的细菌的CRISPR系统很复杂,涉及多种Cas蛋白(Cas的意思是CRISPR-associated——与CRISPR相联的)。经过多年的研究,生物学家们终于找到了一种简单的系统,只用到一种蛋白——Cas9。接下来,他们成功地把这个细菌的系统进行改造用于动植物细胞的基因编辑。率先完成这一实际应用性开发的是张锋的研究小组。本文试图对相关技术与历史进行简单的介绍。
这里我把CRISPR之前漫长的研究历史一笔带过。简单而言,人们之前发现细菌免疫系统依靠一段很短的RNA进行识别,这段RNA称为crRNA(CRISPR RNA)。可想而知,这段crRNA包含有入侵病毒的基因识别码。
CRISPR相关研究在2011年取得了重大突破。这一年,法国女科学家Emmanuelle Charpentier报告,通过基因分析与相关实验,发现一个只有四个组件的细菌免疫系统。除了Csn1蛋白(后来称为 Cas9)与crRNA外,还发现一个他们称之为trans-activating CRISPR RNA(简称tracrRNA)的RNA。顾名思义,这个tracrRNA 起到转写-启动的功能。第四个组件是一个作用于RNA的生成,称为RNase III的蛋白。但这篇2011年的论文对各个组件的具体功能并没有完全确定。其论文中的下图显示:蓝色是Cas9蛋白,红色的是tracrRNA, 绿色+黑色线段是crRNA(其中绿色部分对应需要识别的病毒编码),黄色是RNase III。
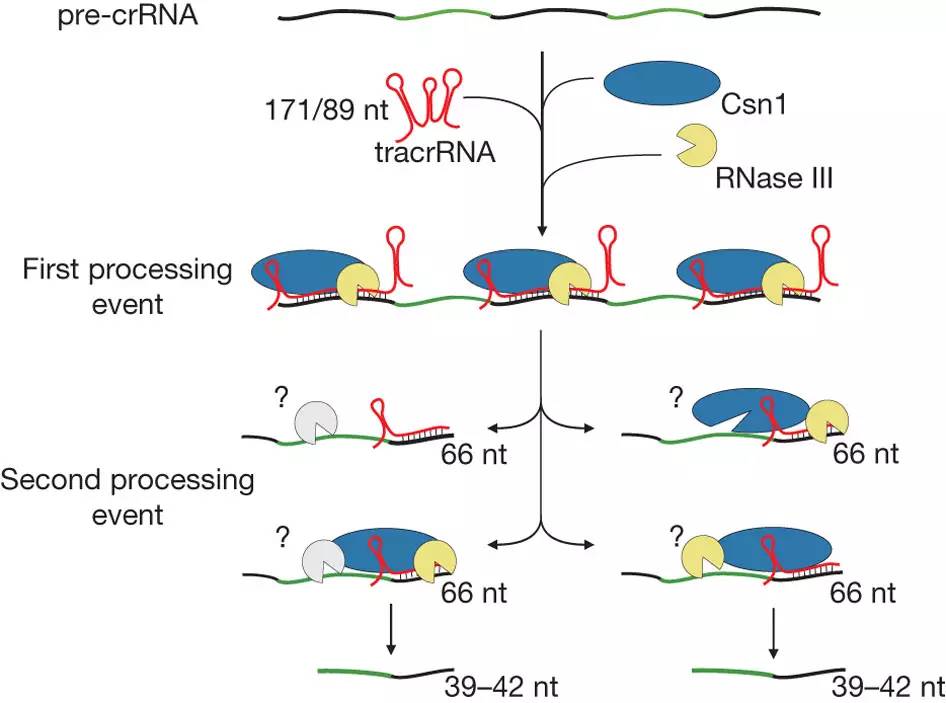
Charpentier 的论文发表后,美国加州大学的 DOUDNA(“道得娜”——有些中文文章音译成“多德娜”属于错误读音)与她的研究小组隔洋合作,进行了进一步研究,于2012年6月发表了一篇重要论文。相关研究人员与主要结果如下图:

DOUDNA、Charpentier 联合小组通过在细胞体外的试管实验发现了负责DNA切割的充分并且必要的三个部分:Cas9, crRNA与tracrRNA(不需要RNase III)。论文还确定了三个部分的作用:其中Cas9是切割机,crRNA的主要作用是定位。而tracrRNA在与crRNA耦合后启动Cas9的切割功能(activate)。他们还成功把 crRNA与tracrRNA 连起来成为一个分子,这样可以把DNA切割的组件由三个变成两个。如上图。左边是自然原核细菌中的机制,两个RNA分子。右边则是人工机制,把两个RNA给连起来了,成为一个带着一个配对圈的RNA分子。但DOUDNA等人的实验并没有在任何细胞内进行,只是在细胞体外的试管里,当然也没有在动植物等真核细胞内实验,也不知道能否可行(“it was not known whether such a bacterial system [the CRISPR-Cas9 system] would function in eukaryotic cells.”)。在该论文发表后几个月,DOUDNA等人表示在真核细胞的实验中遇到了很多困扰("many frustrations")。
现在我们知道,Charpentier 2011年的论文出来后,美国东部 BROAD研究院的张锋小组也展开了研究。在Doudna/Charpentier 2012年6月论文发表前半年,张锋在2012年1月向NIH申请了一个项目:运用Cas9系统对真核细胞进行基因编辑。张锋的项目设计如下(从其项目申请截图):
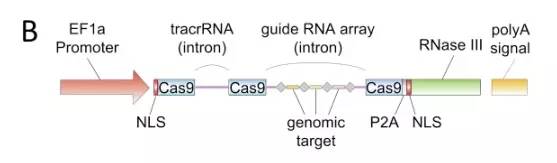
上图是一个哺乳动物 CRISPR 基因编辑系统的设计。其代码进行表达后会生成四个部分:(1)带NLS的Cas9 蛋白,(2)tracrRNA , (3)多个crRNA——注意不同颜色的线段 (图中称为 guide RNA array),(4) 带NLS的RNase III。真核细胞的特点是遗传物质在细胞核内,一般较大的蛋白是进不去的。其中 的NLS是为了使Cas9等生成后能够被拖入细胞核内。可以这么说,张锋的思路是先不管具体机制是什么,直接在高等生物上进行基因编辑实验,而且多点编辑同时进行。


张锋小组的核心人物包括:张锋、丛乐、FEI RAN
张的小组在2013年1月发表论文,报告了他们的发现:(1)他们对四个组件进行了组合实验,发现基因编辑不需要 RNase III;(2)使用Cas9 、crRNA与tracrRNA组合,成功对真核细胞实现编辑,效率相当高(indel达19%);(3)使用DOUDNA论文中的嵌合RNA (chimera),发现长的那个(chimera A )编辑效率较双RNA系统低(最高5.6%, 部分无法探测),短的那个(chimera B)不能编辑(注二)。如下图:
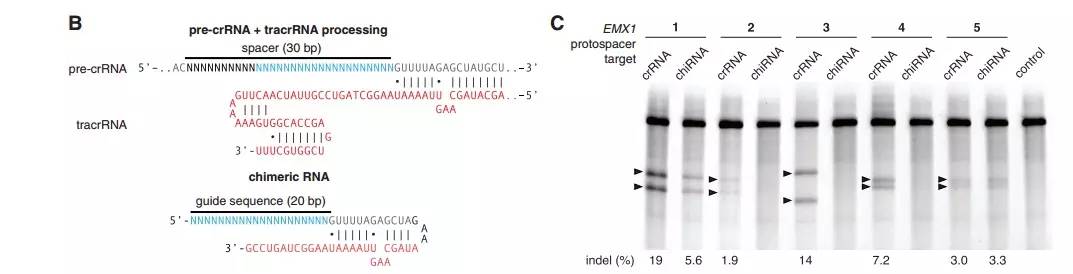
结论:
张锋首次将 CRISPR-Cas9 成功用于高等生物的基因编辑,其主要成果是基于2011年Charpentier的tracrRNA发现(注三)。
注一:Cas9 的工作机制是先找到 DNA上的一个特定的称为 PAM的序列,然后才是导引与DNA链的结合以及切割。所以,可行的DNA切割点不是任意的。PAM是一个限制。不同细菌的Cas9 蛋白的PAM序列不同,有的长些,有的只有三个字符,所以要找到可行的切割点也不是难事。
注二:后来的研究发现组合chimera RNA加长后效率更高。
注三:张锋后来又发现一个系统——CRISPR/Cpf1,蛋白比Cas9小,只需要crRNA(不需要tracrRNA), 切割位置离PAM远。
链接地址:http://blog.sciencenet.cn/blog-684007-1003348.html