#科技之巅#
CD47已成为继PD-1/PD-L1及CTLA-4之后的新一代免疫肿瘤学疗法的热门靶点。成为了不少药企梦想中的蓝海市场,也被寄予了 “下一个PD-1” 的称号,近两年更是频出重磅交易,近百亿美金押注其中。
1.CD47靶点
CD47又称整合素蛋白相关蛋白(integrin-associated protein,IAP),属于免疫球蛋白超家族,是一种具有糖基化的跨膜蛋白,由胞外可变区、跨膜区和亲水羧基端胞内区构成。广泛表达于多种癌细胞表面,胞外区可结合的配体有整合素、SIPRα和TSP1 等,其中SIRPα主要表达于巨噬细胞、树突状细胞等细胞膜表面,二者结合后, 通过传递“别吃我”的信号抑制巨噬细胞的吞噬作用。而且还可通过促进肿瘤内血管增生、抑制效应 T 细胞等机制促进肿瘤细胞增殖和扩散。 CD47抗体因可以阻断此信号,使巨噬细胞攻击肿瘤细胞,故成为目前最有开发前景的肿瘤免疫靶点之一。但CD47抗体在攻击肿瘤细胞的同时,会与正常红细胞的结合从而引起血液学副作用,如 严重贫血,这使得CD47抗体研发和临床应用严重受限 。
CD47和PD-1分别靶向肿瘤免疫治疗中发挥主要作用的两大免疫细胞类群,CD47抗体主要调节巨噬细胞,PD-1抗体主要调节T淋巴细胞。CD47在多种实体瘤细胞及恶性血液瘤细胞上呈现高表达,而且其表达水平与疾病进展呈正相关。这一广泛表达性意味着CD47或将是继PD-1之后肿瘤治疗领域的下一个重要靶点,CD47通路药物理论上可以与PD-1药物一样用于多类型癌症治疗,与PD-1一样具备成为“神药”的潜质。凭借与PD-1相似的广谱治疗特性,CD47药物一旦成功获批上市,其潜在市场也将达到与PD-1接近的规模。
目前靶向CD47药物单药和 联合治疗 在在白血病、淋巴瘤、肺癌、肝癌等常见血液肿瘤和实体瘤的靶向治疗中均显示出良好的抗肿瘤疗效。全球各地已有无数以CD47为靶点的候选药物正处于临床前及临床开发阶段,但目前仍无获批准的抗CD47疗法。
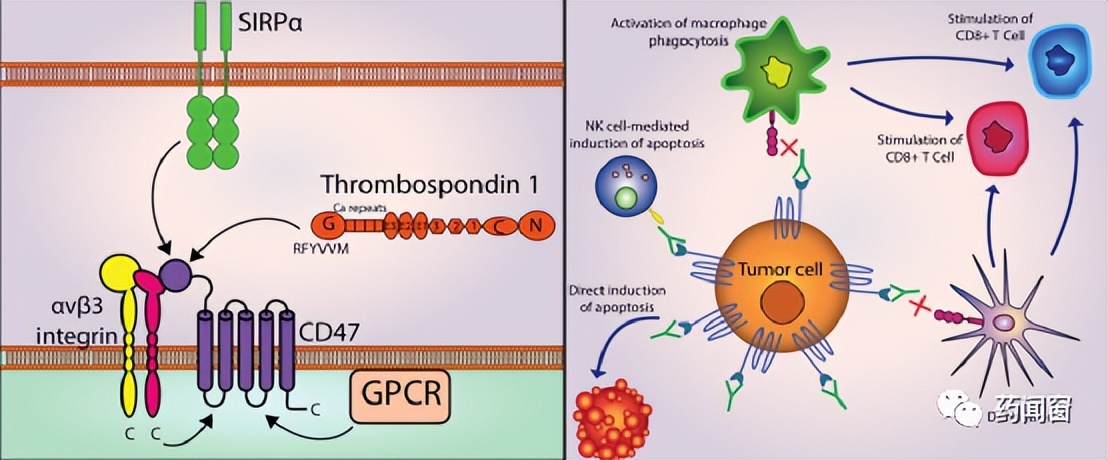
图1 CD47靶点作用机制
2.CD47研究现状
虽然全球范围内尚无CD47单抗获批上市,但据不完全统计,约有超过20家公司正在开发针对CD47或其配体SIRPα的药物,包括单克隆抗体、双特异性抗体、融合蛋白和小分子化合物等,其中10款以上已进入临床研究阶段,最快者已进入临床研究Ⅲ期阶段。针对CD47的开发难点,各大药企选择不同的解决路径,曙光渐现。根据ClinicalTrails以及CDE数据统计显示,截至2021年7月,全球针对靶点CD47药物上市的临床研究达到22个,临床前更是有42个。
围绕CD47巨大金额交易:
- 2020年3月,吉利德公司以49亿美元收购先驱公司Forty Seven针对CD47靶点的格罗格单抗(Magrolimab),其目前研究进展最快,用于治疗MDS的试验已经进入临床Ⅲ期,但副作用较大(贫血发生率高达40%左右);
- 2020 年 7 月,SciClone Pharmaceuticals(赛生医药)与Epicent Rx 公司宣布就 RRx-001达成大中华区的独家授权许可协议,涉及金额高达 1.2 亿美元。这是一款靶向CD47-SIRPα的小分子免疫疗法,目前正在进行针对小细胞肺癌适应症的Ⅲ期临床试验。
- 2020 年 9 月, 辉瑞 股权投资Trillium Therapeutics近2500万美元,而Trillium Therapeutics公司的重点品种即为CD47单抗的TTI 621和TTI 622。
- 天境生物突破性地发现了一种独特的CD47抗体来佐利单抗,lezopaimab(TJC4)。其能有效地靶向肿瘤细胞,同时将对红细胞产生的不良影响降至最低,从而避免严重贫血。目前,除了正在中国进行的急性骨髓性白血病(AML)临床试验以外,天境生物同时也在美国开展来佐利单抗与Keytruda®(派姆单抗)联合治疗实体瘤以及在中国开展来佐利单抗与Rituxan®(利妥昔单抗)联合治疗淋巴瘤的研究。2020年9月,艾伯维公司与天境生物CD47单克隆抗体TJC4达成全球战略合作。艾伯维将获得TJC4在大中华区以外的的国家及地区开发和商业化的许可权,天境生物保留大中华区的开发和商业化权利。艾伯维的对价为:1.8亿美元首付款,额外支付2000万美元作为Ⅰ期临床该研究结果的里程碑付款;最高17.4亿美元的里程碑付款。另外,未来艾伯维有权优先选择进一步开发和商业化目前天境在研的两款基于lemzoparlimab的双特异抗体,潜在交易不低于10亿美元。TJC4高达20亿美元的海外授权,显示了艾伯维对天境生物CD47的认可和渴望。
- 2020年10月,国内药企宜明昂科完成了礼来亚洲基金领投的2500万美元B轮投资,而融资的主要目的即主要用于推进IMM01(SIRPa-Fc)、IMM0306(CD47xCD20 mAb-Trap) 以及 IMM2510(VEGFxPD-L1 mAb-Trap) 三个项目的临床试验研究以及后续几个基于新靶点的单抗、双抗项目临床前研究。
- 2021年8月 辉瑞 (Pfizer)和Trillium Therapeutics公司联合宣布,双方已经达成协议,辉瑞将斥资约22.6亿美元,收购Trillium公司,获得其阻断CD47-SIRPα信号通路的两款在研疗法。
全球CD47靶点研究情况
如表1,针对CD47靶点,多家生物医药公司在开发不同类型疗法,作用机制包括抗CD47单克隆抗体,靶向CD47的融合蛋白,调节CD47/SIRPα蛋白的小分子药物以及靶向CD47信号通路的双特异性抗体。它们用于治疗的癌症类型除了血液癌症以外,还包括多种实体瘤。
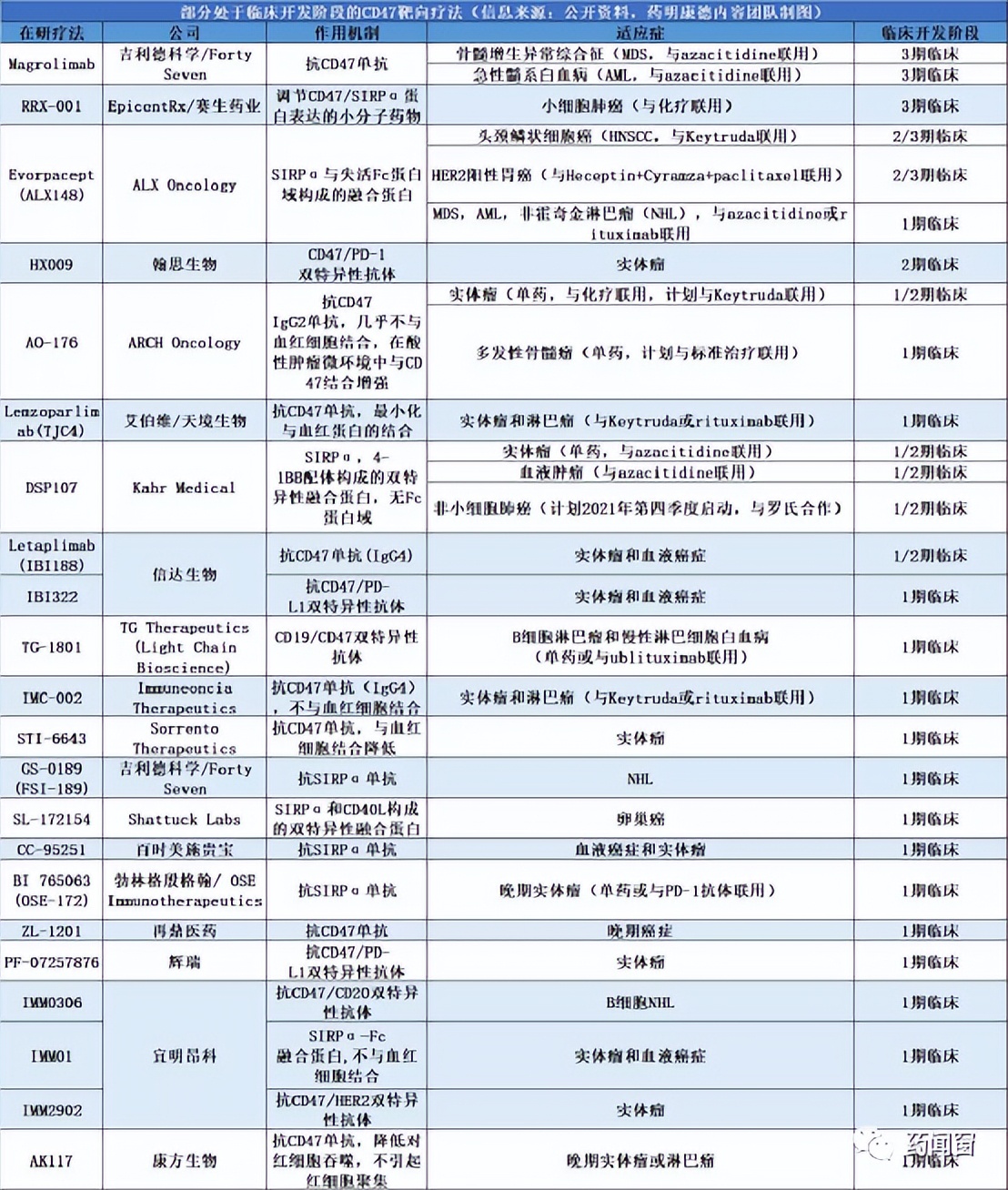
表1 部分CD47靶点疗法情况
除了上表所述的部分研究进展,国内针对CD47靶点的主要研究进展如表2。在降低阻断CD47-SIRPα信号通路的毒副作用方面,可以看到多种研发策略。一种方法是通过对抗CD47抗体的筛选,找出能够与肿瘤表面CD47结合,但是不与血红细胞结合的单克隆抗体。此外,有些公司采用了去除Fc蛋白域或让其失活的方法来降低疗法的毒副作用(例如ALX Oncology的evorpacept和Kahr Medical公司的DSP107)。因为以往的研究显示,抗体的Fc端是导致血红细胞凝集或者被巨噬细胞吞噬的主要原因。 不过在是否保留Fc蛋白域方面,不同的公司有不一样的选择,不少公司选择保留Fc蛋白域,用其它方法降低毒副作用。这些策略孰优孰劣,仍然需要在临床试验中进行验证。
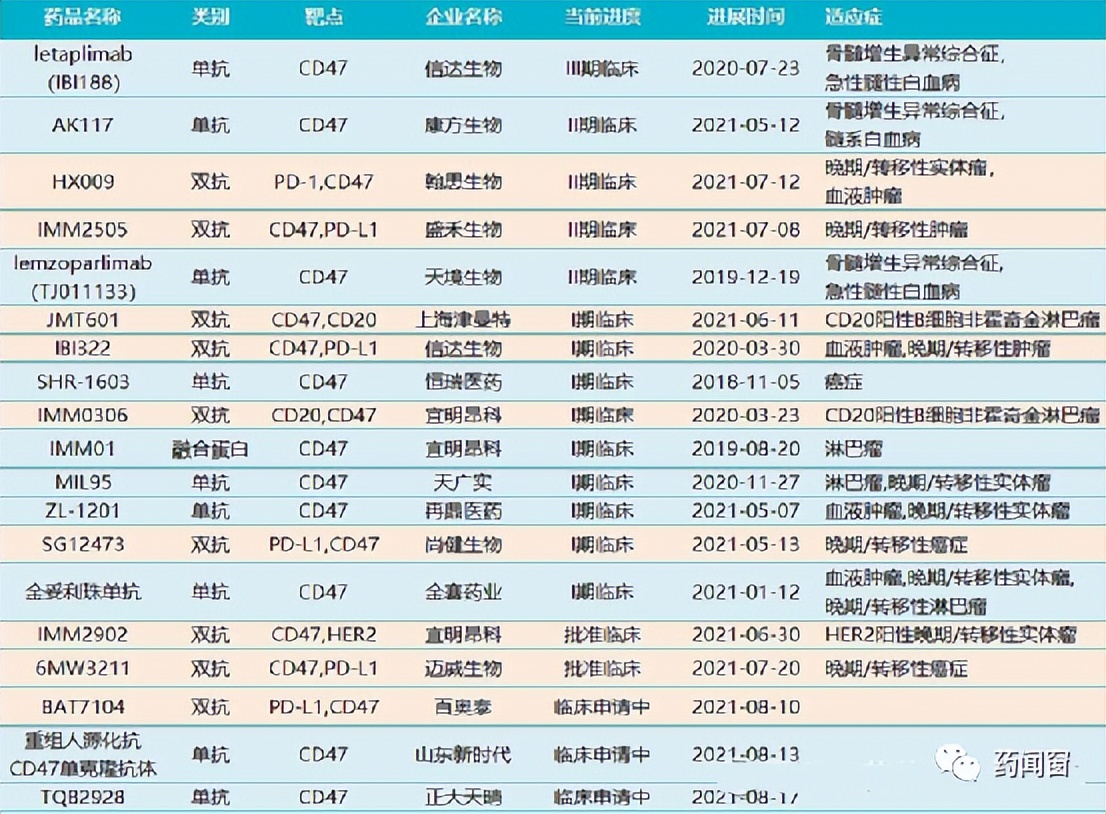
表2 国内CD47靶点疗法情况
在增强疗法的抗癌能力方面,多家公司采用了双特异性分子的策略,这些双特异性分子可以是抗体或者与抗体结构相似的融合蛋白。它们一方面可以阻断CD47-SIRPα信号通路,另一方面可以与另一个靶点相结合。这个靶点可以赋予双特异性分子更好的靶向性(例如靶向CD19或CD20),阻断其它免疫检查点蛋白的功能(例如靶向PD-L1/PD-1),或者增强激发免疫系统的能力(例如激活共刺激受体4-1BB)。它们从不同方面提高了CD47靶向疗法的特异性和抗癌活性。
靶点CD47的单一疗法和联合疗法具有独特的作用机制,越来越多的新药已开展临床研究,但多数仍处于早期阶段,一方面显示该领域具有极大的治疗潜力,临床上对新型、安全、有效的肿瘤免疫治疗药物和技术的需求强烈;另一方面因为CD47靶点潜在的风险问题,其中不少企业也在其中碰了壁,停止了相关研究试验。尽管如此,但众多药企依旧看好该靶点背后巨大的市场前景和应用价值。最终哪款CD47药物能够率先上市,为患者带来福音,我们拭目以待。