关注公众号:佰傲谷BioValley,获取更多优质文章!
近日(3月1日),Athenex发布公告表示,FDA已经就该公司的转移性乳腺癌疗法——口服紫杉醇+Encequidar的新药上市申请(NDA)下发完整回应函(CRL),拒绝该疗法上市。
根据公告内容,拒绝的主要原因是FDA担心相比静脉注射紫杉醇,口服紫杉醇可能会增加中性粒细胞减少相关后遗症的安全风险。除此之外,FDA还对盲态独立中心评估(BICR)得出的19周客观缓解率(ORR)的主要终点结果的不确定性表示关切。FDA认为BICR在进行数据整合/调节与重读过程中可能存在难以测算的偏见。
由此,FDA要求Athenex在可以代表美国转移性乳腺癌人群的患者群体中开展一项新的高质量(adequate and well-conducted)临床研究。FDA认为,如果想要获得批准,就需要采取额外的风险缓解策略来改善产品的毒性问题,包括剂量优化和/或排除被认为具有高毒性风险的患者。
口服紫杉醇+Encequidar(Oraxol)
口服紫杉醇+Encequidar又名Oraxol,最早由韩美药品基于其口服药物发现技术Orascovery开发。2011年,Athenex以750万美元首付款获得了Oraxol的全球开发权(除韩国外)。
机制上来看,该疗法大体思路为通过Encequidar改变紫杉醇的体内药动学,增加其生物利用度。
P-糖蛋白是一种跨膜糖蛋白,具有“药泵”功能,可以通过与药物和ATP酶结合,将细胞内的药物泵出细胞外,减少细胞内的药浓度,使细胞产生耐药。而Encequidar就是一种P-糖蛋白(P-gP)*制剂抑**,通过竞争性结合P-糖蛋白,降低其活性,使得疏水*药性**物顺利透过细胞膜进入血液循环,增加生物利用度。并且Encequidar不会被吸收,可以最小化其副作用。

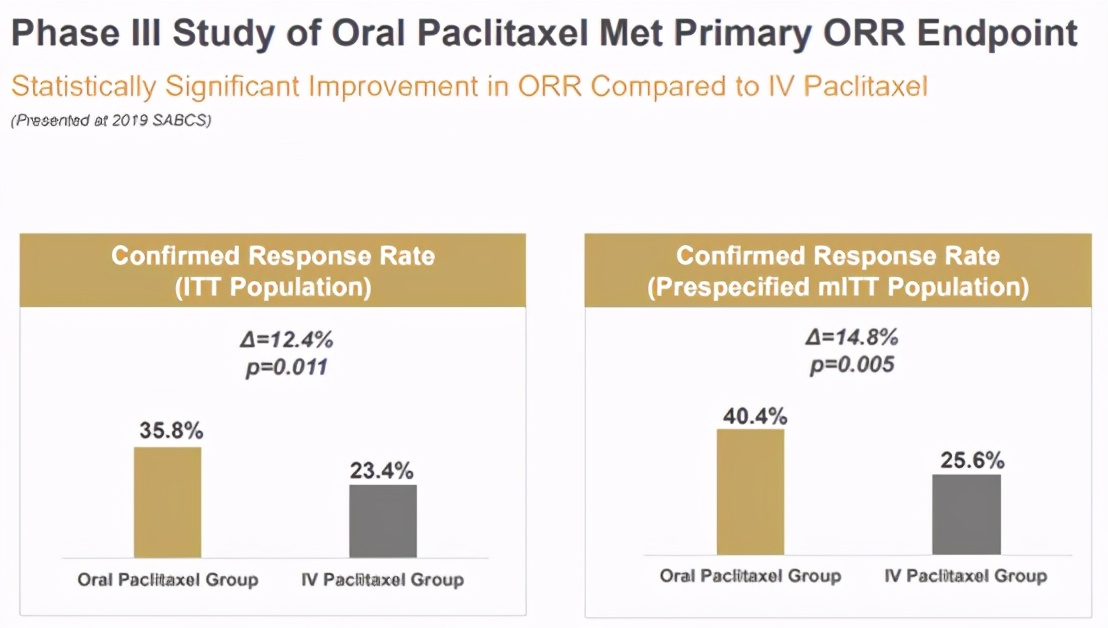
去年9月,Athenex宣布FDA已经受理了口服紫杉醇+Encequidar的新药上市申请,适应症为转移性乳腺癌,并授予加速审批资格。按照原计划,FDA应该在2021年2月28日前做出回复。到了2020年12月,Athenex在圣安东尼奥乳腺癌大会(SABCS)年会上分享了用于支持该产品上市的III期临床研究结果。该研究共入组402名意向治疗患者,并按照2:1比例分别分配于口服紫杉醇+Encequidar(OPE)治疗组和静脉注射紫杉醇(IVP)对照组。结果显示,意向治疗人群中,OPE治疗组ORR为35.8%,IVP对照组为23.4%。
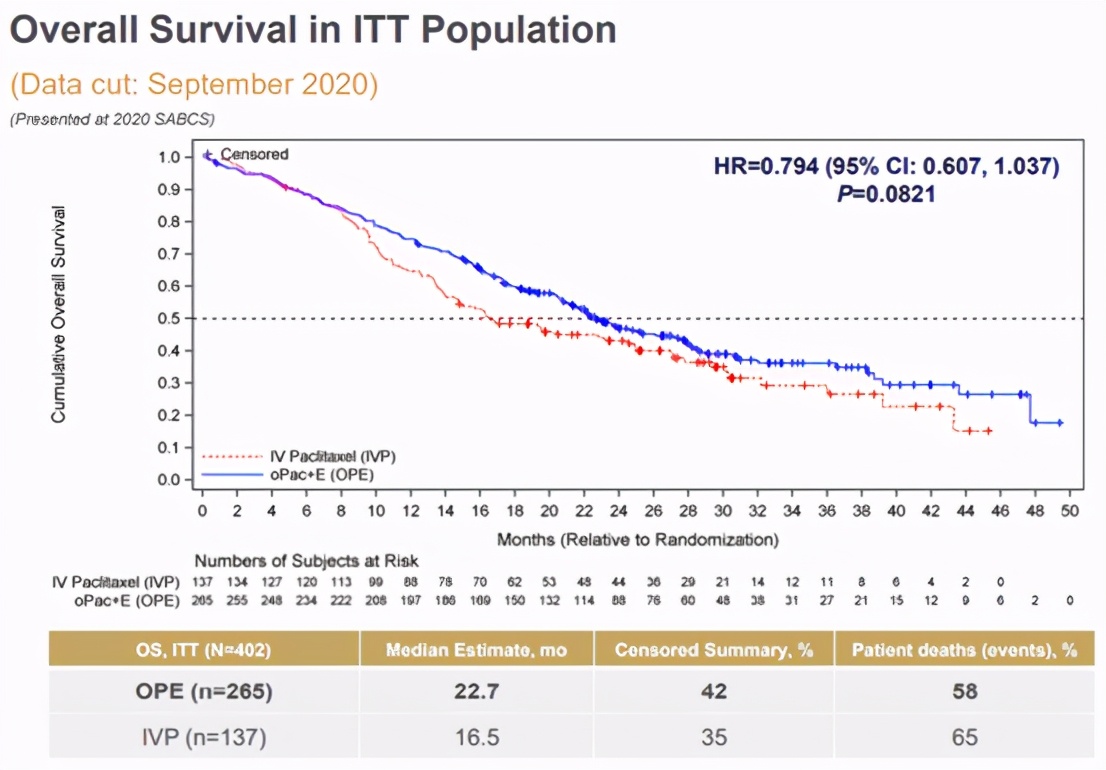
OS方面,OPE治疗组中位估值为22.7月,IVP对照组为16.5个月。
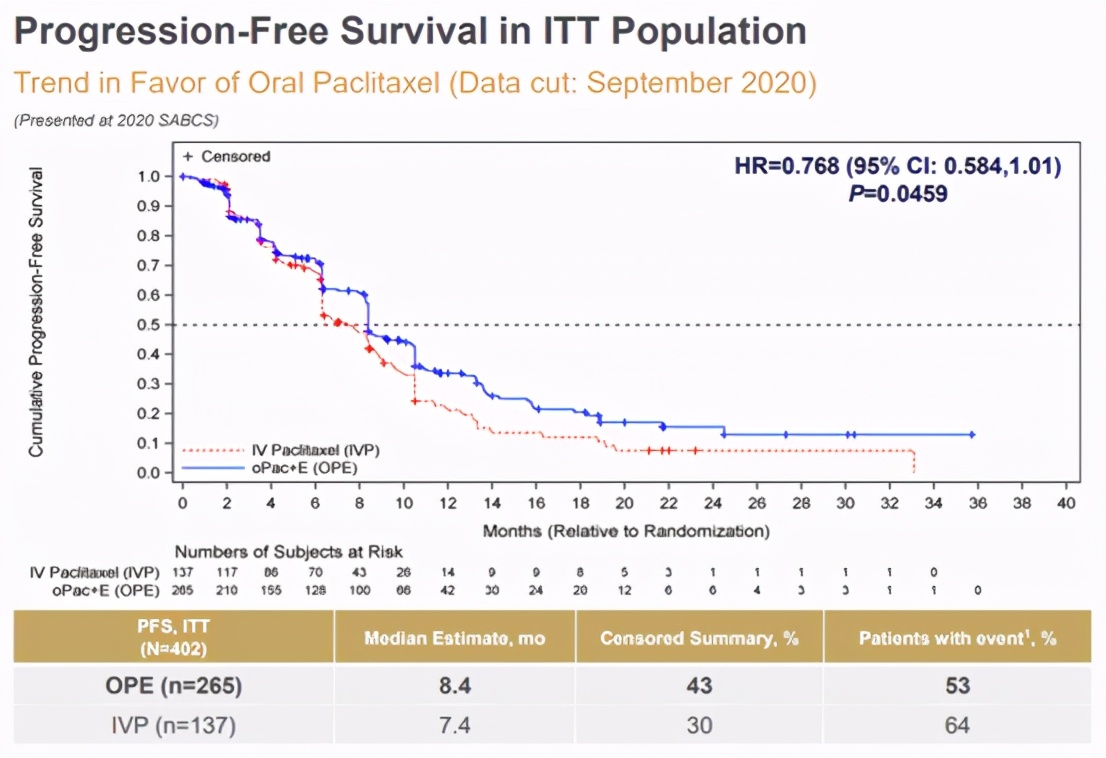
PFS方面,OPE治疗组中位估值8.4个月,IVP对照组为7.4个月。
安全性方面,OPE治疗组和IVP对照组的神经病变不良事件总体发生率分别为22.0%和64.0%。
市场反应
受此利空,Athenex股价腰斩。
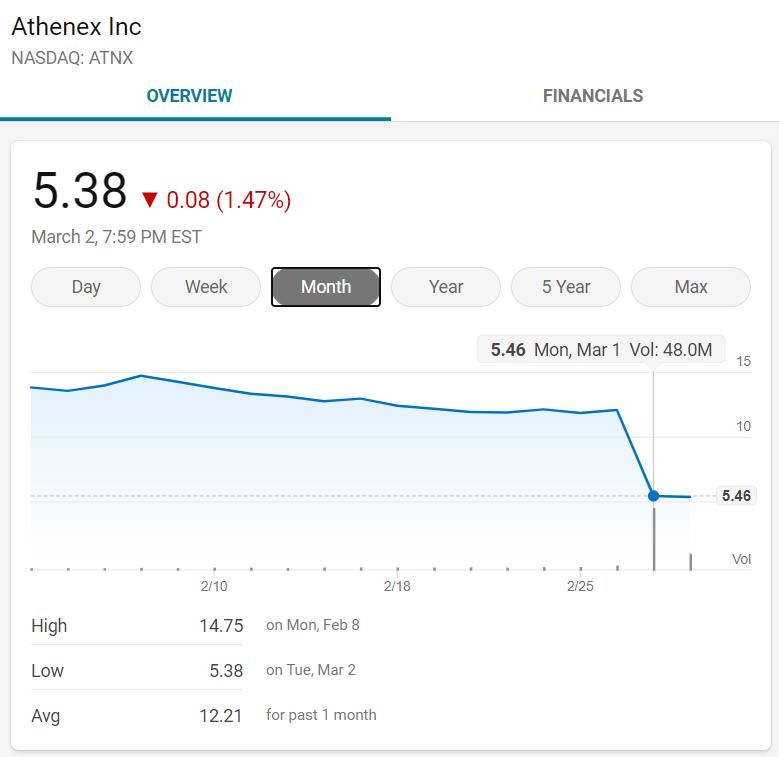
多年来,口服紫杉醇+Encequidar作为Athenex的主要管线,对其市场前景的预估是公司所依赖的重要资金来源。2019年10月,做空机构Viceroy Research曾经发布了一篇做空报告,对Athenex的经营情况和产品发出质疑。
如今,随着FDA拒绝了该产品的上市申请,并且措辞严厉的要求公司开展新的“高质量”临床研究,让这份沽空报告显得十分有趣,其中提出的质疑都能对应到FDA此次在CRL中表现出的担忧。
首先,关于FDA提到的“高质量”,Viceroy Research在报告中认为该产品临床研究中以紫杉醇单药方案作为对照组的设计早在上世纪90年代就已经过时了。
之后,对于FDA强调要针对美国患者进行研究,报告提到现有的临床研究中没有包含美国患者,并认为Athenex之所以要在南美,中美,北美和多米尼加进行临床是因为当地护理标准相比美国更低,美国患者不可能被引诱去接受一种过时的对照组治疗方案。
最后,针对FDA提出毒性担忧,报告中提到Athenex的副作用似乎比美国市场上的白蛋白紫杉醇Abraxane具有更严重的副作用,包括报告了更多的4级中性粒细胞减少,3级呕吐和未确定的胃肠道并发症,而这些副作用可能危及患者生命或者需要住院治疗。
除此之外,报告还认为Athenex宣传的口服紫杉醇+Encequidar可以改善患者生活质量的说法也站不住脚,原因是患者在治疗后仍然需要静脉注射或口服治疗并发症。并且疗法给药机制所依赖的Encequidar成分并没有获得过FDA的审批。由此,FDA可能要求Athenex提交有关该成分的NDA。
其他相关
而在国内,该产品的临床早在2017年7月就获得了CDE受理。根据Athenex官网信息,基本确定这里的紫杉醇胶囊就是此次被拒批的口服紫杉醇+Encequidar疗法。

2019年12月,广州香雪制药以3000万美元首付款,不超过1.1亿美元的研发里程碑款,不超过4000万美元的销售里程碑款与授权使用费,以及按销售净额12%至20%的梯度分成获得了Athenex口服紫杉醇(Oraxol),口服伊立替康和KX2-391软膏(适应症:光化性角化病)在中国内地,香港和澳门区域开发和商业化上述在研产品的独家权利。
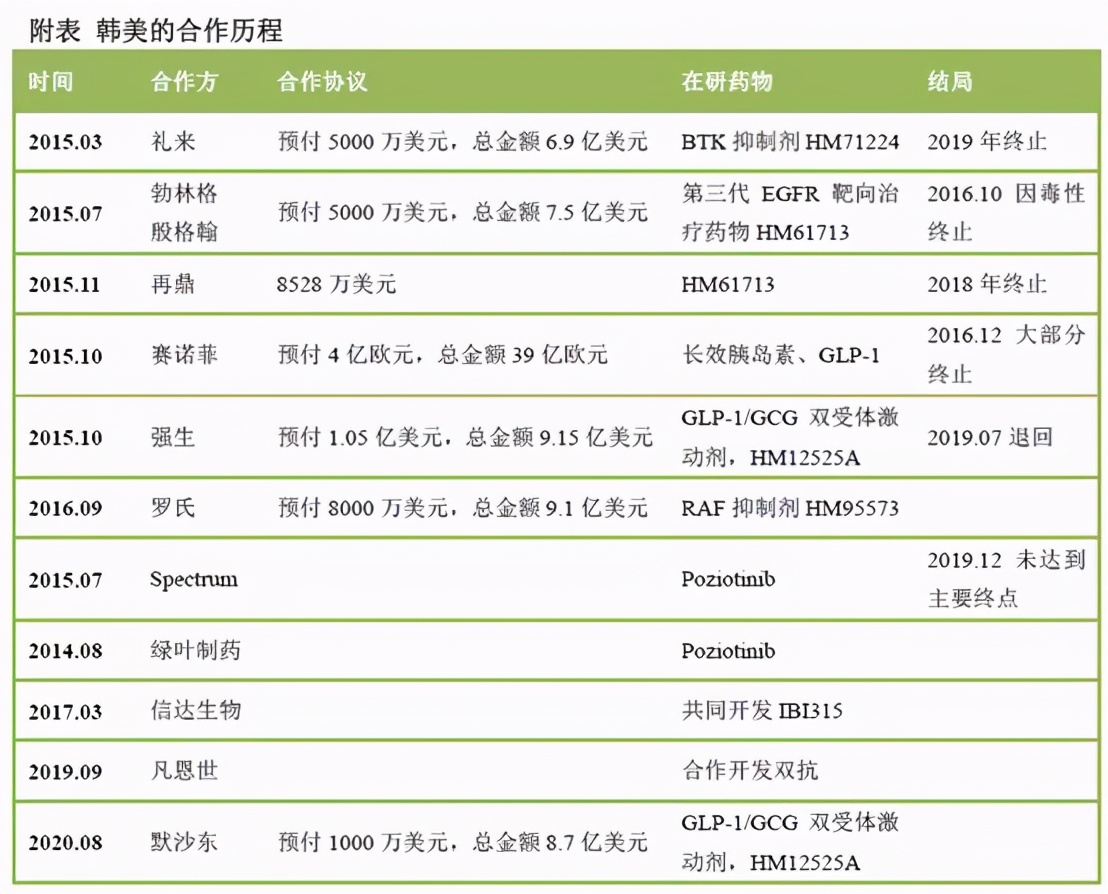
最后,我们也注意到Oraxol最初由韩美研发,而韩美在License-out方面一直颇有一套,但同时槽点也不少。根据Armstrong的医药笔记统计,2015年以来,韩美与包括礼来、勃林格殷格翰、赛诺菲、强生等在内的众多巨头药企都达成过和合作协议,不过其中许多项目都以终止或退回告终。
参考资料:
1. Athenex Receives FDA Complete Response Letter for Oral Paclitaxel Plus Encequidar for the Treatment of Metastatic Breast Cancer/Athenex
2. Athenex – Too little, too late/Viceroy Research, https://viceroyresearch.org/2019/10/22/athenex-too-little-too-late/
3. FDA Grants Priority Review to Oral Paclitaxel/Encequidar for Metastatic Breast Cancer
4. Athenex Corporate Presentation – January 2021, https://ir.athenex.com/static-files/a0751b72-9e2a-478d-98ba-f4b7214c8763
5. 韩美GLP-1/GCG双靶点激动剂授权给默沙东,一年前曾被强生终止合作/Armstrong的医药笔记
6. CDE
版 权 声 明
欢迎个人转发分享。其他任何媒体、网站如需转载或引用本网版权所有内容须获得授权且在醒目位置处注明“转自:佰傲谷BioValley”。