欢迎关注凯莱英药闻
01 Ambrx公司介绍
Ambrx Inc.是一家临床阶段的生物制药公司,于2003年由Scripps 研究所全球著名的化学生物学先驱Peter G Schultz教授联合礼来前副总裁兼速效胰岛素发明者 Richard DiMarchi以及连续创业者Troy Wilson创立于洛杉矶。其 使用扩展的遗传代码技术平台(Expanded Genetic Code) 研发精准生物制品,其中包括用于癌症治疗的下一代抗体药物偶联物(ADC)、双特异性抗体和靶向免疫肿瘤疗法以及用于调节免疫系统的新型细胞因子和用于代谢和心血管疾病的长效治疗肽,均旨在改善药理学特性和新型生物活性。

Ambrx 开创了世界上第一个在细胞内将非天然氨基酸定点整合到蛋白质肽链上的技术平台。传统的偶联技术大多基于半胱氨酸和赖氨酸,它们存在于每个蛋白质的多个位点上,很难在单个位点上进行化学偶联,导致不同DAR的混合。而Ambrx可以将单个合成氨基酸 (synthetic amino acid)结合到蛋白质中,然后使用特定的化学方法将有效载荷稳定地偶联到SAA上,产生均一的偶联产物。Ambrx技术使得对蛋白质进行系统性的结构活性关系(SAR)的研究成为可能。这样可以沿着蛋白肽链选择任何一个位点利用掺入SAA,然后对蛋白质进行精准的化学修饰,这是目前其他技术难以做到的。
扩展的遗传代码技术平台创造原创候选药物潜力:ADC、智能细胞因子、ISACs等

利用Ambrx专有技术平台,Ambrx与百时美施贵宝、安斯泰来、百济神州、赛诺生物制药、Elanco和NovoCodex合作,在临床试验的不同阶段使用Ambrx技术制造药品。Ambrx正在稳健推进多个临床和临床前项目,以期在疗效、安全性和易用性上对多个治疗领域进行优化。
公司产品管线布局
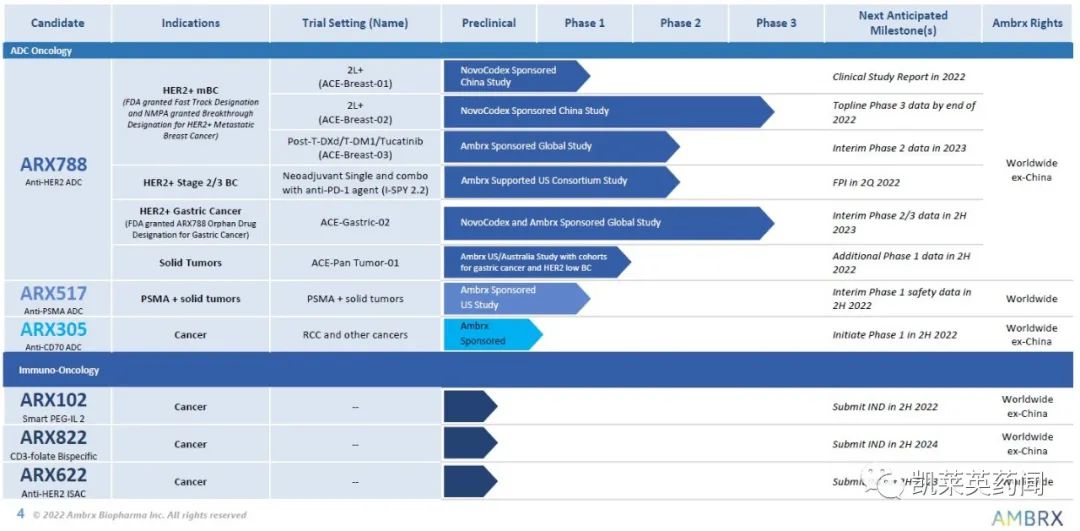
02 新型抗体偶联药物ARX788
ARX788是一种强效且高度稳定的抗体药物偶联物 (ADC),与 T-DM1 作用机制类似, ARX788是由抗 HER2 单克隆抗体赫赛汀和细胞毒性小分子药物 AS269 组成的抗体偶联药物 ,抗 HER2 单克隆抗体可与人HER2特异性结合,AS269为高效微管*制剂抑**,可抑制细胞生长。ARX788与细胞表面HER2结合,通过内吞作用进入细胞,在溶酶体中被水解,释放出pAF-AS269(修饰氨基酸连接毒性分子),pAF-AS269结合微管,诱导细胞周期停滞及死亡。
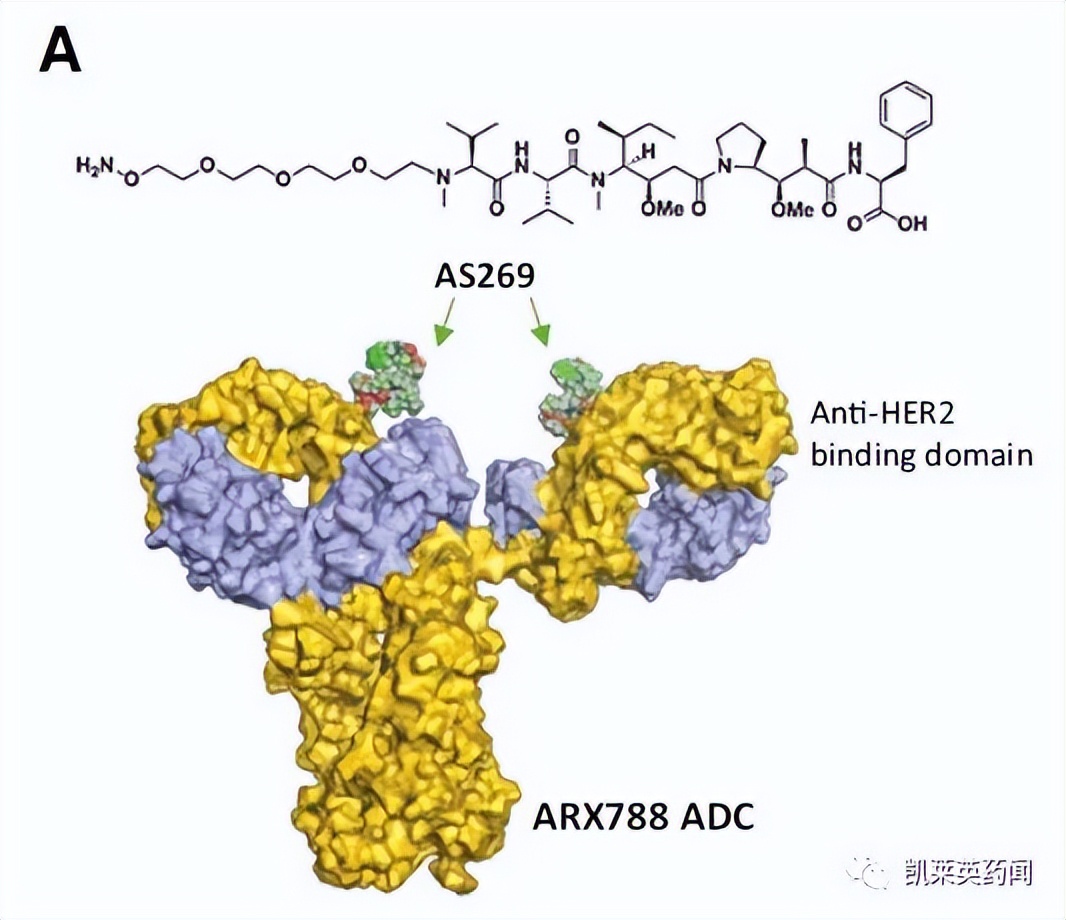
Chemical structure of AS269 drug-linker, which was site specifically conjugated to the heavy chain Ala114 of anti-HER2 mAb to generate ARX788.
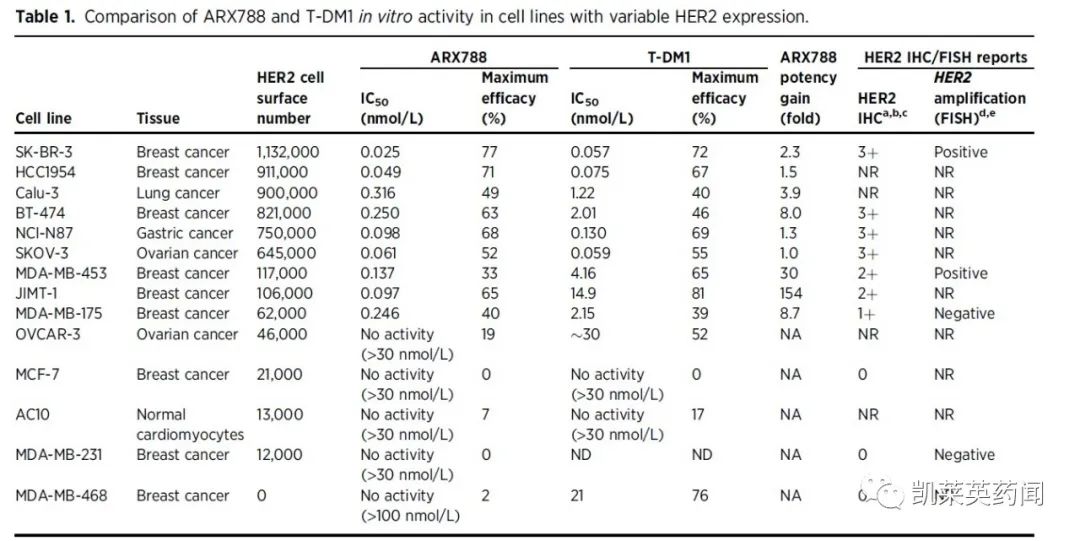
03 ARX788重要里程碑
√ 2020年12月FDA授予ARX788快速通道资格认定,作为单药用于已接受过一种或多种抗-HER2治疗的晚期或转移性HER2阳性乳腺癌患者。
√ 2021年1月FDA 授予ARX788胃癌孤儿药资格认定
√ 2021年5月ARX788获CDE纳入突破性治疗品种,适应症为HER2阳性晚期乳腺癌二线治疗
ARX788针对HER2阳性乳腺癌患者的2期试验中国(ACE-Breast-02),全球(ACE-Breast-03),HER2 阳性胃癌/GEJ患者全球(ACE-Gastric-02)的2/3期试验正在开展。
ARX788重点临床试验总结

04 ARX788合作信息
2013年6月14日,浙江医药和AMBRX公司达成合作协议,浙江医药获得中国区域内AMBRX公司关于ARX788现有专利的独占许可,可以研发、生产、销售该许可产品用于预防和治疗人类疾病。浙江医药将支付相关的研发费用,包括在国内获得产品批准文号前所需的所有费用,以及澳大利亚境内至一期临床完成所需的费用。
根据协议条款,ARX788在中国上市销售后,AMBRX公司将按净销售额不超过20%的比例提取权益金,作为许可费的支付。支付许可费的截止期限为以下二者较晚的期限届满时:
(1)涉及许可产品的现有专利到期之时;
(2)在中国首次商业销售后的20年。
此外,如果AMBRX公司依据I期临床数据在中国以外直接进行转让或许可;或者 AMBRX公司依据I期临床数据在中国以外继续独立开发许可产品并承担一切费用,则根据产品所处的不同阶段,AMBRX公司将按转让收入或产品净销售额不超过20%的比例向公司支付许可费。
05 ARX788国内临床研究进展
2022年5月31日,浙江新码生物医药有限公司临床阶段产品ARX788的HER2阳性晚期乳腺癌I期临床试验结果在国际知名医学期刊《Clinical Cancer Research》在线发表。
该项研究由复旦大学附属肿瘤医院胡夕春教授及其团队主持,是一项单中心、开放、剂量递增的I期临床研究,皆在评价ARX788单药治疗HER2阳性晚期乳腺癌的安全性、耐受性和药代动力学特征。研究设置了0.33 ~1.5mg/kg共9个剂量组。
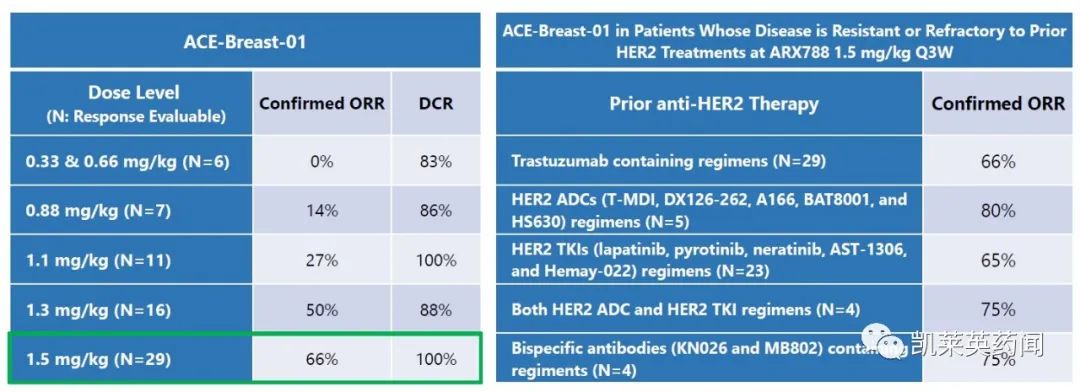
总共有69名受试者参与了该项研究,没有发生DLT或与药物相关的死亡。大多数患者(67/69;97.1%)经历了至少一种与治疗相关的不良事件(TRAE),常见(≥30%)TRAE包括天冬氨酸氨基转移酶升高、丙氨酸氨基转移酶升高、角膜上皮病变、脱发、低钾血症、间质性肺病ILD/肺炎和醛固酮升高。虽有34.8%的受试者发生间质性肺炎,但仅两位的严重程度为3级。在1.5 mg/kg Q3W(II期推荐剂量)下,客观缓解率ORR为65.5%(19/29,95% CI,45.7~82.1),疾病控制率DCR为100%(95% CI,81.2~100),中位无进展生存期PFS为17.02个月(95% CI,10.09至未达到)。
研究显示,ARX788安全性可控,并在HER2阳性晚期乳腺癌患者中表现出优秀的抗肿瘤活性。
ACE-Breast-01临床有效性数据汇总
ARX788临床安全性数据汇总

06 总结
对于ADC药物来说控制DAR的分布区间可以最大程度的平衡药效、人体耐受性和细胞毒性水平,这也成为ADC领域亟待解决的重要难题。Ambrx Inc利用非天然氨基酸来实现定点偶联而制备的ADC药物90%以上实现了DAR为2,目前看起来很有希望解决ADC稳定性、安全性、成药性的问题。