参比信息遴选申请资料现行版为CDE于2020年10月19日发布的《化学仿制药参比制剂遴选申请资料要求》,共分为四个部分:一、申请综述 二、调研信息 三、调研信息网址 四、附件。
接下来我们以三磷酸腺苷二钠注射液为例来调研遴选申请资料中的相关信息。
在申请综述第一部分“品种基本信息”中首先要写明:1.药品通用名称2.药物活性成分名称 3.剂型和规格 4.适应症简述 5.各国药典收载情况6.参比制剂发布/公示情况。上述信息都可以经过简单的调研得到。对于7.品种原研信息,还需要深入调研才可以。
对于各国药典收载情况,可以使用在线药典
(https://www.drugfuture.com/standard/)
或药智网国外在线药典
(https://db.yaozh.com/foreign)进行查询。
不同的药典应将其翻译为相应的语言进行查询。参比制剂发布或公示情况即可通过CDE发布的参比制剂目录来查询。
接下来开始调研,我们按照参比制剂遴选申请资料第二部分调研信息的顺序来进行。
1、国内上市情况
1.1 进口药品批准情况
在国家药监局进口药品下搜索“三磷酸腺苷二钠注射液”,未查询到相关信息。
1.2 国产药品批准情况
在国家药监局国产药品下搜索“三磷酸腺苷二钠注射液”,得到如下信息:

共有66个国产药批准上市。通过查询仿制药参比制剂目录,我们可以推断这些药品均属于仿制药。对于仿制药信息,仅需做相关概述即可。
2、美国上市情况
2.1美国橙皮书收载情况
步骤:
1)美国橙皮书地址:
https://www.accessdata.fda.gov/scripts/cder/ob/index.cfm
在搜索框输入三磷酸腺苷二钠英文,点击search
结果:未查询到相关信息

以地塞米松磷酸钠为例,来看一下如果在橙皮书上有相应药品信息的情况下搜索结果应该是怎样的:
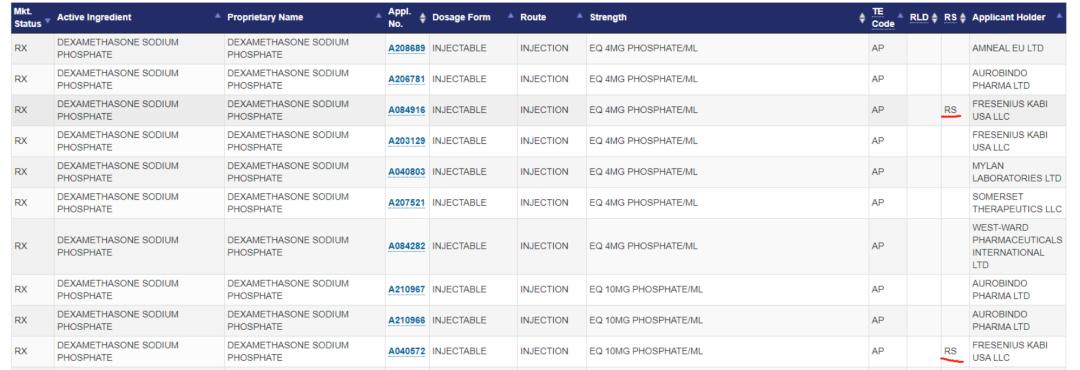
我们可以在上述图中得到地塞米松磷酸钠信息,从左到右依次为:产品状态,市场地位;活性成分;专有名称;批准号;剂型;给药途径;规格;TE code;RLD地位;RS地位;持证商。通过剂型我们便可找到地塞米松磷酸钠注射液的相关信息。从批准号前缀,可知该药品为仿制药还是原研药品,ND为原研药(NDA),A为仿制药(ANDA)。点击批准号,便可得到有关该产品更多的信息。

我们以NDA12071为例,点击批准号之后得到如下信息:
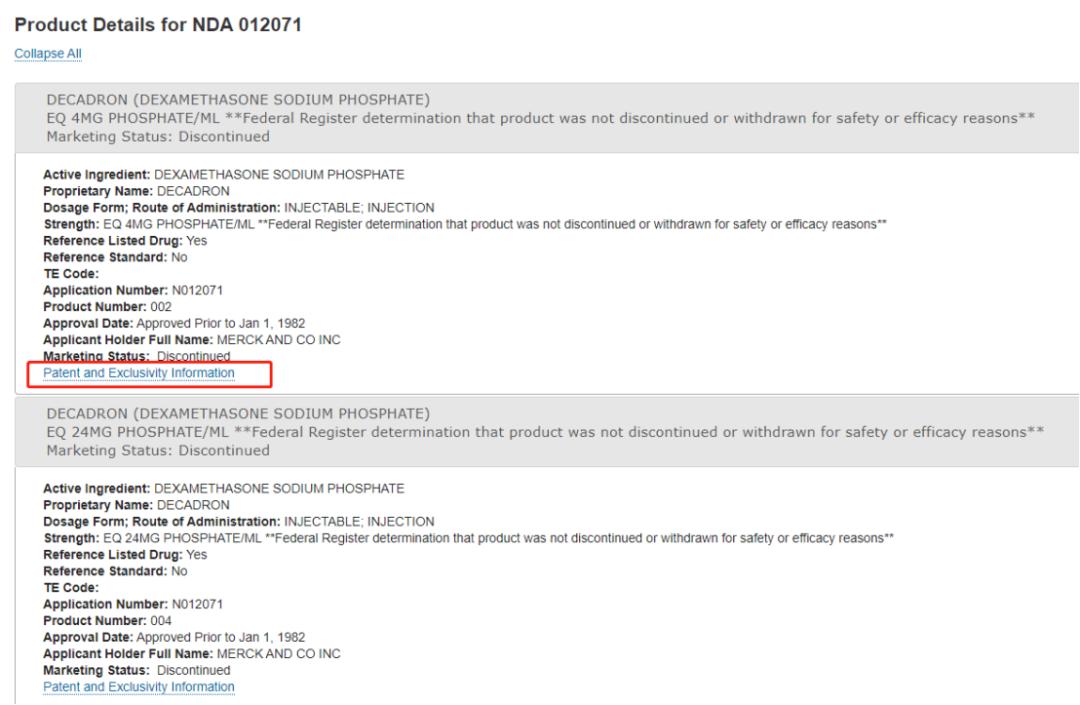
点击patent and exclusivity information ,即可查到相关专利。
2.2 其他上市情况
对于橙皮书未收载的情况应简单进行说明。
OTC Monograph:如果所查药物是OTC药物的话可以去查询,
网址:https://www.govinfo.gov/app/search
3.欧洲上市情况
3.1欧盟EMA官网收载情况
本品种原研药品批准情况应列表进行说明,仿制药简要概述即可。
网址:
https://www.ema.europa.eu/en/human-regulatory/marketing-authorisation
步骤:
1)官网Medicines项下点击Search,
输入“Adenosine Disodium Triphosphate”进行搜索,找到想要的信息。
2)结果:未调研到相关资料。
3.2欧盟HMA官网收载情况
网址:
https://www.hma.eu/search.html?id=6&q=Adenosine+Disodium+Triphosphate&L=0
查询结果:

如果是在欧盟EMA集中审评上市的话,应该如何得到所需的药品信息呢?我们以“阿瑞匹坦胶囊”为例,查询步骤如下:
欧盟(EMA)上市药品信息调研方法
1.输入网址,进入EMA官网。点击“Medicines”,再点击“Search”。

2.在搜索框输入要检索的药品信息:

3.如果所得结果较多,可以通过左边相关信息筛选。


4.找到我们所需的结果:

5.点击获取更多信息。

点击可直达相关内容,其中说明书在Product information,审评报告在Assessment history。

概述中包含了很多和意美有关的信息:

1)什么是“Emend”?
2)Emend的作用是什么?
3)Emend如何使用?
4)Emend如何发挥作用?
5)如何研究Emend?(Emend的研究过程)
6)Emend在研究过程中显示出什么益处?
7)Emend有什么风险?
8)为什么Emend被批准?
9)正在采取什么措施来确保安全有效地使用Emend?
10)其他有关Emend的信息:
此概要可以*载下**。
6.滑动鼠标向下,可以得到官方批准的产品详细信息。
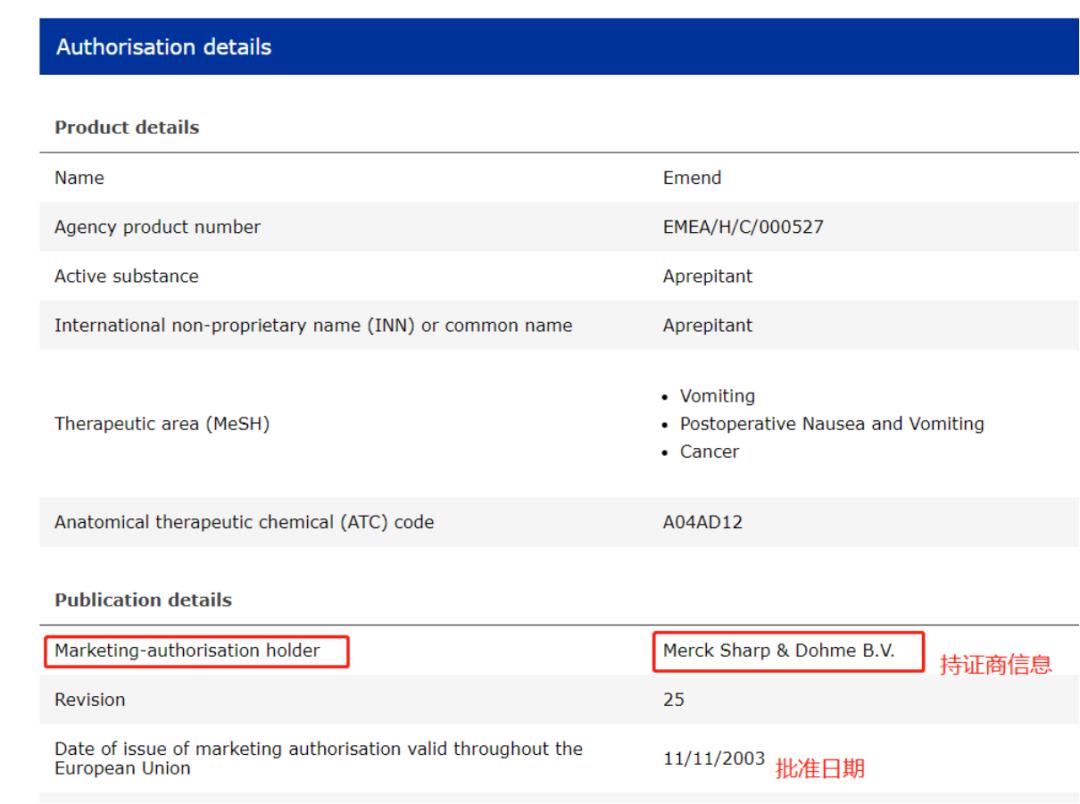
ATC代码:解剖学治疗学及化学分类系统,简称ATC((Anatomical Therapeutic Chemical))系统,是世界卫生组织对药品官方分类系统。
更多产品信息:

找到审评报告,点击即可保存*载下**。


按照《化学仿制药参比制剂遴选申请资料要求》“3.1欧盟EMA官网收载情况”,若拟申请参比制剂是通过EMA集中审批程序上市的原研产品,则3.2“欧盟HMA官网收载情况”和3.3“欧盟各国批准情况”项下可填写为“不适用”。
3.3欧盟各国的批准情况
欧盟成员国及药监局网址:
德国PEI:https://www.pei.de/DE/home/de-node.html
德国BfArM:https://www.bfarm.de/DE/Home/home_node.html
法国ANSM:https://ansm.sante.fr/
意大利AIFA:http://www.agenziafarmaco.gov.it/
荷兰:https://www.igj.nl/
比利时:https://www.famhp.be/en
卢森堡:
https://sante.public.lu/fr/politique-sante/ministere-sante/index.html
奥地利(药品器械局):http://www.basg.gv.at/en/basg-austrian-federal-office-for-safety-in-health-care/
保加利亚(药物署):https://www.bda.bg/bg/
保加利亚(卫生部):http://www.mh.government.bg
塞浦路斯:
http://www.moh.gov.cy/moh/moh.nsf/index_en/index_en?OpenDocument
克罗地亚:http://www.almp.hr/
捷克(国家药物管制所):http://www.sukl.cz
捷克(卫生部):http://www.mzcr.cz
丹麦:https://www.sst.dk/en/English
爱沙尼亚(国家药物署):http://www.sam.ee
芬兰(国家食品署):http://www.nfa.fi/english/index.html
希腊:http://www.mindev.gov.gr
匈牙利:https://ogyei.gov.hu/index.php?lang=en
爱尔兰(药物委员会):http://www.imb.ie
意大利(国家卫生所):http://www.iss.it
意大利(卫生部):http://www.ministerosalute.it
拉脱维亚:https://www.zva.gov.lv/
立陶宛(卫生部):http://www.sam.lt/index_en.html
马耳他(卫生部):http://www.health.gov.mt
波兰(药物所):
https://www.steelprofil.eu/?utm_source=il.waw.pl&utm_medium=301
葡萄牙(卫生部):http://www.min-saude.pt
罗马尼亚(卫生与家庭部):http://www.ms.ro
斯洛伐克(国家药物管制所):http://www.sukl.sk/sukl_en.htm
斯洛文尼亚:http://www.jazmp.si/si/zacetna-stran/seznami/
西班牙(药物署):https://www.mscbs.gob.es/agemed/main.htm
瑞典(药品署):
https://www.researchgate.net/institution/Medical_Products_Agency
这些药监部门查询药物的方法会在后期统一整理分享。
3.4英国MHRA官网收载情况
网址:https://www.gov.uk/government/organisations/medicines-and-healthcare-products-regulatory-agency
英国上市的仿制药说明书中会公布参比制剂的商品名等信息,可通过查询英国仿制药说明书初步确定参比制剂。
步骤:
1.进入官网后点击页面右侧的红框内容

接着点击:
这个页面在网不好的情况下无法跳转,我试过翻墙也没有用。如果这个不能进去的话,直接在此页面最上方的搜索栏里输入要搜索的内容“Adenosine Disodium Triphosphate”,即得到搜索结果。
经查询,未在英国MHRA网站调研到此药品相关信息。
4.日本上市信息
4.1日本PMDA官网收载情况
网址:https://www.pmda.go.jp/
1.进入日本药监局,点击“医疗用医药品”

2.输入活性成分名称,点击检索。

3.搜索结果如下:
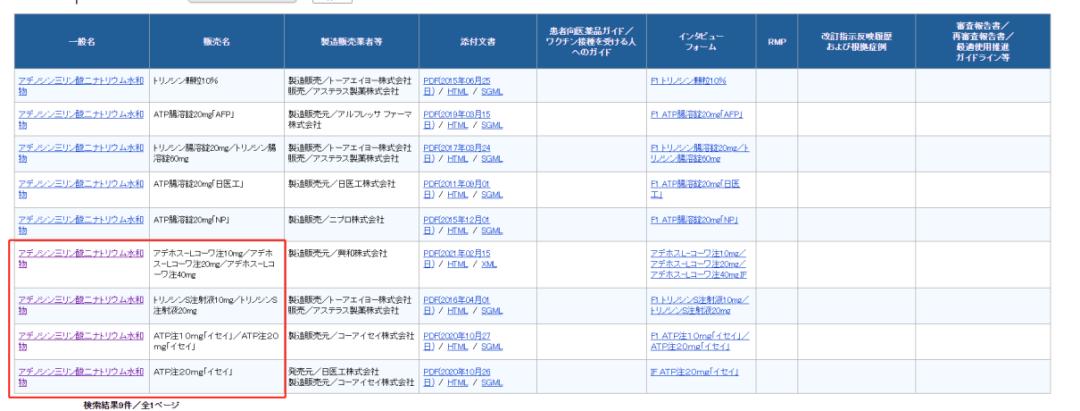
蓝色标题从左到右依次为:通用名、商品名、制造商等、说明书、用药指南、制冷剂管理计划、修订指令反映履历和基础案例。红框里的内容即为我们要找的注射液。
点击进入,可以得到更详细的信息:

此即为IF文件。说明书中有药品上市日期,见下图:
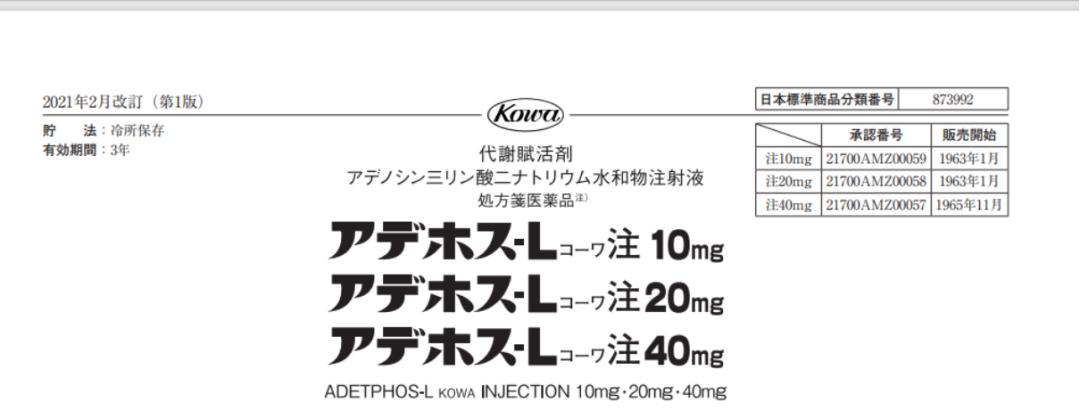
我们将说明书及IF文件中的信息整合,即可撰写 “4.1日本PMDA官网收载情况”项下内容。
4.2 日本厚生省价格目录收载情况
网址:https://www.mhlw.go.jp/index.html
步骤:
1.进入网址,点击“政策”,再点击“分野别XXX”
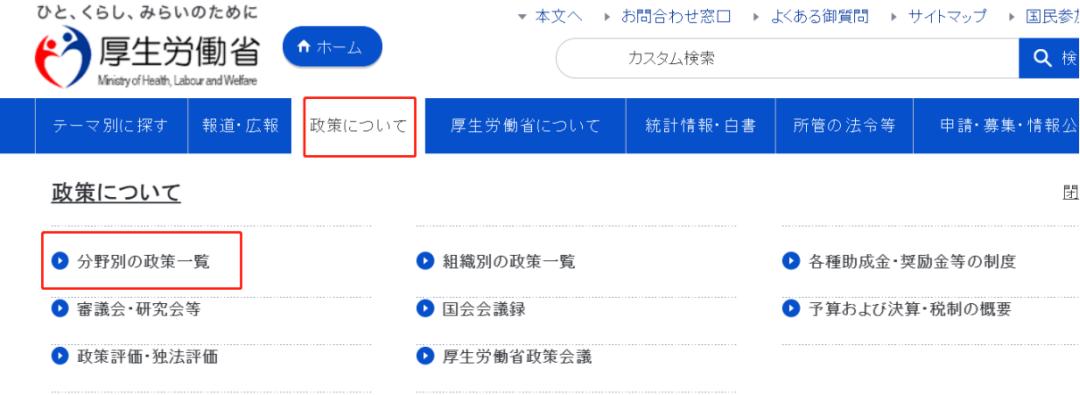
2.点击 “医疗保险”,再找到收载的目录。


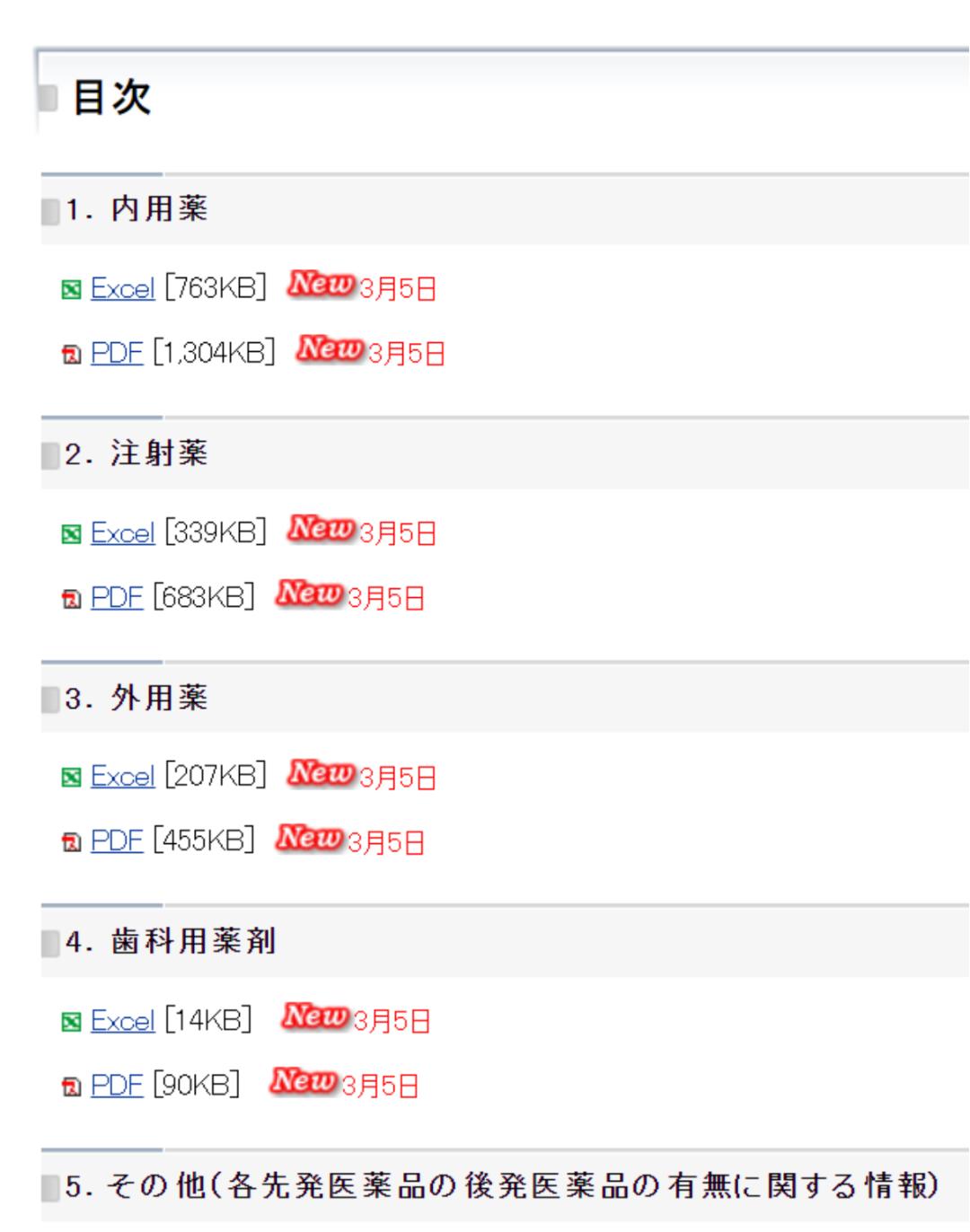
3.通过*载下**注射液相应的目录,搜索有关三磷酸腺苷二钠注射液的信息。结果如下:

4.4日本《医療用医薬品最新品質情報集》(蓝皮书)收载情况
网址:http://www.nihs.go.jp/drug/ecqaged/bluebook/list.html#s
步骤:
1.通过药品名首字,找到相关药品:

2.找到注射液,*载下**PDF。

即可得到相应信息。
5.其他国家上市信息
拟申请参比制剂为美国、欧盟、日本上市产品,此项可填写为“不适用”。
我认为在写参比制剂遴选申请资料之前,公司会在市场及研发层面去考虑,要去仿制三磷酸腺苷二钠注射液,查到不在参比制剂目录上,于是便要进行参比制剂备案,使得此药品的仿制在法规层面上是可行的。采购需要先去联系参比制剂供应商,这样也能得到一些有关此药品的信息,这样的话我们要调研的范围也会相应的缩小。
其他国家的药品上市信息查询,我会在接下来的文章中去总结。
至此,我们的调研就完成了,其中遴选资料正文中需要信息已经全部调研到了,再整合撰写即可。
注:欧盟EMA官网只能查到经欧盟认可的品种,是通过集中审批程序(CP),经欧盟药品管理局批准上市的药品。
欧盟HMA官网可查询上市较早部门欧盟内国家批准上市的品种,是通过互认可程序(MRP),在欧盟部分成员国批准上市的药品。
声明:文章转载于【注册圈】公众号,文章版权归原作者所有,本文仅做转载分享~如有其他疑问,欢迎私信交流~