
2022年7月药品注册审评审批报告
一、2022年7月药品受理情况
1.2022年7月受理总况
2022年7月,国家药品监督管理局药品审评中心(以下称药审中心)共计受理1145个受理号,与去年同期增加17.3%,比上月减少9.5%,生物制品减少70个受理号。
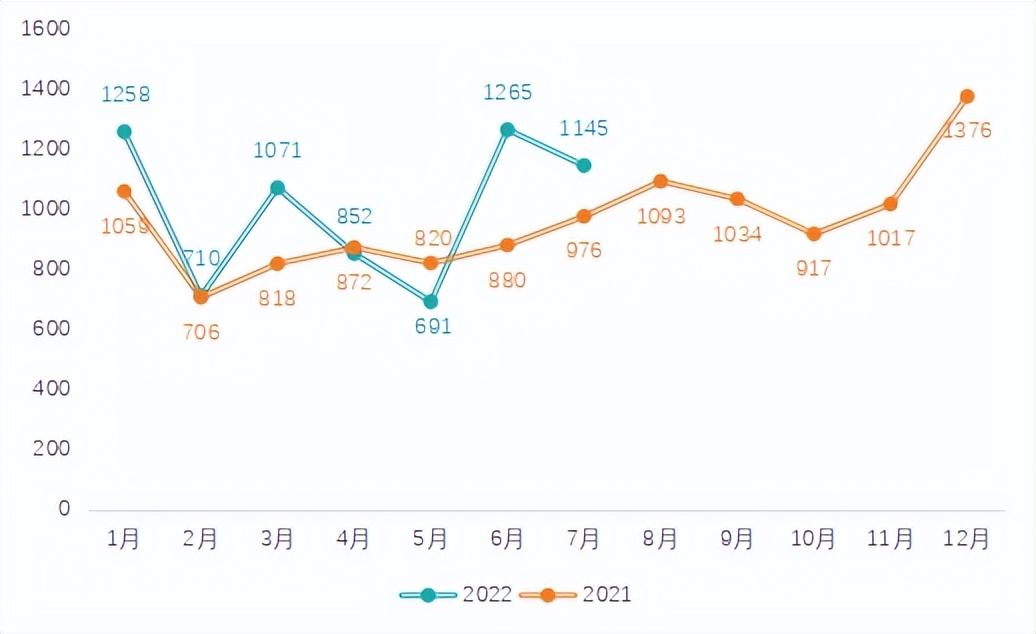
图一 2021和2022年药审中心药品受理情况
受理的药品中,化药占比73%,生物制品14%,中药13%。
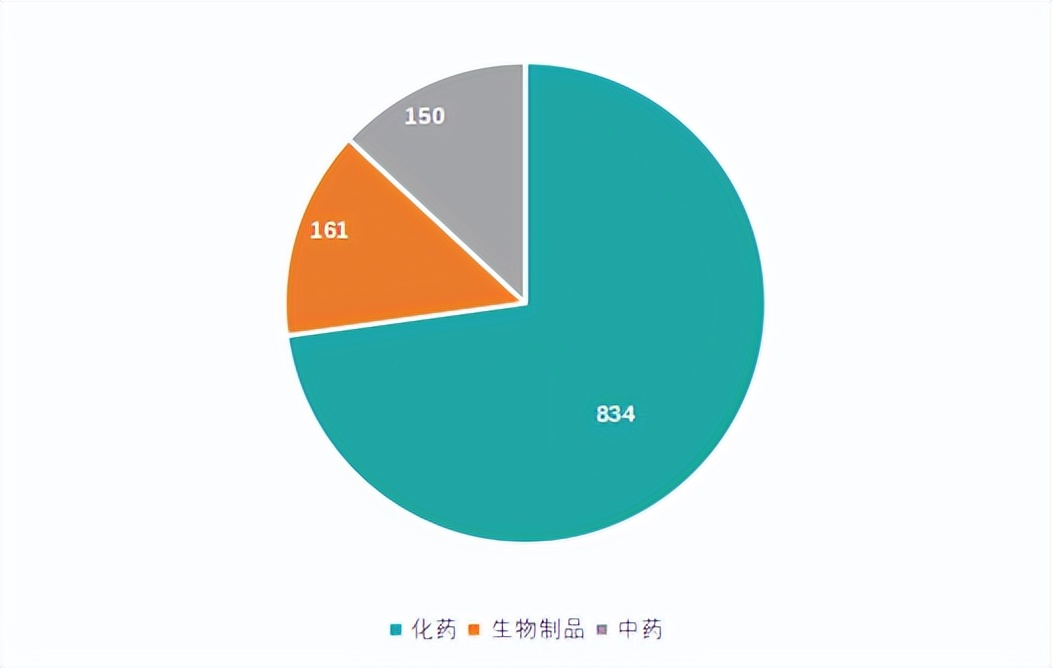
图二 2022年7月各药品类型受理情况
2 .化药受理情况
2022年7月化药受理总数为834个,与7月基本持平,其中2项药械组合产品未计入下图。
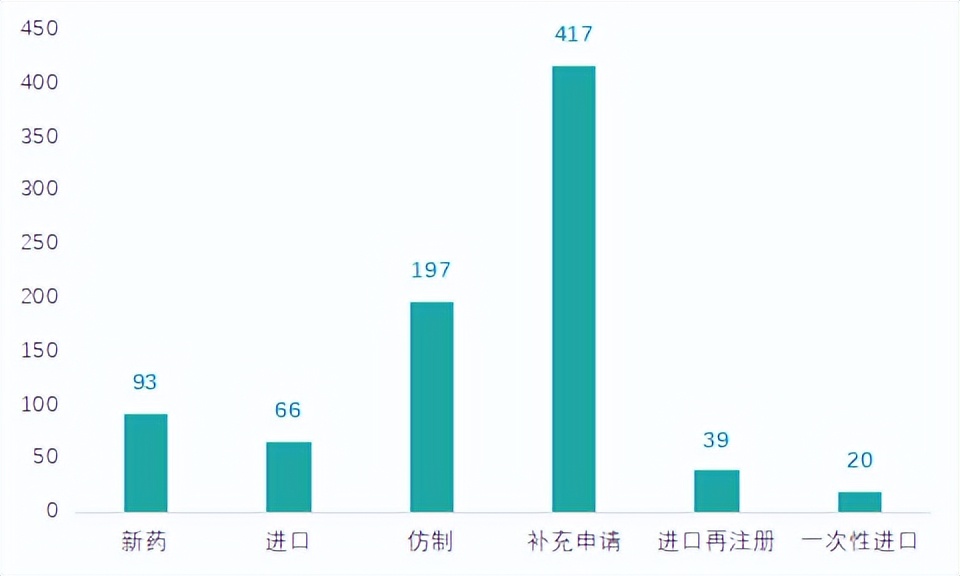
图三 2022年7月化药各申请类型受理情况
化药1类创新药新申报共计110个受理号,包含国产和进口品种。
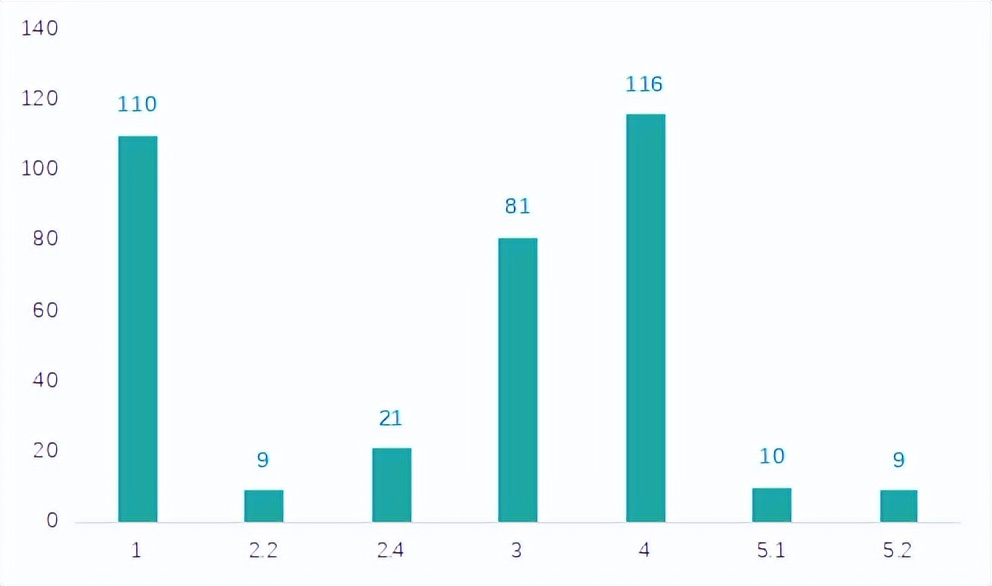
图四 2022年7月化药各注册分类受理情况
本月新申报的1类化药共计34个品种,涉及32个企业。
表1 7月首次申报临床的化药创新药
|
药品名称 |
申请类型 |
企业名称 |
靶点 |
|
AZD5718片 |
进口 |
AstraZeneca AB |
ALOX5AP |
|
BLU-701片 |
进口 |
Blueprint Medicines Corporation |
EGFR |
|
BI 1015550 片 |
进口 |
Boehringer Ingelheim International GmbH |
PDE4B |
|
Mezigdomide(CC-92480)胶囊 |
进口 |
Celgene Corporation |
Ubiquitin-protein ligases |
|
RO6868847薄膜包衣片 |
进口 |
F. Hoffmann-La Roche Ltd |
|
|
RO7223280注射液 |
进口 |
F. Hoffmann-La Roche Ltd |
|
|
LTT462 |
进口 |
Novartis Pharma AG |
ERK2;ERK1 |
|
BGB-15025片 |
新药 |
百济神州(苏州)生物科技有限公司 |
MAP4K1 |
|
GW201片 |
新药 |
北京广为医药科技有限公司 |
|
|
ICP-248片 |
新药 |
北京诺诚健华医药科技有限公司 |
Bcl2 |
|
WXSH0176片 |
新药 |
辰欣药业股份有限公司 |
|
|
STC007注射液 |
新药 |
成都诺和晟泰生物科技有限公司 |
KOR1 |
|
BGC1201片 |
新药 |
赣江新区博瑞创新医药有限公司 |
|
|
LF0001片 |
新药 |
杭州瓴方生物医药科技有限公司 |
|
|
CL-197胶囊 |
新药 |
河南真实生物科技有限公司 |
|
|
HE009片 |
新药 |
南昌弘益药业有限公司 |
|
|
GH55胶囊 |
新药 |
勤浩医药(苏州)有限公司 |
|
|
BT-114143注射液 |
新药 |
赛诺哈勃药业(成都)有限公司 |
|
|
ABP1011T片 |
新药 |
上海爱博医药科技有限公司 |
|
|
YZJ-4729酒石酸盐注射液 |
新药 |
上海海雁医药科技有限公司 |
|
|
YZJ-5053片 |
新药 |
上海海雁医药科技有限公司 |
|
|
RG002片 |
新药 |
上海凌济生物科技有限公司 |
HER2 |
|
RX04胶囊 |
新药 |
上海日馨医药科技股份有限公司 |
|
|
XH-5102片 |
新药 |
上海勋和医药科技有限公司 |
Jak2 |
|
XTN003098 |
新药 |
深圳众格生物科技有限公司 |
|
|
注射用KH617 |
新药 |
四川弘合生物科技有限公司 |
|
|
LV232胶囊 |
新药 |
苏州旺山旺水生物医药有限公司 |
|
|
HT-101 注射液 |
新药 |
苏州星曜坤泽生物制药有限公司 |
|
|
WJB001胶囊 |
新药 |
微境生物医药科技(上海)有限公司 |
|
|
ENC0364 胶囊 |
新药 |
轶诺(浙江)药业有限公司 |
|
|
PA3670片 |
新药 |
浙江柏拉阿图医药科技有限公司 |
|
|
GFH312 片 |
新药 |
浙江劲方药业有限公司 |
RIP1 |
|
JBPOS0101胶囊 |
新药 |
浙江京新药业股份有限公司 |
mGluRs |
|
TUL01101软膏 |
新药 |
珠海联邦制药股份有限公司 |
JAK |
本月共有1个1类新药申报上市。
氘可来昔替尼片
Deucravacitinib是一种口服、选择性TYK2*制剂抑**,具有一种抑制IL-12、IL-23、1型干扰素途径的独特作用机制。TYK2是一种细胞内信号激酶,介导IL-23、IL-12、I型IFN的信号传导,这些细胞因子是参与炎症和免疫反应的天然细胞因子。Deucravacitinib拟开发用于治疗广泛的免疫介导性疾病,包括银屑病、银屑病关节炎、狼疮和炎症性肠病。
2021年11月,deucravacitinib的新药申请(NDA)获FDA受理,用于治疗成人中/重度斑块状银屑病。此外,日本厚生劳动省(MHLW)也已受理了deucravacitinib用于成人治疗中度至重度斑块型银屑病、脓疱型银屑病、红皮病型银屑病的NDA。
2022年7月,氘可来昔替尼片(deucravacitinib)的上市申请获CDE受理。
2.生物制品受理情况
2022年7月生物制品共计受理161个,治疗用生物制品146个。
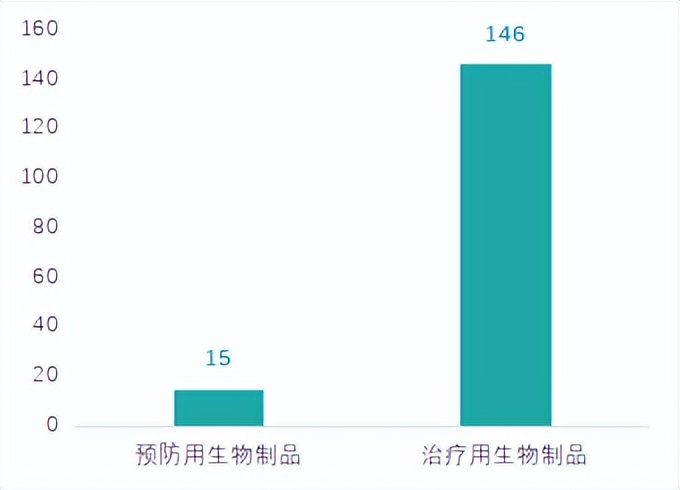
图五 2022年7月生物制品受理情况
本月生物类创新药共计21家企业新申报了21个1类生物药(表2)。
表2 7月新注册临床的治疗用生物创新药
|
药品名称 |
申请类型 |
企业名称 |
靶点 |
|
BN301 |
进口 |
Sutro Biopharma, Inc. |
|
|
Modakafusp Alfa注射液(TAK-573) |
进口 |
Takeda Development Center Americas, Inc. |
CD38 |
|
CAEL-101注射液 |
进口 |
Alexion Pharmaceuticals, Inc. |
SAA |
|
CPI-006注射液 |
进口 |
Corvus Pharmaceuticals, Inc. |
Nt5e |
|
锆[89Zr]吉伦妥昔单抗注射液 |
进口 |
Telix International Pty Ltd |
CA9 |
|
Cendakimab注射液 |
进口 |
Celgene International II Sàrl |
IL13 |
|
Amlitelimab注射液 |
进口 |
Sanofi-Aventis Recherche & Développement |
OX40L |
|
BA1106注射液 |
新药 |
山东博安生物技术股份有限公司 |
|
|
LTC004 |
新药 |
北京志道生物科技有限公司 |
|
|
注射用低分子量岩藻糖化糖胺聚糖钠 |
新药 |
牡丹江友搏药业有限责任公司 |
|
|
靶向GPC3嵌合抗原受体自体T细胞注射液 |
新药 |
原启生物科技(上海)有限责任公司 |
GPC3 |
|
BC008-1A注射液 |
新药 |
四川泸州步长生物制药有限公司 |
PD-1;TIGIT |
|
PM1009注射液 |
新药 |
普米斯生物技术(珠海)有限公司 |
TIGIT;CD112R |
|
注射用重组人凝血因子VIIa-Fc融合蛋白 |
新药 |
江苏晟斯生物制药有限公司 |
|
|
注射用SG1408 |
新药 |
中生尚健生物医药(杭州)有限公司 |
|
|
天然全人源抗狂犬病毒单克隆抗体CBB1注射液 |
新药 |
长春百克生物科技股份公司 |
|
|
重组人源化抗TIGIT单克隆抗体注射液 |
新药 |
乐普生物科技股份有限公司 |
TIGIT |
|
注射用BAT8007 |
新药 |
百奥泰生物制药股份有限公司 |
|
|
因诺替西尔替-ESO细胞注射液 |
新药 |
深圳因诺免疫有限公司 |
NY-ESO-1;HLA |
|
重组结核杆菌融合蛋白(EEC) |
新药 |
成都可恩生物科技有限公司 |
|
|
YH01注射液 |
新药 |
北京因美未来生物医药科技有限公司 |
3.中药受理情况
本月,中药受理150个受理号,其中补充申请148个,2个1.1类新药临床试验申请。
1.1中药复方制剂,系指由多味饮片、提取物等在中医药理论指导下组方而成的制剂。
表3 7月新注册临床的1类中药
|
药品名称 |
申请 |
注册分类 |
企业名称 |
|
抗敏镇咳颗粒 |
新药 |
1.1 |
天津乐敦中药有限公司 |
|
复方野菊花黄酮颗粒 |
新药 |
1.1 |
浙江中医药大学 |
二、2022年7月药品上市情况
不完全统计,本月国家药品监督管理局新批准上市药品共计94个(以批准文号计),其中包含仿制药75个,新药5个(其中1个为创新药,2个为新增适应症),原研进口药4个,增加规格10个。
表4 7月获批上市药品(部分)
|
受理号 |
药品名称 |
申请人 |
批准文号 |
批准日期 |
备注 |
|
CXSS2101041 |
普特利单抗注射液 |
乐普生物科技股份有限公司 |
国药准字S20220022 |
2022/7/19 |
创新药 |
|
JXHS2101087 |
注射用盐酸曲拉西利 |
江苏先声药业有限公司 |
国药准字HJ20220066 |
2022/7/12 |
原研进口 |
|
JXHS2000049 |
贝前列素钠缓释片 |
Toray Industries, Inc. |
国药准字HJ20220067 |
2022/7/26 |
原研进口 |
|
JXHS2101063 |
恩曲替尼胶囊 |
罗氏(中国)投资有限公司 |
国药准字HJ20220068 |
2022/7/26 |
原研进口 |
|
JXHS2101064 |
恩曲替尼胶囊 |
罗氏(中国)投资有限公司 |
国药准字HJ20220069 |
2022/7/26 |
原研进口 |
|
CXHS2101053 |
注射用苯磺酸瑞马唑仑 |
宜昌人福药业有限责任公司 |
国药准字H20200006 |
2022/7/19 |
新增适应症 |
|
CXHS2101054 |
环泊酚注射液 |
辽宁海思科制药有限公司 |
国药准字H20220017 |
2022/7/12 |
新增适应症 |
普特利单抗注射液
普特利单抗是通过使用人IgG4亚型针对人PD-1的人源化单抗。普特利单抗可抑制PD-1信号,以通过阻断PD-1与其配体PD-L1及PD-L2的结合来恢复免疫细胞杀死癌细胞的能力。
普特利单抗能够特异性识别PD-1上的糖基化位点,并采用能够延长普特利单抗蛋白半衰期的创新分子设计。相比已上市或已进入III期临床试验的所有竞争性抗PD-1抗体,所设计的普特利单抗的Fc区能够将蛋白半衰期延长至17.15天至23.51天(单次剂量)及18.41天至38.16天(稳定剂量),其会减少治疗频率,增加患者遵从率,提高患者的便利性及可及性。
普特利单抗是2018年乐普生物收购泰州翰中而获得的PD-1产品。
2021年7月和10月,用于二线或以上黑色素瘤、二线或以上MSI-H/dMMR (微卫星高度不稳定/错配修复缺陷)实体瘤的新药上市申请分别获得NMPA受理。
2022年7月,乐普生物普特利单抗注射液获国家药监局批准上市,适应症为:用于既往接受一线及以上系统治疗失败的高度微卫星不稳定型(MSI-H)或错配修复缺陷型(dMMR) 的晚期实体瘤患者的治疗。
注射用盐酸曲拉西利
Trilaciclib是全球同类首款旨在改善癌症患者化疗预后的创新产品。Trilaciclib在小细胞肺癌(SCLC)患者化疗前给予,根据在美国展开的三项随机、双盲、安慰剂对照临床试验的骨髓保护数据,获得了FDA突破性疗法认定。在一项对转移性三阴性乳腺癌病人的随机试验中,与单纯化疗相比,与化疗联合使用时Trilaciclib显著改善了病人的总体生存期。
在2020年6月,G1向美国食品药品监督管理局(FDA)提交了一份新药申请(NDA),用于小细胞肺癌患者的骨髓保护,并作为I-Spy2试验的一部分开始了乳腺癌新辅助化疗的研究。G1公司预计在2020年第四季度在美国启动一项针对结直肠癌的三期注册性临床试验。
2020年8月,先声药业集团有限公司与G1 Therapeutics公司,签署一项独家许可引进Trilaciclib在大中华地区(中国大陆,香港,澳门和台湾)所有适应症的开发和商业化的权益。
根据协议条款, G1将获得1400万美元的首付款,并将获得至多1.56亿美元的开发和商业化里程碑付款。同时,先声药业将根据Trilaciclib在大中华地区的年度净销售额分段支付销售提成。先声药业将拥有Trilaciclib在大中华地区所有适应症的独家开发和商业化权利,并将参与Trilaciclib的全球临床试验。G1保留Trilaciclib在大中华地区以外地区的开发和商业化权利。
2020年11月18日,中国国家药监局药品审评中心(CDE)承办了由先声药业(2096.HK)和G1 Therapeutics联合申报的1类新药注射用Trilaciclib临床试验申请。
2021年2月,G1 Therapeutics开发的Trilaciclib于今年2月获FDA批准,用于预防扩散期小细胞肺癌成人患者因铂类/依托泊苷方案或拓扑替康方案化学治疗导致的骨髓抑制,同时也是全球唯一一款可降低化疗诱导的骨髓抑制发生率的骨髓保护疗法。
2022年7月12日,注射用盐酸曲拉西利(科赛拉®)获国家药品监督管理局(NMPA)批准在中国附条件上市,用于既往未接受过系统性化疗的广泛期小细胞肺癌患者,在接受含铂类药物联合依托泊苷方案治疗前预防性给药,以降低化疗引起的骨髓抑制的发生率。
恩曲替尼胶囊
恩曲替尼是原肌凝蛋白受体酪氨酸激酶(TRK)(TRKA 、TRKB和TRKC,分别编码神经营养基因受体酪氨酸激酶(NTRK) NTRK1, NTRK2, NTRK3)、原癌基因酪氨酸受体激酶ROS1 和间变性淋巴瘤激酶ALK的*制剂抑**,通过抑制这些信号通路,可抑制肿瘤细胞增殖,达到抗癌作用。
2019年8月15日,美国FDA批准恩曲替尼用于选择NTRK融合阳性局部晚期或转移性实体肿瘤的12岁及以上成人和儿童患者以及转移性ROS1阳性非小细胞肺癌(NSCLC)患者。
2022年7月,恩曲替尼(entrectinib)胶囊获国家药监局批准上市,用于治疗NTRK融合阳性局部晚期或转移性实体瘤。
注射用苯磺酸瑞马唑仑
新增用于支气管镜诊疗镇静的适应症。
环泊酚注射液
新增用于重症监护期间的镇静。