癌症患者的微生物组研究显示,许多实体瘤中存在多种细菌,动物实验显示全身给细菌后,细菌可选择性的定值在肿瘤核心区域,这引起了人们对使用和修饰细菌作为癌症疗法的极大兴趣。因此,细菌工程成为当前的一个研究热点。细菌工程是合成生物学的一个新兴领域,合成生物学将分子生物学、系统生物学与工程学相结合,用以设计人类想要的物质,如抗肿瘤物质等。目前,由于缺乏可快速、动态、高通量筛选细菌的体外测试环境从而限制了其在临床应用中的发展。
鉴于此,来自哥伦比亚大学生物工程系、数据科学研究所、赫伯特·欧文综合癌症中心的 Tal Danino 等人开发了一个3D多细胞细菌球状共培养(Bacteria spheroid coculture,BSCC)系统 ,可适用于多种肿瘤细胞类型和细菌种类,并能利用动物模型进行验证,大大促进了工程微生物疗法的快速发展。 详细方法以protocol形式以题为《A rapid screening platform to coculture bacteria within tumor spheroids》于2022年7月29日发表在《Nature Protocols》上,该系统测试了肿瘤传感基因回路、表征了细菌介导的肿瘤发生、筛选了抗肿瘤有效载荷、概括了体内治疗结果,达到体内系统无法实现的筛选规模,提高了微生物疗法和肿瘤-微生物相互作用研究的通量和可及性。 (图1)
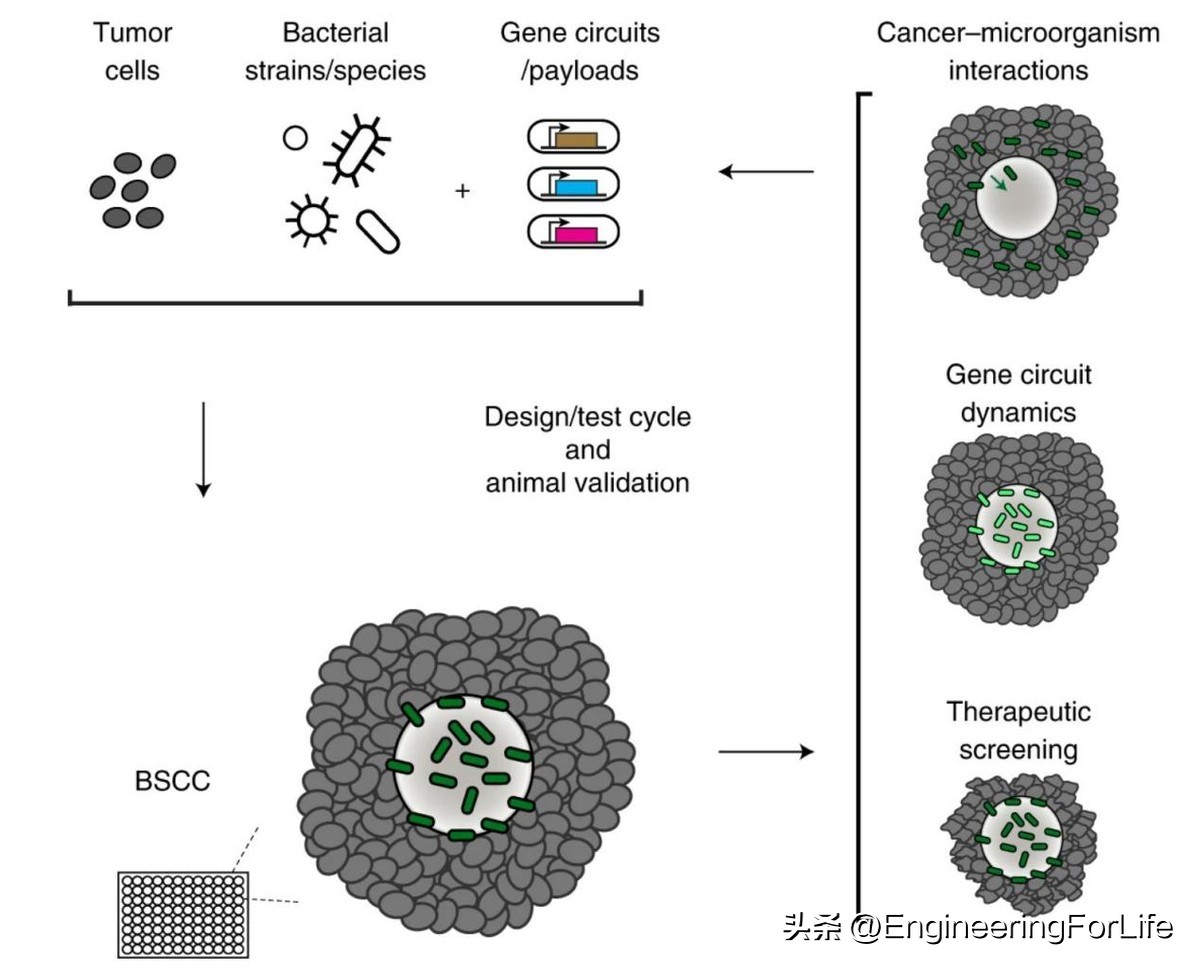
图1. BSCC系统评估微生物-癌症的相互作用和其疗效
简介
1.开发方法
理想的共培养系统必须同时满足几个标准:1)两个群体稳定共存,可纵向检测细胞相互作用和反应;2)很好的模拟生理状态下的细菌和肿瘤反应的实体肿瘤微环境;3)适用于多种肿瘤和菌株,促进该领域的标准化和可及性。表1列举了现有方法,发现其很难同时满足上述功能。在此对比了BSCC和现有的培养体系,其表现出一定优势。
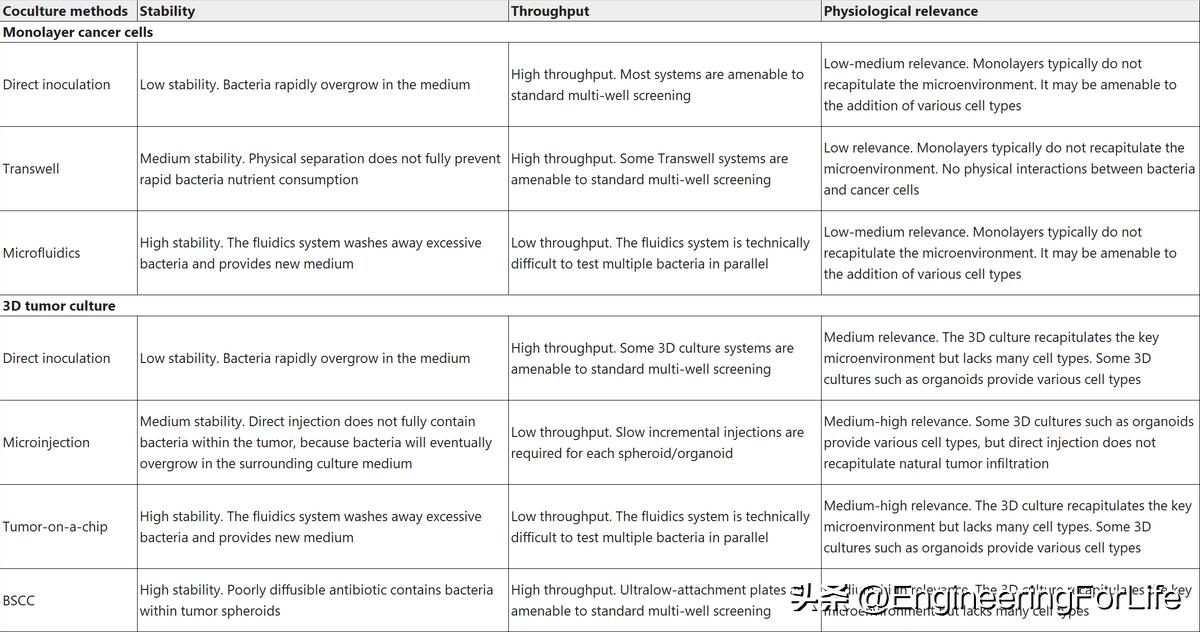
表1. 现有菌癌共培养体系的比较
优势体现在BSCC利用了3D肿瘤球体的优势,同时解决了细菌过度生长造成的限制。这是通过使用重复洗涤步骤、在周围培养基中添加弥漫性差的抗生素(庆大霉素)的方法,将细菌生长限制在肿瘤坏死核心中来实现的(图2)。
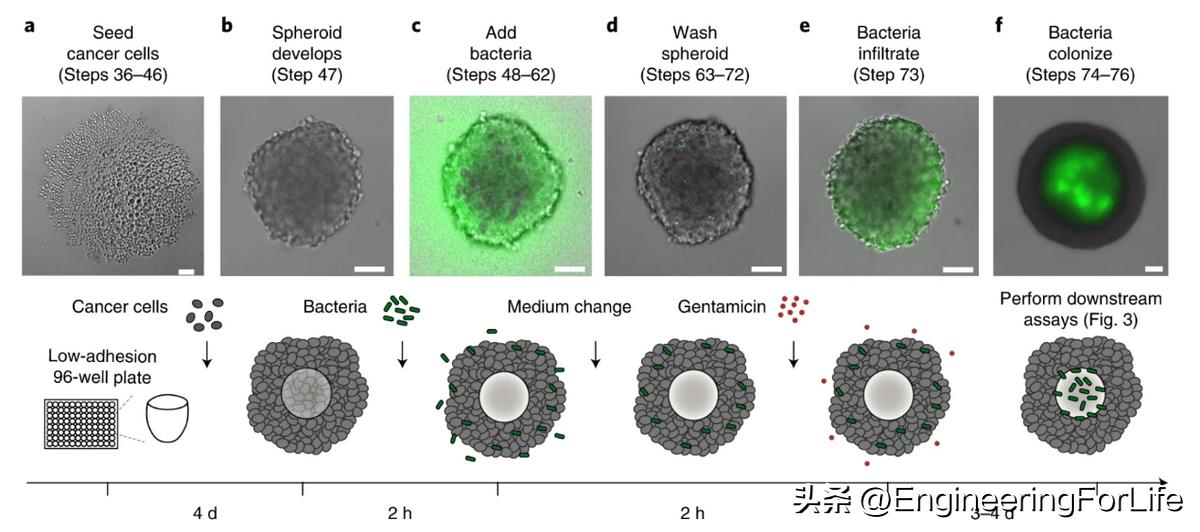
图2. 建立BSCC系统的工作流程示意图
同时,BSCC系统同时表征细菌和肿瘤细胞,并与许多标准测定和仪器兼容,用于下游实验和分析,而这些试验和分析是其他实验装置难以实现的(图3)。例如,延时显微镜可以分析细胞的时空动力学(球体大小、细菌分布和基因表达动力学)。并且在任何时间点,都可以轻松提取单个肿瘤球体以进行测定(活力、组织学和细菌集落计数)。
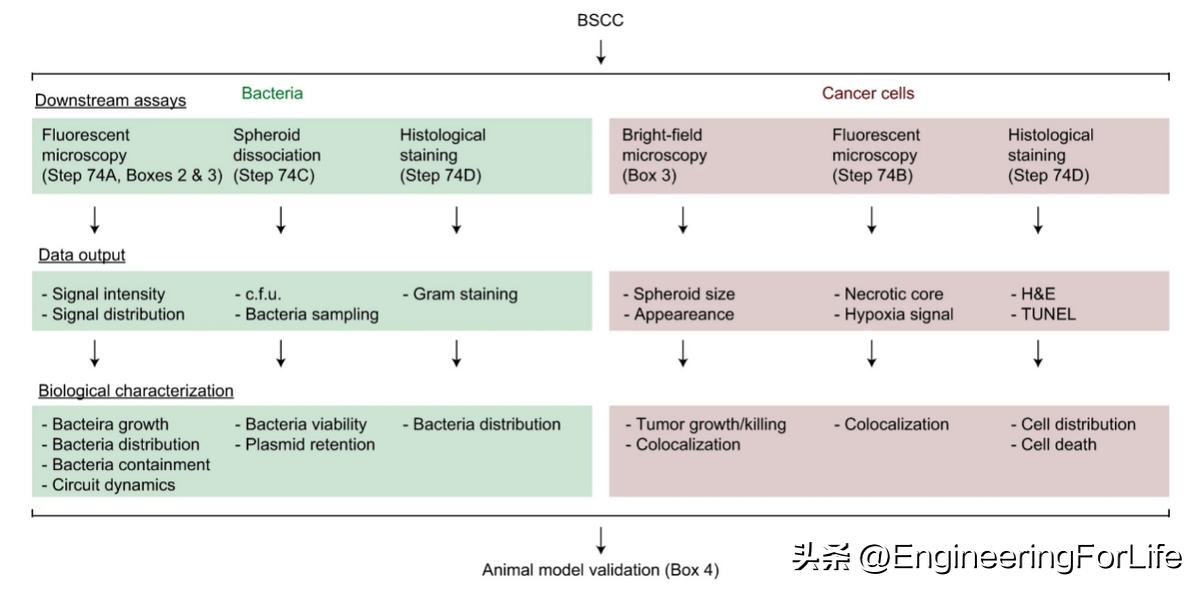
图3.下游检测及其效用
2.方法概述
该方案详细介绍了以下几个方面(具体见全文):
- 细菌培养和肿瘤球体形成:包括肿瘤细胞的扩增和接种,在肿瘤求体内共培养细菌,去除肿瘤球体外细菌,分析细菌生长轨迹等。
- 基因回路动力学。
- 体外治疗效果监测。
- 体内验证BSCC筛选候选药物的疗效。
3.比较其他方法
许多关于细菌与癌细胞相互作用的早期研究都是通过将细菌添加到单层肿瘤细胞上进行的。方法简单,但是忽略了细菌和肿瘤生长速率不同,细菌迅速生长耗尽培养基的营养物质,从而导致肿瘤细胞死亡,使得时间太短,无法观察到细胞相互作用和反应。在此基础上,后人添加了Transwellw物理分离细菌和细胞,这种方法限制了细菌的营养掠夺,但是却有损细菌和癌细胞的相互作用。
进而衍生出微流体系统用于研究细菌和肿瘤细胞的共培养。先将肿瘤细胞接种到微流体通道中,然后接种细菌,这种方法可很好的表征细菌密度和抗肿瘤功效评价。但这需要专门的设备,并难以实现高通量。因此,高通量和可及性并不高。
大多数单层细胞和微流体系统的一个关键缺点是缺乏某些生理条件,如细胞几何形状、代谢物和氧梯度。
因此,3D培养系统越来越多地用于研究广泛的生物学问题,并被认为是进行药物疗效研究的更相关的模型。以前使用3D培养系统的研究试图通过添加微流体来制造肿瘤芯片系统,将细菌显微注射到肿瘤类器官的核心,以促进细菌肿瘤定位,并使用严格的厌氧细菌或灭活细菌来控制肿瘤外细菌的过度生长,来解决微生物快速过度生长的问题。但是,这些方法需要复杂的技术和专业的设备,因此高通量和可及性也不高。
与这些系统相比,BSCC提供了一种简单稳定的3D共培养系统,可在生理肿瘤环境中对细菌进行高通量和纵向表征。
4.BSCC的优势和缺陷
BSCC系统的一个优点是可以很好的模拟肿瘤环境中的细菌定植(可看到肿瘤坏死和细菌在缺氧中心生长)。BSCC可实现高通量并且可及性高,只需要用标准组织培养的96孔板和悬浮培养装置,可同时测量大量的细菌菌株、肿瘤类型、基因回路和治疗手段,并在时空两个层面进行表征。普通实验室也可以实现。
但该技术仍有一定的局限,例如在实体瘤微环境中缺乏细胞类型异质性(免疫细胞、基质细胞、脉管系统等)以及有几种细菌(对庆大霉素耐药的细菌)不相容性等。该系统仍有改进的空间。
5.本文试验设计
肿瘤球体:小鼠结直肠癌细胞系CT26和MC26、小鼠乳腺癌细胞系4T1、人结肠癌细胞系HT29
细菌:衰减型鼠伤寒沙门氏菌(ELH1301)、其他鼠伤寒沙门氏菌菌株(ELH430、SL7207和VNP20009)、单核细胞增多性李斯特菌(L.monocytogenes),奇异变形杆菌(P.mirabilis)和大肠杆菌(E.coli)(细菌可带光学标记便于追踪,如sfGFP)
参数和条件:评估不同浓度庆大霉素共培养的结果。余见表2。
结果:见图4。
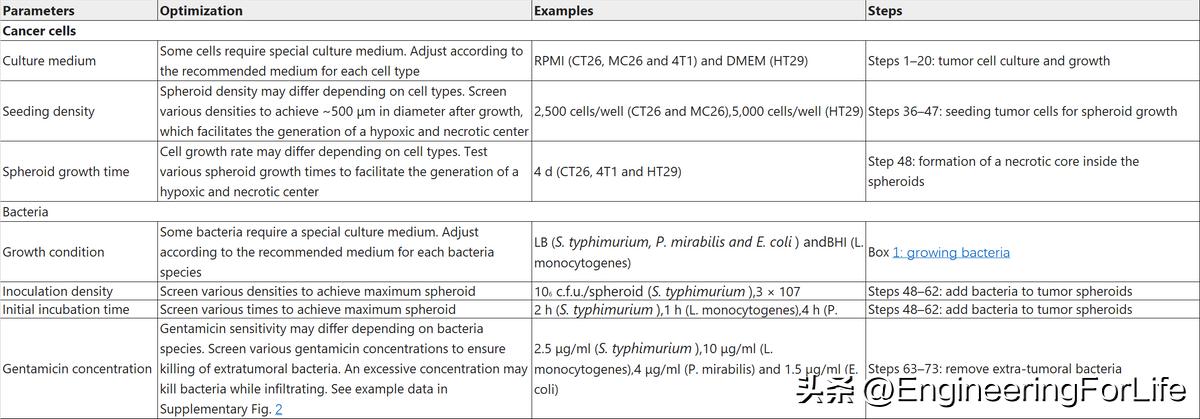
表2.共培养的重要参数
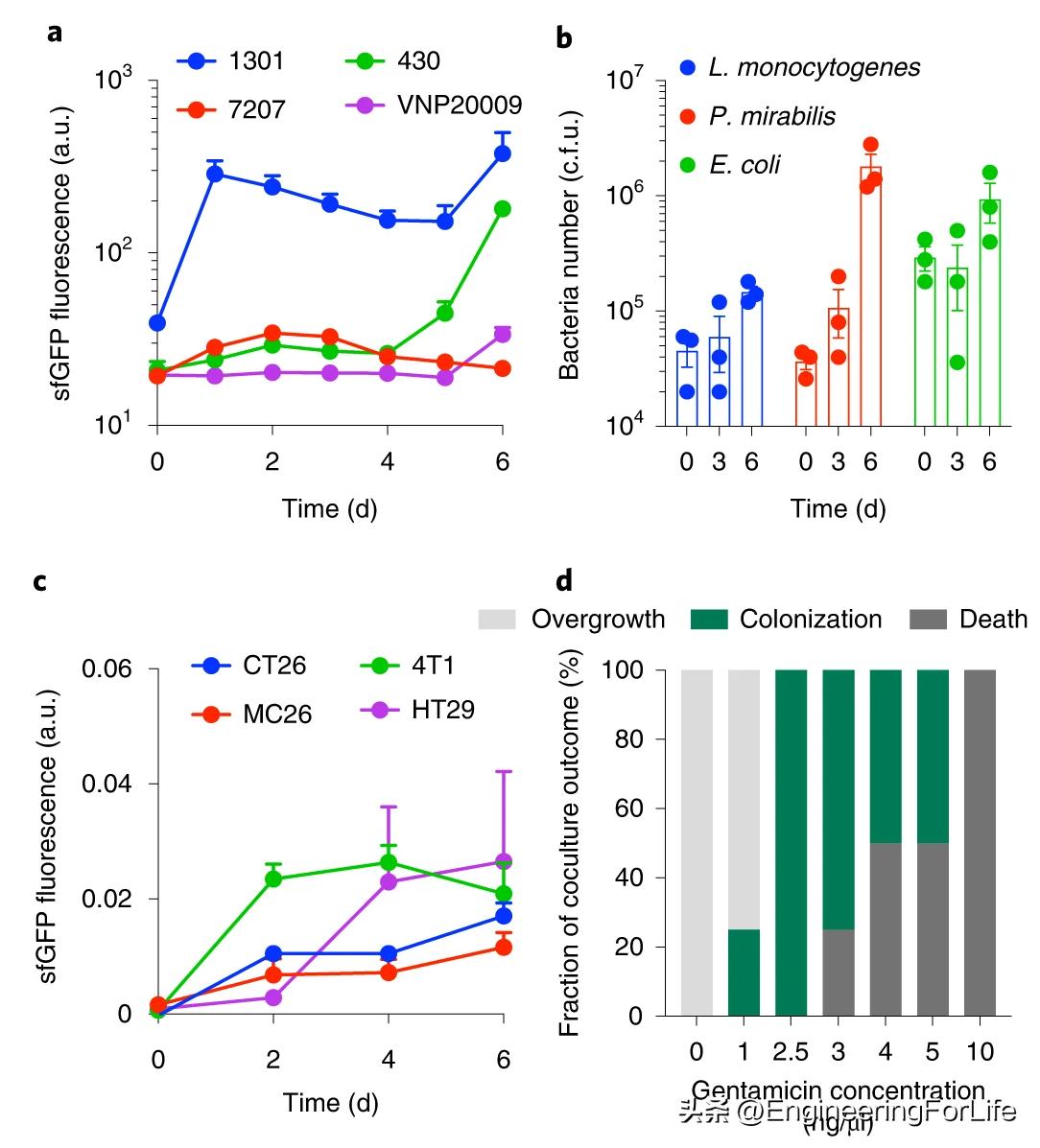
图4.各种细菌和肿瘤细胞共培养
材料
- 生物材料:
- 细胞系:CT26,、4T1 、 HT29 买自ATCC。 cat. nos CRL-2638 (RRID: CVCL_7256), CRL-2539 (RRID: CVCL_0125) , HTB-38 (RRID: CVCL_0320)。从K. Tanabe和B. Fuchs获得的MC26细胞系(马萨诸塞州总医院,RRID:CVCL_0240)。从达尼诺实验室库存获得的红外RFP(iRFP)转染CT26细胞系。菌株:从Elizabeth Hohmann博士获得的鼠伤寒沙门氏菌ELH1301和ELH430的减毒菌株;SL7207从齐格弗里德·魏斯获得。从埃里克·帕默(Eric Pamer)获得的单核细胞增多性乳杆菌。鼠伤寒沙门氏菌菌株VNP20009,奇异疟原虫和大肠杆菌从美国类型培养收藏中购买(分别为202165号,29906和23506)。
- 小鼠:从Taconic Biosciences购买的雌性BALB / c小鼠(4-6周龄)。
PS:所有动物实验均获得机构动物护理和使用委员会(IACUC;哥伦比亚大学,协议ACAAAN8002和AC-AAAZ4470)。所有人员都应接受培训(包括但不限于健康检查、对实验动物和屏障设施的人道处理),并始终遵循批准的规程。生物安全2级细菌(包括本方案中使用的减毒鼠伤寒沙门氏菌菌株)的使用应得到IACUC的批准,符合环境健康和安全的机构指南,并在适当的专用空间进行。在进行动物实验时,重要的是要注意小鼠性别的差异。这可能会影响结果,因此应予以披露。
- 试剂:RPMI 1640 (Gibco Thermo-Fisher, cat. no.11835030)、DMEM F12 GlutaMAX supplement (Gibco; Thermo-Fisher, cat. no. 11320033)、FBS (Gibco; Thermo-Fisher, cat. no.10-437-028)、Penicillin-streptomycin (CellGro; Thermo-Fisher, cat. no. 15-070-063)、LB broth (Lennox; Thermo-Fisher, cat. no. BP9722-500)、Kanamycin (Sigma-Aldrich, cat. no. 10106801001)、Gentamicin (Thermo-Fisher, cat. no. 15-750-060)、0.05% trypsin EDTA (Gibco; Thermo-Fisher, cat. no. 25-300-054)、Hypoxia dye Image-IT hypoxia reagent (Thermo-Fisher, cat. no. H10498)、Dimethyl sulfoxide (Thermo-Fisher, cat. no. 50-147-371)(避免吸入蒸气或雾气)、LB agar (Lennox; Thermo-Fisher, cat. no. 22700025)、1× Dulbecco’s PBS (Thermo-Fisher, cat. no. 14190144)、190 proof ethanol (Thermo-Fisher, cat. no. 22-032-600)、Bleach (Clorox)(避免接触皮肤、眼睛和衣服。每次使用后,请拧紧盖子。)、N-(β-Ketocaproyl)-L-homoserine lactone (Sigma, cat. no. K3007)、Paraformaldehyde (PFA), 4% (vol/vol) in PBS (Fisher Scientific, cat. no. AAJ61899AP)(避免接触皮肤和眼睛。避免形成灰尘和气溶胶。在形成灰尘的地方提供适当的排气通风。远离点火源。采取措施防止静电荷积聚)。
- 设备:
- 肿瘤细胞培养:T75 组织培养瓶、Serological stripettes、Serological pipette gun、Multi-channel pipette、移液器、移液器吸头、细胞计数器载玻片、细胞计数器、15-ml 锥形瓶、50-ml 液体储液罐、96-well透明圆底超低附着板、II类 A2生物安全柜、37 °C CO2 培养箱、37 °C 水浴锅、离心机、真空管路。细菌培养:12-ml培养管、II类 A2 生物安全柜、37 °C恒温摇床、NanoDrop OneC、塑料比色皿、37 °C CO2 培养箱、培养皿。质粒/菌株:Constitutive sfGFP、N-(β-Ketocaproyl)-L-homoserine lactone (AHL)-inducible sfGFP、AHL-inducible therapeutics、Hypoxia-inducible asd、Lactate-inducible glms。成像基软件:EVOS FL Auto 2 细胞成像系统、Celleste 成像分析软件、Nikon TiE 显微镜、Nikon Elements 软件、Image-J 或 FIJI、Graphpad Prism v.8.0。体内实验:1ml注射器、异氟醚异硫化溶液、 压缩氧气、麻醉机、卡钳、老鼠粮食、动物笼子。
- 试剂配制
- 细菌培养基:LB、50μg/ ml卡那霉素。肿瘤细胞培养基:RPMI 1640,含10%FBS和1%青霉素 - 链霉素。球状肿瘤培养基:RPMI 1640,含10%FBS。共培养的培养基:RPMI 1640,含10%FBS和2.5μg/ ml庆大霉素。
步骤
- 肿瘤球体制备(表3)
- 解冻肿瘤细胞:略扩增肿瘤细胞:略种子肿瘤细胞球体:0.25×106/10ml肿瘤细胞取100微升,加入96孔板中,室温下以100g,5分钟离心。将96孔板转移到培养箱中,每天观察肿瘤球体形成情况。孵育球体4天。
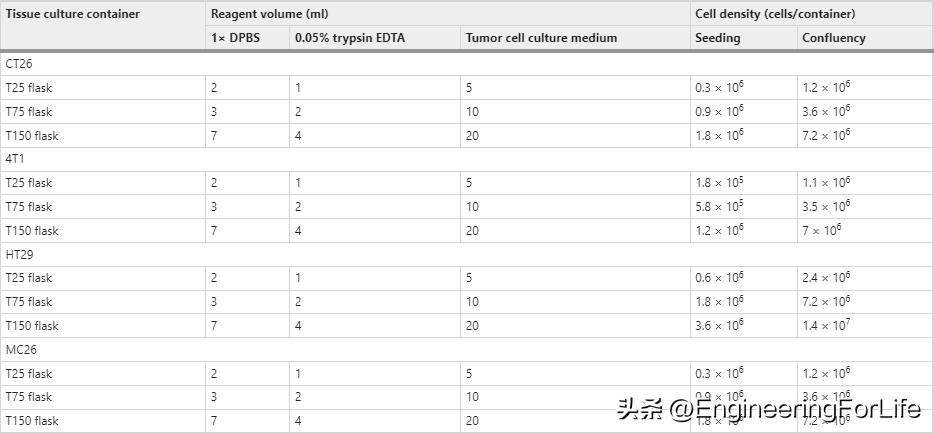
表3. 建议肿瘤细胞培养条件
- 细菌与肿瘤球体共培养
- 将细菌添加到肿瘤球体中:球体播种4 天后,检查肿瘤球体的外观。在明场显微镜下,核心应比外围看起来略暗,表明坏死中心形成。将细菌培养管以3000g, 5分钟离心,收集细菌。2ml 1×DPBS重悬细菌,取1ml于比色皿中,检测细菌光密度。如鼠伤寒沙门氏菌隔夜培养的OD600应该为~3。用1×DPBS将OD600调整为0.5(1ml溶液现在应含有〜0.1-0.2×109鼠伤寒沙门氏菌的c.f.u.)。取出含有肿瘤球体的96孔板,将2μl细菌溶液加入96孔板上的每个球体孔中,将96孔板转移到培养箱并孵育2小时。去除肿瘤外细菌:孵育2小时后,取出共培养板并在明场显微镜下观察。在肿瘤球体周围的孔底部应看到小的细菌斑点。用p200的移液器和160μl 1×DPBS,反复洗涤几次。最终使得96孔板只剩球体。最后,缓慢加入200μl含有庆大霉素的共培养基。
- 细菌浸润和定植
- 对肿瘤球体内的细菌进行成像:略缺氧和肿瘤球体图像:略使用c.f.u.跟踪细菌生长:略制备组织学样本:略
预期成果
本文设想BSCC系统将促进广泛的实验研究,包括细菌-癌症相互作用、遗传回路动力学和高通量治疗测试等。在肿瘤球体中初步建立细菌的肿瘤定植是关键步骤,也是许多下游研究的基础。为了表征细菌的入侵和生长,我们跟踪了随着时间的推移,鼠伤寒沙门氏菌ETH1301中表达的sfGFP荧光。在与肿瘤球体一起孵育后,最初观察到细菌附着在球体表面,将庆大霉素加入培养基以后,细菌在肿瘤球体内部浸润、定位和增殖(图5a)。Typhymurium S. typhymurium位于球体的坏死和缺氧区域,在体内重现细菌定植条件(图5b)。细菌sfGFP和c.f.u.水平都增加了14天(图5c-f)。
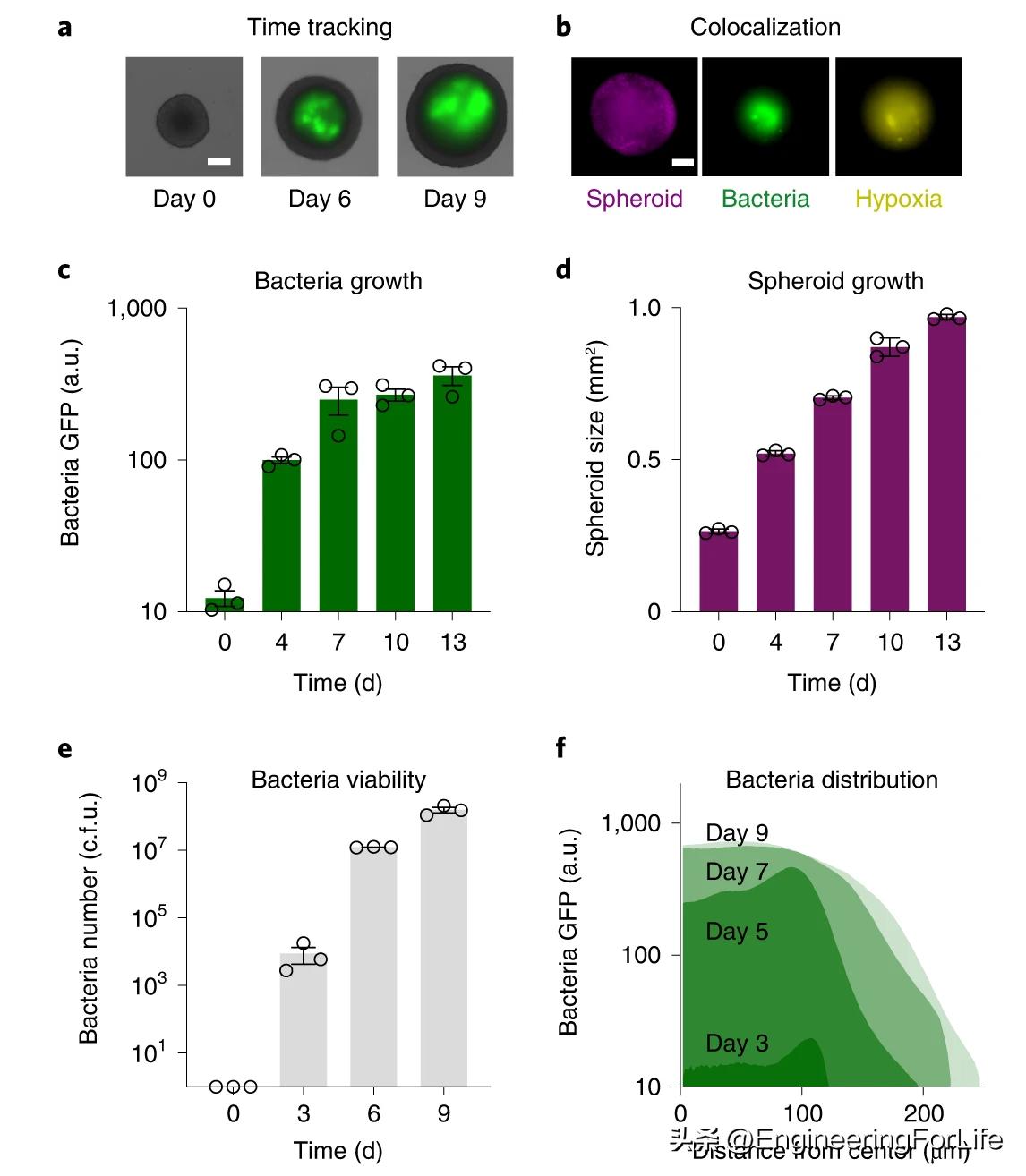
图5.共培养体系中细菌和肿瘤球体的表征
随着时间的推移,维持稳定的共培养能力使该方案适用于细胞动力学的定量监测。我们表征了基因回路的动力学,包括肿瘤球体内的诱导,生物传感和逻辑门构建。通过在培养基中添加诱导剂并通过延时显微镜监测动力学来测试小分子AHL诱导电路(图6a–c)。这揭示了诱导时sfGFP信号的增加,在肿瘤核心附近的约4小时达到最大表达(图6de)。利用3D肿瘤模型提供的自然肿瘤环境,我们还测试了细菌感知肿瘤缺氧,乳酸和酸度的能力。将两个生物传感器耦合到细菌生长,构建了一个AND逻辑门系统,其中细菌只有在遇到两个信号时才允许增殖(图6f)。通过与肿瘤球体共培养来测试细菌的性能,证明工程细菌能够感知肿瘤球体中的环境并响应生长(图6g)。
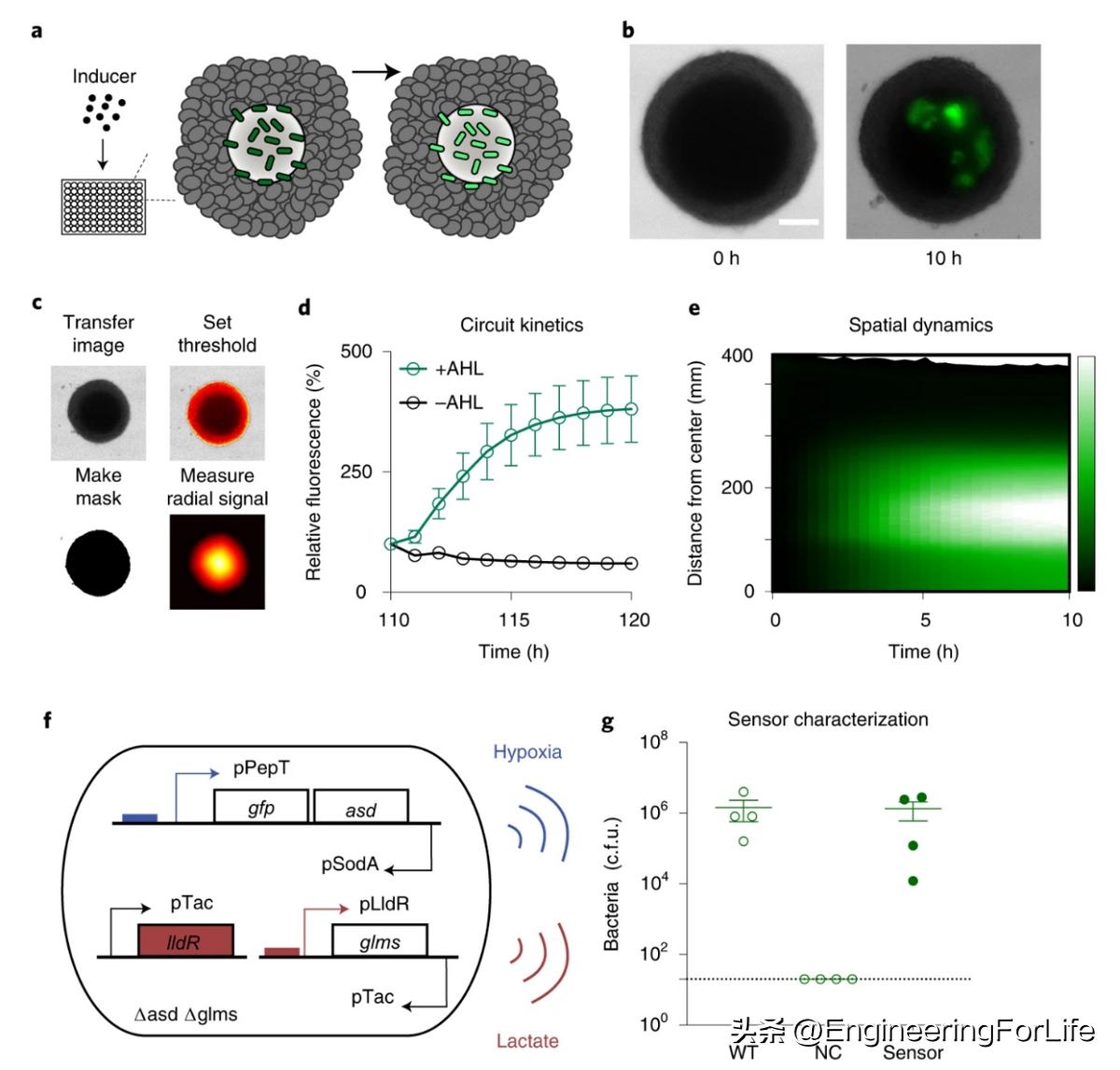
图6. 肿瘤球体中的基因回路性能
该共培养方案与标准的96孔兼容,允许高通量药物测试(图7ab)。由于细菌的癌症治疗研究通常只测试有限数量的治疗有效载荷,并且通常不会并排比较,因此我们测试了可表达细胞毒性抗肿瘤有效载荷库的细菌的功效。当细菌定植在CT26球状体核心上时,我们诱导治疗成分表达,随后观察到许多治疗方法使得肿瘤球状体生长下降(图7c)。通过测量细菌表达的sfGFP来量化有效载荷表达对细菌的生长负担(图7d)。治疗的球体的组织病理学分析(TUNEL染色)显示治疗后肿瘤球体内的肿瘤细胞死亡(图7e)。为了便于对治疗疗效的机制理解,可以通过分别评估细菌c.f.u.,裂解物和荧光表达水平组合测试各种因素,例如细菌生长、载荷有效性和表达水平等。最后,我们通过使用同源CT26小鼠模型验证了体内疗效。与对照菌株相比,从体外筛选中确定有效的菌株在肿瘤生长中引起反应。对疗效的线性回归分析揭示了其高度相关性(图7f),证明了体外筛选平台的预测能力。
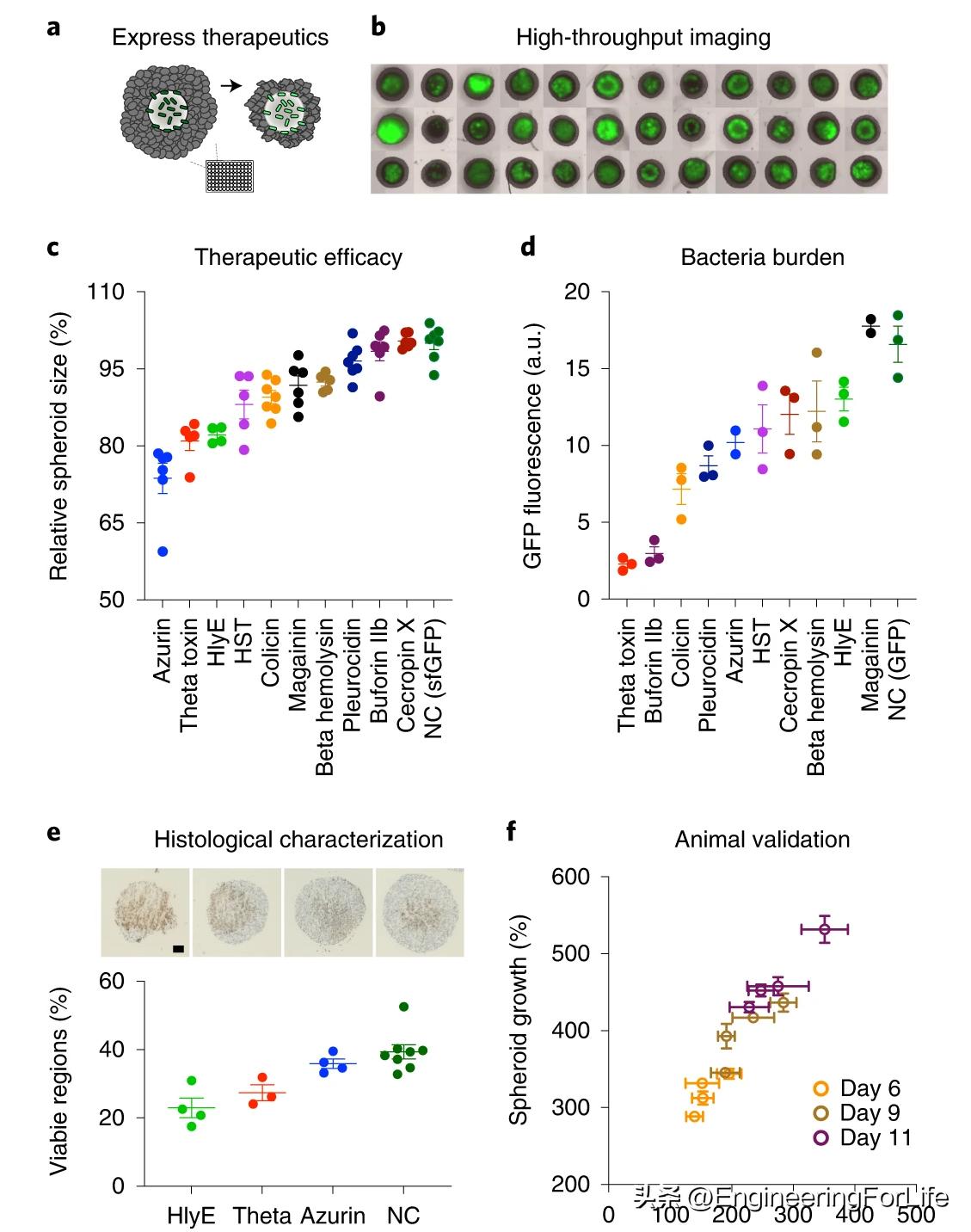
图7.治疗筛查和验证
全文连接: https://www.nature.com/articles/s41596-022-00723-5
入*交群**流
围绕医工交叉领域,EFL建有相关社群,可私信小编入*交群**流~