药物是一种涉及国民健康、社会稳定和经济发展的特殊产品,药物的研发融合了多学科先进技术和高科技产业的精华。近年,医药行业增长速度迅猛,成为国民经济发展最快的行业之一。2016 年,制药产业持续繁荣,同时也呈现出诸多新的特点。本文以2016 年度批准的重磅新药为依据,盘点肿瘤、糖尿病、心血管、阿尔茨海默病、自身免疫性疾病、感染性疾病等治疗领域药物研发的新靶标、新技术、新方法等热点。
2016年,新药研发持续升温,更多新机制新靶标的药物、新的突破性治疗手段问世:肿瘤免疫疗法依旧热度不减,继2015年PD-1*制剂抑**获批,2016年全球首个PD-L1*制剂抑**Tecentriq成功上市,肿瘤免疫疗法的适应症不断扩增,涵盖了更多的肿瘤领域;基因编辑方法成功应用于肿瘤和艾滋病的治疗;抗癌药Lartruvo联合阿霉素用于软组织肉瘤一线治疗,成为40年来重大突破;首个治疗头颈癌的药物——Opdivo获批;科学家首次提出了治疗急性髓性白血病(acute myeloid leukemia,AML)的药物;在治疗慢性淋巴细胞白血病方面,全球首个B 淋巴细胞瘤-2基因(B-cell lymphoma-2,Bcl-2)*制剂抑**Venclexta获美国食品药品监督管理局(FDA)的加速批准;首个治疗帕金森病性精神病的药物Nuplazid问世,成为帕金森病性精神病临床治疗的重大里程碑;FDA批准了首个杜氏肌营养不良(DMD)新药Exondys 51。药物研发不断为人类疾病提供更为精准的治疗手段。
肿瘤:药物研发持续升温
据世界卫生组织(WHO)发布的《全球癌症报告2014》预测,全球癌症病例将呈现迅猛增长态势,由2012年的1400 万人,逐年递增至2025 年的1900 万人,到2035 年将达到2400 万人。新增癌症病例有近半出现在亚洲,中国新增癌症病例高居第一位。抗肿瘤药物是全球医药市场的领军类别,全球抗肿瘤药市场在2008~2013 年复合增长率为7.2%。据艾美仕市场研究公司(IMSHealth)数据统计,2015年全球肿瘤治疗和支持护理药物花费增长11.5%,达1070亿美元。
1)免疫*制剂抑**
近几年,癌症治疗方面最引人瞩目的新方法之一当属癌症免疫疗法。美国癌症研究会发布2016年癌症进展报告显示,2015年8月1日至2016年7月31日,FDA批准了13种新的抗癌治疗药物及11种既往获批抗癌药物的新适应症。在13种新抗癌药物中,4种为免疫治疗药物,免疫疗法正处于快速推进的阶段,并且适用的癌症类型也在不断增加。如免疫检查点*制剂抑**的适应症从最初的黑色素瘤和肺癌扩展到膀胱癌、头颈癌、霍奇金淋巴瘤、肾癌等癌症类型。
在免疫治疗方法中,程序性死亡受体1及其配体(programmed death 1/programmed death ligand 1,PD-1/PD-L1)*制剂抑**是具有代表性的一类。PD-1属于T细胞的抑制性受体,肿瘤细胞通过PD-L1与T细胞表面PD-1结合,产生抑制信号,阻止效应T细胞增殖,不能及时有效地识别危险肿瘤细胞,从而使之逃避免疫细胞追杀。设计阻断PD-1和PD-L1 的单克隆抗体(单抗),是肿瘤免疫治疗手段(图1)。

图1 PD-1/PD-L1 *制剂抑**免疫治疗肿瘤细胞示意
随着首个PD-1单抗的获批,目前FDA已经批准默沙东、百时美施贵宝、罗氏公司的Kertruda、Opdivo 及Tecentriq这3款药物,PD-1/PD-L1类单抗已经开始进入肿瘤的常规治疗。Tecentriq是2016年罗氏旗下基因泰克公司获批的PD-L1类药物,用于膀胱癌的治疗,是30多年来FDA针对特定膀胱癌批准的首个新药,也是FDA 批准的首个PD-L1 抗体,曾先后获得FDA 的突破性疗法认定、优先审评资格及加速审批资格。除此之外,辉瑞公司的PDL1*制剂抑**Avelumab及阿斯利康公司的PD-L1*制剂抑**Durvalumab均已经处于临床III期试验中,有望上市。
近两年,随着国内外PD-1/PD-L1类单抗研发热度的增加,人们也开始尝试使用各种联合疗法,即免疫联合治疗,如百时美施贵宝公司推出的Nivolumab+Ipililumab联合用药,取得了较好的治疗效果;此外,免疫治疗与化疗的联合治疗也取得了一定的效果,如阿特珠单抗与培美曲塞及铂类的抗肿瘤有效率可达77%,被业界广泛看好。肿瘤免疫的目标是唤醒免疫系统的自卫作用及产生靶向抗癌效应,对于缺少免疫抑制而对单一疗法无响应的患者,联合治疗将是一个不错的选择,随着对癌症和免疫系统的深入了解,人们可以期待未来会有更加合理的肿瘤组合治疗方法进入临床。
然而,并不是所有肿瘤对PD-1*制剂抑**都会产生响应,来自埃默里疫苗中心的科学家揭示了一种优化靶向PD-1药物的疗法,发现了T细胞耗竭的系统及PD-1 的免疫制动功能,当被PD-1阻断制剂再次激活时,可以有效区分觉醒T细胞亚群的分子特性,T细胞通过PD-1实现了复活之路,为其他种类的癌症免疫疗法开发及新型的组合性疗法的设计提供思路。除了PD-1 外,破坏其他物质也能够促进肿瘤免疫反应,一项新的研究表明:一种被称作周期蛋白依赖性激酶5(CDK5)的关卡蛋白,能够允许某些脑瘤细胞(如成神经管细胞瘤)躲避免疫系统检测,是脑瘤免疫治疗的潜在靶标。肿瘤免疫疗法药物开发在改善癌症患者生存和生活质量方面有革命性的进步。
2)细胞生物疗法
肿瘤细胞生物疗法是利用生物技术对自身免疫细胞进行体外活化培养,使其具有高效识别和杀灭癌细胞的能力,再输回患者体内,抑制癌细胞转移和复发,在不破坏机体免疫系统功能的前提下,实现治疗肿瘤的目的,成为近年研究的热点。通过细胞生物疗法,人们尝试了改造多种人体免疫相关的细胞,目前表现较为出色的是嵌合抗原受体T细胞技术(chimeric antibody receptor engineered T Cell,CAR-T)和T细胞抗原受体T 细胞技术(T cell receptor Engineered TCell ,TCR-T),这两种技术的共同点在于通过基因改造的手段提高T细胞受体对特异性癌症细胞抗原的识别能力和进攻能力,因此也都统称为“T 细胞受体重新定向”技术(Tcell receptor redirection)。CAR- T/TCR-T技术能够表达特异性受体,靶向识别特异性的肿瘤细胞,受到广泛的关注和研究,由于需要肿瘤细胞有比较特异的抗原分子,故在血液肿瘤中表现出广阔的应用前景,近两年也取得了令人欣喜的成绩:风筝制药(Kite Pharma)治疗非霍奇金淋巴瘤的KTE-C19临床试验显示出高效治疗效果,诺华(Novartis)治疗儿童B 细胞急性淋巴细胞白血病的CTL019获得了快速审批资格,二者均有望获批上市。2016 年7月,CD19-CAR-T三巨头之一的朱诺公司(Juno)由于患者死亡事件,备受期待药物JCAR015 的上市时间被搁置,另有Cellectis公司的UCART19临床试验结果也较为积极。近期,生物疗法也开始尝试在实体肿瘤中的应用,但安全性问题一直是这一技术难以克服的障碍。
利用人体免疫作用,激发人体自身的免疫防御抵抗疾病的治疗方法,在肿瘤免疫治疗中还有其他的尝试,在近期一项新的研究中,德国研究人员开发出一种抵抗癌症的病毒模拟物:将一种含有癌症RNA的纳米颗粒组成的病毒模拟物导入人体,它们随后潜入特定的被称作树突细胞的免疫细胞中,让人体发起抗病毒免疫攻击,从而治疗癌症。
3)基因编辑技术助力肿瘤药物研发
基因编辑技术(如CRISPR-Cas9)于1987年提出,是取自于细菌对抗外来病毒入侵的一种基因编辑器,具有优秀的基因修饰能力,细菌CRISPR系统能够识别外来病毒基因,利用自身的CRISPR-Cas9剪切体进行精准删除实现遗传免疫,从基因层面治疗疾病,目前已经在多个领域中开始尝试。基因编辑技术治疗肿瘤的原理在于,将肿瘤形成基因作为目标基因,构建人体CRISPR-Cas9剪切系统,对人体细胞的肿瘤基因进行精准剪切修饰,达到治疗的目的。2016年,四川大学华西医院卢铀团队采用基因编辑CRISPR-Cas9技术,以PD-1 为目标基因,将患者外周血或肿瘤组织*特中**异性T细胞提取出来,利用CRISPR-Cas9系统敲除PD-1基因,修饰后重新输肺癌患者体内发挥抗癌作用。该研究在全球引起广泛关注,为基因编辑技术与肿瘤的治疗相关研究开辟了新的里程。
糖尿病:复方药物或成主流
糖尿病是困扰人类健康的重大疾病,根据国际糖尿病联盟(Interntionl Dibetes Federtion,IDF)统计,2015年全球糖尿病患者约有4.15亿人,中国糖尿病患者也将达到1.51亿,居世界首位。尽管糖尿病市场已较为成熟,但在临床上仍需要突破性的治疗方式,由于糖尿病发病机制的复杂性,一种药物难以取得良好治疗效果,糖尿病复方药物成为近年批准的热点。2016 年,FDA 批准的糖尿病复方制剂有赛诺菲公司的Soliqua,其成分是来得时(甘精胰岛素)和Lixisenatide(GLP-1受体激动剂);诺和诺德公司的复方制剂Xultophy,该药由Tresiba(Insulin degludec,德谷胰岛素)和Victoza(liraglutide,利拉鲁肽)组成,在此之前,FDA 已经批准了默沙东的二肽基肽酶Ⅳ(Dipeptidyl peptidase-4,DPP4)*制剂抑**和二甲双胍的复方制剂捷诺达,另有武田制药2016年底在日本推出了2型糖尿病复方新药Inisync(阿格列汀/二甲双胍),几乎同一时间,勃林格殷格翰-礼来糖尿病联盟合作开发的2 型糖尿病复方新药Synjardy XR(Empagliflozin/盐酸二甲双胍缓释片)获得FDA批准,用于2型糖尿病成人患者的治疗。在糖尿病领域制药巨头的推动下,糖尿病药物可能会掀起一场复方制剂占据主流治疗市场的革命。
除此之外,糖尿病的心血管并发症在2016年也取得了突破性进展。糖尿病会增加患者发生心脏病、中风等疾病的风险,会显著影响糖尿病患者的身体健康,缩减预期寿命。据估计,在全球范围内,大约有50%的2型糖尿病死亡病例是由心血管疾病引起,因此,该领域迫切需要一种能有效降低这种并发症的糖尿病药物,与此同时,对糖尿病药物的心血管试验的评价也成为近年药物获批的主要依据。2016 年,全球首个可降低心血管死亡风险的降糖药Jardiance(恩格列净)获美国FDA批准,标志着并发心血管疾病的2型糖尿病患者群体在临床治疗上的一个重大里程碑。Jardiance是一种钠-葡萄糖协同转运蛋白-2(SGLT-2)*制剂抑**类药物,在保证总体安全性的前提下,能够显著降低心血管疾病的死亡率(图2)。
图2 10 mg 恩格列净/5mg 利格列汀和25 mg 恩格列净/5 mg 利格列汀两种剂型(图片来源:药物在线)
除此之外,2016年底,糖尿病巨头诺和诺德向FDA 提交了糖尿病新药Semaglutide(索马鲁肽)的新药申请(NDA),同时也向欧洲药品管理局(EMA)提交上市许可申请(MAA)。Semaglutide是一种新型长效胰高血糖素样肽-1(GLP-1)类似物,业界对Semaglutide的前景十分看好,因为它兼具降糖、减肥、降低心血管风险三大功效,无疑将为心血管高风险2型糖尿病群体提供一种非常重要的治疗选择。研究人员也在积极尝试其他改变患者的依从性的方法,近期一项研究使用Cholestosome 技术成功地将胰岛素胶囊化,使口服胰岛素成为一种可能。
心血管:药物研发突破性点少
心血管疾病是全球第一位死亡原因,也是中国高患病率、高病死率的第一大慢性疾病。据世界卫生组织统计,全球每年心脏病导致1700 多万人死亡。心血管药物研发技术难度大,监管对安全性和有效性的要求高,一直被医药产业视为雷区,近年突破性治疗新药也较少。最受瞩目的当属2015年安进公司降脂药PCSK9*制剂抑**依伏库单抗(Evolocumab,商品名Repatha)。2016年,安进公司公布了Repatha治疗心脏疾病的关键III期临床试验数据,表明该药联合他汀类药物能够显着降低患者的冠状动脉粥样硬化症,这一数据也开启了Repatha 除了降低胆固醇之外的其他心血管适应症。
高血压是世界上导致死亡的最重要因素之一,也是中国高发病率性疾病。然而对于这样一个世界性严重疾病,在最近的13年里,只有一款治疗药物在2007年问世,已有药物的副作用及患者的抗性也成为许多药物发挥疗效的限制因素,临床需求远未被满足。近期,一项针对人颈动脉体的研究为新药开发带来了希望,许多高血压患者血压难以控制的主要原因是由于颈动脉的高反应性,这种高反应性被认为是由嘌呤P2X3受体(purinergic P2X3 receptor)的过度表达引起,在高血压患者身上也观察到P2X3水平的显著上升,这就意味着,以P2X3为靶标的*制剂抑**可能成为创新降压新策略,目前Afferent制药开发P2X3*制剂抑**AF-130用于治疗难治性高血压处于I期临床研究中,该公司已被默克制药收购。
此外,得益于精准医疗的发展,研究人员证实,先对心脏病患者基因型进行分类以精确定位药物的适用人群,可降低未来开发该药物的成本。药物基因组学方面研究也有相应进展:安进全资收购的子公司deCODE genetics近期找到了一种保护心脏的罕见基因突变——ASGR1。携带该基因突变的人,患冠心病的风险降低35%,该发现成为有史以来降低冠心病风险最大的基因变异,ASGR1 无疑会是心血管疾病新靶点。同样地,利用人类基因组数据建立全新药物发现模型,还可以预测药物疗效等。
阿尔茨海默病:药物开发艰难中前行
阿尔茨海默病(Alzheimer Disease,AD)是一种起病隐匿的进行性发展的神经系统退行性病症,属神经精神性疾病,当前药物无法治愈。目前FDA 批准的AD治疗药物可包括两种:一种属胆碱酯酶*制剂抑**,如多奈哌齐、卡巴拉汀、加兰他敏;另一种为N-甲基-D-天门冬氨酸受体阻滞剂美金刚胺。过去17年里,仅有这四4种药物获批,另有100多种临床失败或未获批药物。AD药物研发难度大、失败率高,已经被各大制药公司的折戟所证明。2016年11月下旬,礼来宣布其投入数亿美元研究经费的AD药物β淀粉样蛋白抗体Solanezumab的III 期临床试验没有达到预期结果,引起业界一片唏嘘,在此之前,辉瑞/强生的Bapineuzumab、罗氏的Gantenerumab等已经在III期临床试验中付出了惨痛的代价。
通过对病理机制的探寻,AD治疗未来可能的治疗靶点为β-淀粉样蛋白、BACE(β-secretase)*制剂抑**、Tau 蛋白等。尽管礼来β淀粉样蛋白抗体研发失利,人们对β淀粉样蛋白并未失去信心。Biogen的同类药物Aducanumab仍然充满期待,该药于2016年9 月获FDA 快速审批资格,近期公布的临床1b 期(PRIME)研究的最新数据表明,针对早期AD 的治疗功效显著,目前正在进行全球性临床III期评估,成为挽救β淀粉样蛋白机制的一线生机。
AD发病机制复杂,药物开发人员不断探索新的突破点,2016年AD药物研发创新点很多:近期,一项最新的研究表明人们有望开发出首个治疗阿尔兹海默病的疫苗,该研究来自于瑞典卡罗琳学院,该疫苗能够刺激特异性地靶向作用AD病理状态的Tau蛋白的特殊抗体的产生,临床I期试验数据已经公布;在发表于《Science Translational Medicine》的研究报告中,研究人员通过研究开发了一种新型抵御AD 的疗法,该疗法利用了一种名为verubecestat的化合物,通过阻断患者机体的β-淀粉样前体蛋白裂解酶1(Beta-site amyloid precursor protein cleaving enzyme 1,BACE1)酶来降低β 淀粉样蛋白的水平,且该疗法并不会给患者带来任何毒副作用;来自帝国理工学院的研究人员通过利用病毒将特殊的基因片段运输到小鼠大脑中,从而成功抑制小鼠患AD,该研究或为AD 等神经性疾病的新型疗法的药物开发提供思路;来自隆德大学和MIT的研究人员通过合作在原子分辨率水平下同时成功阐明了β淀粉样蛋白肽类1-42原纤维的清晰结构,结构生物学的研究为开发治疗AD的新型药物提供思路;另有一项关于*麻大**及其化合物能够β淀粉样蛋白从细胞中移除的研究引起了业界的关注,研究人员初步明*麻大**中的四氢*麻大**酚和其他化合物可以促进β淀粉样蛋白从细胞中移除,该研究或为药物发现提供思路。
自身免疫性疾病:生物药研发占主导地位
自身免疫性疾病是机体对自身抗原发生免疫反应而导致自身组织损害所引起的疾病,临床常见的类风湿关节炎、系统性红斑狼疮、银屑病等均属自身免疫性疾病,该类疾病无法治愈,死亡率虽不高,但严重影响患者生活质量。由于免疫系统的特异性,近年,大分子药物在该领域的治疗取得了前所未有的成功,多种单克隆抗体类生物制剂成为全球畅销药,如修美乐、恩利等,时至今日,它们的适应症仍在逐步增加。但各类重磅药物专利也陆续开始到期,生物仿制药对自身免疫性疾病的治疗市场会产生一定的冲击。
1)类风湿关节炎
类风湿关节炎(RA)具有多维度性,患者个体病程进展差异较大,缺乏单一有效的普遍性治疗药物,临床治疗药物主要有抗炎药、抗风湿药、激素类药物、生物制剂、联合用药、免疫重建等。近10年来,靶向性更高、毒性更小的生物药物的出现对RA 的治疗发挥了巨大的作用,越来越多治疗RA生物制剂获得批准,靶标主要是肿瘤坏死因子(TNF)和白细胞介素类。2016年,以白介素-6(IL-6)受体为靶标成功被开发出来:Sarilumab 是首个直接靶向白介素-6(IL-6)受体的全人源化单克隆抗体,由Regeneron与赛诺菲公司利用其特有的Veloclmmune 抗体技术开发,该抗体能够阻断IL-6与其受体的结合,中断细胞因子介导的炎症信号级联,Sarilumab用于活动性、中度至重度RA的治疗,临床试验效果优于修美乐,已提交上市申请。Sarilumab被业界普遍看好,全球知名医药市场研究机构Evaluate Pharma 发布报告,预计Sarilumab在2020年的销售峰值将达到18亿美元。此外,另一医药巨头强生旗下杨森生物科技同样开发出一种实验性人抗细胞IL-6单克隆抗体Sirukumab,可高亲和力和特异性地结合细胞因子IL-6,抑制IL-6 介导的炎性作用。Sirukumab 已向FDA 提交皮下注射剂型生物制品许可申请,寻求用于对一种或多种疾病修饰抗风湿药物(DMARDs)治疗失败或不耐受的中度至重度RA成人患者。
2)系统性红斑狼疮
系统性红斑狼疮(SLE)是一种慢性、不可治愈的自身免疫性疾病,累及人体多个器官。如果病情得不到控制,将会导致严重的后果,包括长期的器官损伤甚至过早死亡。Benlytsa(贝利木单抗,静脉输注剂型)是2011年获得美国和欧盟批准用于自身抗体阳性的SLE 成人患者的治疗的药物,是近50多年来获批用于治疗SLE的首个新药,在此之前,美国FDA仅于1948年批准阿司匹林、1955 年批准羟基氯喹和皮质激素治疗狼疮,因此Benlytsa的上市具有划时代的意义。在美国和欧盟,葛兰素史克公司于2016年9月提交了皮下注射剂型Benlysta 的上市申请文件。Benlysta是首个B淋巴细胞刺激因子(B lymphocyte stimulator,BLyS)特异性*制剂抑**,能阻断可溶性BLyS(一种B细胞生存因子)与B细胞上的BLyS受体的结合,抑制B细胞的生存、减少B细胞向制造免疫球蛋白的浆细胞的分化。Benlysta已向日本卫生劳动福利部(MHLW)提交了新药申请,并有意向中国监管机构提交上市申请。
目前中国临床治疗并没有专门针对红斑狼疮的药,临床以糖皮质激素联合使用非特异性抗炎、免疫*制剂抑**来缓解病程。2016 年,昆药集团拟向中国中医科学院中药研究所购买其所持有的诺贝尔奖获得者屠呦呦团队开发的“双氢青蒿素片新适应症-红斑狼疮研发项目”临床前研究所取得的相关专利及临床批件,有意开发治疗SLE新药,弥补目前SLE治疗领域的空白,具有广阔的市场开发价值。
3)银屑病
近两年,银屑病药物开发较快,除了老牌重磅单抗修美乐之外,2015年,瑞士制药巨头诺华的全球首个IL-17单抗Cosentyx(Secukinumab)已经抢先上市,另有默沙东IL-23拮抗类单抗产品MK-3222(Tidrakizumab)及强生IL-23拮抗类单抗产品Guselkumab正在申请上市。2016年3 月,礼来的IL-17A单抗Ixekizumab获得了FDA批准,商品名为Taltz。此外,与RA 一样,小分子治疗药物也开始在银屑病治疗领域发挥作用,已获批治疗RA新颖的口服Janus 激酶(JAK)*制剂抑**Xeljanz(Tofacitinib)目前正在银屑病治疗临床试验中,也是目前唯一个银屑病小分子JAK*制剂抑**,如果获批,将为活动性银屑病关节炎患者群体提供一个重要的治疗选择。
感染性疾病:吉利德公司领先优势明显
病毒是引发人类多种感染性疾病的主要原因,抗病毒药作为抵抗病毒感染的重要产品,在感染性疾病治疗中发挥重要的作用。吉利德公司拥有着强大的感染性疾病药物研发管线,数个重磅药物占领全球艾滋病(HIV)、丙肝(HBV)等细分市场。近年来,其研发并上市的抗HIV感染系列药物几乎垄断了整个HIV市场,2013年,其革命性的产品、“超级重磅*弹炸**”级丙肝新药索非布韦的问世,使之一跃成为丙肝市场的绝对领导者。
1)丙肝
吉利德几年内相继推出了多种口服丙肝治疗药物:2013年,首个丙肝明星药Sovaldi(索非布韦)获批上市,它是一种丙型肝炎病毒核苷酸类似物NS5B聚合酶*制剂抑**(图3);2014年,吉利德首个索非布韦的复方制剂——丙肝鸡尾酒Harvoni疗法(索非布韦/雷迪帕韦)获批,用于治疗基因1型的丙型肝炎感染;2016年,泛基因型丙肝鸡尾酒Epclusa 获批,是索非布韦与新药Velpatasvir的固定组分复方,用于全基因型(基因型1,2,3,4,5或6)丙型肝炎成年感染者,筑成了该公司丙肝强大阵营。在2016年,吉利德又提交了丙肝新药SOF/VEL/VOX(Sovaldi、Velpatasvir、Voxilaprevir)的申请,它作为一种补救治疗药物,用于既往接受直接作用抗病毒方案治疗失败的丙肝患者群体,包括NS5A*制剂抑**治疗失败、无肝硬化或伴有代偿性肝硬化的全部6种基因型丙肝患者,填补了丙肝治疗领域目前尚未完成的最后一块拼图。
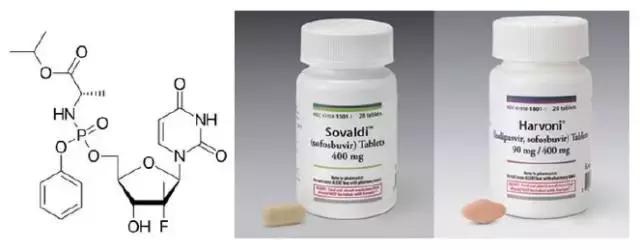
图3 索非布韦分子结构、单药及其复方Harvoni
在丙肝治疗领域,还有百时美施贵宝的Daclatasvir、艾伯维的Dasabuvir及默沙东的Elbasvir,都是目前治疗丙肝有效的药物。但据吉利德公司数据显示,对于既往接受的作用抗病毒方案治疗失败的患者而言,SOF/VEL/VOX 是一种安全性好、治愈率非常高的有效治疗方案。
2)乙肝
据估计,在全球范围内有多达3.5~4亿乙肝患者,乙肝可导致肝硬化,是全球80%原发性肝癌的直接病因。中国是乙肝病患较重的国家,据保守估计,全国13亿人口中有1亿慢性乙型肝炎病毒(HBV)感染者,约占全球乙肝携带者的1/3。吉利德在乙肝治疗领域的表现也较为精彩,2016年,用于慢性乙肝成人感染者治疗药物Vemlidy(TAF,替诺福韦艾拉酚胺富马酸)获得FDA批准,它是一种新型核苷类逆转录酶*制剂抑**(NRTI),该药是吉利德已上市药物Viread(替诺福韦酯,TDF)的升级版。在临床试验中,TAF已被证明在低于TDF 十分之一剂量时,就取得了非常好的抗病毒疗效,同时具有更好的安全性。目前,TAF已经获得欧洲和日本的积极意见,有望近期上市。
另外,2016年初,美国生物技术公司Arrowhead 发布旗下乙肝候选药物ARC-520临床IIb期积极数据,通过与百时美施贵宝(BMS)乙肝药Baraclude联合,用于治疗难治性HBeAg 阴性慢性乙型肝炎患者。结果显示,ARC-520+Baraclude 治疗组,患者血清HBVDNA水平可显著降低99.99%,效果震惊业界。ARC-520,是一款基于RNA干扰(RNAi)技术设计的药物,通过作用于信使RNA(mRNA)靶点,干扰乙肝病毒逆转录过程,用于治疗慢性乙型肝炎。
3)艾滋病
近年来,中国HIV感染人数呈增长趋势。在HIV药物治疗中,吉利德也占据有着一定的优势,目前其旗下拥有9款抗HIV 药物,包括Genvoya、Viread、Stribild、Emtriva、Truvada 等,形成垄断之势。2016年,新产品TAF的临床III期试验数据也显示出了对HIV的治疗效果,成为其感染性疾病领域的又一重磅药物。其他公司如葛兰素史克药物Triumeq 也逐渐扩大其市场,争取在HIV市场分一杯羹。
HIV其他研发方面,有研究表明,一种实验性疫苗与一种先天性免疫刺激剂结合在一起可能有助导致HIV感染者体内的病毒缓解。此外,结构生物学家近期解析出了HIV包膜详细的三维结构,被称为包膜糖蛋白三聚体,绘制出了底部脆弱位点图及能够中和HIV抗体结合位点图,为药物开发提供更多的生物学基础。
结论
2016 年,药物研发继续保持增长势头,尽管FDA 批准的新分子药物数目远远低于2015年,但不乏新的药物治疗理念和明星药物的出现,制药产业持续繁荣,研发产品线不断扩张,医药企业重组并购规模不断扩大。与此同时,药物创新研发热情不减,人们对行业研发创新难度认知也不断增加。特别是,创新成为行业的一致追求,大型制药公司正在引导行业走向一个新的创新阶段,而具有灵活性的小型研发公司也在不断为新药研发提供新鲜血液,尤其给中国制药企业带来新的机遇。(责任编辑 田恬)
本文作者:刘丽丽,毛艳艳,高柳滨
作者简介 :刘丽丽,中国科学院上海药物研究所信息中心,博士,研究方向为药物情报学;高柳滨(通信作者),中国科学院上海药物研究所信息中心,研究馆员,研究方向为情报学。
注 :本文发表在2017年第1期《科技导报》,欢迎关注。