PD-1/PD-L1类药物自研究初就备受关注,这是因为PD-1/PD-L1免疫疗法作为新型抗癌疗法的治疗效果显著,在黑色素瘤、肺癌、膀胱癌、头颈癌、霍奇金淋巴瘤、肾细胞癌和多种血液系统恶性肿瘤的临床试验中表现出极大优势,各制药巨头、临床医生、癌症患者都对这类药物抱有极高的期望。
免疫系统在人体抗癌过程中发挥着极其重要的作用,肿瘤细胞作为抗原,可以激活T细胞免疫应答,从而使T细胞发挥作用杀死肿瘤细胞。

免疫系统与癌症
T细胞识别体内正常细胞和非正常细胞(包括肿瘤细胞)靠的是细胞表面的抗原。一般来说,正常细胞表面会表达PD-L1,PD-1在T细胞表面表达,当PD-1和PD-L1结合时T细胞将其视为正常细胞,就不会发起免疫攻击。细胞不表达PD-L1时,与T细胞表面的PD-1无法结合,两者之间就失去了信号交流,这时T细胞就会把它当作有害细胞,发动免疫攻击。然而,某些肿瘤细胞为了生存,表达大量的PD-L1,能与T细胞表面的PD-1结合,使T细胞将其视为正常细胞,从而逃避免疫攻击。

肿瘤细胞如何逃避T细胞的免疫攻击
而PD-1/L1*制剂抑**能够阻断PD-1/PD-L1通路,促使免疫T细胞发动攻击。
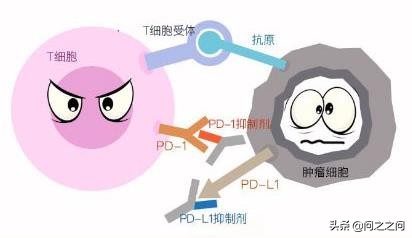
PD-1抗体药物作用原理
简单地说,PD-1/PD-L1免疫疗法就是通过药物阻断PD-1/PD-L1通路,激活人体自身的免疫系统攻击肿瘤细胞,也可能攻击正常组织。该疗法的突出特点是对癌症的持久控制,而且对多种癌症有效。
国外PD-1抗体药物
Nivolumab/ Opdivo(纳武单抗,也称为O药)是全球上市的第一种PD-1药物。
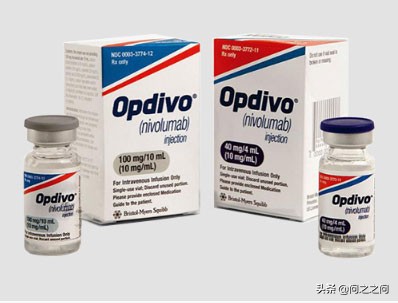
Nivolumab/ Opdivo,O药
2014年12月22日,被批准用于单药治疗BRAF V600野生型或突变型的手术无法切除或转移性黑色素瘤患者或与伊匹单抗合用治疗手术无法切除或转移性黑色素瘤患者;2015年10月9日,被批准用于接受铂类化疗期间或之后出现疾病进展的晚期(转移性)非小细胞肺癌患者;2015年11月23日,被批准用于治疗已接受过抗血管生成治疗的晚期(转移性)肾细胞癌患者;2016年5月17日,被批准用于经自体造血干细胞移植(HSCT)及brentuximab vedotin治疗后疾病复发或进展的典型霍普金淋巴瘤患者;2016年11月10日,被批准用于接受铂类化疗治疗期间或治疗后疾病发生进展的复发性或转移性鳞状细胞头颈癌;2017年2月2日,被批准用于治疗局部晚期或转移性尿路上皮癌患者。
Pembrolizumab/Keytruda(派姆单抗,也称为K药)是另一种PD-1药物。

Pembrolizumab/Keytruda,K药
2014年9月4日,被批准用于治疗无法手术或晚期的黑色素瘤患者;2015年10月2日,被批准用于接受其他治疗后疾病进展且肿瘤表达PD-L1蛋白的晚期(转移性)非小细胞肺癌患者(NSCLC);2016年8月5日,被批准用于经铂类化疗治疗期间或治疗后疾病发生进展的复发性或转移性头颈鳞状细胞癌(HNSCC)患者;2017年3月14日,被批准用于治疗难治性经典型霍奇金淋巴瘤成人和儿童患者,或经受过3种或3种以上前期治疗后疾病复发的患者;2017年5月10日,被批准与培美曲塞和卡铂联用作为转移性非鳞状非小细胞肺癌患者的一线用药;2017年5月18日,被批准用于治疗局部晚期或转移性尿路上皮癌;2017年5月23日,被批准用于治疗带有高微卫星不稳定性(MSI-H)或错配修复缺陷(dMMR)的成人及儿童实体瘤患者,包括经治疗疾病进展和无有效替代疗法选择的患者。
但在国内却迟迟没有上市,原因很简单,这两种药物上市时间较晚,还没来得及在中国进行临床试验(人种差异),癌症患者和临床医生翘首以盼。
进口PD-1抗体药批准上市
终于,2018年06月15日,国家药品监督管理局批准纳武利尤单抗注射液(Nivolumab,即O药)进口注册申请,用于治疗表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性、既往接受过含铂方案化疗后疾病进展或不可耐受的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。纳武利尤单抗注射液也是我国批准注册的首个以PD-1为靶点的单抗药物。

纳武利尤单抗注射液获批上市
2018年7月20日,帕博利珠单抗注射液(Pembrolizumab,即K药) 正式获国家药监局批准,用于治疗一线治疗后疾病进展的局部晚期或转移性黑色素瘤患者,Keytruda成为国内唯一获批的针对这一患者人群的PD-1*制剂抑**。
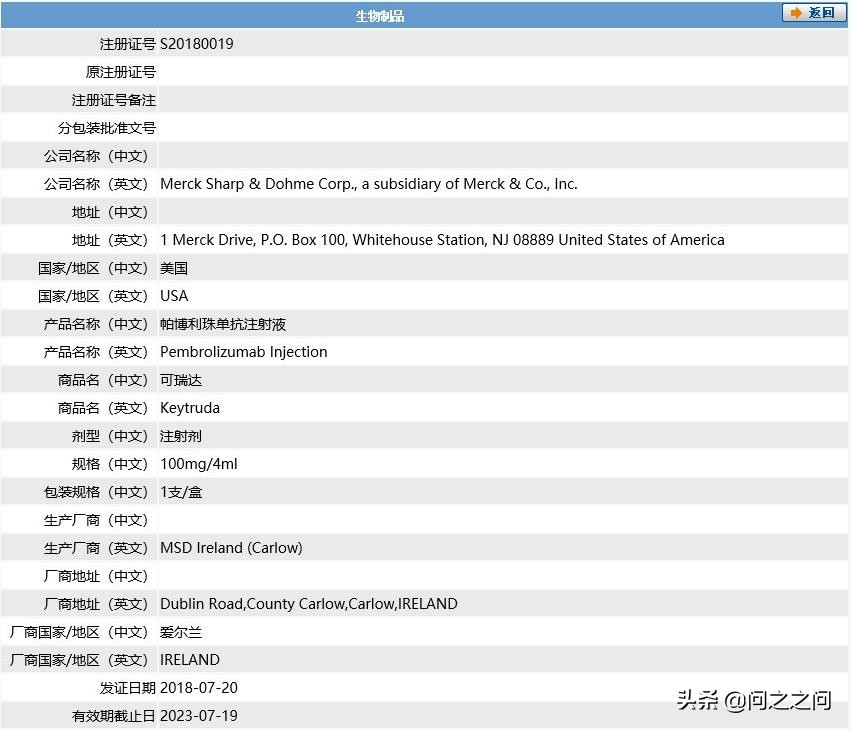
帕博利珠单抗注射液获批上市
然而,上市的这两种PD-1抗体药物均为进口药,价格高昂,使得绝大多数患者望而止步!
国产PD-1抗体药批准上市
这时有一重磅消息袭来,2018年12月17日,首个国产PD-1抗体药物特瑞普利单抗注射液获批上市,这是我国企业独立研发、具有完全自主知识产权的生物制品创新药品,用于治疗既往标准治疗失败后的局部进展或转移性黑色素瘤。
首个国产PD-1抗体药物特瑞普利单抗注射液获批上市
紧接着,2018年12月28日,又一个国产PD-1抗体类药物信迪利单抗注射液(Sintilimab Injection)注册申请获得国家药品监督管理局批准,用于治疗经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤,也是我国企业自主研发并拥有完全自主知识产权的1类创新药。
又一国产PD-1抗体类药物信迪利单抗注射液获批上市
至此,国产抗肿瘤创新药喜讯频传、大快人心!一方面,是因为PD-1抗体类药物全球的起步都比较晚,而中国在生物医药领域紧追不舍,可以说PD-1类药物的研发与国外保持同步水平,所以国产创新药才迎来新的春天。另一方面,在国务院政策的支持下,国家药品监督管理局在加快国外抗肿瘤药品进口上市的同时,积极鼓励和支持国产企业研发申报,并通过采取早期介入、全程指导、优化程序、及时跟进等方式,加快推进国产创新药的注册上市,对于国产抗癌新药纳入优先审评审批品种予以加快审评审批。
可以说,国家对创新药的研发操碎了心,也是为了提升药品质量,提高广大患者临床用药的安全性和可及性,真正让中国老百姓买得起药、看得起病!
目前恒瑞医药、信达生物、百济神州和君实生物均有PD-1抗体药在研,均已进入临川试验阶段,有望在2019年获批上市。我们也相信会有越来越多的国产医药企业生产出创新药,将我国的医药研发实力推向世界前沿。