近年来,随着对结直肠癌发生、发展及耐药机制认识的深入,基于分子分型以及患者体力特征的个体化治疗日益增多,一定程度改善了患者的预后。在此背景下,如何合理为结直肠癌患者制定更精准的治疗策略成为了领域内关注的又一个重点。 岁月不居,时节如流。值此2022年岁末之际,在《胃来肠新 年度回顾》学术活动的《回顾22年mCRC的相关治疗进展》专题分享中,回顾总结了2022年度国际会议中转移性结直肠癌(mCRC)最新治疗进展、探讨“精准施策”,为临床提供更多用药参考。本文整理精彩内容如下,以飨读者。
mCRC的疾病危害及各大会议对mCRC治疗进展的重视
结直肠癌是一种高发的恶性肿瘤,从全球流行病学数据来看,结直肠癌呈现发病率高、死亡率相对较低的特点。其中,中国年龄标准化发病率和死亡率分别为23.9/10万、12.0/10万,与全球发病率和死亡率仍有一定差距,在延长结直肠癌患者生存、改善其生活质量方面任重道远。近年来,在肿瘤领域专家们的积极探索下, mCRC的可选治疗方案越来越多,包括化疗、靶向治疗、免疫治疗及多种联合方案,显著延长了mCRC患者的总生存期(OS)。如何基于现有治疗药物,进一步合理布局、规范用药,为患者带来最大化的生存获益,是临床医生始终孜孜以求的方向。在2022年美国临床肿瘤学会胃肠道肿瘤研讨会(ASCO-GI)、美国临床肿瘤学会(ASCO)、欧洲内科肿瘤学会(ESMO)等国际学术会议中,肠癌领域口头报告、摘要合计501篇,其中mCRC治疗相关内容占45%,足见领域内学者们对mCRC治疗探索的重视。

mCRC晚期一线治疗,更多关注RAS/BRAF 野生型/突变型患者和老年/不适合强烈治疗的mCRC患者的治疗方案优化
(1) RAS/BRAF野生型mCRC: 临床主要聚焦点为优化治疗方案(三药 or 两药)和降低治疗强度(间歇 or 维持)。最新研究进展,如2022 ASCO报道的IMPROVE研究[1]、TRIPLETE研究[2]和ESMO报道的CAIRO5 研究[3]、ERMES试验[4],这些研究表明对于RAS/BRAF野生型患者一线治疗采用三药化疗联合抗EGFR单抗治疗效果并不优于两药化疗联合抗EGFR单抗,且还会增加不良反应发生率;维持治疗阶段采用单药维持治疗或间歇性治疗效果不劣于持续治疗。
(2) RAS/BRAF突变型mCRC: 对于RAS/BRAF突变型患者,给予三药联合治疗可获得更长的OS。CAIRO5研究[5]提示,与两药化疗+贝伐珠单抗相比,RAS/BRAF V600E突变型患者使用三药化疗+贝伐珠单抗可延长无进展生存期(PFS)和客观缓解率(ORR),不良反应增加但可控。此外,化疗+靶向+免疫联合治疗在该类患者中初见曙光,NIVACOR研究[6]表明,纳武利尤单抗+FOLFOXIRI+贝伐珠单抗在未经治疗的RAS/BRAF突变型mCRC患者中表现出初步疗效和安全性。
(3) 老年/不耐受强烈治疗mCRC: 老年mCRC患者是转移性结直肠癌的高发人群,具有合并症多、不耐受强烈治疗的特点,如何优化老年患者治疗方案,改善患者老年群体生存获益已越来越受到临床专家的重视。一项2022年ASCO-GI的口头报告JCOG1018研究[7],研究提示在氟嘧啶+贝伐珠单抗基础上增加奥沙利铂,可提高ORR,但未获得PFS和OS的延长,且不良事件发生率有所提升。该研究结果提示,在为老年mCRC患者初始治疗方案时,选用含奥沙利铂方案需谨慎。
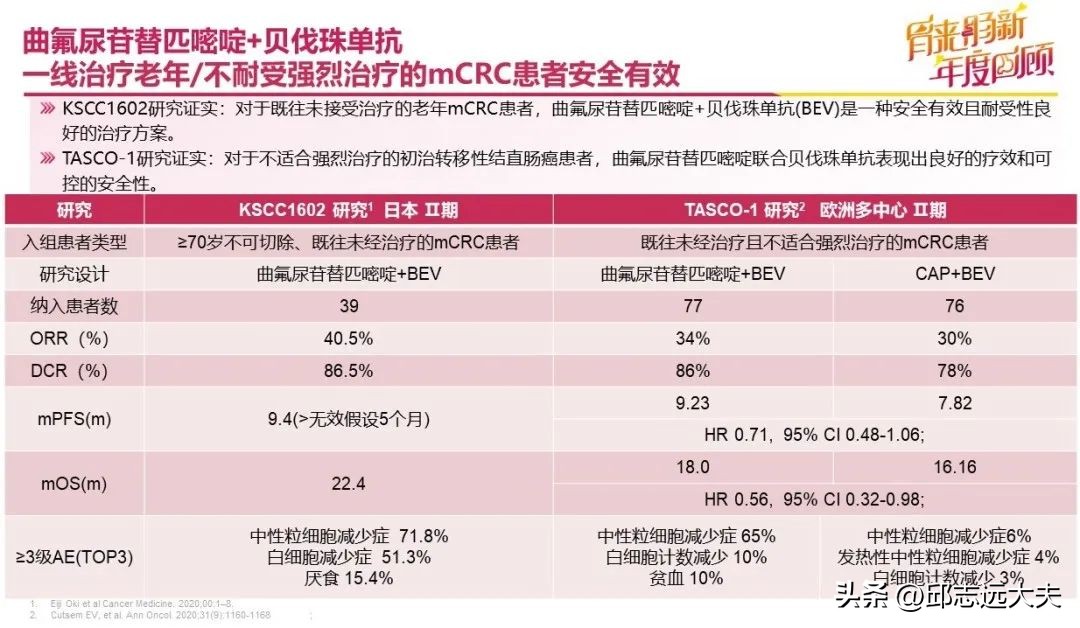
针对老年/不耐受强烈患者的治疗问题,曲氟尿苷替匹嘧啶(通用名简称:FTD/TPI,中文商标:朗斯弗®)开展了KSCC1602和TASCO-1两项研究。KSCC1602研究[8]入组的患者为≥70岁以上的老年mCRC初治患者,给予FTD/TPI联合贝伐珠单抗的治疗方案,研究结果显示中位PFS(mPFS)达到9.4个月,中位OS(mOS)达到22.4个月。此外针对不适合强烈治疗的mCRC初治患者,FTD/TPI开展了TASCO-1研究[9],研究结果显示:FTD/TPI联合贝伐珠单抗对比卡培他滨联合贝伐珠单抗疗效更好(mPFS:9.2个月 vs 7.8月,mOS:18个月 vs 16个月,HR 0.71,95% CI 0.32-0.98,)。2022版中国肿瘤整合诊治(CACA)指南也推荐对于不适合强烈治疗的患者,一线治疗可选择FTD/TPI联合贝伐珠单抗的治疗方案。
mCRC晚期≥二线治疗,更多从分子分型角度关注KRAS G12C突变患者、MSI-H和MSS型患者,进行治疗方案探索
(1) KRAS G12C突变mCRC: 2022 ESMO报道了Yasutoshi等[10]和KRYSTAL-1研究[11],其中Yasutoshi研究提示KRAS G12C*制剂抑**(Sotorasib)+抗EGFR单抗用于晚期二线及以后治疗KRAS G12C突变的mCRC患者,疗效较既往报道的Sotorasib单药治疗ORR高了3倍;KRYSTAL-1同样提示KRAS G12C*制剂抑**(Adagrasib)+抗EGFR单抗优于KRAS G12C*制剂抑**单药(ORR:46% vs 19%,DCR:100% vs 86%,PFS:6.9个月 vs 5.6个月),且显示出良好的安全性。更多在研的分子靶向药物也将进一步丰富mCRC患者治疗选择,带来生存获益。
(2) MSI-H/dMMR型mCRC: 对于前线治疗未使用免疫治疗的MSI-H/dMMR型mCRC患者,三线治疗推荐使用PD-1/PD-L1单抗。另外,关于双免联合对比免疫单药的研究也在进行中,其中Checkmate142研究5年生存随访结果提示双免联合治疗可实现更好的生存获益[12]。
(3) MSS/pMMR型mCRC: MSS型患者占mCRC患者比例的95%,对于这些患者的临床治疗也一直在积极探索中,今年ESMO报道的FRESCO-2研究[13]是一项呋喹替尼针对mCRC后线患者的国际多中心随机对照研究,超过90%患者接受过FTD/TPI治疗,超过45%的患者接受过瑞戈非尼的治疗,结果表明,对于FTD/TPI或瑞戈非尼治疗后进展或不耐受的mCRC患者,呋喹替尼可能是又一治疗选择。因此面对三线可选药物TKI和FTD/TPI,如何“排兵布阵”进行“合理选择”也是目前临床治疗的热点问题。2022年ASCO-GI报道了一项针对FTD/TPI和TKI的真实世界研究数据给我们一些用药启示,这项回顾性真实世界研究[14]纳入1477例患者,其中892例(60%)起始使用FTD/TPI治疗,585例(40%)起始使用瑞戈非尼治疗。结果显示FTD/TPI组患者治疗的持续性和依从性更高;处方数量上,FTD/TPI组患者在治疗期间接受多次处方的比例高于瑞戈非尼组,可见FTD/TPI为mCRC后线治疗选择合适的药物提供更多参考。
对于MSS型mCRC患者的联合治疗也一直是临床探索的热点问题,自2019年REGONIVO研究开启了TKI类药物联合免疫治疗的研究尝试后,多项瑞戈非尼联合免疫治疗的II期小样本探索性RCT研究陆续开展。此外,参照“REGONIVO模式”,呋喹替尼也进行了TKI+免疫用于标准治疗失败MSS型患者的后线治疗研究探索,研究结果提示呋喹替尼联合免疫治疗方案虽然带来较好的PFS,但是没有转化成更好的OS,这可能与研究纳入人群的肿瘤转移情况有关。对于TKI联合免疫用于MSS型患者的后线治疗,尚须等待III期临床(LEAP-017)研究结果。对于MSS型患者的联合治疗方案,目前多项国际权威指南推荐为FTD/TPI联合贝伐珠单抗。2022年ASCO会议中发表的Meta分析[15],从875篇文献中筛选出29篇,合计10285例患者,头对头对比FTD/TPI联合贝伐珠单抗与FTD/TPI单药治疗mCRC的有效性和安全性。结果显示,与FTD/TPI单药治疗相比,FTD/TPI联合贝伐珠单抗可获得更高的DCR(64% vs 43%),更长的mPFS(4.2个月 vs 2.6个月)和mOS(9.8个月 vs 8.1个月),且安全性相当。这项Meta分析结果提示FTD/TPI联合贝伐珠单抗与既往前瞻性II期临床研究结果及临床实践一致。据悉,2023年ASCO-GI将发表FTD/TPI联合贝伐珠单抗的III期SUNLIGHT研究,为FTD/TPI联合贝伐珠单抗治疗mCRC提供更高级别的循证医学证据,指导临床治疗选择。

综上所述,晚期肠癌治疗更多地关注分子分型,其中一线研究主要围绕RAS/BRAF野生型和突变型患者及老年/不耐受强烈治疗患者的治疗方案优化。对于二线及以后治疗,对于KRAS G12C突变mCRC患者,KRAS G12C*制剂抑**+抗EGFR单抗具有良好的疗效和安全性;对于MSI-H型mCRC患者,免疫治疗疗效明确,单免或双免均可带来生存获益;对于MSS型mCRC患者,在单药治疗方面,研究显示初始使用FTD/TPI可提高患者依从性和用药持久性;在联合治疗方面,TKI联合免疫治疗疗效尚有待进一步研究证实,FTD/TPI联合贝伐珠单抗治疗mCRC患者生存获益显著,已被美国国家综合癌症网络(NCCN)、中国临床肿瘤学会(CSCO)、日本结直肠癌研究会(JSCCR)以及中国抗癌协会(CACA)等多项国内外权威指南推荐为mCRC标准治疗,III期临床研究SUNLIGHT结果可期。
参考文献
[1]. Antonio Avallone, et al. 2022 ASCO; abstract 3503
[2].Chiara Cremolini et al. 2022 ASCO; abstract LBA3505
[3]. Marinde J G et al. 2022 ESMO; abstract LBA21
[4]. Armando Orlandi et al. 2022 ESMO; abstract LBA22[5]. Cornelis J et al. 2022 ASCO; LBA3506[6]. Damato A et al. 2022 ASCO; abstract LBA3509[7]. Hamaguchi T, et al. 2022 ASCO-GI Abstract 10[8]. Eiji Oki et al Cancer Medicine. 2020;00:1–8. [9]. Cutsem EV, et al. Ann Oncol. 2020;31(9):1160-1168[10]. Yasutoshi Kuboki, et al. 2022 ESMO 315O.[11]. Samuel J. Klempner, et al. 2022 ESMO LBA24
[12]. Michael J.et.al.2022 ASCO; abstrac 3510[13]. Dasari A et al. ESMO 2022,Presentation LBA25[14]. Braiteh F S, et al. 2022 ASCO-GI abstract 49[15]. Yoshino T,et al,2022 ASCO Abstract 3568