引用本文: 杨秋瑾, 郑杰, 杨婧, 等. 幽门螺杆菌感染对非酒精性脂肪性肝病及其相关结直肠息肉的影响研究 [J] . 中国全科医学, 2021, 24(30) : 3855-3862. DOI: 10.12114/j.issn.1007-9572.2021.00.549.

随着肥胖和代谢综合征(MetS)的流行,非酒精性脂肪性肝病(NAFLD)已成目前为全球最常见的慢性肝病,据报道,NAFLD覆盖了全球约25%的人口,其中10%~30%为非酒精性脂肪性肝炎(NASH)[1]。从非酒精性单纯性脂肪肝(NAFL)向NASH的转变使肝硬化、肝衰竭及肝细胞癌发生风险显著增加,约40%的NASH患者进展为肝纤维化,而肝纤维化可使NAFLD患者的死亡风险增高[2]。NAFLD发病率高、病因复杂,目前尚未明确其具体的发病机制和自然史,且无确切的治疗方法。因此,探究NAFLD进展过程中的危险因素至关重要。近年研究表明,幽门螺杆菌( H.pylori )感染可能在MetS相关疾病中起作用,包括NAFLD、心血管疾病及结直肠肿瘤等[3],但有部分高质量研究否定了这种观点[4,5]。 H.pylori 是一种广泛流行的革兰阴性螺旋杆菌,约感染全世界一半的人口,且治疗相对简单、便宜[6]。 H.pylori 感染与NAFLD关系的确立可能为NAFLD及其并发症的防治提供新的策略。因此,本研究对昆明医科大学第二附属医院合并 H.pylori 感染的NAFLD患者进行了回顾性研究,以阐明 H.pylori 感染是否加重NAFLD的进展,并探索 H.pylori 感染在NAFLD患者结直肠息肉发生发展中的作用。
本研究背景:
研究表明,幽门螺杆菌( H.pylori )感染可能与非酒精性脂肪性肝病(NAFLD)及结直肠息肉均相关。鉴于 H.pylori 感染、NAFLD及其相关结直肠息肉的高患病率,探讨 H.pylori 感染是否会加重NAFLD的严重程度和血糖、血脂、血压等代谢指标并评估合并 H.pylori 感染的NAFLD患者发生严重结直肠息肉的风险可能为NAFLD及其相关结直肠息肉提供新的防治手段。
本研究局限性:
本研究为回顾性研究,且样本量较小,同时缺乏肝脏穿刺活检结果,未对肝脏组织学进行评估。
1 对象与方法1.1 研究对象
选取2018年12月至2020年5月在昆明医科大学第二附属医院经腹部B超检查诊断为NAFLD的118例患者为研究对象,其中男60例,女58例;年龄20~85岁,平均年龄(51.4±14.7)岁。根据是否感染 H.pylori 将所有患者分为NAFLD合并 H.pylori 感染组及NAFLD不合并 H.pylori 感染组。所有患者在同一时间段内完善腹部超声检查、肝弹性成像检查、13C尿素呼气试验及血液生化学检查。
NAFLD的诊断参考中华医学会肝脏病学分会脂肪肝和酒精性肝病学组于2010年修订的《非酒精性脂肪性肝病诊疗指南》中的超声诊断标准[7]以及2012年美国胃肠病学协会、美国肝病研究协会和美国胃肠病学院发布的《NAFLD诊断和管理指南》[8],具体如下[7,8]:(1)空腹行腹部B超检查发现肝脂肪变性,满足以下超声表现中的两项为弥漫性脂肪肝:①肝脏附近回声呈弥漫性增强,并强于肾脏和脾脏;②肝脏远场回声逐渐减弱;③肝内导管结构不清晰。(2)无过量饮酒史(男性饮酒折合乙醇量<30 g/d,女性<20 g/d)和其他可以导致脂肪肝的特定原因。(3)无其他慢性肝病(包括病毒性肝炎、自身免疫性肝炎、药物性肝病、原发性胆汁性肝硬化、胆管阻塞、血色病、威尔逊病和α-1抗胰蛋白酶缺乏相关的肝病)。
排除标准:(1)每周乙醇摄入量:男性≥140 g、女性≥70 g;(2)其他慢性肝病;(3)有肿瘤病史或当前患有肿瘤;(4)严重感染或器官衰竭;(5)纳入研究前4周内使用铋剂、抗生素、质子泵*制剂抑**或H2受体阻滞剂;(6)严重的精神或神经疾病;(7)处于妊娠期或哺乳期;(8)既往肝脏、胃部手术史;(9)有他莫昔芬、胺碘酮、丙戊酸钠、甲氨蝶呤、糖皮质激素等药物应用史;(10)全胃肠外营养、炎症性肠病、乳糜泻、甲状腺功能减退症、库欣综合征、β脂蛋白缺乏血症、脂质萎缩性糖尿病、Mauriac综合征等导致脂肪肝的特殊情况;(11)根除 H.pylori 治疗史;(12)检查资料不完整;(13)有结直肠病史,包括结直肠癌、结直肠息肉、炎症性肠病等;(14)结直肠手术史。
1.2 方法
1.2.1 人口学资料采集
在入院当天详细记录患者的性别、年龄、身高、体质量、烟酒史、服药史及既往病史(如高血压、高脂血症、糖尿病、肥胖等),体质指数(BMI)使用以下公式计算:体质量(kg)/﹝身高(m)﹞2。
1.2.2 H.pylori 检测
由经验丰富的检查员使用13C尿素呼气试验(HG-IRIS200A测试仪;北京海德润医药集团有限公司,中国)检测 H.pylori 感染情况。
1.2.3 脂肪肝和肝纤维化检测
患者均进行FibroTouch(FT3000剪切波组织定量超声诊断仪;无锡海斯凯尔医学技术有限公司,中国)检测,获取受控衰减参数(CAP)和肝脏硬度(主要以E值反映),根据CAP将NAFLD患者脂肪衰减程度分为轻度(≥240 db/m)、中度(241~265 db/m)、重度(266~295 db/m);根据E值将NAFLD患者肝脏硬度分为轻度(<7.0 kPa)、中度(7.0~11.8 kPa)、重度(>11.8 kPa)。
1.2.4 结肠镜检查
患者经复方聚乙二醇电解质散进行肠道准备后,由经验丰富的内镜医师完成结肠镜检查,发现息肉后记录息肉的数量、位置和大小,并活检或内镜下切除后送病理检查。息肉位置:近端结肠为盲肠至结肠脾曲,远端结肠为结肠脾曲至肛门,两侧多个息肉定义为全结肠。息肉数量分为单个息肉和多个息肉(≥2个)。息肉大小分为直径≥1 cm和<1 cm的息肉,多个息肉以最大直径为准。根据病理检查结果,分为增生性息肉和腺瘤性息肉。根据息肉有无上皮内瘤变,分为息肉合并上皮内瘤变和息肉不合并上皮内瘤变。
1.2.5 血液生化检测
入院后24 h内抽取患者空腹静脉血,应用大型全自动生化仪和配套试剂盒进行血生化、血常规、急性感染检查。采集的指标包括:①肝功能指标:白蛋白(ALB)、丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)、谷氨酰转肽酶(GGT)、总胆红素(TBiL)、直接胆红素(DBiL);②血脂指标:总胆固醇(TC)、三酰甘油(TG)、低密度脂蛋白(LDL)、高密度脂蛋白(HDL);③血糖:血浆空腹葡萄糖(GLU)、三酰甘油葡萄糖指数(TyG)(即TG和葡萄糖乘积的自然对数[9]);④炎性指标:白细胞计数(WBC)、中性粒细胞计数/淋巴细胞计数(NLR)、降钙素原(PCT)、白介素6(IL-6)、C反应蛋白(CRP)。
1.2.6 NAFLD纤维化评分(NFS评分)、AST和血小板计数(PLT)比率指数(APRI)
使用NFS评分、APRI来评估肝纤维化程度。NFS=-1.675+0.037×年龄(岁)+0.094×BMI(kg/m2)+1.13×空腹血糖受损/糖尿病(是=1,否=0)+0.99×(AST/ALT)-0.013×PLT(×109/L)-0.66×白蛋白(g/dl)[10];APRI=AST/正常上限×100/PLT(×109/L)[11]。
1.2.7 MetS诊断标准
MetS的诊断依据《非酒精性脂肪性肝病防治指南(2018年更新版)》[2]中的MetS诊断标准。
1.3 伦理学审查
本研究方案严格遵守赫尔辛基宣言,且经昆明医科大学第二附属医院伦理委员会审批(审批号:审-PJ-2020-86)。
1.4 统计学方法
采用SPSS 22.0统计软件进行数据分析。符合正态分布的计量资料以(x± s )表示,两组间比较采用成组 t 检验;非正态分布的计量资料以 M ( P 25, P 75)表示,两组间比较采用Mann-Whitney U 检验;计数资料以相对数表示,两组间比较采用χ2检验;等级资料分析采用秩和检验;NAFLD患者结直肠息肉数量、息肉大小、息肉病理、上皮内瘤变的影响因素分析采用多因素Logistic回归分析。以 P <0.05为差异有统计学意义。
2 结果
2.1 患者 H.pylori 阳性情况
118例NAFLD患者中 H.pylori 阳性62例(NAFLD合并 H.pylori 感染组), H.pylori 阴性56例(NAFLD不合并 H.pylori 感染组)。
2.2 NAFLD合并 H.pylori 感染组、NAFLD不合并 H.pylori 感染组人口学资料、脂肪衰减程度、肝纤维化程度、肝功能指标、血脂指标、炎性指标、肝纤维化评分比较
两组性别、年龄、ALB、HDL、GLU比较,差异无统计学意义( P >0.05);NAFLD合并 H.pylori 感染组BMI、CAP、E值、ALT、AST、GGT、TBiL、DBiL、TC、TG、LDL、TyG、WBC、NLR、PCT、IL-6、CRP、NFS评分、APRI高于NAFLD不合并 H.pylori 感染组,差异有统计学意义( P <0.05),见表1。
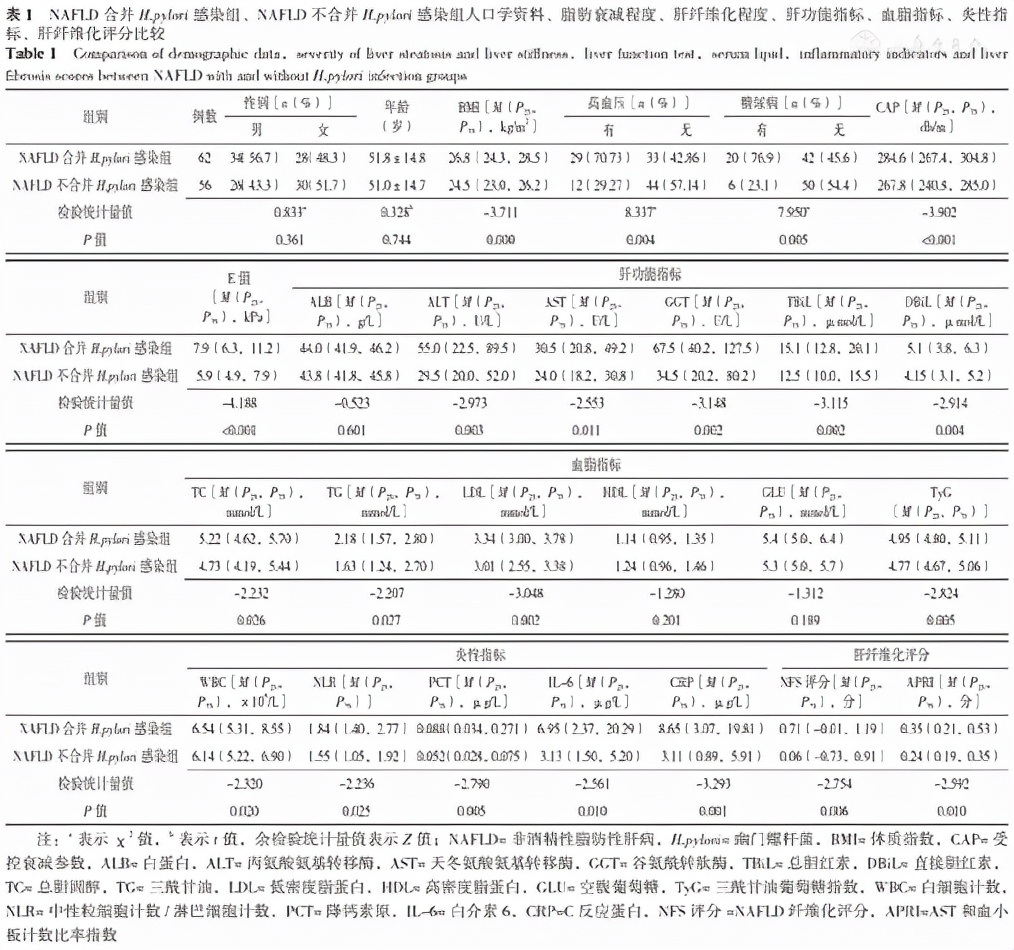
表1 NAFLD合并 H.pylori 感染组、NAFLD不合并 H.pylori 感染组人口学资料、脂肪衰减程度、肝纤维化程度、肝功能指标、血脂指标、炎性指标、肝纤维化评分比较
Table 1 Comparison of demographic data,severity of liver steatosis and liver stiffness,liver function test,serum lipid,inflammatory indicators and liver fibrosis scores between NAFLD with and without H.pylori infection groups
2.3 NAFLD合并 H.pylori 感染组、NAFLD不合并 H.pylori 感染组脂肪衰减程度和肝脏硬度比较
NAFLD合并 H.pylori 感染组脂肪衰减程度、肝脏硬度差于NAFLD不合并 H.pylori 感染组,差异有统计学意义( P <0.05),见表2。
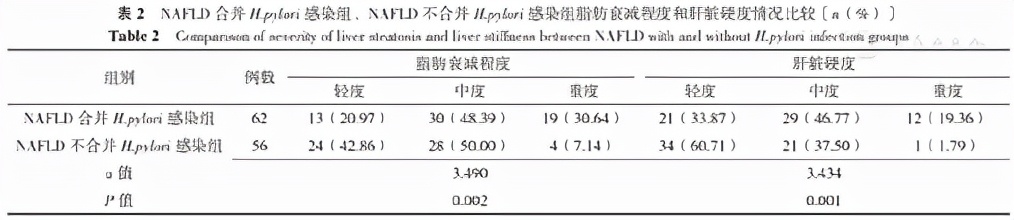
表2 NAFLD合并 H.pylori 感染组、NAFLD不合并 H.pylori 感染组脂肪衰减程度和肝脏硬度情况比较〔 n (%)〕
Table 2 Comparison of severity of liver steatosis and liver stiffness between NAFLD with and without H.pylori infection groups
2.4 NAFLD合并 H.pylori 感染组、NAFLD不合并 H.pylori 感染组息肉位置、息肉数量、息肉病理、上皮内瘤变情况比较
118例NAFLD患者中75例(NAFLD合并 H.pylori 感染组37例,NAFLD不合并 H.pylori 感染组38例)行结肠镜检查,结果示存在结直肠息肉者51例,其中NAFLD合并 H.pylori 阳性组26例。
75例行结肠镜检查的患者中,NAFLD合并 H.pylori 感染组存在近端结肠、远端结肠、全结肠息肉者分别为8、6、12例,NAFLD不合并 H.pylori 感染组中分别为10、6、9例,两组患者息肉位置情况比较,差异无统计学意义(χ2=0.631, P =0.729);NAFLD合并 H.pylori 感染组中存在单个、多个息肉者分别为5、21例,NAFLD不合并 H.pylori 感染组中分别为12、13例,NAFLD合并 H.pylori 感染组中多个息肉发生率高于NAFLD不合并 H.pylori 感染组,差异有统计学意义(χ2=4.747, P =0.029);NAFLD合并 H.pylori 感染组中息肉直径≥1 cm和<1 cm者分别为6、20例,NAFLD不合并 H.pylori 感染组中分别为0、25例,NAFLD合并 H.pylori 感染组中息肉直径≥1 cm发生率高于NAFLD不合并 H.pylori 感染组,差异有统计学意义(χ2=6.538, P =0.011)。
75例行结肠镜检查患者*共中**41例进行病理检查。NAFLD合并 H.pylori 感染组中存在腺瘤性和增生性息肉者分别为18、1例,NAFLD不合并 H.pylori 感染组中分别为9、13例,NAFLD合并 H.pylori 感染组中腺瘤性息肉发生率高于NAFLD不合并 H.pylori 感染组,差异有统计学意义(χ2=13.137, P <0.001);NAFLD合并 H.pylori 感染组中存在高级别、低级别上皮内瘤变和不存在上皮内瘤变者分别为4、8、5例,NAFLD不合并 H.pylori 感染组中分别为0、6、18例,NAFLD合并 H.pylori 感染组中上皮内瘤变发生率高于NAFLD不合并 H.pylori 感染组,差异有统计学意义(χ2=10.752, P =0.005)。
2.5 NAFLD患者结直肠息肉数量、息肉大小、息肉病理、上皮内瘤变影响因素的单因素、多因素Logistic回归分析
考虑到高血压、糖尿病等代谢危险因素和脂肪肝严重程度本身对肠腺瘤的影响,进一步行单因素、多因素Logistic回归分析。分别以NAFLD患者结直肠息肉数量(赋值:单个=0,多个=1)、息肉大小(赋值:<1 cm=0,≥1 cm=1)、息肉病理(赋值:增生性息肉=0,腺瘤性息肉=1)、上皮内瘤变(赋值:无=0,有=1)为因变量,以 H.pylori 、脂肪衰减程度、高血压、糖尿病为自变量进行单因素Logistic回归分析,结果显示, H.pylori 是NAFLD患者结直肠息肉数量、息肉病理、上皮内瘤变的影响因素( P <0.05),见表3。
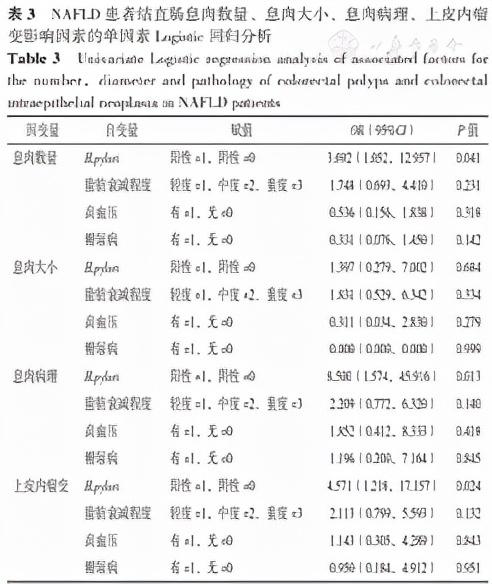
表3 NAFLD患者结直肠息肉数量、息肉大小、息肉病理、上皮内瘤变影响因素的单因素Logistic回归分析
Table 3 Univariate Logistic regression analysis of associated factors for the number,diameter and pathology of colorectal polyps and colorectal intraepithelial neoplasia in NAFLD patients
分别以NAFLD患者结直肠息肉数量、息肉大小、息肉病理、上皮内瘤变为因变量,以表4中 P <0.2的指标为自变量(赋值同单因素Logistic回归分析)进行多因素Logistic回归分析,结果显示, H.pylori 阳性、合并糖尿病是NAFLD患者结直肠息肉数量的影响因素( P <0.05); H.pylori 阳性是NAFLD患者结直肠息肉病理、上皮内瘤变的影响因素( P <0.05),见表4。
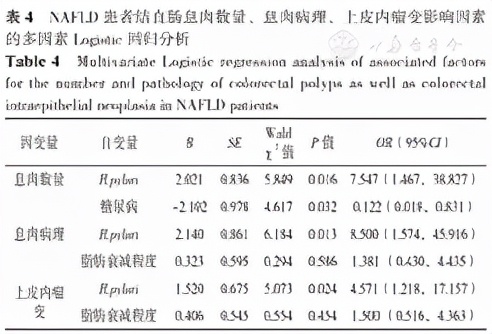
表4 NAFLD患者结直肠息肉数量、息肉病理、上皮内瘤变影响因素的多因素Logistic回归分析
Table 4 Multivariate Logistic regression analysis of associated factors for the number and pathology of colorectal polyps as well as colorectal intraepithelial neoplasia in NAFLD patients
3 讨论
研究表明,NAFLD与胰岛素抵抗(IR)相关的MetS密切相关,合并MetS的NAFLD患者通常存在更严重的肝组织学损伤,并且进展为NASH和肝纤维化的概率更高[2]。有研究表明 H.pylori 感染可能与IR及MetS相关疾病有关, H.pylori 在NAFLD及结直肠息肉的发生发展中均具有重要作用[3],但关于 H.pylori 、NAFLD及结直肠息肉三者的证据存在矛盾[4,5]。本研究旨在阐明 H.pylori 感染能否加重NAFLD及其相关结直肠息肉,以期为NAFLD的防治开辟新的思路。
本研究结果显示, H.pylori 阳性NAFLD患者TyG明显升高,根据近年的研究,TyG已被描述为反应IR的生化指标[9]。此外 H.pylori 阳性的NAFLD患者高血压发生率、糖尿病发生率和血脂明显高于 H.pylori 阴性者,WBC、NLR、PCT、IL-6、CRP也明显升高,证明 H.pylori 阳性的NAFLD患者更容易MetS和发生炎性反应。本研究结果显示, H.pylori 阳性的NAFLD患者ALT、AST、GGT明显升高,提示 H.pylori 感染加重了NAFLD患者的肝功能障碍。NLR除了被广泛用于评估炎性反应程度外,还可以预测NAFLD纤维化分期和其他组织学特征[12],结合 H.pylori 阳性的NAFLD患者CAP、E值、NFS评分、APRI明显升高,可证实 H.pylori 感染加重了NAFLD患者肝纤维化程度。GLU在是否合并 H.pylori 感染的NAFLD患者中并无统计学差异,但是TyG却在 H.pylori 阳性的NAFLD患者中明显升高,这可归因于部分糖尿病患者服用降糖药物。综上,本研究表明 H.pylori 感染可能通过引发代谢紊乱和炎性反应增加NAFLD患者病情严重程度,包括肝脂肪变性程度、肝纤维化和肝细胞的损伤,这与CHEN等[13]最近发表的研究结果相似,该研究指出 H.pylori 感染与NAFLD患者的脂肪变性情况、严重程度、碳水化合物代谢异常、肝功能障碍、炎性反应加重以及MetS的发生呈正相关, H.pylori 感染可能通过影响上述指标而成为预测NAFLD进展的自发性危险因素。此外,部分前瞻性研究表明,对NAFLD患者进行 H.pylori 根除治疗可以改善患者肝纤维化及其代谢指标[14,15,16],本研究进一步证实了该结论。但也有部分研究表明 H.pylori 感染与NAFLD无明显相关或仅有微弱的联系[4,5,17]。这可能是由于 H.pylori 的检测方法以及研究设计不同,部分研究中反映 H.pylori 感染的血清IgG抗体阳性不能区分既往和当前感染,可能对研究结果具有干扰性。
NAFLD的临床负担不仅限于肝脏相关疾病,如心血管相关疾病和包括结直肠肿瘤在内的肝外恶性肿瘤是NAFLD患者主要死亡原因[18,19]。据报道,NAFLD患者患结直肠腺瘤(CRA)的风险增加,NAFLD是CRA的重要危险因素[20,21]。CRA与结直肠癌(CRC)密切相关,早期发现和切除可能在CRC的一级预防中具有重要意义。本研究结果显示, H.pylori 阳性的NAFLD患者更易出现多个肠息肉、直径≥1cm的肠息肉、腺瘤性肠息肉,且更多的肠息肉发生上皮内瘤变;而是否合并 H.pylori 感染对NAFLD患者肠息肉的位置无明显影响。上述研究结果在一定程度上表明 H.pylori 感染可加重NAFLD患者CRA的严重程度,这与AHN等[22]研究结果相似,其提出合并 H.pylori 感染并伴有MetS的NAFLD是大肠肿瘤的危险因素。KOUNTOURAS等[23]研究也表明 H.pylori 感染伴有NAFLD、MetS及肠道菌群紊乱(GM-D)可能参与CRA-CRC的发展。本研究多因素Logistic回归分析结果显示, H.pylori 阳性是NAFLD患者结直肠息肉数量、息肉病理、上皮内瘤变的影响因素。WANG等[24]研究结果显示, H.pylori 感染与结直肠多发性息肉、腺瘤性息肉的发生独立相关,与息肉大小和位置无关。另有研究表明, H.pylori 感染诱发的CRA主要累及左侧结肠和直肠,这可能与高胃泌素促有丝分裂作用仅限于左侧结肠有关; H.pylori 感染可导致高胃泌素血症及远端结肠腺瘤发生风险增加[25]。
尽管上述研究结果存在争议,但笔者分析认为 H.pylori 感染可能通过以下机制参与NAFLD及其相关CRA的发展:(1)引发或加重与IR相关的MetS。 H.pylori 感染可能通过调节脂联素和胎球蛋白-A水平、引发炎性反应、改变肠道菌群以及c-Jun/miR-203/SOCS 3信号通路介导IR的发生[3]。IR可刺激肝细胞微粒体脂质过氧化物,引发氧化应激,诱导炎性反应,导致肝细胞中脂肪分解和代谢异常,并进一步加重IR,形成恶性循环,加速肝纤维化进展[26]。IR时代偿性升高的胰岛素使胰岛素结合蛋白1(IGFBP-1)水平降低而胰岛素样生长因子1(IGF-1)水平升高,后者被认为与CRC的病理、生理有关[27]。胰岛素还是重要的结肠肿瘤细胞和结肠黏膜细胞生长因子,参与CRA细胞的增殖和转移[28],同时可以促进肝内TG蓄积,使胆汁酸合成增加而促进结直肠肿瘤的发生。(2) H.pylori 感染导致NAFLD患者脂联素减少,脂联素具有抗炎作用,可抑制结直肠肿瘤细胞增殖[29,30]。(3)改变肠道微生态。 H.pylori 感染可使胃黏膜萎缩,胃酸分泌减少,从而使得肠道菌群发生改变及肠道黏膜屏障破坏,这可能是NAFLD和CRA发生、发展的共同机制之一[31,32]。肠道微生态改变不仅可影响体内葡萄糖和短链脂肪酸的摄取和代谢并造成肝脏脂质代谢异常,还可通过增加甲基胺水平而在NASH的进展中起作用[34,35]。肠道黏膜屏障的破坏使细菌及内毒素通过门静脉异位至肝脏,与肝细胞Toll样受体结合,激活肝库普弗细胞,诱导炎性细胞因子、活性氧(ROS)及血管活性因子的释放,促进肝星状细胞活化和增殖,导致促炎反应,最终引起肝细胞的凋亡、坏死及纤维化[35]。此外,长期 H.pylori 感染还可使胃泌素释放增加,而高胃泌素血症可能促进结直肠肿瘤进展[25]。(4)CD44被证明在 H.pylori 诱导的上皮细胞增殖及炎性反应中发挥功能性作用[36]。值得注意的是,CD44可能与NASH的进展相关,且可能在NAFLD相关结直肠肿瘤的进展中具有重要意义[37,38]。
本研究具有一定的局限性:首先本研究为单中心、小规模研究,样本量较小;其次,本研究中NAFLD的诊断基于超声和FibroTouch检测结果,未进行肝脏穿刺活检,不能准确评估 H.pylori 感染对NAFLD患者肝脏组织学变化的影响,但是肝穿刺活检有创,目前尚不能推广到普通人群。本研究中 H.pylori 感染与NAFLD患者结直肠息肉严重程度关系的多因素Logistic回归分析的 OR 值及95% CI 偏大,可能与样本量较小相关,未来需要大样本研究进一步验证。
综上所述, H.pylori 感染可加重NAFLD患者肥胖、高血压、糖尿病、肝功能障碍、血脂紊乱、炎性反应、肝纤维化程度、脂肪衰减程度,此外, H.pylori 感染还是NAFLD患者结直肠息肉数量、息肉病理、上皮内瘤变的影响因素。尽管机制未明,但这对于临床医生来说仍是一个非常重要的警示,对于合并 H.pylori 感染的NAFLD患者需要谨慎考虑CRA发生风险,进一步完善结肠镜检查。
利益冲突
本文无利益冲突。
参考文献 略