本文来自微信公众号:X-MOLNews
在临床肿瘤治疗中,放疗、免疫治疗以及其联合治疗占据着重要地位。放疗可以引起免疫原性细胞凋亡,激活抗肿瘤免疫反应,产生远端效应抑制转移肿瘤的生长。将放疗与免疫治疗相结合可以进一步增强免疫反应,通过局部放疗实现全身治疗反应,抑制远端转移肿瘤。但是肿瘤微环境(TME)中乏氧和免疫抑制等特征会抑制放疗与免疫治疗的效果。一氧化氮(NO)作为一种内源性的气体信号递质,被认为是一种非常有效和独特的肿瘤微环境调节因子。近年来,报道了多种纳米系统向肿瘤递送一氧化氮,但是大多数一氧化氮供体释放一氧化氮依赖于外界刺激,例如光、热或超声,阻碍了进一步的临床转化。
近日,苏州大学刘庄教授(点击查看介绍)领导的先进生物材料和纳米医学团队提出了一种新策略,利用原位切伦科夫荧光激发释放一氧化氮调节肿瘤微环境。研究人员通过临床药物制备单层二维纳米材料,然后进行无螯合剂放射性标记,构建出一个自激发纳米器件。放射性核素诱导的切伦科夫荧光刺激纳米片持续的释放一氧化氮,调节肿瘤乏氧和免疫抑制微环境,增强肿瘤放疗、放射-免疫联合治疗的效果。相关成果近期发表在Cell Press旗下材料学旗舰期刊 Matter 上,第一作者为博士生田龙龙。

刘庄教授(前排居中)团队。图片来源:苏州大学
刘庄团队在前期的免疫治疗与核素治疗的基础上(Nat. Biomed. Eng., 2018, 2, 611-621; Nat. Commun., 2017, 8, 902)进一步提出了原位切伦科夫荧光激活二维纳米片,增强核素-免疫治疗。研究者选取临床一氧化氮供体药物硝普钠与锌离子构建材料,在合成过程中调节表面活性剂,制备出纳米立方块、纳米球和纳米片三种不同形貌的材料。粉末X射线衍射、透射电子显微镜、原子力显微镜和X射线光电子能谱等多种表征手段证明纳米片为单层ZnFe(CN)5NO(图1A-H)。低功率的紫外灯辐照可以有效地激发纳米片释放一氧化氮,但是并不能激发纳米立方块和纳米球(图1I),这说明二维纳米结构才具备响应-释放能力。
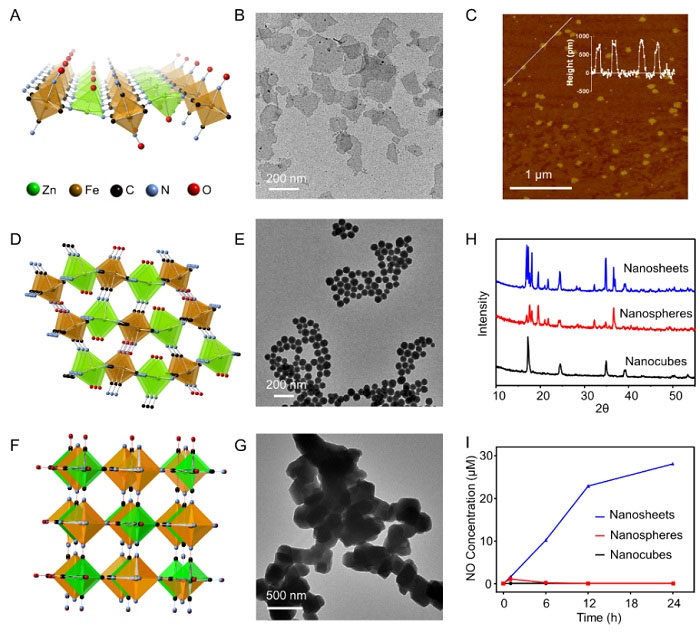
图1. 合成和表征材料。图片来源:Matter
32P(32PO4 3-)可以诱导介质水发射强烈的切伦科夫荧光,而且可以与纳米片表面裸露的锌离子配位。因此,研究者采用无螯合剂标记法,直接在纳米片上稳定、高效地标记放射性核素32P,激发纳米片持续地释放一氧化氮(图2A-D)。在细胞水平进一步验证了32P标记的纳米片释放一氧化氮,增强32P
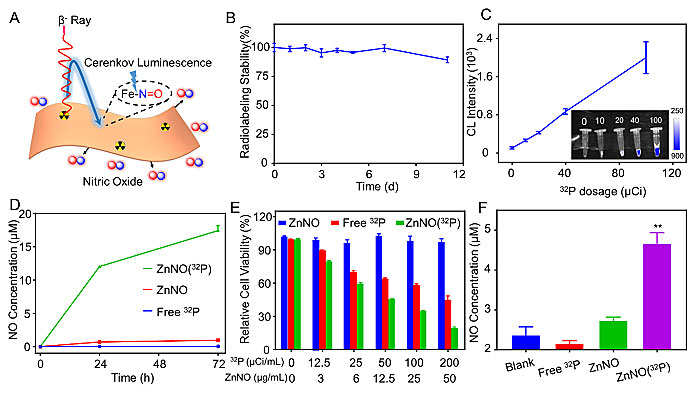
图2. 切连科夫荧光激发纳米片释放一氧化氮。图片来源:Matter
研究人员在肿瘤局部注射32P核素,通过核素成像和切伦科夫成像监测放射性核素的踪迹。结果表明,游离的核素会很快从肿瘤逃逸,肿瘤内滞留较差;而标记在纳米材料上的放射性核素会长期的滞留在肿瘤局部(图3A-E)。在较低放射性剂量下对肿瘤进行核素治疗,游离的核素和纳米片抑制肿瘤生长的能力较弱;核素标记的无一氧化氮对照纳米材料只能略微地抑制肿瘤生长;而32P标记的纳米片能够完全清除局部肿瘤(图3F-H),具有优异的肿瘤治疗能力。
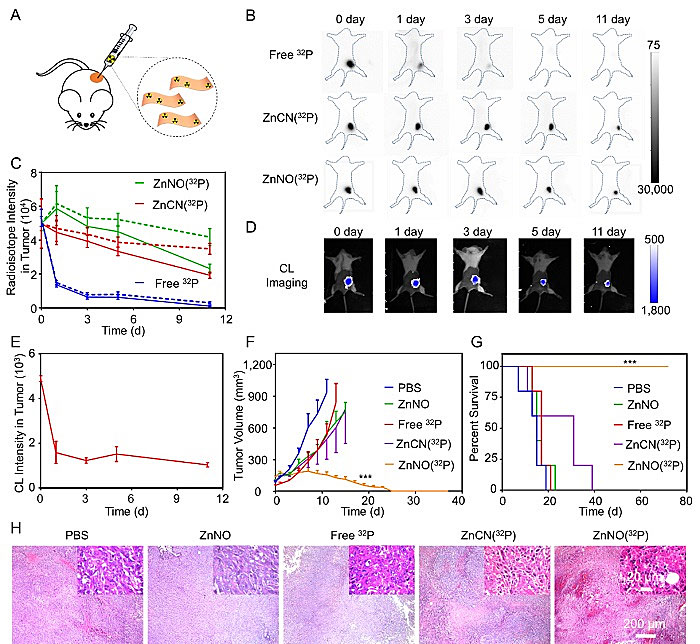
图3. 局部核素治疗。图片来源:Matter
研究者为了揭示32P标记纳米片的抗肿瘤机制,通过免疫荧光染色探究了肿瘤微环境的变化。通过特异性抗体对体内一氧化氮标志物3-硝基酪氨酸(3-Nitrotyrosine,3-NT)染色,结果表明32P标记的纳米片可以在体内明显的释放一氧化氮,抑制肿瘤乏氧诱导因子(HIF-1a)表达,增强肿瘤对放疗的敏感性(图4A-B)。同时研究发现,切伦科夫荧光激发纳米片释放的一氧化氮可以降低免疫抑制性细胞(调节性T细胞Treg和肿瘤相关巨噬细胞TAMs)的募集,增强肿瘤*伤杀**性T细胞的浸润,显著的改善肿瘤免疫微环境(图4C-G)。
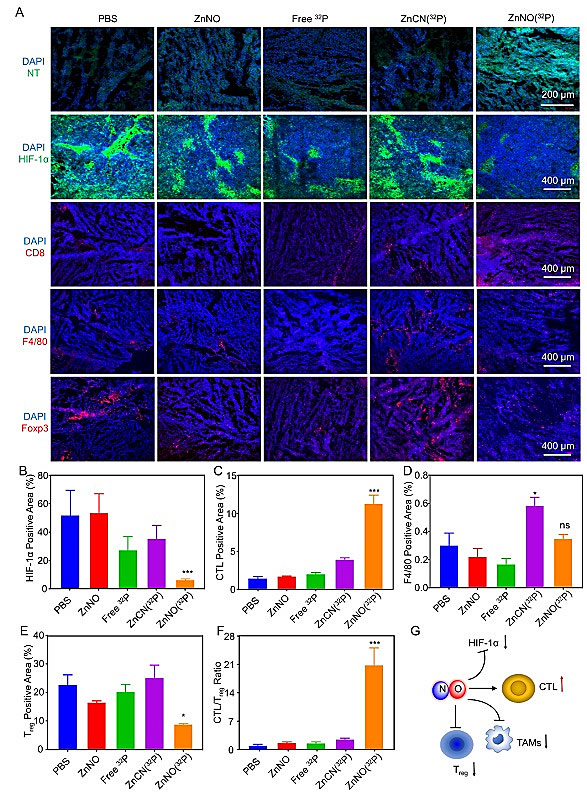
图4. 调节肿瘤微环境。图片来源:Matter
在临床中,肿瘤转移是造成癌症病人死亡的主要原因,利用局部核素治疗抑制远端转移肿瘤具有重要的临床价值。核素治疗能够使癌细胞产生免疫原性凋亡,同时切伦科夫荧光激发纳米片释放的一氧化氮可以显著的改善肿瘤免疫微环境,因此将32P标记的纳米片局部核素治疗与肿瘤免疫治疗相结合,具有抑制远端转移肿瘤的潜力。研究人员将32P标记的纳米片治疗与程序性死亡受体1抗体治疗相结合,不仅可以清除局部肿瘤,而且可以通过持续的激活机体的免疫系统清除远端转移肿瘤(图5)。
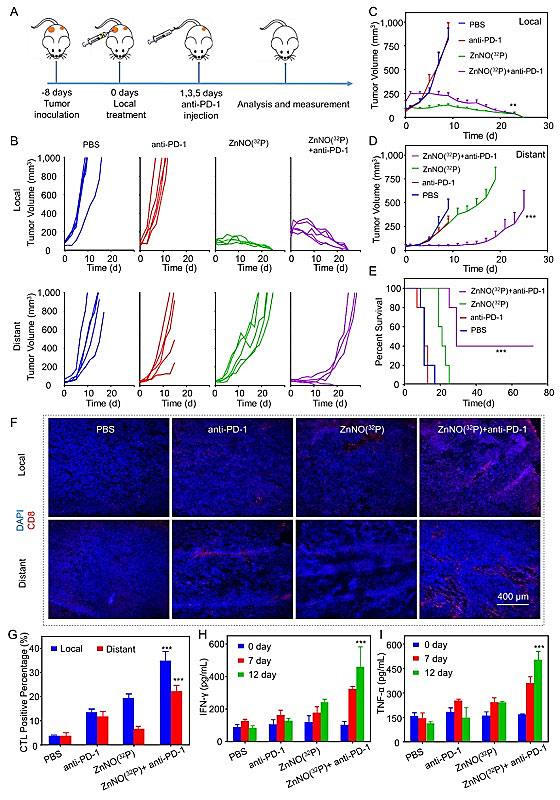
图5. 联合核素治疗和免疫治疗抑制远端转移肿瘤。图片来源:Matter
总结
刘庄教授团队提出了一种简单方法,由锌离子和临床药物硝普钠构建出单层二维纳米片,并通过无螯合剂标记放射性核素32P,组成了一个自激发纳米反应器。32P诱导的切伦科夫荧光刺激纳米片持续的释放一氧化氮,调节乏氧和免疫抑制性的肿瘤微环境,完全清除局部肿瘤。研究人员进一步联合核素治疗-免疫治疗,激活强大的抗肿瘤免疫,有效抑制远端转移肿瘤。这种由临床药物构建的二维纳米医学平台在临床核素治疗以及联合免疫治疗等方面显示出巨大的转化潜力。
Cerenkov Luminescence-Induced NO Release from 32P-Labeled ZnFe(CN)5NO Nanosheets to Enhance Radioisotope-Immunotherapy
Longlong Tian, Yaxing Wang, Lele Sun, Kai Yang, Shuao Wang, Zhuang Liu
Matter, 2019, DOI: 10.1016/j.matt.2019.07.007
导师介绍
刘庄
https://www.x-mol.com/university/faculty/18393
(本稿件来自 Matter )